���±�ţ�1004-0609(2016)-12-2686-08
ʪ�����շ�Ǧ���м����������ǦPb3(C6H5O7)2��3H2O���ȷֽ�
���·�1��������1��������2���� ΰ2�����곽2����ҿ�2���� ��1����һ��1
(1. ���ϳǽ�ѧԺ �����뻷������ѧԺ��ƽ��ɽ 467036��
2. ���пƼ���ѧ ������ѧ�빤��ѧԺ���人 430074)
ժ Ҫ��
ժ Ҫ����������ƽ���������������ǡ�X���������ǡ�ɨ��羵�����ֶ��о�������ǦPb3(C6H5O7)2��3H2O���ȷֽ���̺Ͳ�����������������ǦPb3(C6H5O7)2��3H2O���ȷֽ���̷�ˮ���ѳ�����ˮ��ֽ��ȼ��3���Σ��ᾧˮ����ˮ��ֽ��ɢʧ���¶ȴﵽ100~200 ��ʱ���������л���������¶�ʱ������Ҫ��CO2�����ղ���Ϊ����Ǧ�����Ǧ��������Ǧ�ڿ����зֽ��ܱ����¶�Ӱ���Ϊ������������Ǧǰ����Pb3(C6H5O7)2��3H2O���±���ʱ�������Ҫ�ɷ��Ǧ�-PbO����-PbO�����Ǧ�����±���ʱ������Ҫ�ɷ��Ǧ�-PbO��
�ؼ��ʣ�
������Ǧ���ȷֽ���������Ǧ���м������
��ͼ����ţ�TG156���� ���ױ�־�룺A
Ǧ������������۸���Խ�Ϊ����������ʹ��ʱ�ɿ���ǿ���ܹ����ܴ�����ŵ缰�Ͽ������˻����¶ȷ�Χ���ŵ���ڻ�ѧ��Դ��һֱռ�о������ơ�Ǧ�������������ϸ������в�������ڽ�ͨ��ͨ�š����������µ�����ʹ����㷺������Ǧ��������ʹ������ֻ��2~4�꣬��ʹ���������ϵ�Ǧ�������������ڲ����������ԷϾ�Ǧ�����صĻ�����Ϊ��Ҫ����Ǧ�����ص���Ҫ��ɲ�����4��[1]�����Һ����դ��Ǧ���Լ��л����س�ŵ�����л���ɽ�״���ʵĻ��ۣ����ֽ�״���ʾ���Ǧ�࣬Լռ�������30%~40%��Ǧ�����Ҫ�ɷ��Ǵ����������κͲ�ͬ��̬��Ǧ����������гɷֵĸ�������Ǧ���ػ������ѵ���Ҫԭ��ͨ�õĻ�ұ�����̻����SO2��Ǧ������Ⱦ�ͬʱ�����Ÿߺ��ܺ͵ͻ����ʵı�[2-3]����ˣ��������������Ŷ��о����÷�Ǧ��ʪ���������±����Ʊ���ϸǦ���¹���[4-10]���¹����������ؼ����裺1) ���ٸ�Ч�ػ��������Ǧ��2) ������Ǧ��˳���ֽ��Ʊ����Ϲ�ҵӦ�õ�Ǧ�ۡ�ǰ���о����֣�������-����������ϵ�еõ����ǰ�״������Ǧ������ʽΪPb(C6H6O7)��H2O�������¶ȼ��ӳ�����ʱ���Բ�����ɡ����μ���ò�нϴ��Ӱ��[6, 9]��Ϊ����߷�Ӧ�ٶȣ���������-����������ϵ��ʪ���������±����Ʊ���ϸǦ�۹��գ�����-����������ϵ���Ʊ��õ���������Ǧ����״�ṹ������ʽΪPb3(C6H5O7)2��3H2O�����ǰ�õ��İ�״������Ǧ�����нϴ������[11]��Ϊ��ȷ��������Ǧ����ķ��ӽṹ����ò�Ա��ղ����Ӱ�죬�������������״�ṹ������ǦPb3(C6H5O7)2��3H2O���ȷֽ���̼��Ʊ���ϸǦ�۹��ɽ����о���
1 ʵ��
1.1 ԭ�ϼ��Լ�
ʵ��ԭ��Ϊʵ��Ǧ�࣬��ּ���1����Һ��ϵΪ����-����������ϵ������������Ǧ��Ħ����Ϊ4:3����ҺpHΪ5~6��������Ǧ����ʼ����Ϊ10 g�����ձ��������֪������������Ϊ14.2 g��������Ǧ��Ħ����Ϊ8:3����֪��������ΪΪ5.8 g��˫��ˮ�������ǦĦ����Ϊ2:1����Һ��Ϊ1:5������������-����������Һ������Ǧ�࣬�ٻ�������˫��ˮ�������·�Ӧ2 h���������ֺ�����ʽ�õ�������Ǧ��Ʒ��һ�ַ����ǻ��Һֱ�ӹ��ˡ�ϴ�ӣ���ɵõ�ֱ�ӹ��˵�������Ǧ������һ�ַ����Ƿ�Ӧ��Ļ��Һ��55 ��ˮԡ�����³»��ᾧ4 h���й��ˣ�ϴ�ӡ���ɵõ��ᾧ������Ǧ���Եõ���Ʒ����SEM��XRD��TG/DTA�ȱ�����û������˵��ָ�ľ�Ϊ�ᾧ��������Ǧ��Ʒ��
�ڲ�ͬ�¶��¶�������Ǧǰ������б��գ������¶�Ϊ200��250��300��350��400��450��500 �棬���α�����5.0 g������ʱ��1 h������XRD��SEM/EDX���ֶζԱ��ղ�����б������о�������Ǧ�ȷֽ������
��1 Ǧ����Ʒ�����
Table 1 Chemical compositions of lead paste sample (mass fraction, %)

����Diamond TG/DTA�ȷ����ǵ��¶�Ϊ��Χ25~800 �棬��������5 ��/min����Ʒ������������ʧ������XRD��FSEM�����ֱ���ú�����X��Pert PRO��X���������Ǻ�Sirion 200��XRDʵ��������ͭ�вģ�Ni�˲�����ѹ40 kV������40 mA������۲⼰����������SEM/EDS����ǡ�������Ǧ���ȷֽ�����������ͺ�����ı仯�۲�����ͺ�ΪPyris1TGA����ƽ����������������(TG-FTIR)�����ֽ��������ͨ������ҽ��к���ɨ�裬��֤��ͨ�豸��©����ɨ���IR������Χ500~4000 cm-1���ֱ���2.5 cm-1��ɨ������ÿ5 s/�Σ���������0.12 L/min�����Ҽ���·�¶�200 �棬����ӷ��Լ���ӷ����������������������յķ�Ӧ��
1.2 ������Ǧ�����
Pb2+�İ뾶Ϊ0.119~0.149 nm������λ���ϸߣ��������������γ�������ǦPb(C6H6O7)��H2O[12]��Pb6(H2O)2(C6H5O7)4��3H2O[13]�ȡ���ˣ���ʵ�����������ɵ�������Ǧ��ϸԪ����ֶ��ں�����ϸǦ�۵��ȷֽ��Ʊ�ʮ����Ҫ��ֱ�ӹ��˵�������Ǧ��55 ���»���õ�ǰ����������Ǧ�����������ǦXRD����ͼ1��ʾ��
��ͼ1��֪����3��������Ǧ��XRD���нϴ�IJ��죬������ɺ�Ǧ���XRD����û��PbSO4��PbO��PbO2������壬֤ʵ�˽�����Ӧ��ȫ���ᾧ����������ǦXRD�����������Ǧ(������ɯ��˾����)������ǦPb3(C6H5O7)2��3H2O��XRD���нϸߵ����ƶȡ���ֱ�ӹ��˵�������Ǧ��ǰ������ȱ��ֳ��ϴ�IJ����ԡ���SONMEZ��[14]�о�����Ǧ��������-�������Ƶõ�������ǦXRD��һ�¡�

ͼ1 ��ͬ������ʽ�õ���������Ǧ��XRD��
Fig. 1 XRD patterns of different lead citrate filtering immediately after leaching(a), recrystallization (55��, 4 h)(b), lead citrate purchased from Alfa Aesar China (Tianjin) Co., Ltd(c)
������Ǧ��C��HԪ�ط�����ʾ��C��HԪ�ص������ȷֱ�Ϊ6.82��1.49�����������ΪPb3(C6H5O7)2��3H2O��������ǦC��HԪ�ص�������Ϊ6.837��1.519�����������ݾ��нϸߵ��Ǻ϶ȣ�������С��2 %�������������ݺ�XRD�����ȷ������������Ǧ�ķ���ʽΪPb3(C6H5O7)2��3H2O���ܽ����������Ǧ���ⶨǦ�����������ʾ������Ǧ�Ĵﵽ��99.9%��ͼ2��ʾΪ������ǦPb3(C6H5O7)2��3H2O��SEM����ͼ2��֪��������Ǧ�ʹ���ij���״������Ϊ10~50 ��m���������ԼΪ4 ��m2��

ͼ2 ����������Ǧ��SEM��
Fig. 2 SEM image of lead citrate Pb3(C6H5O7)2��3H2O
2 ��������
2.1 ������Ǧ��������ʧ�������߷���
�ڿ��������жԲ���������ǦPb3(C6H5O7)2��3H2O����TG-DTA������������ͼ3��ʾ����ͼ3��֪��������Ǧ�ڿ����е��ȷֽ����Կɷ�Ϊ3���Σ���һ����200 �����£�Ϊʧˮ�Σ��ý�������ʧԼΪ5.5 %���Դ��ڽᾧˮ�������ڶ�����200~350 ��֮�䣬�ڴ�������300 ���335 ���DTA���ֽ�Ϊ�����ķ��ȷ壬�������ڲ���������Ǧ�ֽʼ�������ȣ��˽�������ʧ��31%���ң��������¶���350 �����ϣ���345 ��ʱ����ǿ���ȷ壬�÷��ȷ�����Ǧȼ�շ��ȣ�����415 ���µķ��ȷ�Ϊ̿ȼ�շ��ȣ��ý�������ʧԼ4.0%����450 �漰���Ϸֽ�ﵽ�ȶ�״̬����������ʧԼΪ39.6%��
2.2 ������Ǧ�ȷֽ���̷���
�ڲ�ͬ�ı����¶��²���������FTIR����ͼ4��ʾ����Ӧ������������������ղ������1��ʾ����ϱ�1��ͼ4��֪�������¶���230 ������ɷ���ҪΪCO2���¶ȴﵽ330 ��ʱ��CO2�ĺ�����������������������CO2ռ90%���ϣ����¶ȵ�����CO2���������٣��¶ȴﵽ450 ��ʱ�������������������һ�������������Ǧ��TG-DTA���ȷֽ�����������¶ȸ���200 ��ʱ���ڲ���Ϊ1700~1900 cm-1�ķ�Χ�ڳ���һЩ���շ壬���ǿ�������ȩ(CH3CHO)����ȩ(CH2O)���״�(CH3OH)�ͼ���(HCOOH)��[15-16]�����ȷֽ���¶�������������ǦPb3(C6H5O7)2��3H2O�����ֽ⡣����ǰ�о��������[9]�е���������ǦPb(C6H6O7)2��H2O���ȷֽ�����Ƚϣ�������ǦPb3(C6H5O7)2��3H2O�ֽ����������������������ǦPb(C6H6O7)2��H2O�ȷֽ�������壬���ȷֽ���¶�������������ǦPb3(C6H5O7)2��3H2O�ķֽ��¶ȸ��͡�
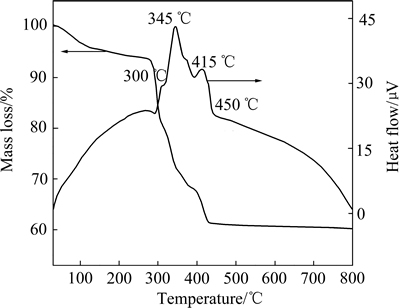
ͼ3 ������Ǧ��TG-DTA����
Fig. 3 TG-DTA curves of lead citrate

ͼ4 ������Ǧ��ͬ�¶��ȷֽ��FTIR��
Fig. 4 FTIR spectra of lead citrate at different temperatures in air
��1 ��������������岨��
Table 1 Absorption peaks of typical gases

2.3 ����������Ǧ�����Ʊ���ϸǦ��
2.3.1 �¶ȶ�������Ǧ��ʧ����Ӱ��
��ͬ���¶���������Ǧ����ʧ����ͼ5��ʾ����ͼ5��֪����200~250 ��֮�䣬������Ǧ����ʧ��ѭѸ��������250 ���������Ǧ����ʧ����������ƽ����������350 �����ʧ���������ٱ仯����Ҫԭ����250 ��֮ǰ��������Ǧ�����ķ�Ӧ����ˮ�Լ�������Ǧ���ȷֽ⣬���������������ʧ����Ҫԭ���ǽᾧˮ�Լ�������Ǧ�ֽ�Ϊ�л������Լ�������̼�������ʧ���������ӡ���Ӧ������Ҫ��ʣ��̼��ȼ�գ���ˣ���Ӧ����������ʧ�仯����
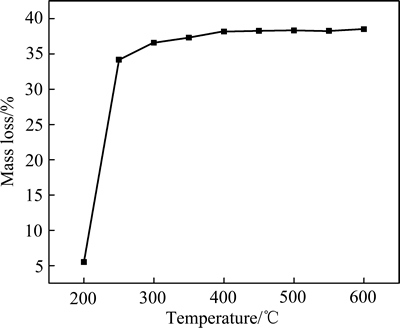
ͼ5 ��ͬ�¶���������Ǧ��������ʧ����
Fig. 5 Mass loss curves of lead citrate at different temperatures
2.3.2 ��ͬ�¶��µı��ղ���XRD��
��ͬ�����¶��Լ���ͬ����ʱ����������Ʊ��õ�Ǧ����Ʒ��XRD����ͼ6��ʾ����ͼ6(a)��֪������仯�뱺���¶�������ء���300~350 ��ʱ�����ղ��������-PbO����-PbO�����Ǧ�����ű����¶ȵ����ߣ�����Ǧ�ĺ�����ͣ�����-PbO�ĺ��������࣬500 ���º���1 h�IJ����Ѿ���ȫ�Ǧ�-PbO����������[17]�б���һ�¡������Ϸ�����֪�����¶����ߣ���������������Pb������С�������¶ȿɿ���Pb�������̶ȼ�PbO����ɡ�

ͼ6 ��ͬ�����¶Ȳ�ͬ����ʱ���²����XRD��
Fig. 6 XRD patterns of combustion-synthesis products at different temperatures and different time
���Ʊ���ʱ��Ϊ3 h�Բ�ͬ�¶��±��յ�������Ǧ��Ʒ����XRD������ʵ������ͼ6(b)����ͼ6(b)��֪����ͬ�����¶��µ���Ʒ�������нϴ�IJ��졣�����¶���300~350 ��ʱ�����������-PbO����-PbO�����Ǧ�����ű����¶ȵ����ߣ���-PbO���-PbOת������500 ���¶��º���3 h����Ʒ��ȫת��Ϊ��-PbO������1 h�IJ��������3 h�IJ������ƣ�������3 h�IJ���ȱ���1 hʱ�IJ����Ц�-PbO���ࡣ������ǦPb3(C6H5O7)2��3H2O��ͬ�����¶��º���6 h����Ʒ����XRD������ʵ������ͼ6(c)����ͼ6(c)��֪��XRD��������뱺��3 h��Ǧ�۽������û�в��죬û�г���Pb3O4������֮ǰ���о����[9]��ͬ���������������Ǧ�ֽ��������ṩ����Pb��ϵ���ԭ�������IJ����йء�
2.3.3 ��ͬ�¶��±��ղ����SEM�����
������ǦPb3(C6H5O7)2.3H2O��ͬ���¶��±��յ�Ǧ�۵�SEM���ͼ7����ͼ7��֪�������¶�Ϊ300 ��ʱ��������ƽ����״ת��Ϊ�����״�����������������ӣ����DZ��չ��������������ɵģ���350 ��ʱ�������״���ʸ����ԣ�450 ��ʱ�������г����˴�������״���ʣ�����ԼΪ20 mm��
������ǦPb3(C6H5O7)2��3H2O��350 ���º��²�ͬʱ��õ����ղ����ͼ8����ͼ8�ɿ��������ű���ʱ����ӳ����ž�״̬��ǿ�������״�ṹ�������ο���ת�������������������������״�ṹ�������ο���ת���Ļ��ƿ������ڷ�Ӧ���̷ų����������壬�γ���״��ṹ��ͬʱ�������¶����ߺ����ο������ӣ�˵���ž�������ǿ����������дٽ�����״�ṹ�������ž۽ṹ��ת������ˣ��ɳ����ж�������ǦPb3(C6H5O7)2��3H2O ��350 ���º���1 h�Ǻ��ʵ��Ʊ�Ǧ�۵ı���������
2.4 ������Ǧ�ȷֽ�Ļ���

ͼ7 ��ͬ�����¶ȱ���1 h�Ʊ�Ǧ�۵�SEM��
Fig. 7 SEM images of combustion-synthesis products at different temperatures for 1 h
����������Ǧ����ʽΪPb3(C6H5O7)2��3H2O�����ֻ��Ǧ������̼3��Ԫ�أ���ˣ����յ��ȷֽ����ֻ���ܰ���Ǧ������̼3��Ԫ�ء����ȷֽⷽ��ʽ�����������ڿ������ڹ�����Ӧ��״̬��������ǦPb3(C6H5O7)2��3H2O������ȫ����̬����ΪPbO������ʽ��ʽ(1)��ʾ��
Pb3(C6H5O7)2��3H2O+9O2��3PbO+12CO2+8H2O (1)
�ڴ�����¹������ΪPbO��������ǦPb3(C6H5O7)2.3H2O������ʧ��Ϊ36.4%��
����������Ӧ���㣬�ֽ��̬�����Խ���PbΪ�����䷽��ʽ��ʽ(2)��ʾ��
Pb3(C6H5O7)2��3H2O+7.5O2��3PbO+12CO2+8H2O (2)
�ڴ�����£���̬����ΪPb��Pb3(C6H5O7)2.3H2O��������ʧ�ﵽ41.0%��
�����������ּ�����������ۼ��㣬��ʵ�ʹ����У�����������������Ҫ�ģ������ڷ�Ӧ�����л��в���̼����Ҫ�������ڱ�֤̼�ij��ȼ�գ��Է�ֹ�������㣬̼��PbO��ԭΪ����Ǧ������PbO��Ǧ��Ħ���ȡ����ܻᷢ����Ҫ��Ӧ������ʽ(3)~(5)��
C+O2��CO2 (3)
2Pb+O2��2��-PbO (4)
2��-PbO+C��2Pb+CO2 (5)
Pb3(C6H5O7)2.3H2Oǰ�����ڿ������ȷֽⷽ��ʽ�ɱ�ʾΪʽ(6)��ʽ��x��yֵ�ֱ�������ղ�����PbO��Pb�ĺ�����������ͨ���ı䱺������(�����¶ȡ�����ʱ��)��ʵ�ֲ�ֵͬ��
 ��
�� (6)
(6)
��ʵ��������������ʧ�ȶ���38.0%��������ΪPbO��Ǧ����˲������Ҫ���֡�EDS������ʾ��350 �決��1 h�����Ԫ�����ֻ��Ǧ��������ˣ�������Ϊ���ﻯѧ�ɷ�ΪPbO��Ǧ��������������֪��������Ǧ���ȷֽ������Ҫ����200 ���ڵĽᾧˮɢʧ��200~450 ����������Ǧ�ֽ����CO2��CO�Ȳ��450 �����ϵ�����ȼ�����ղ���ΪǦ������Ǧ��

ͼ8 ��350 �決�ղ�ͬʱ���ϸ�۵�SEM��
Fig. 8 SEM images of combustion products of precursor at 350 ��
3 ����
1) ������Ǧ�ڿ��������е��ȷֽ��������ˮ����ˮ���ȷֽ⼰̿�������Ρ�������Ǧ��ʼ�ȷֽ��Ϊ�ᾧˮɢʧ����100~200 �淶Χ�ڣ������л������������˺���Ҫ����Ϊ������̼��
2) ������Ǧ��ʧ�����¶����߶���350 ������ʱ��������Ǧ��ʧ���ȶ��������ֽ���ȫ�����ȷֽ�����Ǧ�-PbO����-PbO��Ǧ�������¶����ߣ�Ǧ����ΪPbO����-PbO���-PbOת����500 ���¶��º���1 h������ȫת��Ϊ��-PbO��
3) �決���¶�����뱺��ʱ���ӳ������ղ��ᄃ�����-PbOת������װ�״�ṹ�������ת���������˱����¶�Ϊ350 �棬����ʱ��Ϊ1 h��
REFERENCES
[1] FERRACIN L C,  A E, DAYOGLIO R A, ROCHA L O, CAFFEU D J, FONTANETTI A R, ROCHA-FILHO R C, BIAGGIO S R, BOCCHI N. Lead recovery from a typical Brazilian sludge of exhausted lead-acid batteries using an electrohydrometallurgical process[J]. Hydrometallurgy, 2002, 65(2/3): 137-144.
A E, DAYOGLIO R A, ROCHA L O, CAFFEU D J, FONTANETTI A R, ROCHA-FILHO R C, BIAGGIO S R, BOCCHI N. Lead recovery from a typical Brazilian sludge of exhausted lead-acid batteries using an electrohydrometallurgical process[J]. Hydrometallurgy, 2002, 65(2/3): 137-144.
[2] VAYSGANT Z, MORACHEYSKY A, DEMIDOY A. A low-temperature technique for recycling lead-acid battery scrap without wastes and with improved environmental control[J]. Journal of Power Sources, 1995, 53(2): 303-306.
[3] COLE J, ERNEST R, LEE A Y. Update on recovering lead from scrap batteries[J]. Journal of Metals, 1985, 37(2): 79-83.
[4] YANG J K, ZHU X F, KUMAR R V. Ethylene glycol-mediated synthesis of PbO nanocrystal from PbSO4: A major component of lead paste in spent lead acid battery[J]. Materials Chemistry and Physics, 2011, 131(1/2): 336-342.
[5] ZHU X F, LI L, SUN X J, YANG D N, GAO L X, LIU J W, KUMAR R V, YANG J K. Preparation of basic leady oxide from spent lead acid battery paste via chemical conversion[J]. Hydrometallurgy, 2012, 117/118: 24-31.
[6] LI L, ZHU X F, YANG D N, GAO L X, LIU J W, KUMAR R V, YANG J K. Preparation and characterization of nano-structured lead oxide from spent lead acid battery paste[J]. Journal of Hazardous Materials, 2012, 203/204(4): 274-282.
[7] LIU J W, YANG D N, GAO L X, ZHU X F, LI L, YANG J K . Effect of iron doped lead oxide on the performance of lead acid batteries[J]. Journal of Power Sources, 2011, 196(20): 8802-8808.
[8] ���·�, ��ҿ�, ���, ������, ��һ��, ������. �ӷ�Ǧ���Ʊ���ϸ̼��Ǧ�ı������ȷֽ������о�[J]. ���ܲ���, 2012, 43(27): 2343-2347.
ZHU Xin-feng, YANG Jia-kuan, YANG Dan-ni, SUN Xiao-juan, GUO Yi-fei, CHEN Song-tao. Study on preparation and thermal decomposition of ultra-fine carbonated lead powder[J]. Journal of Functional Materials, 2012, 43(27): 2343-2347.
[9] ���·�, ��ҿ�, ���곽, �� ��, �� ��, �� ΰ, ������, ��һ��, ������. ������ǦPb(C6H6O7)��H2O�ȷֽ������о�[J]. �����ȴ���ѧ��, 2014, 35(6): 10-14.
ZHU Xin-feng, YANG Jia-kuan, HU Yu-chen, LI Lei,WANG Xiao, ZHANG Wei, SUN Xiao-juan, GUO Yi-fei, CHEN Song-tao. Study on behavior of thermal decomposition of lead citrate[J]. Transactions of Materials and Heat Treatment, 2014, 35(6): 10-14.
[10] ���·�, ����, ���, �� ��, ��ҿ�. �Է�Ǧ����Ǧ���Ʊ���ϸ����Ǧ��ĩ[J]. �й���ɫ����ѧ��, 2010, 20(1): 132-136.
ZHU Xin-feng, LIU Wan-chao, YANG Hai-yu, LI Lei, YANG Jia-kuan. Preparation of ultra-fine PbO powders from lead paste in spent lead acid battery[J]. The Chinese Journal of Nonferrous Metals, 2010, 20(1): 132-136.
[11] ZHU X F, YANG J K, HE X, LI L, GAO L X, YANG D N, SUN X J, ZHANG W, WANG Q, LIU J W, KUMAR R V. Leaching of spent lead acid battery paste components by sodium citrate and acetic acid[J]. Journal of Hazardous Materials, 2013, 250/251(8): 387-396.
[12] KOURGIANTAKIS M, RAPTOPOULOU C P, MATAZPETAKIS M. Lead-citrate chemistry. synthesis, spectroscopic and structural[J]. Inorganica Chimica Acta, 2000, 297(1/2): 134-138.
[13] ʯ ��, �����, �� Ƽ. [Pb6(H2O)2(cit)4]��3H2O��Pb(tar)- (H2O)2�����������Ǧ����λ�ۺ����ˮ�Ⱥϳ������[J]. �ߵ�ѧУ��ѧѧ��, 2007, 28(9): 1617-1621.
SHI Jing, XU Jia-ning, ZHANG Ping. Hydrothermal synthesis and characterization of two coordination polymers of flexible acid and lead: [Pb6(H2O)2(cit)4]��3H2O and Pb(tar)(H2O)2[J]. Chemical Research in Chinese Universities, 2007, 28(9): 1617-1621.
[14] SONMEZ M S, KUMAR R V. Leaching of waste battery paste components. Part 2: Leaching and desulphurisation of PbSO4 by citric acid and sodium citrate solution[J]. Hydrometallurgy, 2009, 95(1): 82-86.
[15] BASSILAKIS R, CARANGELO R M, WOJTOWICZ M A. TG-FTIR analysis of biomass pyrolysis[J]. Fuel, 2001, 80 (12): 1765-1786.
[16] JONG W D, PIRONE A,  M A. Pyrolysis of miscanthus giganteus and wood pellets: TG-FTIR analysis and reaction kinetics[J]. Fuel, 2003, 82(9): 1139-1147.
M A. Pyrolysis of miscanthus giganteus and wood pellets: TG-FTIR analysis and reaction kinetics[J]. Fuel, 2003, 82(9): 1139-1147.
[17] MUNSON M J, RIMAN R E. Observed phase transformations of oxalate-derived lead monoxide powder[J]. Journal of Thermal Analysis, 1991, 37(37): 2555-2566.
Thermal decomposition of lead citrate Pb3(C6H5O7)2��3H2O from recovery spent lead paste by hydrometallurgy process
ZHU Xin-feng1, WANG Xian-li1, NIE Peng-ru2��ZHANG Wei2, HU Yu-chen2, YANG Jia-kuan2, WANG Xiao1, GUO Yi-fei1
(1. College of Municipal and Environmental Engineering, Henan University of Urban Construction, Pingdingshan 467036, China;
2. College of Environmental Science and Engineering, Huazhong University of Science and Technology, Wuhan 430074, China)
Abstract: Thermal decomposition behavior and product were systematically investigated by TG-FTIR, XRD, SEM analysis. The results show that the thermal decomposition process of lead citrate is divided into dewatering, organic constituent decomposition and burning stages. The dehydrating crystal water occurs in the initial decomposition followed by the generation of intermediate organic matters at 100-200 ��. Subsequently, the ultimate gas and solid products from this decomposition process are CO2 and a mixture mainly containing PbO and Pb, respectively. The major products of Pb3(C6H5O7)2��3H2O at relatively low temperature are ��-PbO, ��-PbO and Pb, whereas, ��-PbO is the dominant product at relatively higher temperature.
Key words: lead citrate; thermal decomposition; mechanism; lead paste
Foundation item: Project(50804017) supported by the National Natural Science Foundation of China; Project (152102210299) supported by Science and Technology Project of Henan Province Science and Technology Department, China; Project(15A610002) supported by the Key Scientific Research Project of Colleges and Universities in Henan Province, China
Received date: 2015-08-11; Accepted date: 2016-07-28
Corresponding author: YANG Jia-kuan; Tel: +86-27-87792207; E-mail: yjkuan@126.com
(�༭ ����)
������Ŀ��������Ȼ��ѧ����������Ŀ(50804017)������ʡ�Ƽ�������Ŀ(152102210299)������ʡ��У�ص������Ŀ(15A610002)
�ո����ڣ�2015-08-11�������ڣ�2016-07-28
ͨ�����ߣ���ҿ������ڣ���ʿ���绰��027-87792207��E-mail: yjkuan@126.com


