���±�ţ�1004-0609(2014)05-1285-08
þ�Ͻ�������þ��Ĥ�γɻ��Ƽ������︯ʴ����
������1��������1���� ǿ2����־��1��������1
(1. �Ͼ�����ѧԺ ���Ϲ���ѧԺ���Ͼ�211167��
2. ���տ���ҽ����е����˾��������212300)
ժҪ�����ý��ݷ���Mg-Nd-Zn-Zrþ�Ͻ�����Ʊ�����þ��Ĥ�����õ�η����绯ѧ���ͽ��ݷ�����þ�Ͻ����ͷ���þ��Ĥ����ʴ�ԣ�����ɨ��羵(SEM)��������(EDS)��������þ��Ĥ������ʴǰ�����ò���ɷ֡�������������ת�������¶ȿ�������С����þ�ƿ����ߴ磬��ת������ʱ��Կ����ߴ�Ӱ���С������þ�ƿ���ͨ����ά�κ˺��̨���������ƺ������������Ƴ�����þ��Ĥ����������Mg-Nd-Zn-Zrþ�Ͻ���ģ����Һ�е�ƽ���������ʣ���ģ����Һ�У�����þ��Ĥ��ת��Ϊ������������λ��Ĥ�㣬��Ĥ���������þ�Ͻ��������á�
�ؼ��ʣ�
þ�Ͻ���NaMgF3Ĥ��ģ����Һ��������������ʴ������
��ͼ����ţ�TG146��R318.08���� ���ױ�־�룺A
Formation mechanism and bio-corrosion properties of NaMgF3 film on surface of magnesium alloy
FANG Xin-xian1, ZHANG Xiao-bo1, WANG Qiang2, BA Zhi-xin1, WANG Zhang-zhong
(1. School of Material Engineering, Nanjing Institute of Technology, Nanjing 211167, China;
2. Jiangsu Konsung Equipment Co., Ltd., Danyang 212300, China)
Abstract: The NaMgF3 films on the surface of Mg-Nd-Zn-Zr magnesium alloy were fabricated by immersion method. Their corrosion properties were valuated by dripping test, electrochemical test and immersion method, respectively. The microstructures of the original and corrosive samples were observed by SEM and their chemical compositions were analyzed by EDS. The results show that the size of NaMgF3 particle is obviously reduced with the increase of conversion treatment temperature; however, it is little affected by the conversion treatment time. The NaMgF3 particles grow by two-dimensional nucleation, step growth mechanism and screw growth mechanism. The average hydrogen evolution rate of Mg-Nd-Zn-Zr magnesium alloy in simulated body fluid (SBF) solution can be significantly decreased by NaMgF3 film. The NaMgF3 films gradually transform into a new film consisting of fluoride and phosphate in the SBF solution, which will continue to protect the magnesium alloy from the corrosion.
Key words: NaMgF3 film; SBF; magnesium alloy; hydrogen evolution rate; corrosion mechanism
����þ�Ͻ���пɽ��⡢�ܶ�������ǵĽӽ�������ģ��������ǿ�Ƚӽ�����ǡ�����Ч���͡�Ӧ���ڵ�ЧӦ�����ص�[1]�����ҽ����γɵ�þ������������賣��Ԫ��֮һ[2]�����˹��ؽڡ��������ϡ��˹����ݡ������������˹��ڶ��缫����Ѫ��֧�ܵ�[1-4]ҽ������������ھ��Ӧ��ǰ����
þ�Ͻ������ڽ����ٶȿ죬������ʵ�ʷ�������������������ƥ�䣬��Լ������ҽ�������Ӧ�á�����Ͻ�[5]�ͱ������[6-15]�����þ�Ͻ���ʴ�Ե�������Ҫ;�����о���������þ�Ͻ�����Ʊ���������þĤ[6]��������Ĥ[7]������Ϳ��[8-9]��PLGA�߷���Ĥ[10]������þ���临��Ĥ [11-15]�Ƚ��б�����ԣ��������Խ���þ�Ͻ�����オ���ٶȡ�
�����ε�[14]���о�����������þĤ�������н���þ�Ͻ����オ���ٶȵ����ã����ҷ���þĤ�еķ����дٽ�ֲ�������Χ�����ɵ����á���ͳ�����Ʊ�����þĤ�����ø�Ũ�ȵ��������Һ����ת��������Ϊ��ýϺ�ķ���þת��Ĥ���乤��ʱ��dz���������粵�[11]�������ε�[14]�Ʊ�����þĤ��ת����������ʱ��ֱ�ﵽ48��72 h�������ơ�þ��������賣��Ԫ��[2]�������дٽ�����������[14]��Ϊ�ˣ����������о��������ת������ʱ��϶̵�һ�����ͷ���þ��ת��Ĥ������þ�Ͻ����オ�����ܵĹ��룬�봫ͳ����þת��Ĥ�Ʊ�������ȣ���ת��Ĥ�Ĵ���ʱ���Ϊ0.5 h���ҡ������������ͷ���þ��ת��Ĥ���Ʊ���������ʴ�Լ����オ����Ϊ��δ�����ױ�������ˣ��������߶Է���þ��Ĥ�Ʊ����ա��γɻ��ơ���ʴ�Ա�����������ģ����Һ�еĽ�����Ϊ�Ƚ����о���
1 ʵ��
1.1 ת��Ĥ���Ʊ�
�������иֱ��Ϊ20 mm��Mg-Nd-Zn-Zr��ѹ���и�ɺ��Ϊ4 mm��ԲƬ��Ϊ����ʵ��ʱ�������ң���̨����������Ե��ֱ��Ϊ2 mm��Բ�ף�Ȼ����ɰֽ��ĥ���⣬�õ�ԭʼþ�Ͻ����������
��þ�Ͻ�����������Գ��ͺ�ˮϴ�ֱ�����¶�Ϊ80��90 ���ת������Һ1(40 g/L NaF+50 mL/L HF)�зֱ�ת������10��20��30��60 min���Լ�90 ���ת������Һ2(40 g/L NaF+300 mL/L HF)��ת������30 min��ת����������������ȡ�����Ⱥ���ˮ�;ƾ���ϴ���������ɣ��õ����渲�Ƿ���þ��ת��Ĥ��þ�Ͻ�������
1.2 ת��Ĥ����ʴ��ʵ��
�ֱ���õ�η��ⶨ��ɫʱ�䡢�绯ѧ��������ʴ��λ��ʴ�����ܶȣ����ݷ�(���ⸯʴ)����ƽ����������������þ�Ͻ����ͷ���þ��ת��Ĥ����ʴ�ԡ�
��η�����QJ/Z134-85�����У����Һ��30 mL��65%HNO3��0.5 g KMnO4��950 mL��ȥ����ˮ���ƶ��ɣ���ɫʱ��Խ������������ʴ��Խ�á�
��PARSTAT2273�绯ѧ����վ����þ�Ͻ����ͷ���þ��Ĥ�����Ķ���λ�������ߡ����ñ����缫ϵͳ���αȵ缫Ϊ���ʹ��缫�������缫Ϊ���缫�������缫Ϊ��Ʒ���������������缫ʱ�������Ĺ�����ߴ�Ϊ10 mm��10 mm�����������������û�����֬�̷⡣
�绯ѧ�������ý���Ϊģ����Һ(SBF)����ɷ����1���У��¶�Ϊ(37��1) �棬��HH-Sˮԡ�����ȱ��¡�
��1 ģ����Һ(SBF)�ijɷ�
Table 1 Composition of SBF solution (g/L)
���ݷ�������������ʵ��װ��ԭ����ͼ1��ʾ��ģ����Һ��������������֮��Ϊ30 mL/cm2��ÿ����24 h����һ��ģ����Һ������¼�����������������5 d��ȡ���������ֱ���ȥ����ˮ�;ƾ���ϴ�����ɡ����ݸ�ʴʵ����ƽ����������v�ļ��㹫ʽΪ
v=V/(St)
ʽ�У�VΪ�����������mL��SΪ�����������cm2��tΪ����ʱ�䣬d��
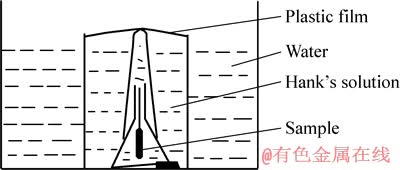
ͼ1 ����������ԭ��ͼ
Fig. 1 Principle diagram of hydrogen evaluation test

ͼ2 ��ͬת�������Ʊ���NaMgF3ת��Ĥ��SEM����XRD��
Fig. 2 SEM images ((a), (b), (c), (d)) of NaMgF3 films and XRD pattern (e) under different conversion treatment conditions
1.3 ת��Ĥ����֯���ɷַ���
��JSM-6360LV��ɨ���������(SEM)�Խ��ݸ�ʴǰ������������֯��ò���й۲죬��GENESLS2000XMS60������(EDS)������������ɷ֣�����NaMgF3ת��Ĥ�ĵ����Խϲ����ת�����������ڸ߱��۲�ǰ���б������������Ultma����X����������(XRD)�ͱ�ĤXRD���Լ�����ת��Ĥ�������������
2 ��������
2.1 ת���������ն�NaMgF3ת��Ĥ��֯��Ӱ��
��ת������Һ1���¶�Ϊ80 ��ʱ���ֱ�ת������10��20��30 min�õ���ת��Ĥ���ɱ߳�ԼΪ2 ��m�ĵ���״������������(��ͼ2(a)~(c))������ת������ʱ���ӳ���ת��Ĥ�еĺ�ɫ��϶(��ͼ2(a)��ͷA)�ߴ��С���������٣�ת��Ĥ��ø��Ӿ������ܡ�
��ת������Һ1���¶�Ϊ90 ��ʱ��ת������30 min�õ���ת��Ĥ��Ҳ�ɵ���״�����������ɣ�������������ߴ�����ϸ������߳�ԼΪ0.5 ��m(��ͼ2(d))���ҿ�����Ľ���Ҳ��ñȽ�ģ������80 ��ת������30 min��ת��Ĥ��ȣ�ת��Ĥ�����ܶ�������ߡ�XRD����������80 ��ת������������ת��ĤΪ����þ��(NaMgF3)ת��Ĥ(��ͼ2(e))��������������80��90 ��ת������30 min�Ʊ���ת��Ĥ����F��Mg��NaԪ����ɣ���80 ��ת������������F��Na��MgԪ�ص�Ħ�������ֱ�Ϊ32.66%��11.68%��56.66%����90 ��ת������������F��Na��MgԪ�ص�Ħ��������ֱ�Ϊ5.75%��1.51%��92.74%������������ʱ��������ת��Ĥ��90 ��ת������Ĥ�ϱ�����ˣ��������������Ϣ����������Mg��
�����������Mg�ĺ����ɼ���90 ��ת����������������������а����������Ի������Ϣ��
2.2 NaMgF3ת��Ĥ���γɻ���
þ�Ͻ����NaMgF3ת��Ĥ�γɹ��̴��¿ɷֳ����¼����Σ�1) ��þ�Ͻ���������ת��Һʱ���������������Ĥ������ת��Һ�е�H+����������Ӧ�ܽ⣺MgO+2H+��Mg2++H2O������þĤ�ܽ����¶����þ�Ͻ���彫��ת��Һֱ�ӽӴ�����ʱ����λ�ϸ���þ����ת��Һ�е�H+�ڽ����Ϸ���������Ӧ��Mg+2H+��Mg2++H2��������ת������ʱ�۲쵽�������������滺���ݳ���ʵ����һ�£�2) �ڽ������ڣ�������Ӧ������Mg2+��������ڵ�F-��Na+����������Ӧ��Na++Mg2++3F-��NaMgF3������Ӧ�γɵ�NaMgF3�������������棬�γ�NaMgF3���ģ���������Mg2+Ũ��Խ�ߣ�NaMgF3�κ���Խ��3) ��þ�Ͻ�����γ�NaMgF3���ĺ�����ת������ʱ���ӳ���NaMgF3���Ľ����ϳ���NaMgF3ת��Ĥ��֯�߱��۲��������NaMgF3����������ڶ�ά�κ˻���(��ͼ3(a)��ͷC)����ά�κ˺��̨����������(��ͼ3(b) �м�ͷD)��������������(��ͼ3(a)�м�ͷE)������NaMgF3�����κ�ʱ�估�����������죬NaMgF3�����ߴ�Ҳ������ͬ����ߴ�ϴ��NaMgF3������϶�г��ɼ����ߴ����Խ�С��NaMgF3����(��ͼ2(a)��ͷB)��4) ����ת������ʱ���ӳ���һ���棬���γɵ�NaMgF3���������ϳ�����һ���棬��NaMgF3������϶�л��������µ�NaMgF3���ĵ��γɼ�����NaMgF3��������������ʱ������þ�Ͻ����������γ�һ����NaMgF3ת��Ĥ��5) NaMgF3ת��Ĥ�����ܶ�����ת������ʱ����ӳ���������(��ͼ2(a)~(c))��������NaMgF3ת��Ĥ���ܶ�����ת��Һ��þ�Ͻ��������ĽӴ����Խ��ԽС��NaMgF3�����κ˺����������Mg2+�������ʱ��Խ��ԽС����ˣ���ת������ʱ��ﵽijһֵ��һ���ӳ�ת������ʱ�䣬ת��Ĥ���ܶȺ�ת��Ĥ��ȵ��������ʽ����½���

ͼ3 NaMgF3ת��Ĥ�ĸ߱�SEM��
Fig. 3 High magnification SEM images of NaMgF3 films
NaMgF3ת��Ĥ����������е�Na��Fȫ������ת��Ĥ��һ����Mg����ת��Ĥ��һ���������Ի��壬����Na��FĦ����Ϊ1:1��ʣ��F��Mg��Ħ����Ϊ2:1���۳�����þ��Ϣ��ļ��������þ�Ͻ���80 ���ת������Һ1��ת������30 min�õ���NaMgF3ת��Ĥ��Mg��Na��Ħ����Ϊ0.89:1������90 ���ת������Һ1��ת������30 min�õ���NaMgF3ת��Ĥ��Mg��Na��Ħ������Ϊ1.40:1������ת�������γɵ�Ĥ����Na��Mg��Ħ���������κ˺����������н�������Mg2+���������йء����ݻ�ѧ��Ӧ����ѧ���ۣ���ѧ��ӦMg+2H+��Mg2++H2���ķ�Ӧ�������ŷ�Ӧ�¶ȵ����߰�ָ������������90 ��ת������Һ1�Ľ�������Mg2+����������������80 ��ת������Һ1�Ľ������ڵ�Mg2+�������ʣ�����90 ��ת�������õ���NaMgF3������Mg��Na��Ħ����������������Mg2+�������ʽ�һ������ʱ��NaMgF3ת��Ĥ�������þת��Ĥת�䡣Ϊ��֤������������þ�Ͻ���������90 ���ת������Һ2��ת������30 min��ת��Ĥ����֯�۲������ת��Ĥ�ɻ�ɫĤ���ϽϾ��ȷֲ��İ�ɫ������������(��ͼ4(a)~(b))����������������ɫ������Na��Mg��FԪ����ɣ�����ɫ����ΪNaMgF3���壬NaMgF3������Mg��Na��Ħ����Ϊ1.04:1����ɫĤ���в���Na����ˣ���ɫĤΪMgF2����Ĥ(��ͼ4(c)~(d))����ʵ�����������������һ�¡�
����NaMgF3ת��Ĥ�γɻ��ƣ�ת������Һ�̶�ʱ��ת��Ĥ��NaMgF3������ƽ���ߴ���Ҫȡ����ת�������¶ȣ����ת�������¶�ʹNaMgF3����ƽ���ߴ��С����Ϊ���ת�������¶Ȳ���ʹ��������Mg2+Ũ�������һ����ٻ�ѧ��ӦNa++Mg2++3F-�� NaMgF3���Ľ��У�NaMgF3�κ�������ʹ���˺��������ռ��С������NaMgF3����ƽ���ߴ��С��ת������ʱ���NaMgF3�����ߴ�Ӱ���С����Ϊת��Һ��ת�������¶�һ��ʱ��NaMgF3�κ��ʺ;��˺��������ռ�һ�����ӳ�ת������ʱ����������ת��Ĥ���ܶȣ���Ϊ���γɵ�NaMgF3������ϳ��������ڿ�϶�л����γ��µ�NaMgF3��������������������ͼ2��ʵ����һ�¡�
����NaMgF3ת��Ĥ�γɻ��ƣ�þ�Ͻ����NaMgF3ת��Ĥ�����ת�������¶Ⱥ�ת������Һ�е�HFŨ���йء�һ���棬ת�������¶Ⱥ�HFŨ��Խ�ߣ���������Mg2+Ũ��Խ��NaMgF3�κ���Խ���ļ��ԽС��NaMgF3������������������ʱ��Խ�̣���һ���棬ת�������¶Ⱥͽ�������Mg2+Ũ��Խ�ߣ�Na++Mg2++3F-��NaMgF3����Ӧ�ٶ�Խ�죬NaMgF3������������Խ�죬��һ��NaMgF3��������������ʱ�����þ�Ͻ�����ת������Һ��ĸ������õ���NaMgF3Ĥ������������Mg2+�����ܵ����ƣ�������ߵ�ת�������¶Ⱥ�HFŨ�Ȳ����ڻ�ýϺ��NaMgF3ת��Ĥ��ת������Һ��ת������ʱ����ͬʱ��90 ��ת��������������ת��Ĥ�ĺ�ȵ���80 ��ת�����������ġ�����������þ�Ͻ�������90 ���ת������Һ1��2��ת������30 min����������������þ����������80 ���ת������Һ1��ת������30 min�Ľ��һ�£���Ϊת��Ĥ�ܱ���������ʱ��ĤԽ��������ϢԽ�࣬þ����Խ�ߡ�
2.3 ת���������ն���ʴ�Ե�Ӱ��
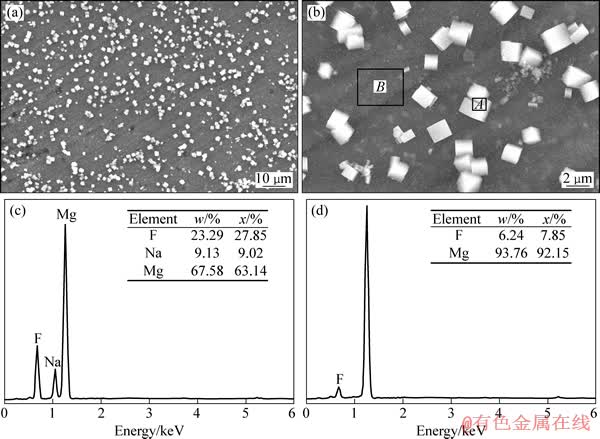
ͼ4 NaMgF3ת��Ĥ��ò��EDS����ͼ
Fig. 4 SEM images of NaMgF3 conversion films ((a), (b)) and EDS patterns of white particle A (c) and dark zone B (d) shown in Fig. 4(b)
ͼ5��ʾΪ��ͬת�������¶�ʱת������ʱ��Ա�ɫʱ���Ӱ�졣��ͼ5�ɼ���ת�������¶�һ��ʱ����ɫʱ������ת������ʱ���ӳ�������ת�������¶ȶԱ�ɫʱ��Ҳ��Ӱ�죬��ת������ʱ��϶�ʱ��90 ��ת��������ת��Ĥ��ɫʱ�����80 ��ת������ʱ�ģ�����ת������ʱ�����ijһֵ��80 ��ת������ת��Ĥ�ı�ɫʱ�䷴������90 ��ת������ʱ�ġ�

ͼ5 ��ͬת�������¶�ʱת������ʱ��Ա�ɫʱ���Ӱ��
Fig. 5 Effect of conversion time on color change time at different conversion temperatures
���ζ�Һ������������ʱ��һ���棬�ζ�Һ��ֱ�Ӵ�ת��Ĥ�п�϶����������Ӵ���������������þ����������ԭ��Ӧʹ�ζ�Һ��ɫ����ˣ�ת��Ĥ���ܶ�Խ�ͣ���ɫʱ��Խ�̣���һ���棬ת��Ĥ��ϡ������Һ���Dz��ȶ��ģ�ת��ĤԽ����ת��Ĥ�ܽ�����ʱ��Խ�̣���ɫʱ��ҲԽ�̣���ˣ���ɫʱ����ת��Ĥ���ܶȺͺ�ȵ��ۺϷ�ӳ����ת������ʱ��϶�ʱ������90 ��ת�������κ��ʸ��������ʿ죬�����ܶȽ�80 ��ת������ʱ�ĸߣ�������ɫʱ���80 ��ת�������ij�������ת������ʱ��ϳ�ʱ��ת��Ĥ�����ܶȾ��ϸߣ���ʱת��Ĥ����Ǿ�����ɫʱ��Ŀ������أ�����80 ��ת��������ת��Ĥ��90 ��ת������ʱ�ĺ�������ɫʱ��Ҫ��90 ��ת������ʱ�ij���
ͼ6��ʾΪþ�Ͻ�������80 ���ת������Һ1��ת������30 minþ�Ͻ������Ķ�̬�������ߣ�ת�������������Ը�ʴ��λԼΪ-1.42 V����þ�Ͻ������Ը�ʴ��λ-1.53 V������110 mV���ң�ת�������������Ը�ʴ�����ܶ�Ϊ3.504��10-5 A/cm2����Ϊþ�Ͻ�����Ը�ʴ�����ܶ�7.518��10-5 A/cm2��46.6%���ɼ���ת�����������Ը���þ�Ͻ����ʴ�ԡ�
2.4 SBFҺ���������ʼ���ʴ����
ͼ7��ʾΪþ�Ͻ�����ת������������SBF�е�ƽ���������������ʱ��Ĺ�ϵ���ߡ���ͼ7�ɼ���þ�Ͻ�����ת������������ƽ�������������Ž���ʱ���ӳ����ֳ���ͬ�ı仯���ƣ�����δת��������þ�Ͻ�������������Ž���ʱ����ӳ���ƽ���������ʳ��ֵ����½����������ȶ��������ȣ�ת�����������ڽ��ݳ������Ž���ʱ���ӳ���ƽ�������������½������ڽ��ݴ�Լ3 d��һ���ӳ�����ʱ�䣬ƽ���������ʿ�ʼ��������ͼ���ɼ���ת������������ƽ������������ת�����������йأ�ת������ʱ��һ��ʱ��80 ��ת������������ƽ�������������Ե���90 ��ת�����������ģ�ת�������¶�һ��ʱ���ӳ�ת������ʱ��ɽ���ƽ���������ʡ�
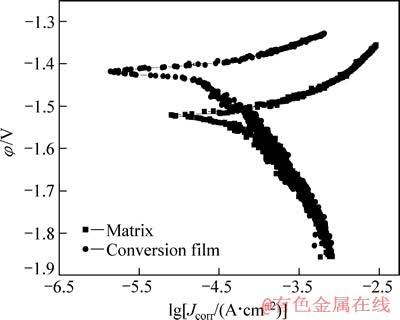
ͼ6 þ�Ͻ��ת��Ĥ�Ķ���λ��������
Fig. 6 Potentiodynamic polarization curves of magnesium alloy and conversion film

ͼ7 þ�Ͻ���ת��Ĥ��SBF�н�����������
Fig. 7 Hydrogen evolution curves of magnesium alloy and conversion film soaked in SBF
��SBF�н�������������ò�۲������δת������þ�Ͻ������ͱ��±�����ò�ɰ��ݵ�ƽ̹������Ĵֲ������������(��ͼ8(a)�м�ͷF��G��ָ)���߱���һ���۲�ɼ���ƽ̹���ʹֲ��������ָɿݺӴ��ġ�����͡���״��֯������������͡���ijߴ�͡�����͡���֮��ķ�϶�Ͽ�(��ͼ8(b)��(c))����3��������͡��齻�紦���ɼ����ߴ�ϴ�Ŀ�����(��ͼ8�м�ͷH��I��ʾ)���ֲ�����ʴ������Ƚ�ƽ̹���������ȣ�ת�����������ͱ��±���Ƚ�ƽ̹(��ͼ8(d))���߱����������ò��Ҳ���С�����͡���״��֯��������������͡���ijߴ��Ϊδת������þ�Ͻ��������ķ�֮һ���ң��ҡ�����͡���֮��ķ�϶����Ҳ����С��δת������������(��ͼ8(e)��(f))����3��������͡��齻�紦Ҳδ������δת������þ�Ͻ�������������ֿ�����ͬ�¶�ת��������þ�Ͻ���������ת������ʱ���Ϊ30 minʱ��80 ��ת�����������ġ�����͡���ߴ缰������͡���֮��ķ�϶������С��90 ��ת������þ�Ͻ������ġ��Խ�����������(��ͼ8(e)��(f))������������ת������þ�Ͻ�����������͡���״��֯�к���FԪ��(��ͼ8(g)��(h))���������ݸ�ʴ5 d���ڡ�����͡���״��֯����Ȼ���ڽ϶�����ܷ����
��������������ò�۲�����������������ݸ�ʴ���̴��¿ɷֳ�����4���Σ�1) ���ݳ��ڣ�����δת���������������������治�ȶ��ı�����þĤ��SBF���ܽ��SBFҺ����þ�Ͻ����ֱ�ӽӴ�����¶��������Mg���нϸߵĻ�ѧ���ԣ��ڽ����Ͻ�ֱ�ӷ���Mg+2H2O��H2��+Mg(OH)2��Ӧ������SBF��þ�Ͻ��ֱ�ӽӴ���������ƽ���������ʽϴ������ȣ�����ת����������������SBF��þ�Ͻ���屻���ܵ�NaMgF3ת��Ĥ���룬SBF��þ�Ͻ������������Ӧֻ����ת��Ĥ�еĿ�϶�����Ͻ��У�����ֱ�ӽӴ������С�����ƽ���������ʽ�С������ͼ7��ʾ��ƽ���������ʵIJ������һ�£�2) ����������SBF�н���ʱ����ӳ���δת����������������ڣ�����ͼ8��ʾ������������������������γ����ɸ�þ��������ɵĸ�ʴ����Ĥ����þ������Ĥ�Ĵ��ڽ�����SBF��þ�Ͻ�����������������ɢ���ʣ�����ƽ�������������½�������ת������������һ���棬������ת��Ĥ��϶�����ϸ�ʴ�γɵĸ�þ�����ζԿ�϶�Ķ���������SBF��þ�Ͻ�����ֱ�ӽӴ���ӽ�һ����С����һ���棬NaMgF3ת��Ĥ�����ܽ������F-�븯ʴ������Mg2+ ��SBF�е�Ca2+��Ӧ�γɵķ������ת��Ĥ�������ã�������ƽ���������ʽ�һ�����ͣ�3) ��������3 d���Һ���δת���������������������γ���һ����ȵ��ȶ���ʴ����㣬�����һ���ӳ�����ʱ�䣬��ƽ���������ʻ��������ȶ�(��ͼ7)������ת����������������NaMgF3ת��Ĥ�IJ����ܽ⣬NaMgF3ת��Ĥ����ʴ�γɵĸ�þ�����Ρ�δ��NaMgF3�����γɵķ���������Ĥ����ȡ�������Ĥ��ı���Ч������NaMgF3ת��Ĥ��������ƽ����������������4) ����5 d��δת�������������ڱ��港ʴ�γɵİ��̬��ʴ����㺬ˮ�ʸߣ�������ɺ��γɵġ�����͡���ߴ�ϴ���ͼ8(g)��(h)��ʾ�������������ת������������ʴĤ���ɸ�þ�����κͷ�������ɣ���Ĥ�����ں�ˮ�ʵͣ�������ɺ��γɵġ�����͡���ߴ��С��

ͼ8 ����(5 d)��ʴ��������SEM����EDS��
Fig. 8 SEM images ((a)-(f)) and EDS patterns ((g), (h)) of samples after dipping corrosion for 5 d
3 ����
1) �ӳ�ת������ʱ������NaMgF3ת��Ĥ�����ܶȣ�����NaMgF3�����ߴ�Ӱ���С�����ת�������¶ȿ�ʹNaMgF3�����ߴ��С��NaMgF3��������������Ҫ�ж�ά�κˡ�̨���������ƺ����������������֡�
2) ת������ʹMg-Nd-Zn-Zrþ�Ͻ�ı�ɫʱ���ӳ���ƽ�����������½����Ը�ʴ�����ܶȽ��͡���ʴ��λ���ơ�
3) ���Ž���ʱ����ӳ���δת������Mg-Nd-Zn-Zrþ�Ͻ�ƽ���������ʵ�����С�������ȶ�����ת����������ƽ���������������Ϊ�ɴ��С����������������ơ�
4) ת������Mg-Nd-Zn-Zrþ�Ͻ���ݸ�ʴ�γɵġ�����͡���״��֯�ߴ�͡�����͡�����϶���Ⱦ�С��δת�����������ġ�
REFERENCES
[1] �� ��, �� ��, Ԭ����, ������, ������, ���Ľ�. ����ҽ��Mg-Nd-Zn-Zrþ�Ͻ���ģ����Һ�еĽ�����Ϊ[J]. �й���ɫ����ѧ��, 2010, 20(10): 1989-1997.
ZHANG Jia, ZONG Yang, YUAN Guang-yin, CHANG Jian-wei, FU Peng-huai, DING Wen-jiang. Degradable behavior of new-type medical Mg-Nd-Zn-Zr magnesium alloy in simulated body fluid[J]. The Chinese Journal of Nonferrous Metals, 2010, 20(10): 1989-1997.
[2] �ƾ���, ������, �ű���, �� ��. þ��þ�Ͻ�������������о�[J]. ϡ�н��������빤��, 2007, 36(6): 1102-1105.
HUANG Jing-jing, REN Yi-bin, ZHANG Bing-chun, YANG Ke. Study on biocompatility of magnesium and its alloys[J]. Rare Metal Materials and Engineering, 2007, 36(6): 1102-1105.
[3] YANG J X, CUI F Z, LEE I S. Surface modification of magnesium alloys for biomedical applications[J]. Annals of Biomedical Engineering, 2011, 39(7): 1857-1871.
[4] ���λ�, �� ��, �Ŵ���, ��ѧ��, �����, Ҧ����, �� ·, �� ��. ҽ��þ�Ͻ�����︯ʴ���߷���Ϳ�㴦��[J]. ϡ�н��������빤��, 2008, 37(7): 1225-1228.
XU Xin-hua, CHENG Jing, ZHANG Chun-huai, YAN Xue-liang, ZHU Tian-bing, YAO Kang-de, CAO Lu, LIU Yin. Bio-corrosion and polymer coating modification of magnesium alloys for medicine[J]. Rare Metal Materials and Engineering, 2008, 37(7): 1225-1228.
[5] ������, Ԭ����, ������. ����þ�Ͻ�Mg-Nd-Zn-Zr�����︯ʴ����[J]. �й���ɫ����ѧ��, 2013, 23(4): 905-911.
ZHANG Xiao-bo, YUAN Guang-yin, WANG Zhang-zhong. Biocorrosion properties of as-cast Mg-Nd-Zn-Zr magnesium alloy[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(4): 905-911.
[6] �� ��, �� ��, ������, �ƾ���, ̷����, �� ��. ����þĤAZ31Bþ�Ͻ���ϵ�ϸ�������о�[J]. ϡ�н��������빤��, 2008, 37(6): 1027-1031.
GUO Lei, LIU Kui, ZHANG Shi-liang, HUANG Jing-jing, TAN Li-li, YANG Ke. Cytotoxicity of AZ31B magnesium alloy covering with magnesium oxide[J]. Rare Metal Materials and Engineering, 2008, 37(6): 1027-1031.
[7] YE Cheng-hong, XI Ting-fei, ZHENG Yu-feng, WANG Shu-qin, LI Yang-de. In vitro corrosion and biocompatibility of phosphating modified WE43 magnesium alloy[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(4): 996-1001.
[8] XU Li-ping, ZHANG Er-lin, YANG Ke. Biocorrosion property and cytocompatibility of calcium phosphate coated Mg alloy[J]. The Chinese Journal of Nonferrous Metals, 2012, 23(8): 2014-2020.
[9] MAREIKE LALK, JANIN REIFENRATH, NINA ANGRISANI, ALEXANDR BONDARENKO, JAN-MARTEN SEITZ, PETER P MUELLER, ANDREA MEYER-LINDENBERG. Fluoride and calcium-phosphate coated sponges of the magnesium alloy AX30 as bone grafts: A comparative study in rabbits[J]. Journal of Materials Science: Materials in Medicine, 2013, 24(2): 417-436.
[10] LI J N, CAO P, ZHANG X N, ZHANG S X, HE Y H. In vitro degradation and cell attachment of a PLGA coated biodegradable Mg-6Zn based alloy[J]. Journal of Materials Science, 2010, 45(22): 6038-6045.
[11] �� �, ���½�, ��ͤ͢, ̷����, �ű���, �� ��. ��������AZ31Bþ�Ͻ�������ʴ������Ϊ��Ӱ��[J]. ϡ�н��������빤��, 2011, 40(10): 1859-1863.
LI Qi, LIU Xin-jie, YAN Ting-ting, TAN Li-li, ZHANG Bing-chun, YANG Ke. Effect of fluoride conversion treatment on bio-corrosion behavior of AZ31B magnesium alloy[J]. Rare Metal Materials And Engineering, 2011, 40(10): 1859-1863.
[12] YAN Ting-ting, TAN Li-li, XIONG Dang-sheng, LIU Xin-jie, ZHANG Bing-chun, YANG Ke. Fluoride treatment and in vitro corrosion behavior of an AZ31B Mg alloy[J]. Materials Science and Engineering A, 2010, 30(5): 740-748.
[13] WITTE F, FISCHER J, NELLESEN J, VOGT C, VOGT J, DONATH T, BECKMANN F. In vivo corrosion and corrosion protection of Mg alloy LAE442[J]. Acta Biomaterialia, 2010, 6(5): 1792-1799.
[14] ������, �� ��, ���ΰ, ����ƽ, �ܿ���. ����þͿ��AZ31Bþ�Ͻ����ڳɹ����õ��о�[J]. �й�ҽ�ƴ�ѧѧ��, 2011, 40(10): 870-873.
WANG Xian-tao, GUO Lei, CHAI Hong-wei, FU Yu-ping, GUAN Jun-lin. In vivo evaluation of osteogenesis of fluoride treated AZ31B[J]. Journal of China Medical University, 2011, 40(10): 870-873.
[15] BAKHSHESHI-RAD H R, IDRIS M H, ABDUL-KADIR M R. Synthesis and in vitro degradation evaluation of the nano-HA/MgF2 and DCPD/MgF2 composite coating on biodegradable Mg-Ca-Zn alloy[J]. Surface and Coatings Technology, 2013, 222(15): 79-89.
(�༭ ������)
������Ŀ���Ͼ�����ѧԺ���»����ش���Ŀ(CKJA201202)������ʡ��У��Ȼ��ѧ�о�����(12KJB430007)
�ո����ڣ�2013-09-05�������ڣ�2014-01-14
ͨ�����ߣ������ͣ������ڣ���ʿ���绰��025-86118276��E-mail��fangxinxian@njit.edu.cn


