ͭ�����Ի���̿������������β���е�PH3
����Ƽ����꣬�������������ۣ�Ҷ����
(����������ѧ ������ѧ�빤��ѧԺ, ���� ������ 650093)
ժҪ�����ý��շ��Ʊ�ͭ�����Ի���̿���������������壬��Ҫ���������֡��������������¶ȡ����ٶ��������������ߵ�Ӱ�죬���о�������ͭ�����Ի���̿�ϵĶ���ѧ���̡��о������������������Cu��Fe��Ce���ʵ�����Ϊ20.0:1.0:0.4�Ļ�ϸ���Һ���غ�Cu-Fe-Ce/AC��PH3�������������ɴ�62 mg/g��ͭ�����Ի���̿����ѷ�Ӧ����Ϊ�������¶�70 �棬������(�������)3%������3 000 h-1������ѷ�Ӧ�����£�ͭ�����Ի���̿�����⾻��Ч��Ϊ100%ʱ������ۻ����������ɴ�0.055 m3/g��������Cu-Fe-Ce/AC�������ϵ�ƽ�����Ϊ30.9 kJ/mol��Ϊ-0.2����Ӧ����������������������������λ���٣��Ӷ�ʹ�������ʼ�С��
�ؼ��ʣ�
ͭ�����Ի���̿������������������
��ͼ����ţ�X511 ���ױ�־�룺A ���±�ţ�1672-7207(2011)05-1489-06
Adsorptive purification of PH3 in yellow phosphorus off-gas by Cu-based modified activated carbon
YANG Li-ping, YI Hong-hong, TANG Xiao-long, YU Qiong-fen, YE Zhi-qing
(Faculty of Environmental Science and Engineering, Kunming University of Science & Technology, Kunming 650093, China)
Abstract: The Cu-based modified activated carbons prepared by impregnation were used for adsorbents of PH3 purification. The effects of oxygen concentration, adsorption temperature and space velocity on phosphine adsorption breakthrough curve were studied. And the kinetics process of PH3 adsorption on the Cu-based modified activated carbon was also analyzed. The results show that the maximum of phosphine adsorption capacity is 62 mg/g when the molar ratio of Cu, Fe and Ce is 20.0:1.0:0.4. The optimum parameters of adsorptive reaction are oxygen concentration of 3%, adsorption temperature of 70 ��, and space velocity of 3 000 h-1. At the optimum parameters, the maximum handling capacity is up to 0.055 m3/g. The average activation energy is 30.9 kJ/mol and the order of reaction is -0.2 for PH3 on the Cu-based modified activated carbon.
Key words: Cu-based modified activated carbon; adsorptive removal; phosphine
������һ����Ҫ�Ļ�����Ʒ������β���ǵ�¯�������������еĸ����ÿ����1 t������β�� 2 500~3 000 m3(���幤����)����ֱ���ŷŽ��Կ�����ɼ������Ⱦ[1]������β������CO������CO����(�������)Ϊ85% ~95% [2]���DZ����̼һ�������ϣ������ں����ʽ϶࣬���������Ѷȴ��谭�˻���β�����ۺ����á�����β���е�����������ҪΪ�ס������飬��������Ҫ������(PH3)������(P4��P6)����̬����[3]������β���е��ס�����������ʻᵼ�º���ϳɴ����ж�[4]��������Լ����β����Ϊ̼һ����ԭ�Ϻϳ��������ᡢ�����Լ��״��ȸ߸���ֵ��Ʒ��ƿ������[5]����ʵ��Ի���β������������PH3�ö�̬����װ�ý�������ʵ���о���������������PH3���������ԣ�Ϊ����β����Ϊ��������̼-������Ʒԭ�����ṩһ����ʵ���еķ����������������뷽�����ѵ����ڿ���һ�ֶ���������ѡ���ԽϺ����������������������Ӷ�����ʵ������β���ľ�����PH3�������Դ��������̿��һ��Ӧ�ù㷺���������������нϴ�ıȱ�������ֻ��Ի� ��[6]������̿���Ե�����Ϊ������[7]�����[6]����������ҵ�����еĸ�����Ⱦ���������������ѡ���ϡ�ͨ���Ի���̿�ı�����Ž��и����������̿���������ܣ����ڻ���̿�н���ijЩ���������������Լ�������������ǿ����̿�Ĵ����ԣ��ȿ��Խ��ͷ�Ӧ���¶ȣ��ֿ��������������[8]���ڴˣ������������ý��շ��Ʊ�����ͬ������ֵĻ���̿����������PH3���壬�����˻�����֡������¶ȡ� �������Ϳ��ٶԸ��Ի���̿��������PH3��Ӱ�죻����ͭ�����Ի���̿��������PH3�Ķ���ѧ�����о���
1 ʵ�鲿��
1.1 ʵ�����
����̿(AC)������ͨ����ú�ʿ�������̿�������Բ�������1���Ƚ��հ���̿ˮϴ���ȡ����õĻ���̿25 g�����ں��ض�Ũ��Cu2+��Fe3+��ϡ���Ļ����Һ�У���������40 min��������110 ����� 12 h�������������¯����350 ���±���6 h���õ���
����������PH3�ĸ��Ի���̿�����Ի���̿���õĽ�����ΪCu(NO3)2��3H2O(99.5%), Fe(NO3)3��9H2O(98.5%)��Ce(NO3)3��6H2O(99%)��La(NO3)3��nH2O(44%����La2O3��)�ȣ�ʹ����Һ��Cu2+Ũ��Ϊ0.05 mol/L����������Ũ�Ȱ�һ�������ʵ����������ƣ�������Һ��Cu��Fe �����ʵ�����Ϊ20:1��Cu��Fe��Ce(Ag, La)�����ʵ�����Ϊ20.0:1.0:0.4��
��1 ����̿�����Բ���
Table 1 Parameters of activated carbon

1.2 ʵ��װ��
ʵ����ö�̬�����ķ�����ʵ������ͼ��ͼ1���ɸ�ƿ��������PH3��N2(��Ϊ����)��O2Ҫ�Ⱦ�����Ϲ�Ͼ��ȣ��Դﵽʵ��Ҫ���PH3����Ũ���ٽ�����������������Ӧ����һ�������Բ���������н��У��ú���װ�ý��м��ȣ��������β��������ͭ��Һ���պ����ŷš�
1.3 ʵ�鷽��
PH3�IJⶨ����C16��Яʽ��������C16 PortaSens��(Analytical Technology, Inc, ����ATI)����С����Ϊ0~200��10-6���������Ϊ0~2 000��10-6���ֱ���Ϊ1��10-6��
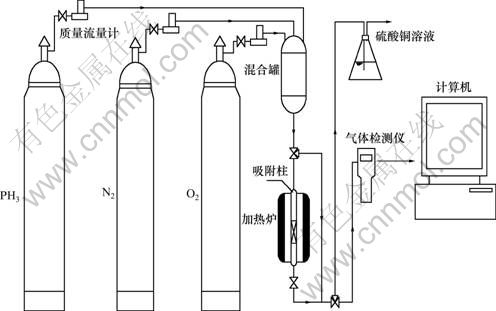
ͼ1 ʵ��װ������ͼ
Fig.1 Schematic diagram of experimental system
��PH3 1 550~1 650 mg/m3�����崩��װ��һ�����������IJ������������ʵ����25~80 ���½��С�����������90%ʱ��ʵ��ֹͣ��ʵ������Ը������´����߰�(1)ʽ���ֿɵö�Ӧ�Ļ��������������� PH3��������[9]��
![]() (1)
(1)
ʽ�У�XΪ����������mg/g��QΪ����������mL/min����0Ϊ�������������Ũ�ȣ�mg/m3��tΪ����ʱ�䣻��Ϊ��������������Ũ�ȣ�mg/m3��mΪ������������g��
2 ���������
2.1 ������ֵ�ɸѡ
��������Ӧ�¶�Ϊ70 �棬������Ϊ3%����������Ϊ450 mL/min������Ϊ3 000 h-1ʱ������̿��ͬ������ֶ�PH3��������������ͼ2��ͼ3��ʾ��
��ͼ2��֪�������ͭ(Cu2+Ϊ0.05 mol/L)���Ի���̿�Ʊ��������������������Ч��Ҫ�������ڿհ���̿�͵������(Fe3+Ϊ0.05mol/L)���صĻ���̿��̷�Ǿ���[10]����ͭϵ�����������нϺõĴ��������Ե�ԭ����������������ʧ�Ƚ����ף�����ͭ����Ϊ���õ��������塣Cu/AC��PH3�нϺõ���������Ч����������ΪPH3��ͭ���Ի���̿�Ϸ����˻�ѧ����[11]�����������μ��˷�Ӧ��������ͭ�������õ��������塣��ˣ�����ʵ�����Ʊ����ض���ֻ���̿����������Ҫѡ��ͭΪ������֡�
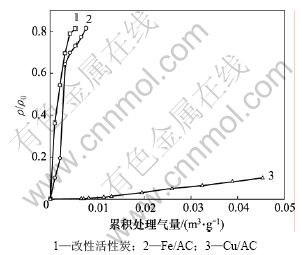
ͼ2 ����ָ��Ի���̿��PH3���������ߵ�Ӱ��(��0 =1.6 g/m3)
Fig.2 Effects of active component on breakthroughs of PH3 by modified activated carbon (��0 =1.6 g/m3)
ͼ3��ʾΪ����̿����˫��ֺͶ���ֶ�PH3��������Ч����Ӱ�졣�ڸ���ͭ��ϵ�л���̿�������Ļ���������ϡ��������(Ag)������������������ߣ�������Cu-Fe-Ag/AC��������������ɴﵽ65 mg/g(��1%����������)��������(Ce)�Ļ���̿�������������ۻ����崦��������������(La)�ĸߣ���˵��ϡ��Ce������������Ļ��ԣ��������� CeO2������ߴ����Ĵ����������Ӷ�ʹ���������ܵõ��������[12-13]�����⣬Ce�����ڼ���ЧӦ������������ͭ�ڻ���̿����ķ�ɢ�ȣ��γɽ϶�Ļ���λ�����ƴ������ս�[14]����Ȼ��������и��Ժ��ȶ��Ե��۸�ʮ�ְ�����ˣ�ѡ��ϡ��Ce���ӵ�����ͭ���Ļ���̿���Ʊ���������PH3�������������и���Һ��Cu��Fe��Ce�����ʵ�����Ϊ20.0:1.0:0.4��
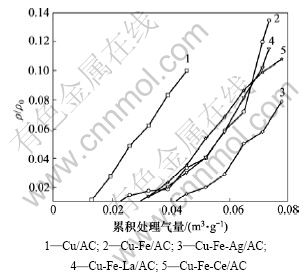
ͼ3 ����ָ��Ի���̿��PH3���������ߵ�Ӱ��(��0=1.6 g/m3)
Fig.3 Effects of multi-active component on breakthroughs of PH3 by modified activated carbon (��0 =1.6 g/m3)
2.2 ��������PH3����������Ӱ��
������Ӧ����������ɸ�ƿ�ṩ���������¶�Ϊ70 �棬��������Ϊ450 mL/min������Ϊ3 000 h-1��������(�������)Ϊ0%��1.0%��2.0%��3.0%��4.0%�����£�Cu-Fe-Ce/AC��PH3����������Ӱ����ͼ4 ��ʾ��
��ͼ4��֪��ʵ�鷶Χ�����������(�������)Ϊ3%����������Ϊ3%ʱ��Cu-Fe-Ce/AC��PH3������ۻ����崦����Ϊ0.09 m3/g�����������ͻ���߶�������Ӧ�������������������£����Ի���̿��PH3���ۻ����崦������С������PH3��Ҫ������������ʽ�����ڸ��Ի���̿��[3]�����������ͻ�ʹ����PH3
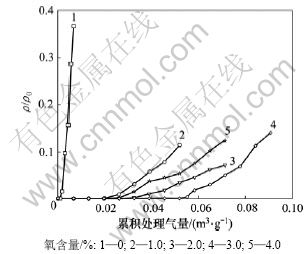
ͼ4 ��������Cu-Fe-Ce/AC��������PH3��Ӱ��(��0 =1.622 g/m3)
Fig.4 Effects of oxygen content on breakthroughs of PH3 by Cu-based modified activated carbon (��0=1.622 g/m3)
���ӵò���������������PH3��������Ӧ�����������ߣ������ӻ�ԭ�ӻ�ռ�ݴ����Ļ�������λ����PH3���ӷ�����������[15]��Ҳ����������������PH3���ӵ��������������Ӷ�������PH3��������Ӧ�����������������ӣ����Ի���̿��PH3���ۻ����崦��������������������ߣ���������������4%ʱ��PH3�ľ���Ч���Ѳ�����ߣ�ʵ��ȷ�����������Ϊ3%��
2.3 �����¶ȶ�PH3����������Ӱ��
��������Ϊ3%����������Ϊ450 mL/min������3 000 h-1ʱ��Cu-Fe-Ce/AC�ڲ�ͬ�����¶��¶�PH3���������ߵ�Ӱ����ͼ5��ʾ����ͼ5��֪������
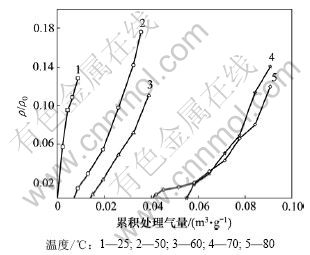
ͼ5 �¶ȶ�Cu-Fe-Ce/AC��������PH3��Ӱ��(��0=1.565 g/m3)
Fig.5 Effects of reaction temperature on breakthroughs of PH3 by Cu-based modified activated carbon (��0=1.565 g/m3)
�¶���Ӱ��PH3������������Ҫ����֮һ�������¶�̫��̫�Ͷ�������PH3���������¶�Ϊ70 ��ʱ��������Ч����á�PH3�ڸ��Ի���̿�����������Ӧ�Ƿ��ȿ��淴Ӧ�������¶ȿ�������PH3���ӻ���ʺ�������ͬʱ���������������еķ���ЧӦ�����²���������ƽ�������һ���ƶ�����ͼ5��֪�����¶ȴ�70 �����ߵ�80 ��ʱ��PH3���ۻ����崦������û�����ӡ�����������Ӧ����ѷ�Ӧ�¶�70 �档
2.4 ���ٶ�PH3����������Ӱ��
�������¶�Ϊ70 �棬��������Ϊ450 mL/min��������Ϊ3%ʱ��Cu-Fe-Ce/AC�ڲ�ͬ���������¶�PH3���������ߵ�Ӱ����ͼ6��ʾ����ͼ6��֪������Ҳ��Ӱ��PH3����������һ����Ҫ���ء����ٹ�С��ɢ�����Ի���̿���漰�ڲ��� PH3 �������ӽ��٣��Ӷ������� PH3��������Ӧ�����ٹ�����������������ͣ��ʱ��϶̣��Ӷ�Ҳ������ PH3��������Ӧ��������Ϊ2 000 h-1��3 000 h-1�����ۻ����崦�����ﵽ0.055 m3/gʱ���侻��Ч�ʻ�������100%����������Ϊ2 000 h-1ʱ�����Ի���̿��PH3��������Ӧ����̫С�����ԣ�ʵ�鷶Χ����ѿ���Ϊ3 000 h-1��
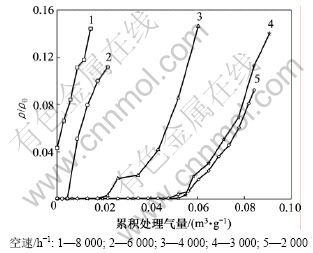
ͼ6 ���ٶ�PH3���������ߵ�Ӱ��(��0=1.611 g/m3)
Fig.6 Effects of space velocity on breakthroughs of PH3 by Cu-based modified activated carbon (��0=1.611 g/m3)
2.5 ����ѧ�о�
����ѧʵ���������[16]����2�еIJ������У�ʵ��ɻ�ø����¶��µĴ����ߣ�Ȼ�Ը����¶��µĴ����߰�ʽ(1)���ֿ��Եõ�PH3�����������ߣ����ͨ����Ӧ���ʷ���(2)����õ���ܺͷ�Ӧ������
![]() (2)
(2)
ʽ�У�rΪPH3Ϊ���ķ�Ӧ���ʣ�mg/(g��min)��kΪ��Ӧ���ʳ�����tΪ��Ӧʱ�䣬min��nΪ��Ӧ������
Ϊ�˱����������¶��µ�ƽ�����ʳ���k��ʽ(2)��ת��Ϊʽ(3)��
![]() (3)
(3)
![]() (4)
(4)
![]() (5)
(5)
ʽ�У�k0Ϊ���¶��صij�����EΪ��ܣ�RΪ���峣����R=8.314 J/mol��TΪ��Ӧ����ѧ�¶ȣ�K��
����ʽ(2)ͨ�������������ֿɽ����¶������ʳ�����ƽ����Ӧ���������ͨ���ֽ����-lgr��-lgx�Ĺ�ϵ���ߣ�PH3 �����ڽ������Ի���̿�ϵķ�ӦΪ-0.2(n=-0.2)����Ӧ���������ʽ(4)��(5)�ɵ� PH3���Ի���̿��ƽ�����Ϊ30.9 kJ/mol���ﵽ�˻�ѧ��Ӧ����Ļ��[17]��PH3ƽ��������������ͼ7��ʾ�����У����ϵ��Ϊ0.979������Ϊ 0.180 02��
��2 ����ѧʵ�����
Table 2 Parameters of thermal dynamic experiment
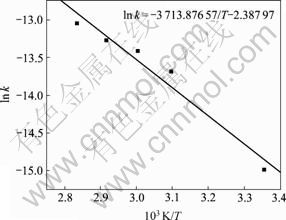
ͼ7 PH3ƽ������������
Fig.7 Resolving curve of average activation energy of PH3
3 ����
(1) ���ý��շ����Ժ�Ļ���̿��PH3��������Ч���ܺã�����������Ч���PH3������������������������������ɴ�62 mg/g��
(2) Cu-Fe-Ce/AC��������PH3�����������¶ȼ������е���������Ӱ����������Ч���Ĺؼ����أ����������еĺ���������߷�Ӧ�¶Ⱦ���������߾���Ч�ʣ������ӵ�һ��ֵ��(�¶ȣ�70 �棬��������3%)����Ч����������ߣ���������������ѷ�Ӧ������������Ϊ3%�������¶�Ϊ70 �棬����Ϊ3 000 h-1���ڸ÷�Ӧ�����£�Cu-Fe-Ce/AC��PH3����Ч��Ϊ100%ʱ������ۻ����������ɴ�0.055 m3/g��
(3) Cu-Fe-Ce/AC������������β���е�PH3���壬PH3�ڸ��Ի���̿�Ϸ�Ӧ��ƽ�����Ϊ30.9 kJ/mol��Ϊ-0.2����Ӧ��������������������������������������Ӧ��ʹ��Ӧ�����½���
�ο����ף�
[1] Ning P, Xie Y C, Yi H H. Study on a four-bed PSA process for the manufacture of pure CO[C]//Proceedings of Seventh International Conference of Fundamentals of Adsorption. Nagasaki, 2001: 613-617.
[2] �ܻ�, ������, �����. �������������ѳ�����β���е���������[J]. ��������, 2002, 22(3): 161-164.
XIONG Hui, YANG Xiao-li, LI Guang-xing. Removal of sulfur and phosphorus from tail gas in yellow phosphorus production by sodium hypochlorite oxidation process[J]. Environmental Protection of Chemical Industry, 2002, 22(3): 161-164.
[3] ��ƽ, Bar H J, ��ѧǫ, ��. ��������������β���е�����[J]. �й����̿�ѧ, 2005, 7(6): 27-35.
NING Ping, Bar H J, WANG Xue-qian, et al. Removal of P4 , PH3 and H2S from yellow phosphoric tail gas by a catalytic oxidation process[J]. Engineering Science, 2005, 7(6): 27-35.
[4] MA Li-ping, NING Ping, ZHANG Yuan-yuan. Experimental and modeling of ?xed-bed reactor for yellow phosphorous tail gas puri?cation over impregnated activated carbon[J]. Chemical Engineering Journal, 2008, 137(3): 471-479.
[5] Wang X Q, Ning P, Shi Y, et al. Adsorption of low concentration phosphine in yellow phosphorus off-gas by impregnated activated carbon[J]. Journal of Hazardous Materials, 2009, 6(4): 1-6.
[6] ��ϼ, ���ľ�, ����, ��. ���Ի���̿�ڻ��������е�Ӧ��[J]. ������ѧ�뼼��, 2003, 26(5): 34-36.
JIANG Xia, JIANG Wen-ju, JIN Yan, et al. Modified activated carbon and its application in environmental protection[J]. Environmental Science & Technology, 2003, 26(5): 34-36.
[7] Teresa J B. On the adsorption/oxidation of hydrogen sulfide on activated carbons at ambient temperatures[J]. Journal of Colloid and Interface Science, 2002, 246(1): 1-20.
[8] Pak B, Cho Y I, Stephen U S. Study of turbulent heat transfer in a sudden- expansion pipe with drag- reducing viscoelastic fluid[J]. International Journal of Heat and Mass Transfer, 1991, 34(4): 1195-1208.
[9] Teresa J B. Effect of pore structure and surface chemistry of virgin activated carbons on removal of hydrogen sulfide[J]. Carbon, 1999, 37(3): 483-491.
[10] ̷�Ǿ�, ��չ��, ף����, ��. �����л���Ⱦ��ʪʽ������ͭϵ���������о�[J]. ��������, 2000, 20(3): 6-10.
TAN Ya-jun, JIANG Zhan-peng, ZHU Wan-peng, et al. Study on activity of copper catalysts for the wet oxidation of organic pollutants[J]. Environmental Protection of Chemical Industry, 2000, 20(3): 6-10.
[11] Li W C, Bai H, Hsu J N, et al. Metal loaded zeolite adsorbents for phosphine removal[J]. Ind Eng Chem Res, 2008, 47(5): 1501-1505.
[12] Kaspar J, Fornasiero P, Graziani M. Use of CeO2-based oxides in the three-way catalysis[J]. Catalysis Today, 1999, 50(2): 285-298.
[13] Trovarelli A. Catalytic properties of ceria and CeO2-containing materials[J]. Catalytic Reviews-Science Engineering, 1996, 38(4): 439-520.
[14] ��ѩ��, ������, �²���. ϡ���硢���Cu/ZnO/Al2O3����ˮ���任���ܵ�Ӱ��[J]. ��Ȼ������, 2007, 32(6): 1-4.
FENG Xue-feng, JIN Wei-gen, CHEN Chang-lin. Effects of rare earths on the performances of Cu/ZnO/Al2O3 catalysts for water-gas shift reaction[J]. Natural Gas Chemical Industry, 2007, 32(6): 1-4.
[15] ����, ��ƽ, ��ƶ�, ��. ���Ի���̿������������β���е�PH3[J]. ��������ѧ��, 2007, 1(5): 74-78.
ZHANG Yong, NING Ping, XU Hao-dong, et al. Adsorptive removal of PH3 in off-gas of yellow phosphorus by modified activated carbon[J]. Chinese Journal of Environmental Engineering, 2007, 1(5): 74-78.
[16] ����, ��ƽ, ��ѧǫ, ��. ������̼�����ѳ�����β���е�H2S��PH3[J]. ��ѧ����, 2007, 35(7): 7-10.
ZHANG Yong, NING Ping, WANG Xue-qian, et al. Adsorbing removal of H2S and PH3 in off-gas of yellow phosphorus by activated carbon modified through acid and alkali[J]. Chemical Engineering, 2007, 35(7): 7-10.
[17] �����. ��ѧ��Ӧ����[M]. ����: ��ѧ��ҵ������, 2002: 17-19.
ZHU Bing-chen. Chemical reaction engineering[M]. Beijing: Chemical Industry Press, 2002: 17-19.
�ո����ڣ�2010-03-24�������ڣ�2010-06-20
������Ŀ�����Ҹ����о���չ�ƻ�(��863���ƻ�)�ص���Ŀ(2008AA062602)������ʡ������ѧ���ͼ�����ͷ�˺��˲���Ŀ(2007PY01-10)
ͨ�����ߣ����(1976-)��Ů���½������ˣ���ʿ�����ڣ����´�����Ⱦ���ƣ��绰��0871-5170905��E-mail: yhhtxl@126.com


