���±�ţ�1004-0609(2015)-05-1236-08
���������������xLi2MnO3��(1-x)LiNi0.8Co0.15Al0.05O2���Ʊ��͵绯ѧ����
�� �������㿵������ǣ��� �ϣ������ѣ���鲨����ɽ���ϲ�ΰ����ΰ��
(��̶��ѧ ��ѧѧԺ����̶ 411105)
ժ Ҫ��
ͨ���ܽ�-�������ϳ��˺��������������xLi2MnO3��(1-x)LiNi0.8Co0.15Al0.05O2��̽���˻�ѧ���(x=0.5��0.6��0.7��Ħ������)�������¶�(850��900��950 ��)�Բ�����ò���ṹ�����ܵ�Ӱ�졣����XRD��SEM�͵�س�ŵ�����ǶԲ��Ͻ������������͵����ܲ��ԡ�������������Ʊ��IJ��Ͼ��е��͵Ħ�-NaFeO2��״�ṹ����x=0.6�������¶�Ϊ900 ��ʱ�����ϳɵIJ��Ͼ��нϺõ���ò�������ĵ绯ѧ���ܣ���2.0~4.6 V��0.1C��ŵ������£�0.6Li2MnO3��0.4LiNi0.8Co0.15Al0.05O2���״ηŵ�������ɴ�229.9 mA��h/g�����״ο���Ч��Ϊ80.0 %����0.5C������ѭ��100�κ���ŵ��������Ϊ192.7 mA��h/g�����������ʴ�83.8 %����ʾ��������ѭ�����ܡ����⣬������ʾ�����õı������ܣ���2.0C�����£���ŵ��������Ϊ173.1 mA��h/g��
�ؼ��ʣ�
����ӵ����������������������ܽ�-���������绯ѧ������
��ͼ����ţ�TM912.9���� ���ױ�־�룺A
Synthesis and electrochemical performance of Al-doped Li-rich layered xLi2MnO3��(1-x)LiNi0.8Co0.15Al0.05O2 cathode materials
GE Long, YANG Xiu-kang, YU Rui-zhi, WANG Di, WANG Xian-you, SHU hong-bo,
ZOU Gui-shan, JU Bo-wei, WEN Wei-cheng
(School of Chemistry, Xiangtan University, Xiangtan 411105, China)
Abstract: Al-doped Li-rich layered xLi2MnO3��(1-x)LiNi0.8Co0.15Al0.05O2 cathode materials were synthesized via sol-gel method, and the influence of chemical component (x=0.5, 0.6, 0.7, mole fraction) and calcination temperature (850, 900 and 950 ��) on the morphology, structure and performance of the as-prepared materials were discussed. The physical characterization and electrochemical performance test of the as-prepared materials were conducted by means of XRD, SEM and electrochemical measurements. The results demonstrate that the prepared material has a typical ��-NaFeO2 layered structure, and the xLi2MnO3��(1-x)LiNi0.8Co0.15Al0.05O2 exhibits the optimal electrochemical performance when the Li content x is equals to 0.6 and sintering temperature at 900 ��. The resultant 0.6Li2MnO3��0.4LiNi0.8Co0.15Al0.05O2 sample shows an high initial discharge capacity of 229.9 mA��h/g and coulomb efficiency of 80.0% for the first time when cycled in the voltage range of 2.0~4.6 V at 0.1C. In addition, the material exhibits good cycling stability with capacity retention of 83.8 % after 100 cycles at 0.5C. Furthermore, the material also shows good rate capability, delivering high discharge capacity of 173.1 mA��h/g at 2.0C.
Key words: lithium-ion battery; Al-doped Li-rich cathode material; sol-gel method; electrochemical performance
����ӵ�ؾ��������ܶȴ�����ѹ�ߡ�ѭ�����������Էŵ�С�ͻ����Ѻõ������ŵ㣬���㷺Ӧ���ڱʼDZ����ԡ��ƶ��绰�������Ʒ�ȱ�Яʽ�����豸���������ǶԻ�������ȫ����Ҫ������������Լ��綯�����ķ�չ������ӵ�ص�Ӧ������Խ��Խ�㡣������ӵ�صijɱ������У���������ռ�ı������ͬʱҲ��Ӱ�����ۺ����ܵĹؼ����ء�Ȼ������ͳ���������ϣ���LiCoO2����Ԫ���ϡ�LiFePO4��LiMn2O4�ȣ���������������ܶȵ��г�Ӧ�����������������������xLi2MnO3��(1-x)LiMO2 (M=Mn, Ni, Co�ȹ��ɽ���֮��������ϣ�0��x��1)������и߱�������������ѭ�������Լ��µĵ绯ѧ��ŵ���Ƶ��ص����Ϊ�о��ȵ�[1-5]��
�ڸ����������xLi2MnO3��(1-x)LiMO2�У�Mn�����ɽ���M��һ����Li��ͬ����˽����㡣�������ھ��в�ͬ��ԭ�Ӻ͵��ӽṹ��������xLi2MnO3��(1-x)LiMO2�д������ֲ�ͬ�Ŀռ�Ⱥ������Li2MnO3Ϊ��б���壬���ڿռ�ȺC2/m����LiMO2Ϊ�������壬���ڿռ�ȺR-3m������б����(001)�����������(003)�����4.7 pm�IJ��ࡣ���ڽ��ܶѻ���ļ����ԣ������е�Li2MnO3��LiMO2�ܹ�ʵ��ԭ��ˮƽ�ϵ�����[6]��
Ŀǰ�����������б����ĸ���������ϵ��Ʊ�������Ҫ�и��¹��෨���ܽ�-���������������������������ˮ�Ⱥϳɷ��ȡ����У��ܽ�-������������кϳ��¶ȵ͡���Ӧ���ڿ��ơ������ɲ����Ի�ѧ��ֻ����Ի�ѧ��ֵ��ŵ㣬���ϳɵIJ��ϻ�ѧ�����Ժá������ֲ�խ�����ȸߣ����Ʊ�����������ϵ�һ����Ҫ����[7]��KIM��[8]��������Ϊ��ϼ���������Ϊԭ�ϣ�ʹ�ð�ˮ����pH�����ܽ�-�������ϳɳ�Li[Li0.1Ni0.35-x/2CoxMn0.55-x/2]O2����������ϣ����Խ����������0.2C��2.5~4.6 Vʱ�ŵ�����ά����184~195 mA��h/g��TANG��[9]��������Ϊ��ϼ����ܽ�-�������ϳɳ�Li1+yNi0.5AlxMn0.5-xO2���绯ѧ���Խ����������2.5~4.7 V֮�����״ηŵ�����Ϊ192 mA��h/g����30��ѭ��֮��ķŵ�����Ϊ188 mA��h/g��LEE��[10]����C2H3O2Li��2H2O��Mn(CH3COO)2��4H2O��LiNO3��Ni(NO3)2��6H2O��Co(NO3)2��6H2OΪԭ�ϣ������ܽ�-�������ϳɵõ������������Li[Li0.2Mn0.55Co0.1Ni0.15]O2���ò�����20 mA/g��2.0~4.8 V֮����״ηŵ�����Ϊ240 mA��h/g��������40 mA/g �ŵ�ʱ��ѭ��50�κ�������ֻ��140 mA��h/g��
������ӵ�����������У�������Ԫ�ؿ��Ը��Ʋ��ϵĽṹ�ȶ��ԣ�ͨ������������߲��ϵij�ŵ�ѭ���ȶ���[11]�������������Ʊ����������ĸ���������ϣ�ͨ���ܽ�-�������Ʊ���xLi2MnO3��(1-x)- LiNi0.8Co0.15Al0.05O2�����ص�̽�ֻ�ѧ���(x=0.5��0.6��0.7)�������¶�(850��900��950 ��)�Բ��Ͻṹ����ò���绯ѧ���ܵ�Ӱ�졣
1 ʵ��
1.1 ���ϵ��Ʊ�
���Ƚ���ѧ�����ȵ�Li(CH3CO2)��2H2O��Mn(CH3CO2)2��4H2O��Ni(CH3CO2)2��4H2O��Co(CH3CO2)2�� 4H2O��Al(NO3)3��9H2O����50 mL��ȥ����ˮ���γɽ�������Һ��Ȼ��������������Һ50 mL��������������������ӵ�Ħ����Ϊ1:1������������Һ��μ��뵽��������Һ�У������Ͻ��裬�õ����ȵĻ����Һ��ͬʱ�μӰ�ˮ��Һ���ƻ����Һ��pHֵ��7.5���ҡ�Ȼ�õ�����Һ��80 ����ԡ���в��Ͻ�������������ɫ��״��֮������120 ����ո������и���12 h�õ����壬��������ĥ�ɷ�ĩ����500 ������¯������6 h����ȥ�л����ŵõ�Ԥ����ǰ���壬���ǰ������ĥ����850~950 ������12 h���õ��˸����������xLi2MnO3��(1-x)- LiNi0.8Co0.15Al0.05O2��
1.2 ���ϵı��������ܲ���
�����ձ���ѧD/max-3C��X����������(XRD)����Ʒ���нṹ����������ԴΪCu K�����ܵ���20 mA���ܵ�ѹ36 kV��ɨ������4 (��)/min��ɨ�跶Χ2��Ϊ10��~80�㡣���ձ�JEOL��˾JSM-5600LV��ɨ���������(SEM)�۲���Ʒ����ò��
1.3 ���ϵĵ绯ѧ���ܲ���
���������Բ��ϡ���Ȳ�ڡ�ʯī��ճ�ϼ�(PVDF)��������Ϊ80:5:5:10�ı�����Ͼ��ȣ��Ʊ���״���ʣ�������Ⱥ�Ϳ�������ϣ�����120 ����ո������и���12 h�õ���Ƭ����Ϊ�������Ƭ��Ϊ������Celgard2400Ϊ��Ĥ��1 mol/LLiPF6/(EC+DMC�������1:1)Ϊ���Һ���������������������װ��ʵ���ء�ʵ���ز������������Գ�ŵ���(CT-3008)�Ͻ��У������¶�Ϊ25 �档
2 ���������
2.1 ��ѧ��ֱ����Բ��Ͻṹ�͵绯ѧ���ܵ�Ӱ��
���ڲ�ͬ�Ļ�ѧ��ֶԸ����������xLi2MnO3��(1-x)LiNi0.8Co0.15Al0.05O2������Ӱ��ܴ��Ƚ������¶ȹ̶�Ϊ900 �棬����̽�ֲ�ͬ��ѧ���(x=0.5��0.6��0.7)�Բ��Ͻṹ����ò�͵绯ѧ���ܵ�Ӱ�죬��ȷ����ѵĻ�ѧ��֡�
ͼ1��ʾΪ��ͬ��ѧ��ֵĸ����������xLi2MnO3��(1-x)LiNi0.8Co0.15Al0.05O2 (x=0.5��0.6��0.7)��XRD�ס���ͼ1���Կ��������Ʊ��IJ��Ͼ����е��͵Ħ�-NaFeO2��״�ṹ��(006)/(102)��(108)/(110)�����������ԡ����⣬x=0.6��x=0.7ʱ�����õ��IJ�����2��Ϊ20��~25��֮�������������壬��������Li+��Ni2+��Mn4+�ڹ��ɽ��������������к��γ��˵�бLi2MnO3��[12-16]������x=0.5ʱ����20��~25��֮�������岻���ԣ����������ڲ������̵ĺ������١�

ͼ1 ��ͬ��ѧ��ֵ�xLi2MnO3��(1-x)LiNi0.8Co0.15Al0.05O2��XRD��
Fig. 1 XRD patterns of xLi2MnO3��(1-x)LiNi0.8Co0.15Al0.05O2 with different chemical components
ͨ��ɨ����������Բ�ͬ��ѧ��ֵĸ����������xLi2MnO3��(1-x)LiNi0.8Co0.15Al0.05O2(x=0.5��0.6��0.7)������ò���з�����������ͼ2��ʾ����ͼ2�ɼ������ϳɵ�3����ͬ��ѧ��ֵIJ��Ͼ������պ���ϸС���������ȣ������ܽ�-�����������Ʊ����ϵ�һ�������[17]��
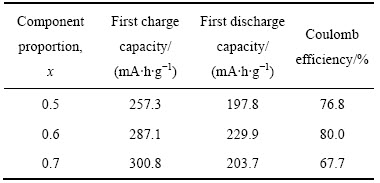
Ϊ�˱Ƚ����Ʊ����ϵĵ绯ѧ���ܣ��ֱ�����װ�ɿ�ʽ��ؽ��г�ŵ���ԡ�ͼ3��ʾΪ��ͬ��ѧ��ֵĸ����������xLi2MnO3��(1-x)LiNi0.8Co0.15- Al0.05O2(x=0.5��0.6��0.7)��2.0~4.6 V��ѹ��Χ��0.1C�����µ��״γ�ŵ����ߡ�3����Ʒ���״γ�����߶�������������ѹƽ̨�����е�һ��ƽ̨��4.5 V���£���Ӧ��Li+��LiMO2��ѧ������ѳ����������Ź��ɽ�������Co3+��Ni2+������[18]����һ��ƽ̨��4.5 V���ң���Ӧ�Ų�����������������[19]�������е�Li2MnO3��ת��Ϊ���е绯ѧ���Ե�MnO2�࣬�Ӷ����״γ�ŵ���̵õ��ϸߵķŵ����������xΪ0.5��0.6��0.7ʱ�����Ʊ��IJ��ϵ��״ηŵ���������Ϊ197.8��229.9��203.7 mA��h/g���������1���С���Ȼ����x=0.6ʱ����0.6Li2MnO3��0.4LiNi0.8Co0.15Al0.05O2���״ηŵ�����������䲻����������С������Ч�ʿɴ�80.0%��

ͼ2 ��ͬ��ѧ��ֵ�xLi2MnO3��(1-x)LiNi0.8Co0.15Al0.05O2��SEM��
Fig. 2 SEM images of xLi2MnO3��(1-x)LiNi0.8Co0.15Al0.05O2 with different chemical components
ͼ4�Ƚ��˲�ͬ��ѧ��ֵĸ����������xLi2MnO3��(1-x)LiNi0.8Co0.15Al0.05O2(x=0.5��0.6��0.7)��2.0~4.6 V��ѹ��Χ�ڡ�0.5C�����µ�ѭ���������ߡ���xΪ0.5��0.6��0.7ʱ�����Ʊ��IJ��Ͼ���100��ѭ�������������ʷֱ�Ϊ68.9%��83.8%��71.9%����Ȼ������Li2MnO3��ѧ��ֵ����ӣ����ϵ�ѭ����������һ����������С�����ơ����У���x=0.6ʱ��0.6Li2MnO3��0.4LiNi0.8Co0.15Al0.05O2���Ͼ�����õ�ѭ�����ܣ�100��ѭ������ŵ��������Ϊ192.7 mA��h/g���ɼ�����ѧ��ֱ����Ը�﮲��ϵĵ绯ѧ���ܾ��нϴ��Ӱ�졣

ͼ3 ��ͬ��ѧ��ֵ�xLi2MnO3��(1-x)LiNi0.8Co0.15Al0.05O2���״γ�ŵ�����
Fig. 3 First charge and discharge curves of xLi2MnO3��(1-x)LiNi0.8Co0.15Al0.05O2 with different chemical components
��1 ��ͬ��ѧ��ֵ�xLi2MnO3��(1-x)LiNi0.8Co0.15Al0.05O2���״γ�ŵ�����
Table 1 First charge and discharge data of xLi2MnO3��(1-x)LiNi0.8Co0.15Al0.05O2 with different chemical components
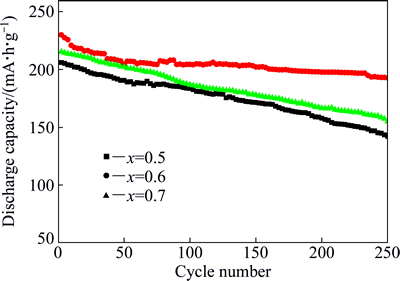
ͼ4 ��ͬ��ѧ��ֵ�xLi2MnO3��(1-x)LiNi0.8Co0.15Al0.05O2��ѭ����������
Fig. 4 Cycle performance curves of xLi2MnO3�� (1-x)LiNi0.8Co0.15Al0.05O2 with different chemical components
ͼ5��ʾΪ��ͬ��ѧ��ֵĸ����������xLi2MnO3��(1-x)LiNi0.8Co0.15Al0.05O2 (xΪ0.5��0.6��0.7)��2.0~4.6 V��ѹ��Χ��0.1C��0.2C��0.5C��1C��2C�����µı����������ߡ����ŷŵ籶�ʵ����ӣ���Ʒ�ķŵ����������١���x=0.5��0.6��0.7ʱ��������0.1C�����µķŵ����������Ϊ201.3��229.9��210.2 mA��h/g������2.0C����ʱ����ŵ�������ֱ�Ϊ152.1��173.1��159.5 mA��h/g���ɼ���x=0.6ʱ�����Ʊ��ĸ���������Ͼ�����õı������ܡ�

ͼ5 ��ͬ��ѧ���xLi2MnO3��(1-x)LiNi0.8Co0.15Al0.05O2�ڲ�ͬ�����µı�����������
Fig. 5 Rate capability curves of xLi2MnO3�� (1-x)LiNi0.8Co0.15Al0.05O2 with different chemical components at different rates
2.2 �����¶ȶԲ��Ͻṹ�͵绯ѧ���ܵ�Ӱ��
ͼ6��ʾΪ��ѧ���x=0.6ʱ��ͬ�����¶��ºϳɵ�0.6Li2MnO3��0.4LiNi0.8Co0.15Al0.05O2��XRD�ס���ͼ6���Կ������ò��Ͼ��е��͵Ħ�-NaFeO2��״�ṹ����(006)/(102)��(108)/(110)������������ԡ����������¶ȵ����ߣ���XRD���е��������ü���(101)/(006)��(018)/(110)���Է����Ҳ��������ͨ����(003)��(104)����ǿ�ȱ�(I(003)/I(104))����ʾ�����Ӷ�ά����ȣ���ֵ����1.2ʱ����Ϊ����������Ƚ�С������������ӵ�Ƕ����ѳ������ϵĵ绯ѧ���Ը�[20]���ݱ�������c/aֵ����4ʱ�����Ͼ��кܺõIJ�״�ṹ[21]������ͼ6 �Ľ�����м��㣬����������2���������¶�Ϊ850��900��950 ��ʱ����c/a������4.9��I(003)/I(104)��ǿ�Ⱦ�����1.2��˵�����Ͼ������õ������״�ṹ���ر���900 ���½�������ʱ����c/aֵ��I(003)/I(104)��ǿ��ֵ�������õ������״�ṹ��
ͼ7��ʾΪ��ͬ�����¶��¸����������0.6Li2MnO3��0.4LiNi0.8Co0.15Al0.05O2��SEM����ͼ7�ɼ�����ͬ�����¶��£���������״�ʹ�С�����¶ȵ����߱仯��Ϊ���ԡ����������¶ȹ���ʱ(��ͼ7(c))������������Ϊ���صĽ�顢�ž����Ӷ�Ӱ����ϵĵ绯ѧ���ܡ����¶Ƚϵ�ʱ�����������Ϊ����(��ͼ7(a))��������������ȫ���ᾧ�Ȳ��ߣ���ʵ�ܶȵͣ���900 ��ʱ�����ѻ�����(��ͼ7(b))�����ٷ����žۣ��ᾧ�Ƚϸߣ���ˣ�900 ���ǽ�Ϊ���ʵ������¶ȡ�

ͼ6 ��ͬ�����¶����Ʊ���0.6Li2MnO3��0.4LiNi0.8- Co0.15Al0.05O2��XRD��
Fig. 6 XRD patterns of 0.6Li2MnO3��0.4LiNi0.8Co0.15Al0.05O2 at different calcination temperatures
��2 ��ͬ�����¶����Ʊ���0.6Li2MnO3��0.4LiNi0.8- Co0.15Al0.05O2���ϵľ�������
Table 2 Cell parameters of 0.6Li2MnO3��0.4LiNi0.8- Co0.15Al0.05O2 material prepared at different calcination temperatures

Ϊ�˱Ƚ����Ʊ����ϵĵ绯ѧ���ܣ��ֱ�����װ�ɿ�ʽ��ؽ��г�ŵ���ԡ�ͼ8��ʾΪ��ͬ�����¶��ºϳɵĸ����������0.6Li2MnO3��0.4LiNi0.8- Co0.15Al0.05O2��2.0~4.6 V��ѹ��Χ�ڡ�0.1C�����µ��״γ�ŵ����ߡ���ͼ8���Կ�����3����Ʒ���״ηŵ�����������ͬ�������¶ȷֱ�Ϊ850��900��950 ��ʱ����ŵ���������Ϊ210.2��229.9��202.5 mA��h/g���ɼ���900 �����Ʊ��IJ��Ͼ�����ߵ��״ηŵ�������������Ϊ�ڽϵ͵������¶��£����ϵĽᾧ�Ȳ��ߣ����巢������ȫ�����ڲ��־���ȱ�ݣ�����绯ѧ���ܽϲ�����¶ȹ���ʱ���ᵼ��һ�����ӳߴ����Li+�ڲ����е���ɢ�������ӣ��һή�ͱȱ�����������ڵ��Һ�Ľ���ʹ�ò��ϵij�ŵ���������͡���ˣ������˵������¶�Ϊ900 �档

ͼ7 ��ͬ�����¶��Ʊ���0.6Li2MnO3��0.4LiNi0.8- Co0.15Al0.05O2��SEM��
Fig. 7 SEM images of 0.6Li2MnO3��0.4LiNi0.8Co0.15Al0.05O2 at different calcination temperatures
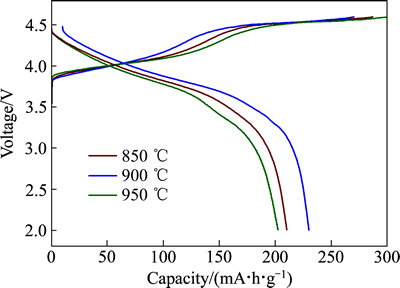
ͼ8 ��ͬ�����¶����Ʊ���0.6Li2MnO3��0.4LiNi0.8- Co0.15Al0.05O2��2.0 ~ 4.6 V��0.1C�µ��״γ�ŵ�����
Fig. 8 First charge and discharge curves of 0.6Li2MnO3��0.4LiNi0.8Co0.15Al0.05O2 at different calcination temperatures and 2.0-4.6 V, 0.1C
ͼ9��ʾΪ��ͬ�����¶����Ʊ��ĸ����������0.6Li2MnO3��0.4LiNi0.8Co0.15Al0.05O2��2.0~4.6 V��ѹ��Χ��0.5C�����µ�ѭ���������ߡ��������¶ȷֱ�Ϊ850��900��950 ��ѭ��100�κ������������ʷֱ�Ϊ75.1%��83.8%��68.8%����ԭ������������¶Ƚϵ�ʱ�����巢������ȫ����ŵ�����нṹ���ȶ���������ѭ�����ܽϲ�ڽϸߵ������¶��£�﮵Ļӷ����أ���ɾֲ�ȱﮣ�ʹ��ѭ�����ܲ��ѡ��������¶�Ϊ900 ��ʱ������ṹ������ȫ����ò���۽ṹ���ֽϺã����н�������ѭ�����ܡ�
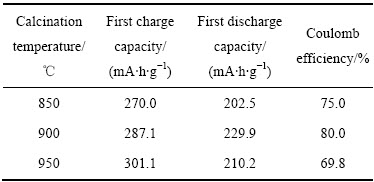
ͼ10��ʾΪ��ͬ�����¶��ºϳɵĸ�﮲���0.6Li2MnO3��0.4LiNi0.8Co0.15Al0.05O2��2.0~4.6 V��ѹ��Χ�ڡ�0.1C��0.2C��0.5C��1C��2C�����µ�ѭ���������ߡ���ͼ10�ɼ���950 ���ºϳɵ���Ʒ�ı�������������0.1C�ŵ籶���£����״ηŵ������Ϊ209.1 mA��h/g������2C�ŵ籶���µķŵ����������156.5 mA��h/g��˵������������850 ��ϳɵ���Ʒ�ı������ܴ�֮��2C�ŵ籶���µı�����Ϊ164.9 mA��h/g��900 ���ºϳɵ���Ʒ����������ã���0.1C��0.2C��0.5C��1C��2C���ʷŵ�ʱ���ŵ�������ֱ�Ϊ229.9��219.2��207.1��193.0��173.1 mA��h/g�����н������ı������ܡ�
��3 ��ͬ�����¶����Ʊ���0.6Li2MnO3��0.4LiNi0.8- Co0.15Al0.05O2��2.0~4.6 V��0.1C�µ��״γ�ŵ�����
Table 3 First charge and discharge data of 0.6Li2MnO3��0.4LiNi0.8Co0.15Al0.05O2 at different calcination temperatures and 0.1C, 2.0-4.6 V

ͼ9 ��ͬ�����¶����Ʊ���0.6Li2MnO3��0.4LiNi0.8- Co0.15Al0.05O2��2.0~4.6 V��0.5C�µ�ѭ����������
Fig. 9 Cycle life curves of 0.6Li2MnO3��0.4LiNi0.8- Co0.15Al0.05O2 at different calcination temperatures and 2.0-4.0 V, 0.5C

ͼ10 ��ͬ�����¶����Ʊ��IJ���0.6Li2MnO3��0.4LiNi0.8Co0.15Al0.05O2�ڲ�ͬ�����±�����������
Fig. 10 Rate capability of 0.6Li2MnO3��0.4LiNi0.8Co0.15- Al0.05O2 at different calcination temperatures and rates
3 ����
1) �����ܽ�-�������Ʊ�������ӵ����������xLi2MnO3��(1-x)LiNi0.8Co0.15Al0.05O2(x=0.5��0.6��0.7)���ò��Ͼ��е��͵Ħ�-NaFeO2��״�ṹ��
2) XRD��SEM�Լ��绯ѧ�������Ա�������ѧ���(x=0.5��0.6��0.7)�������¶�(850 �棬900 �棬950 ��)�Բ��Ͻṹ����ò���绯ѧ�����������Ե�Ӱ�졣
3) ��x=0.6ʱ����900 �������¶��ºϳɵ�0.6Li2MnO3��0.4LiNi0.8Co0.15Al0.05O2��������ĵ绯ѧ���ܡ���2.0~4.6 V��0.1C��ŵ籶���£����״ηŵ�������229.1 mA��h/g���״ο���Ч�ʴ�80.0 %��0.5C������ѭ��100�κ���������������Ϊ83.8%����ʾ�����õ�ѭ�����ܡ�0.6Li2MnO3��0.4LiNi0.8Co0.15- Al0.05O2�������õı������ܣ�2.0C�����µķŵ��������Ϊ173.1 mA��h/g��
REFERENCES
[1] �� ��, ������, ���, ��ʫ��, Ф����. ����ӵ���������ϵ��о���չ[J]. ������ͨ��, 2013, 32(1): 77-84.
WANG Ling, GAO Peng-zhao, LI Dong-yun, HUANG Shi-ting, XIAO Han-ning. Research progress in cathode materials for power Li ion batteries[J]. Bulletin of the Chinese Ceramic Society, 2013, 32(1): 77-84.
[2] �� Ө, �� ��, ����ϼ, �� ʵ, �� ��, �� ��. ����ӵ�ظ�﮹��ɽ�������xLi2MnO3��(1-x)LiMO2(M=Ni, Co��Mn)��������[J]. ��ѧ��չ, 2014, 26(2): 259-269.
BAI Ying, LI Yu, ZHONG Yun-xia, CHEN Shi, WU Feng, WU Chuang. Li-rich transition metal oxide xLi2MnO3��(1-x)LiMO2 (M=Ni,Co or Mn) for lithium ion batteries[J]. Progress in Chemistry, 2014, 26(2): 259-269.
[3] ������, �� ��, ����ƽ, ������, �� ǿ. ����ӵ�ظ���̻��������ϵ��о���չ[J]. ��ع�ҵ, 2014, 19(3): 157-162.
RAO Yuan-yuan, ZENG Hui, WANG Kang-ping, LIU Xing-liang, WANG Qiang. Research states of lithium-rich manganese-based cathode material for Li-ion batteries[J]. Chinese Battery Industry, 2014, 19(3): 157-162.
[4] ���Ͼ�, �뺣��, �Դ���, ������. ����ӵ�ظ����������xLi2MnO3��(1-x)LiMO2(M=Co, Fe, Ni1/2Mn1/2��)���о���չ[J]. ������ѧ��, 2011, 26(7): 673-679.
ZHAO Yu-juan, FENG Hai-lan, ZHAO Chun-song, SUN Zhao-qin. Research progress in Lithium-rich cathode materials xLi2MnO3��(1-x)LiMO2 (M=Co, Fe, Ni1/2Mn1/2��) for power Li ion batteries[J]. Journal of Inorganic Materials, 2011, 26(7): 673-679.
[5] ��ΰ��, ���º�, ��־��, ������. ����ӵ�ظ����������Li[Li0.2Ni0.2Mn0.6]O2���Ʊ������Ӹ���[J]. �й���ɫ����ѧ��, 2013, 23(4): 1047-1052.
ZHU Xiong-wei, LI Xin-hai, WANG Zhi-xing, GUO Hua-jun. Synthesis and modification of Li rich cathode Li[Li0.2Ni0.2Mn0.6]O2 for Li ion batteries[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(4): 1047-1052.
[6] �� ��, ������, �� ��. ����ӵ�ظ���������ϵ��о���չ[J]. �й���ɫ��ѧ��, 2013, 23(3): 215-223.
ZHANG Jie, WANG Jiu-lin, YANG Jun. Research progress in Lithium-rich cathode materials for power Li ion batteries[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(3): 215-223.
[7] �� ��, �� ��, ������, ����ӱ, �� ��, �� ��, �� ʵ. ����ӵ����������xLi2Mn03��(1-x)Li[Nil/3Mnl/3Col/3]02���Ʊ�������[J]. ������ѧѧ��, 2012, 28(7): 823-830.
WANG Zhao, WU Feng, SU Yue-feng, BAO Li-ying, CHEN Lai, LI Ning, CHEN Shi. Synthesis and characterization of lithium-rich cathode materials xLi2Mn03��(1-x)Li[Nil/3Mnl/3- Col/3]O2[J]. Acta Physico-Chimica Sinica, 2012, 28(7): 823-830.
[8] KIM J H, PARK, C W, SUN Y K. Synthesis and electrochemical behavior of Li[Li0.1Ni0.35-x/2CoxMn0.55-x/2]O2 cathode materials[J]. Solid State Ionics, 2003, 164(1): 43-49.
[9] TANG A, HUANG K. Structure and electrochemical properties of Li1+yNi0.5AlxMn0.5-xO2 synthesized by a new sol-gel method[J]. Materials Chemistry and Physics, 2005, 93(1): 6-9.
[10] LEE S H, KOO B K, KIM J C, KIM K M. Effect of Co3(PO4)2 coating on Li[Co0.1Ni0.15Li0.2Mn0.55]O2 cathode material for lithium rechargeable batteries[J]. Journal of Power Sources, 2008, 184: 276-283.
[11] �� ��, ����̩, ����. �����ӵĸ����������Li[Li0.2Mn0.6Fe0.3Al0.1]O2�ĺϳɼ��绯ѧ�����о�[J]. �й���ɫ����ѧ��, 2011, 27(1): 79-83.
WANG Hong, GUO Chun-tai, WANG Da-an. Research in Synthesis and electrochemical performance of Al-doping lithium-rich cathode materials Li[Li0.2Mn0.6Fe0.3Al0.1]O2[J]. The Chinese Journal of Nonferrous Metals, 2011, 27(1): 79-83.
[12] KANG S H, KEMPGENS P, GREENBAUM S, KROPF A J, AMINE K, THACKERAY M M. Interpreting the structural and electrochemical complexity of 0.5Li2MnO3��0.5LiMO2 electrodes for lithium batteries (M=Mn0.52-xNi0.52-xCo2x, 0��x��0.5)[J]. Journal of Materials Chemistry, 2007, 2071: 2069-2077.
[13] JOHNSON C S, KIM J S, LEFIER C, LI N, VAUGHEY J T, THACKERAY M M. The significance of the Li2MnO3 component in composite xLi2MnO3��(1-x)LiMn0.5Ni0.5O2 electrodes[J]. Electrochemistry Communications, 2004, 87(6): 1085-1091.
[14] ARMSTRONG A R, HOLZAPFEL M, NOVAK P, JOHNSHON C S, KANG S H, THACKERAY M M, BRUCE P G. Demonstrating oxygen loss and associated structural reorganization in the lithium battery cathode Li[Ni0.2Li0.2Mn0.06]O2[J]. Journal of the American Chemical Society, 2006, 128(6): 8694-8698.
[15] THACKERAY M M, KANG S H, JOHNSHON C S, VAUGHE J T, BENEDEK R, HACKNEY S A. Li2MnO3-stabilized LiMO2 (M=Mn��Ni��Co) electrodes for lithium-ion batteries[J]. Journal of Materials Chemistry, 2007, 17(5): 3112-3125.
[16] REN Ha-bo, HUANG Yang-hui, WANG Yun-hong, LI Zhong-jing, CAI Ping, PENG Zheng-he, ZHOU Yun-hong. Effects of different carbonate precipitators on LiNi1/3Co1/3Mn1/3O2 morphology and electrochemical performance[J]. Material Chemistry Physical, 2009, 117(1): 41-45.
[17] PARK S H, SUN Y K. Synthesis and electrochemical properties of layered Li[Li0.15Ni(0.275-x/2)AlxMn(0.575-x/2)]O2materialsprepared by sol-gel method[J]. Journal of Power Sources, 2003, 119/121: 161-165.
[18] KIM J M, TSURUTA S, KUMMAGAI N. Electro-chemical properties of Li[Li(1-x)/3CoxMn(2-2x)/3]O2 solid solutions prepared by poly-vinyl alcohol (PVA) method[J]. Electrochemistry Communications, 2007, 9(1): 103-108.
[19] GONG Zheng-liang, LIU Han-san, GUO Xiao-jian, ZHANG Zhong-ru, YANG Yong. Effects of preparation methods of LiNi0.8Co0.2O2 cathode materials on their morphology and electrochemical performance[J]. Journal of Power Sources, 2004, 136(7): 139-144.
[20] SHAJU K M, SUBBA Rao G V, CHOWDARI B V R. Performance of layered Li(Ni1/3Co1/3Mn1/3)O2as cathode for Li-ion batteries[J]. Electrochemical Acta, 2002, 48(2): 145-151.
[21] JIAO Li-fang, ZHANG Ming, YUAN Hua-tang, ZHAO Ming, GUO Jiang, WANG Wei, ZHOU Xing-di, WANG Yong-mei. Effect of Cr doping on the structural, electrochemical properties of Li[Li0.2Ni0.2-x/2Mn0.6-x/2Crx]O2 (x=0, 0.02, 0.04, 0.06, 0.08) as cathode materials for lithium secondary batteries[J]. Journal of Power Sources, 2007, 167(1): 178-184.
(�༭ ������)
������Ŀ������ʡ�ش�Ƽ��ɹ�ת����Ŀ(2012CK1006)������ʡս�������˲�ҵ��Ŀ(2013GK4018)
�ո����ڣ�2014-10-10�������ڣ�2015-03-09
ͨ�����ߣ������ѣ����ڣ���ʿ���绰��0731-58292060�����棺0731-58292061��E-mail��wxianyou@yahoo.com
ժ Ҫ��ͨ���ܽ�-�������ϳ��˺��������������xLi2MnO3��(1-x)LiNi0.8Co0.15Al0.05O2��̽���˻�ѧ���(x=0.5��0.6��0.7��Ħ������)�������¶�(850��900��950 ��)�Բ�����ò���ṹ�����ܵ�Ӱ�졣����XRD��SEM�͵�س�ŵ�����ǶԲ��Ͻ������������͵����ܲ��ԡ�������������Ʊ��IJ��Ͼ��е��͵Ħ�-NaFeO2��״�ṹ����x=0.6�������¶�Ϊ900 ��ʱ�����ϳɵIJ��Ͼ��нϺõ���ò�������ĵ绯ѧ���ܣ���2.0~4.6 V��0.1C��ŵ������£�0.6Li2MnO3��0.4LiNi0.8Co0.15Al0.05O2���״ηŵ�������ɴ�229.9 mA��h/g�����״ο���Ч��Ϊ80.0 %����0.5C������ѭ��100�κ���ŵ��������Ϊ192.7 mA��h/g�����������ʴ�83.8 %����ʾ��������ѭ�����ܡ����⣬������ʾ�����õı������ܣ���2.0C�����£���ŵ��������Ϊ173.1 mA��h/g��


