���±�ţ�1004-0609(2011)02-0450-09
������ϵ��пǦ�Ȼ��ﱥ������ѹ�IJ���
�����ᣬ���л�����ʿ��������գ����Ա�
(�����Ƽ���ѧ ұ������̬����ѧԺ ��̬��ѭ��ұ��������ص�ʵ���ң����� 100083)
ժ Ҫ��
Ϊ�˸��õؿ���Zn��Pb���ؽ��������ڴ��������еĻӷ���Ϊ����Ҫȷ���˽⸴����ϵ��Zn��Pb���ؽ���������ı�������ѹ�ͻ�ȵ���Ҫ������ѧ������Ӧ������Я�����ⶨFeO-CaO-SiO2-Al2O3��ϵ��Zn��Pb�Ȼ���ı�������ѹ�����������������¶Ⱥ����ɷֵȶ�Zn��Pb�Ȼ��ﱥ������ѹ��Ӱ�졣����������ڱ�ʵ��ⶨ�¶��£�Zn��Pb�Ȼ���ı�������ѹ�����¶ȵ����߶����ߣ�������ѹֵ�Ķ������¶ȵĵ���֮��ʽϺõ����Թ�ϵ����ϵ�����ɷ����Ⱥ�FeO��������Zn��Pb�Ȼ���ı�������ѹ�кܴ�Ӱ�죻���ż�Ƚ��͡�FeO�������ߣ�Zn��Pb�Ȼ���ı�������ѹ���������ƣ����ӱ��о������������������Pb�Ȼ�����ȣ��¶Ⱥ����ɷֵȶ�Zn�Ȼ��ﱥ������ѹ��Ӱ���Ϊ���������о���������ݶ����ڴ�����������Ч����Zn��Pb���ؽ����Ļӷ���Ϊ�ṩ���������ݡ�
�ؼ��ʣ�
Zn�Ȼ�����Pb�Ȼ���������Я��������������ѹ��Ӱ��������
��ͼ����ţ�TF 803.1���� ���ױ�־�룺A
Vapor pressure measurements of zinc and lead chlorides in complex system
ZHANG Yan-ling, FU Zhong-hua, LI Shi-qi, WANG Yu-gang, FU Xian-bin
(Key Laboratory of Ecological and Recycle Metallurgy, Ministry of Education, School of Metallurgical and Ecological Engineering, University of Science and Technology Beijing, Beijing 100083, China)
Abstract: In order to effectively control the vaporization behaviors of heavy metals, such as zinc and lead in smelting process, it is necessary to obtain the basic knowledge, such as the saturated vapor pressure and activities of heavy metals in complex system. The transpiration method was used to measure the saturated vapor pressures of zinc and lead chlorides in FeO-CaO-SiO2-Al2O3 system and the effect of influencing factors, such as temperature, slag compositions and so on, was discussed. The results show that the saturated vapor pressures of zinc and lead chlorides increase with the increase of temperature, and the logarithmic value of pressure has a good linear relationship with the reciprocal of the temperature. Additionally, the slag compositions, such as basicity and FeO content, give great influence on the saturated vapor pressure. The low basicity and high FeO content tend to enhance the saturated vapor pressure of ZnCl2 and lead chlorides, while the vapor pressure of ZnCl2 shows a stronger function of temperature and slag composition compared with that of the lead chlorides. The data acquired in this study are able to supply important theoretical foundation for effectively controlling the vaporization of heavy metals in the melting process.
Key words: zinc chlorides; lead chlorides; transpiration method; saturated vapor pressure; influence factors
�������շɻҼ�����ұ�������в����IJ��ַ۳������ؽ�����Zn��Pb��Cd�Ⱥ����ϸߣ��ѱ����������ȷ�涨ΪΣ�շ�������뾭������������ڴ���Ŀǰ��һ�ֱȽ���Ӧ��ǰ���ķ���[1-2]��Ϊ����Ч�ؿ������ڴ���������Zn��Pb���ؽ����Ļӷ���Ϊ����Ҫȷ���˽����������������ϵ�еı�������ѹ�ͻ�ȵ���Ҫ������ѧ�������������շɻҼ���ҵ�۳��г����Ļ��������CaO��SiO2��FeO/Fe2O3��Al2O3��ͬʱ���в���K��Na��S��Cl�Լ��ؽ���Zn��Pb��Cr��[3-5]�������ڴ��������У���Щ�ɷֹ�����һ�����ӵĶ�Ԫ����/������ϵ�������ؽ�����˵���ڸ�����/������ϵ�еı�������ѹ�Ǿ�����ӷ���Ϊ����Ҫ����ѧ����������Zn��Pb���ؽ����ڸ����µĻӷ���Ϊ���о��������д��������������������������еķ����[6-7]���ӷ�����ѧ[8-9]�Լ�����ѧƽ��� ��[10-11]�ȡ����ӿɻ�õ��������������ڸ�����ϵ��Zn��Pb���ؽ����ı�������ѹ����ȵ���Ҫ������ѧ���������˱�������ǰ���о�[12]�л�õIJ��ֽ���⣬��δ������������ı�����
������о�����[13-15]���ڸ��������£��Ȼ�����Zn��Pb���ؽ�������Ҫ�ӷ��������ࡣ����������ǰ���о�[16]�Ļ����ϣ���������Я�������Ի������CaO-SiO2-FeO/Fe2O3-Al2O3��Ԫ��ϵ��Zn��Pb��������ʱ�Ȼ���ı�������ѹ�����������¶Ⱥ����ɷֵ����ض�Zn��Pb�Ȼ��ﱥ������ѹ��Ӱ�졣�ڱ�����ĺ����о��н��ص�̽��Zn��Pb������������ϵ��ʱ���Ȼ��ﱥ������ѹ�IJ�����������������Zn��Pb�Ȼ���֮�估��������֮��ġ����ܵ����Ӧ��������Щ���ݵĻ�ý�Ϊ��Ч�ؿ������ڴ����������շɻҼ���ҵ�۳�������Zn��Pb���ؽ����ķ�����չ����ṩ��Ҫ���������ݡ�
1 ʵ��
������[16]����������Я�����������ʱ�������ѹ��ԭ����ѡ��һ�ֶ��������ڴ��ڲ����¶��µ������Ϸ�������������������������Я�����履��ʱ����������������ķ�ѹ�����ڸ�������ͬ�¶��µı�������ѹ���ڲ����¶������£�������Ʒ�ı�������ѹ��ͨ�����ڻӷ��������Ʒ������ʧ����õ������㹫ʽ���£�
![]() (1)
(1)
ʽ�У�pΪ�������ʵı�������ѹ��Pa��mΪ�ӷ������Ħ��������g/mol��RΪĦ�����峣����8.314 J/(K��mol)��TΪ�¶ȣ�K����mΪ������ʧ��g��VΪ���������m3��
ʽ(1)˵������������ɿ�����T��V��R֮�⣬Ϊ�˵õ�����p����Ҫ��æ�m��mֵ����m���Ժ�����ͨ������ǰ������Ʒ������ã���mֵ�Ļ����Ҫ������ȷ����ӷ����࣬����Ϊ�˱�֤�������ݵ�ȷ�ԣ���Ʒ������ʧ��mӦ����ȫ��Ħ������Ϊm����������ӷ���������ˣ�Ϊ��ʹ�����������Ϊ�����о�������ǰ������������ѧ����ȷ����Zn��Pb����������CaO-SiO2-FeO/Fe2O3-Al2O3��ϵ��ʱֻ��һ��(�����ٵ�)�ӷ���������γɵ��¶������������о�[13, 17]������п����Ҫ�ӷ���������Ϊ����Zn��ZnCl2��Ǧ�Ļӷ�����������ҪΪ����Pb��PbCl��PbCl2���ϸ��¶������£�PbOҲ��ӷ������о��ص�̽�ֵ����������շɻҼ���ҵ�۳����ڴ���������Zn��Pb�Ļӷ���Ϊ���������������о�����һ����ClԪ�أ��о�[14-15]�����������������£�Zn��Pb�Ļӷ����Ȼ���Ϊ������ˣ����о�����ȷ����������ϵ��Zn��Pb�Ȼ���������ɵ��¶����䣬��ͨ������֤�����ڸ��¶������ڳ���Zn��Pb�Ȼ���֮�⣬����������FeCl2�Ļӷ��������Ժ��ԡ�
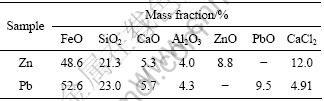
����ѧ������õ���FactSage����ѧ����[18]�����ڼ���˹��������С��ԭ��������ģ�������Zn��Pb�ں�Cl��FeO-CaO-SiO2-Al2O3��ϵ�еĻӷ���Ϊ������ʱʹ�õ���FactSage��������������ѧ���ݿ⣬�궨���������ࡢҺ�ࡢ�����塢����������ȣ��¶�����Ϊ673~1 873 K����ѹ��Ϊ1.01��105 Pa��ָ������Ϊ��Ar����Cl��FeO-CaO-SiO2-Al2O3��ϵ�и�������������1����(��ϵ������ZnO��PbO��ClԪ�ص�Ħ����Ϊ1?2����n(ZnO/PbO)?n(CaCl2)= 1?1)��
��1 ����ѧ�����и���ֵĺ���
Table 1 Mass fraction of each component in thermodynamical calculation
ͼ1(a)��(b)��ʾ�ֱ�ΪZn��Pb���ӷ������¶ȵı仯��ϵ������Ϊ�ӷ����������������Ʒ������Zn��PbԪ�ص���֮�ȡ���ͼ1(a)���Կ�������������Ҫ��ZnCl2����ʽ�ӷ���ZnCl2�Ļӷ������¶ȵı仯Ϊ�����������1 000 K���Ҵﵽ���ֵ��������Zn��1 000 K���¼���û�����ɣ��γɵ�FeCl2������ռ����Ҳ�ܵ͡�ͬ����ͼ1(b)���Կ�����Pb��PbO��1 000 K�¶��¼������ӷ���Pb��Ҫ��PbCl2��PbCl����ʽ�ӷ������Pb��˵��FeCl2�Ļӷ���Ҳ�ϵ͡�����֮�⣬���о���������Ҳ��֤����(1 000��30) K���¶ȷ�Χ�ڣ�����Zn��Pb�������ɣ�������̲μ�����[16]�������������Ʒ�����������۲��ֻ�֤���ڸ��¶�������Χ��û������FeCl2���塣��������о������¶�ѡ��Ϊ(1 000��30) K����ʱZn�Ļӷ�����������ҪΪZnCl2����Pb�Ļӷ�������ҪΪPbCl2��PbCl��
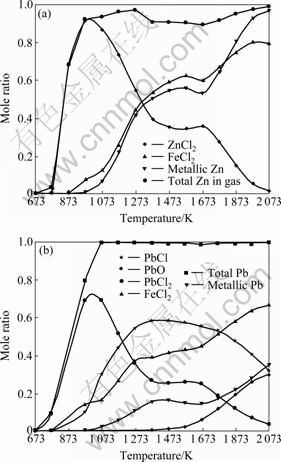
ͼ1 Zn��Pb�ӷ����������¶ȵı仯
Fig.1 Vapor species of zinc and lead as functions of temperature
���о�����Ʒ�Ʊ���Ϊ���������������֡�����ȡ������Ҫ��CaO-SiO2-FeO/Fe2O3-Al2O3�������ټ���ZnO/PbO�Լ�CaCl2(ģ����ϵ�е�ClԪ��)�Լ���֮����ĥ�顢������Ϊ������Ʒ���������������������[16]�����ò�ͬ�����Ļ�ѧ�ɷ����2���С���2�м����ָCaO��SiO2Ũ��֮�ȵĶ�Ԫ��ȡ�
Ԫ��Zn��Pb�ֱ���ZnO��PbO��ʽ���룬��ClԪ����CaCl2����ʽ���롣ZnO/PbO������ij�ʼŨ�ȷֱ�����Ϊ10%��90%������֮��Ϊ5 g��CaCl2������ZnO/PbO��ͬ���ʵ������ӣ�����ʵ����Ʒ �����Ϊ90%��+10%ZnO/PbO+CaCl2(Ħ����n(ZnO/PbO)?n(CaCl2)=1?1)��
ʵ��װ�õ���ơ���װ�Լ�������Ч�Լ�����̲μ�����[16]����װ��ʾ��ͼ��ͼ2��ʾ��
�Դ�ArΪ�������壬ʵ������п���Ar��������ʵ���¶ȡ�ʵ���������Ʒ����Ar�����ı�������ȴ��������ʵ������е���Ʒ������ʧ?m���������鲽�����£�����Ӧ�����֮һ������ƽ�ֱ��������4.5 g��ZnO��PbO��Ʒ0.5 g����Ӧ��CaCl2���������Ⱥ����ڴ����У�����������������m1����������λ��ʹ�䴦��ʯӢ���м䣻Ԥͨ���1 h������������4~5 L/min������¯�ſ�������ֹ��������������ʵ���¶ȣ�������³�����ͼ3��ʾ��������20 min�������¼�����450 ��(��ͼ1������ѧ�������������Ϊ�����¶��»���û�����ʻӷ�)������30 min����15 min�ڽ��¶�����ָ����ʵ���¶ȣ�����ʵ�鴵Ar�����������ֺ���40 min��ʹ����ȴ�����£�ʵ�������ȫ�̴�Ar��ȡ����Ʒ�������Ʒ��������m2����ʵ��������ʧΪ?m=m1-m2��
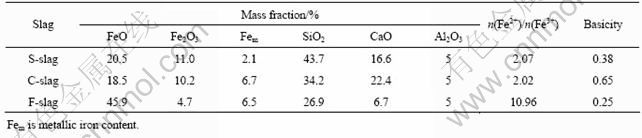
��2 �����и���ֵĺ���
Table 2 Mass fractions of components in slag
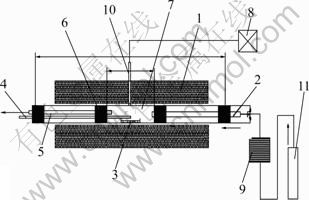
ͼ2 ����װ��ʾ��ͼ
Fig.2 Sketch of equipment: 1��Electric frnace; 2��Gas inlet; 3��Alumina boat; 4��Thermocouple; 5��Gas outlet; 6��Plug; 7��Reaction tube; 8��Temperature controller; 9��Mass flow controller; 10��Thermocouple; 11��Ar
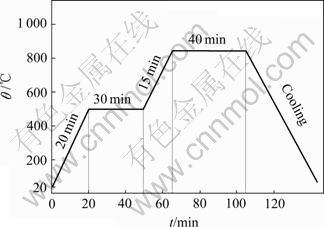
ͼ3 ʵ����³���ʾ��ͼ
Fig.3 Schematic diagram of controlling program of experimental temperature
1.4.1 ��Zn��Ʒ����
������Ʒ��ȴ��ICP�����ӹ������Dz������Ԫ��Zn��Fe��Ũ�ȣ�������ǰZn��Fe���������жԱȣ������ɵõ����������Zn��Fe�Ļӷ������ֱ��ʾΪml(Zn)��ml(Fe)����ǰ��ʵ�鼰����ѧ������֪��Znֻ��ZnCl2����ʽ�ӷ�����������
ml(ZnCl2)=136ml(Zn)/65 (2)
ʽ�У�ml(ZnCl2)ΪZnCl2����ӷ��������Ʒ������ʧ��g��
����������ʧ����ʽ(1)�����ɵõ������¶������¡�������ϵ��ZnCl2�ı�������ѹ��
1.4.2 ��Pb��Ʒ����
ͬ����������Ʒ��ȴ��Ӧ��ICP����������������Pb��Fe�������ɴ˵õ�ʵ��ǰ��Pb��Fe��������ʧ���ֱ��Ϊml(Pb)��ml(Fe)��������ѧ����(��ͼ1(b))��֪���ڱ�ʵ�������£���Ʒ�ӷ�������ΪPbCl2��PbCl���ٲ���FeCl2��������FeCl2�ӷ��������Ʒ������ʧml(FeCl2)�ɱ�ʾΪ
ml(FeCl2)=127ml(Fe)/56 (3)
���ڸ���Ʒ��Pb�Ļӷ���������ΪPbCl��PbCl2��Ϊ�˼���������о����Ե���PbCl��PbCl2������ܵ�����ѹ�����ս��ɸ���PbԪ�ص�������ʧ����ʽ(1)�ɼ�����ߵ�����ѹ֮�͡������Ƶ�����������ʾ��
1) �ٶ�p1��?m1��m1�ֱ����PbCl�ı�������ѹ���ӷ��������Ʒ������ʧ��Ħ��������
2) p2��?m2��m2�ֱ����PbCl2�ı�������ѹ���ӷ��������Ʒ������ʧ��Ħ��������
��������Я�����IJ���ԭ����ʽ(4)��(5)������
p1=?m1RT/(m1V) (4)
p2=?m2RT/(m2V) (5)
����ߵ�������ѹpΪ
p= p1+ p2=(?m1/m1+?m2/m2)RT/V=(n1+n2)RT/V=
nPbRT/V=?m(Pb)RT/m(Pb)V (6)
ʽ�У�n1��n2��nPb�ֱ�ΪPbCl��PbCl2�Լ��ӷ�����Pb��Ħ������?m(Pb)ΪPbԪ�صĻӷ�������Ϊml(Pb)��g��m(Pb)ΪPb��Ħ��������207 g/mol��VΪЯ�����������m3��
�����ڱ������о��У���ʽ(6)��������ǰ��PbԪ��������ʧ�õ�PbCl/PbCl2����������ѹ��
���⣬����Pb�ӷ�������PbCl��PbCl2�ı���������PbԪ�ػӷ����ߵ�Cl������Pb�����ı�ֵ������n(Cl)/n(Pb)�����Թ��ƣ�n(Cl)/n(Pb)��ֵ��ʽ(7)����õ���n(Cl)/n(Pb)ֵԽ��˵��PbCl2��ռ����Խ�ߣ���֮��PbCl����Լ���������»����n(Cl)/n(Pb)ֵ����2�����������Ҫ�����ڷ���������£���
![]() (7)
(7)
ʽ�У�?mΪʵ���������Ʒ������ʧ������g��
1.4.3 ��������������������
������F�������µķ�������Ϊ�������۱��о��������õķ�������������������������3����Ϊ������������ñ����������õ��ĸ����ʻӷ��������к�Pb��Ʒ�У�����Pb��PbCl��PbCl2������ʽ�ӷ������ӷ������������ʧ��PbCl1.5��ʽ���㣬��
ml(PbCl1.5)=255ml(Pb)/207 (8)
��ˣ���Zn��Ʒ����Pb��Ʒ���ɱ��������������������ǿɷֱ���ʽ(9)��(10)�õ�
![]() (9)
(9)
![]() (10)
(10)
��3 �����ʵĻӷ������������
Table 3 Amount of each volatile specie and analysis error
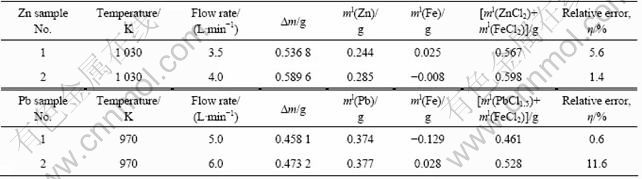
����ml(FeCl2)����ָ�ֵ����Ҫԭ����ICP���������������������õ����������Ʒ��FeԪ�غ���ƫ�ߣ������������ΪFeCl2�ӷ���Ϊ�㡣
�ӱ�3���Կ���������Ʒ��������õ�����Ʒʧ����ʵ��ʧ��֮����������С(0.6%~5.6%)��˵�������������������õ��������ǿɿ��ġ�����Pb��Ʒ��������ﵽ��11%���ң�����Ҫԭ����Pb�Ȼ���Ļӷ�����PbCl1.5��ʽ���㣬��ʵ���������п���PbCl��ռ�����ϸ߶�PbCl2�����ͣ������PbCl1.5��ʽ����õ��ķ���������ʧ��ʵ�����ƫ�����¡�
ͬʱ�ɱ�3Ҳ���Կ�������������FeCl2�ӷ����dz�С(��3��ml(Fe)��ֵ��С)���������Ժ��ԣ�����ǰ�ĵ�����ѧ��������һ�¡�
2 ����������
������Я�����IJ���ԭ����֪�����������Я�����������Ƿdz���Ҫ�IJ�����Ϊ�˱�֤�������ʵ�������Я�������дﵽ���ͣ���ֹ�����ͻ�δ�����������������ҵ�һ�����е��������䣬�ڴ������ڣ�����������������ѹ(������ѹ)��Я������������أ������������²�õ�����ѹֵ��Ϊ�������¶������´������ʵı�������ѹ��
�ڱ��о��У����ÿ�������µ����鶼Ҫ�ڲ�ͬ�����½��У�����õ����������صķ�ѹ���Ǹ��������´�����Ʒ�ı�������ѹ��ͼ4(a)��(b)��ʾ�ֱ�Ϊ��Zn��Ʒ�뺬Pb��Ʒ��ʵ�������ں�Zn��Ʒ���ԣ��ڶ�Ӧ�����£�3~4.5 L/minΪ���ʵ��������䣬�������ڶ�Ӧ������ѹΪ�������µ�ZnCl2������ѹ�������ں�Pb��Ʒ���ԣ�6~6.5 L/minΪ��Ӧ�����µĺ��ʵ����ٿռ䣬���Ӧ������ѹΪ��������PbCl/PbCl2���ߵ�����ѹ֮�͡�
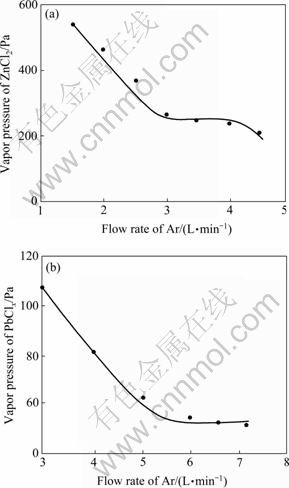
ͼ4 ZnCl2����ѹ��Ar���ٵĹ�ϵ����PbCl/PbCl2����ѹ��Ar���ٵĹ�ϵ
Fig.4 Relationships among vapor pressure of ZnCl2 and flow rate of Ar(a) and vapor pressure of lead chlorides versus flow rate of Ar(b)
2.2.1 �¶ȵ�Ӱ��
��ͬ�¶�������C����ZnCl2��������ѹ���¶ȵĹ�ϵ��ͼ5��ʾ��
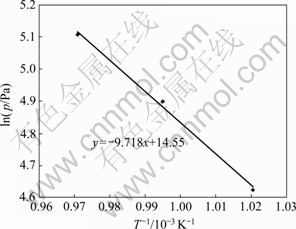
ͼ5 C����ZnCl2��������ѹ���¶ȵĹ�ϵ
Fig.5 Saturated vapor pressure of ZnCl2 versus temperature in C-slag
��ͼ5���Կ�����ZnCl2�ı�������ѹ���¶ȵ����Ӷ��������ߣ�����980~1 030 K�¶���CaO-SiO2-FeO-Al2O3��ϵ��ZnCl2�ı�������ѹ�Ķ������¶ȵĵ���֮������Ե�ֱ�߹�ϵ����ʽ(11)��ʾ��ǰ�˵��о�Ҳ���������Ƶı仯����[19]��
ln p = -9 718/T+14.55 (11)
2.2.2 ���ɷֵ�Ӱ��
��ͬ��ϵ��ZnCl2�ı�������ѹ��ͼ6��ʾ��ͼ�����������ݷֱ�ΪFeO�����ͼ��R��
��ͼ6���Կ�������ϵ��������������ɷֶ�ZnCl2��������ѹ������Ӱ�졣��ZnCl2����ѹ�ɴ�С�����˳��ΪF����ϵ��S����ϵ��C����ϵ��F����ϵ��ZnCl2�ӷ�������ǿ�ɹ��Ϊ��������ԭ��1) F�������ͣ�ZnCl2���ɷ�Ӧ����ʽ(12)��ʾ���ͼ�������ڽ�����ϵ��CaO��ȣ������ٽ���Ӧʽ(12)���ҽ��У����⣬ǰ�˵��о����������м��Խ��Cl���Խ��[20-21]����˸�Ȼ������Ȼ���ӷ���2) F��������ߵ�FeO��������ϵ�нϸߵ�FeO���������ZnO��ȣ�������Ч�ٽ�ZnCl2�γɺͻӷ�(ʽ(12))������C����S����ϵ�Ľ������������������FeO��������(�ֱ�Ϊ18.5%��20.5%)����ZnCl2������ѹֵ����һ���̶ȵIJ����Ҫԭ����S����ϵ�м�Ƚϵͣ�ʹ��S����ϵ��ZnCl2�ı�������ѹ���Ա�C����ϵ�д�˵�����ɷ��У���ȶ�ZnCl2����ѹ��Ӱ���FeO������������
ZnO+CaCl2=CaO+ZnCl2 (12)
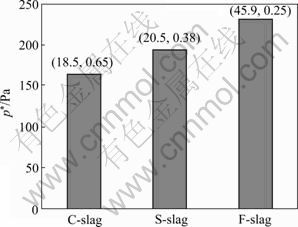
ͼ6 ��ͬ����ϵ��ZnCl2�ı�������ѹ
Fig.6 Saturated vapor pressure of ZnCl2 in different kinds of slag
2.3.1 �¶ȵ�Ӱ��
�ڲ�ͬ�¶������£�C����ϵ��PbCl/PbCl2����ѹ���¶ȵı仯��������ͼ7��ʾ����ͼ7���Կ�����PbCl/PbCl2����ѹ���¶����߶����ߣ���PbCl/PbCl2
����ѹ�Ķ������¶ȵĵ���֮��Ҳ���ֽϺõ����Թ�ϵ����
ln p = -3 315/T+7.236 (13)
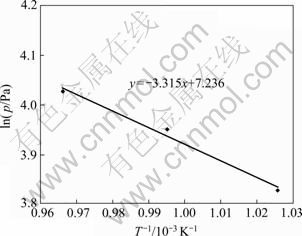
ͼ7 C����Pb�Ȼ��ﱥ������ѹ���¶ȵı仯
Fig.7 Change of saturated vapor pressure of lead chlorides with temperature in C-slag
ͨ����ZnCl2�ȽϿ�֪(��ͼ5)��PbCl/PbCl2������ѹ���¶����߶����ߵķ�����Խ�С��ͼ8��ʾΪ��C����ϵ��n(Cl)/n(Pb)���¶ȵı仯��ϵ����ͼ8���Կ�����n(Cl)/n(Pb)���¶����߶����ͣ�˵������������������PbCl���γɣ��Ӷ�����PbCl2�����ɣ�����ǰ������ѧ����Ľ��(��ͼ1(b))��һ�¡������ڴ�PbCl2���ʵı�������ѹ�ȴ�PbCl��[22]������ͬ����������£���FeO-CaO-SiO2-Al2O3��ϵ�����ʱ��PbCl����ѹҪ��PbCl2�ĵ͡���ˣ������¶ȵ����ߣ�PbCl�������ߣ��ᵼ��C����ϵ��PbCl/PbCl2��������ѹ֮�����¶����߶�����ij̶����ޣ���Ҳ����ZnCl2��ȣ�PbCl/PbCl2����ѹ���¶ȱ仯���仯���Ƚϲ����Ե���Ҫԭ��
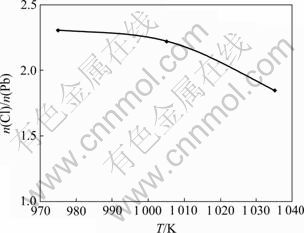
ͼ8 ��C����ϵ��n(Cl)/n(Pb)���¶ȹ�ϵ
Fig.8 Relationship between n(Cl)/n(Pb) and temperature in C-slag
2.3.2 ���ɷֵ�Ӱ��
ͼ9��ʾΪ��ͬ����ϵ��PbCl/PbCl2����ѹ�ı仯��ͼ�����������ݷֱ�ΪFeO��Fe2O3�����Լ����R��
��ͼ9���Կ�������ϵ�е����ɷֶ���PbCl/PbCl2������ѹ��һ��Ӱ�졣��PbCl/PbCl2����ѹ��С�������ɴ�С��˳����ZnCl2�е������ͬ����F����ϵ��S����C����ͬ����F����ϵ��PbCl/PbCl2�ӷ�������ǿ�ɹ��Ϊ��������ԭ��1) F�������ͣ�PbCl2��PbCl�����ɷ�Ӧ�ɷֱ���ʽ(14)��(15)��ʾ���ͼ�������ڽ�����ϵ��CaO��ȣ������ٽ�ʽ(14) ��(15)���ҽ��У�������������Cl�Ļ�ȳ��½�����[20-21]��Ҳ˵�����ͬ��������Pb�Ȼ���ӷ���2) F��������ߵ�FeO������һ�����FeO������ٽ�ʽ(14)���ҽ��У���һ����FeO�����������PbO����ϵ�еĻ�ȣ�������Ч�ٽ�Pb�Ȼ�����γɺͻӷ�����
PbO+CaCl2=PbCl2+CaO (14)
2PbO+CaCl2+2FeO=PbCl+Fe2O3+CaO (15)
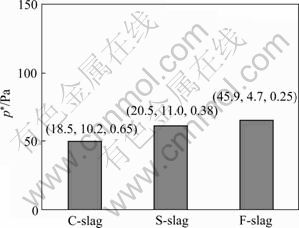
ͼ9 ��ͬ����ϵ��Pb�Ȼ��������ѹ
Fig.9 Saturated vapor pressure of lead chlorides in different kinds of slag
ͼ10��ʾΪ��ͬ��ϵ������n(Cl)/n(Pb)ֵ�治ͬ��ϵ�ı仯���(ͼ�����������ݷֱ�ΪFeO������R)����ͼ10���Կ�����n(Cl)/n(Pb)�ɴ�С�ݼ���˳��ΪC����S����F����˵��F����ϵ��PbCl��ռ������ߣ���C����ϵ��PbCl2������ߡ���ԭ��������£���C����S����ȣ�F���нϸߵ�FeO�������ƶ�ʽ(15)���ҽ��У������ٽ�PbCl�����ɡ������Ͻ���F�������ͣ���Ӧ���������о������֪��Cl������[20-21]����PbCl��ȣ�PbCl2������Ӧ�ø�Ϊ��������ʵ�ʽ��������ˣ�˵�������ɷ��У�������ȣ�FeO������Pb�Ȼ�����������(PbCl��PbCl2)��Ӱ���Ϊ���ԡ�
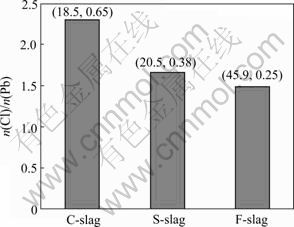
ͼ10 975 Kʱn(Cl)/n(Pb)������ɵı仯
Fig.10 Change of n(Cl)/n(Pb) with slag components at 975 K
���⣬��ͼ7 ZnCl2������ѹ�����ɷֵı仯�����ȣ�ͼ9��ʾ��PbCl/PbCl2�ܵ�����ѹֵ�����ɷֱ仯���Ƚ�С����ԭ�����ڲ�ͬ����ϵ�У�PbCl��PbCl2�ı��������˱仯����Ȼ��F���У��ͼ�Ⱥ�FeO������������Pb�Ȼ�����γɺͻӷ�������C����S����ȣ�����PbCl��ռ�����ϸߣ�����PbCl2��ȣ�PbCl����ѹ�ϵͣ���ʹF����ϵ��PbCl/PbCl2���ߵ�����ѹ֮�����ӷ������ޡ���ˣ���ͬ��ϵ�����ɷ���Ȼ��PbCl��PbCl2���ɱ�����һ��Ӱ�죬���Զ��ߵ�����ѹ֮��Ӱ����Ȳ�����
3 ����
1) ��970~1 030 K�¶������£�������ϵ��ZnCl2��PbCl/PbCl2����ѹ���¶����Ӷ����ӣ��Ҷ�������ѹ�Ķ������¶ȵĵ���֮��ʽϺõ����Թ�ϵ��
2) �ں�Pb��Ʒ�����У�n(Cl)/n(Pb)���¶����߶����ͣ�˵����������������PbCl���γɣ�������PbCl����ѹ��PbCl2����Ƚϵͣ���ˣ�PbCl/PbCl2����ѹ���¶��������ӵķ�����ZnCl2����Ƚ�Ϊ�����ԡ�
3) ���ɷֶ���ZnCl2��PbCl/PbCl2����ѹ������Ӱ�졣�ڲ�ͬ��ϵ�У�ZnCl2��PbCl/PbCl2����ѹֵ�ɴ�С�ݼ���˳��ΪF����S����C��������Ҫԭ����F���нϵ͵ļ�ȣ��ϸߵ�FeO������ٽ�Zn��Pb�Ȼ�����γɺͻӷ���
4) �ں�Pb��Ʒ�������У�n(Cl)/n(Pb)��С���� ������˳��ΪF����S����C����˵����FeO����������PbCl���γɣ�������ڼ�ȶ��ԣ�FeO������Pb�Ȼ������������Ӱ���Ϊ������
REFERENCES
[1] CHOU S Y, LO S L, HSIEH C H, CHEN C L. Sintering of MSWI fly ash by microwave energy[J]. Journal of Hazardous Materials, 2009, 163(1): 357-362.
[2] REIJNDERS L. Disposal, uses and treatments of combustion ashes: A review[J]. Resources, Conservation and Recycling, 2005, 43(3): 313-336.
[3] YOO J M, KIM B S, LEE J C, KIM M S, NAM C W. Kinetics of the volatilization removal of lead in Electric Arc Furnace dust[J]. Materials Transactions, 2005, 46(2): 323-328.
[4] HUANG S J, CHANG C Y, MUI D T, CHANG F C, LEE M Y, WANG C F. Sequential extraction for evaluating the leaching behavior of selected elements in municipal solid waste incineration ?y ash[J]. Journal of Hazardous Materials, 2007, 149(1): 180-188.
[5] JUNG C H, OSAKO M. Thermodynamic behavior of rare metals in the melting process of municipal solid waste (MSW) incineration residues[J]. Chemosphere, 2007, 69(2): 279-288.
[6] JAKOB A, STUCKI S, KUHN P. Evaporation of heavy metals during the heat treatment of municipal solid waste incinerator fly ash[J]. Environ Sci Technol, 1995, 29(9): 2429-2437.
[7] WOBST M, WICHMANN H, BAHADIR M. Distribution behavior of heavy metals investigated in a laboratory-scale incinerator[J]. Chemosphere, 2001, 44(5): 981-987.
[8] ABANADES S, FLAMANT G, GAUTHIER D. Kinetics of heavy metal vaporization from model wastes in a fluidized bed[J]. Environ Sci Technol, 2002, 36(17): 3879-3884.
[9] FALCOZ Q, GAUTHIER D, ABANADES S, FLAMANT G, PATISSON F. Kinetic rate laws of Cd, Pb, and Zn vaporization during municipal solid waste incineration[J]. Environ Sci Technol, 2009, 43(6): 2184-2189.
[10] �� �, ������, ɽ����. �������ջ������ڴ����ؽ�������-�ӷ���Ӧ����[J]. ������ѧѧ��, 2005, 26(9): 874-877.
WANG Nan, ZOU Zong-shu, YAMAGUCHI S. Thermodynamic analysis of chlorination-evaporation of heavy metals during melting of ash from municipal waste incineration[J]. Journal of Northeastern University, 2005, 26(9): 874-877.
[11] ABANADES S, FLAMANT G, GAGNEPAIN B, GAUTHIER D. Fate of heavy metals during municipal solid waste incineration[J]. Waste Manage Res, 2002, 20 (1): 55�C68
[12] SAKAI S, HIRAOKAB M. Municipal solid waste incinerator residue recycling by thermal processes[J]. Waste Management, 2000, 20(2): 249�C258
[13] RIO S, VERWILGHEN C, RAMAROSON J, NZIHOU A, SHARROCK P. Heavy metal vaporization and abatement during thermal treatment of modified wastes[J]. Journal of Hazardous Materials, 2007, 148(3): 521-528.
[14] WANG K S, CHIANG K Y, CHU W T. Fate and partitioning of heavy metals affected by organic chloride content during a simulated municipal solid waste incineration process[J]. Journal of Environmental Science and Health, 1997, A32(7): 1877-1893.
[15] CHAN C C Y, KIRK D W. Behaviour of metals under the conditions of roasting MSW incinerator fly ash with chlorinating agents[J]. Journal of Hazardous Materials, 1999, B64(1): 75-89.
[16] ���л�, ������, �����, ��ʿ��, ���Ȼ�. ������ϵ�����ʱ�������ѹ����װ�õ���Ƽ���Ч�Լ���[J]. �й���ɫ����ѧ��, 2010, 20(7): 1433-1439.
FU Zhong-hua, ZHANG Yan-ling, WANG Yu-gang, LI Shi-qi, HAN Xian-hui. Designing and testing of the apparatus to measure matter��s saturated vapor pressure in complex system[J]. The Chinese Journal of Nonferrous Metals, 2010, 20(7): 1433-1439.
[17] ABANADES S, FLAMANT G, GAGNEPAIN B, GAUTHIER D. Fate of heavy metals during municipal solid waste incineration[J]. Waste Manage Res, 2002, 20(1): 55-68.
[18] BALE C W, CHARTRAND P, DEGTEROV S A, ERIKSSON G, HACK K, MAHFOUD R B, MELAN?ON J, PELTON A D, PETERSEN S. FactSage thermochemical software and databases[J]. CALPHAD, 2002, 26(2): 189-228.
[19] ZHANG Yan-ling, SHIBATA E, KASAI E, NAKAMURA T. Vapor pressure of zinc and chloride in the FetO-CaO-SiO2-Al2O3 slag system[J]. Materials Transaction, 2006, 47(5): 1341-1346.
[20] MIWA M, MORITA K. Chloride capacities of CaO-SiO2- A12O3(-FeO, MgO, MnO) slags and their application in the incineration processes[J]. ISIJ Int, 2002, 42(10): 1065-1070.
[21] HIROSUMI T, MORITA K. Solubility of chlorine in alumino silicate slag systems[J]. ISIJ Int, 2000, 40(10): 943-948.
[22] ���л�, ������, �����, ��ʿ��. ���������·ɻ���Zn��Pb�Ļӷ���Ϊ����Ӱ������[J]. ���̹���ѧ��, 2009, 9(S1): 473-481.
FU Zhong-hua, ZHANG Yan-ling, WANG Yu-gang, LI Shi-qi. Vaporization behaviors of Zn and Pb in fly ash and the effects of influential factors in smelting process[J]. The Chinese Journal of Process Engineering, 2009, 9(S1): 473-481.
������Ŀ��������Ȼ��ѧ����������Ŀ(50704004)����������ʿ��(�½�ʦ)����������Ŀ(20070008004)����ѧ���������������������Ŀ
�ո����ڣ�2009-12-19�������ڣ�2010-03-09
ͨ�����ߣ������ᣬ�����ڣ���ʿ���绰��13699223791��E-mail: zhangyanling@metall.ustb.edu.cn


