���±��: 1004-0609(2005)12-1974-06
����ǰ�����Ʊ�AlN�մɷ�ĩ
������1, ��ѧ��1, 2, �� ˧1, �� ΰ1, ��ѡ��1, 3
(1. �����Ƽ���ѧ ���Ͽ�ѧ�빤��ѧԺ, ���� 100083; 2. ���������ѧ ���Ͽ�ѧ�빤��ѧԺ, ��� 300191;
3. ���ϴ�ѧ ��ĩұ������ص�ʵ����, ��ɳ 410083)
ժ Ҫ��
����������̼��Ϊԭ��, ���û�ѧ�������Ʊ�����Ͼ��ȵ�Al2O3+Cǰ����, ���Ը�ǰ����Ϊԭ�ϲ���̼�Ȼ�ԭ���Ʊ���AlN��ĩ�� �о��˵�����Ӧ�¶ȡ� pHֵ�� ������Լ��� ��ҺŨ�ȡ� ����������̼���ȵȹ��ղ����Ե�����Ӧ��Ӱ��, �ó�����ѹ��ղ����ֱ�Ϊ: ��0.4mol/L����������Һ�ͱȱ����Ϊ156m2/g��̼��Ϊԭ��, ����ԭ����̼����Ϊ3��1, ����������Ӳ֬��(SA)�;��Ҷ���(PEG)��Ϊ������Լ�, ���Ƴ���������pH=9, ͨ�����������յõ���ɢ�Ժá� �ž۳̶�С��ǰ����, ������ǰ�����ڳ�ѹ�͵�������Ϊ5L/min����������1550������4h, ���Ӧ������650��Ŀ����г�̼4h, �Ʊ���������Ϊ33.20%, ������Ϊ0.98%, �ȱ����Ϊ4.26m2/g��AlN��ĩ��
�ؼ���: AlN��ĩ; ����ǰ����; ̼�Ȼ�ԭ ��ͼ�����: TB484.5
���ױ�ʶ��: A
Preparation of AlN powders from precipitated precursor
QIN Ming-li1, DU Xue-li1, 2, LI Shuai1, SUN Wei1, QU Xuan-hui1, 3
(1. School of Materials Science and Engineering,
University of Science and Technology Beijing, Beijing 100083, China;
2. School of Materials Science and Engineering,Tianjin University of Technology, Tianjin 300191, China;
3. State Key Laboratory of Powder Metallurgy,Central South University, Changsha 410083, China)
Abstract: A homogenous mixture precursor of Al2O3+C was prepared by the chemical precipitation method and AlN powders were fabricated by carbon thermal reduction nitridation of the precipitated precursor. The effect factors on the nitridation conditions and the properties of AlN powders, including nitridation temperature, pH value, surface active agent, solution concentration, N2 flow rate and molar ratio of carbon to aluminum, were investigated. An optimal process was obtained through synthesizing fine and pure AlN powders. Firstly, a homogenous and good dispersion precursor was prepared by the precipitation process using 0.4mol/L Al(NO3)3 solution and 156m2/g carbon black as materials at pH=9, the molar ratio of carbon to aluminum was controlled to 3��1 and a certain amount of stearic acid and ethylene glycol was added as surface active agents. Then, the precursor was heated at 1550�� for 4h under common pressure at N2 flow rate of 5L/min. Finally, AlN powders with nitrogen content of 33.20%, oxygen content of 0.98%, specific surface area of 4.26m2/g were produced after decarbonization of the nitridation products in air for 4h at 650��.
Key words: AlN powders; precipitated precursor; carbothermal reduction
������(AlN)�����ȵ��ʸ� (�����ȵ���Ϊ320W��m��K, ʵ��ֵ�ɴ�260W��m��K, Ϊ�������մɵ�10~15��)�� ��糣����(ԼΪ8.8)�� ���Ե�Կɿ�(������>1016 ����m)�� ���¡� ��ʴ�� ���� ���õ���ѧ�����Լ������ƥ���������ϵ��(20~500��, 4.6��10-6 K-1)��һϵ����������, �Ǽ������������������һ�����ܶȼ��ɵ�·�߹��ʵ��������������Ƭ�ͷ�װ����, ���ڵ��ӹ�ҵ�е�Ӧ�������ܵ�����[1-3]�� AlN��ĩ���Ʊ������ж���, ����̼�Ȼ�ԭ���ϳɵķ�ĩ�ڴ��ȡ� �����Լ��ȶ��Եȷ���ռ�ϴ����ơ� ����, �÷���Ҳ���ڲ���֮��, ���������ԭ�����ڻ�Ͼ���, ��Al2O3��̼�ڵ�����Ҫ��ϸ�, ��Ӧ�¶ȸ�, �ϳ�ʱ�䳤, ��˳ɱ��ߡ� Ϊ�˸��Ƶ�����������߷�ĩ����, ���ǽ����˴������о�����, �����о�����[3-5], ԭ�ϵ����ࡢ �����Լ���ϵľ��ȳ̶ȶ�̼�Ȼ�ԭ���ķ�Ӧ�¶Ⱥͷ�ĩ��������ҪӰ��, ѡ��ͬ�����ԭ�ϺͲ�ͬ�Ļ��Ϲ���, �����¶ȿ������200�����ҡ� ���, ѡ����ʵ�ԭ���Լ�����Ʊ�����ϸС�� ��ɢ���ȵķ�Ӧǰ�����ѳ�Ϊ̼�Ȼ�ԭ���ϳɵ������մɷ�ĩ�Ĺؼ�����֮һ��
ͨ����ѧ�����Ʊ� Al2O3+C ���ǰ������Ը�����������ĩ��̼�����Ի�ϵ�ȱ��, �������Դ��̼Դ��ϵľ�����, ͬʱ��С��ԭ�ϵ�����, ʹ����������ֱ�ӽӴ���Ӧ, �Ӷ�����˷�Ӧ����, �����˷�Ӧ�¶�[6]�� ʪ��ѧ���ϳɷ�������Һ�������ɿ���, ͨ�������ʵ��Ĺ�������, ���������ߴ��� ��ϸ�� �ž۳̶�С�� �ɷ־�ȷ�����ȵķ���[7, 8]�� ���ھ��������ص�, ʪ��ѧ���ѱ��㷺�����Ʊ������մɷ�ĩ, ���г��������ڹ��ռ�, �ʺϹ�ģ������, ���ڹ�ҵ�����еõ��㷺Ӧ��[9-11]�� �봫ͳ����������̼��Ϊԭ�Ϻϳɵ�������ĩ�Ĺ�����Ƚ�, ���ó������Ʊ���Al2O3+C���ǰ����, ������������Դ��̼Դ�ij�ַ�ɢ���, ����ʡȥ�������������������������չ���, �����˹���, �����˳ɱ���
1 ʵ��
ʵ��ԭ����Ҫ��: ������������(Al(NO3)3��9H2O); �ߴ���ҵ̿��(�ۺ�), �ҷ�С��0.05%, �ȱ����Ϊ156m2/g; ��ˮ, ����(CO(NH2)2), ���Ҷ���(PEG), Ӳ֬��(SA)��
�������Ƴ��ʵ�Ũ�ȵ���������Һ, ��һ������ȼ�������������, ��80~90��ʱ����ˮ��, ����������PEG��Ϊ������Լ�, ��ɢ���á� ��̼�ڼ��백ˮ��Һ��, �Ʊ����ȶ�������Һ, ����������ˮ������Һ�μӵ�������̼�ڵİ�ˮ��Һ�С� ������Ӧ������, �����ý�״�����ᆳ���ˡ� ϴ�ӡ� ��� ���顢 ��ɸ������õ�ǰ���
ǰ����ĵ�����Ӧ����ʽ̼��¯�н��С� ����ˮ������ǰ��������ʯī������װ¯, �Ƚ�¯�ڳ����, �õ���ϴ¯��, ά��¯��������������, ��ǰ���������������м�����1250~1650����з�Ӧ, ��Ӧ������600~700��Ŀ����н�����̼������õ�AlN��ĩ��
��ͬ�¶��µ������������������ձ���3014-Z2��X�����������Ͻ���(XRD), Cu K�����䡣 ����JSM-5600LU ��ɨ��羵�۲���������Ⱥ���ò(SEM)�� ����ST-03�ͱȱ�����ⶨ�Dzⶨǰ���P��Ӧ����ıȱ����(BET)�� ���ü��ܷ��ⶨ��ĩ������, SP-2304����ɫ���Dzⶨ�������� �������� ������������������ ����ԭ�Ӽ��������ⶨ����Ԫ�غ���(ICP)��
2 ���������
2.1 ǰ���ﵪ����Ӧ�����е����
ͼ1��ʾΪ�Գ������Ʊ���ǰ����Ϊԭ��ʱ,
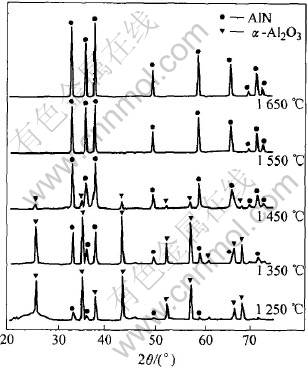
ͼ1 ����ǰ������ϵ������Ӧ���̵�X��������
Fig.1 XRD patterns of precipitated precursor during nitridation process
��ͬ�¶��·�Ӧ3h��Ӧ�����X���������ס� ��ͼ1���Կ���, ��1250��ʱ, ������Ϊ��-Al2O3, ���ᾧ������, ������Թ۲쵽�����������, �������������ǿ�ȼ��㵪��������Ժ���ԼΪ17%; ��1350��ʱ, ������������ǿ, ��-Al2O3�ᾧ����; ���¶�Ϊ1350~1450��ʱ, �����������Ѹ����ǿ, ������������ǿ������, �������������1550����ȫ��ʧ��ת��Ϊ�������� ֱ�Ӳ��æ�-Al2O3��̼��Ϊԭ��ʱ, ��Ҫ����1600��ķ�Ӧ�¶�, ��Ӧʱ����������5h, ���ó���ǰ����Ϊԭ���Ʊ���������ĩʱ, ���Խ����˷�Ӧ�¶�, �ӿ��˷�Ӧ���ʡ�
2.2 pHֵ��Ӱ��
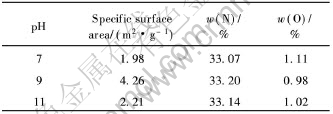
����Al(OH)3Ϊ���Ի�����, �ȿ���������, �ֿ������ڼ�, ���, ��Ҫ����������ȫ����, ��Ҫ��ֹ���ɵij��������ܽ�, �Ӷ������Դ����ʧ, ���Ƴ�����������Һ��pHֵ��һ���ؼ����ء� ����������̼�ڰ���C��AlĦ����Ϊ3��1�������ϡ� ��1����Ϊ��������pHֵ��ǰ�����ĩ��C/Al��Ӱ�졣 �ɱ�1�ɼ�, ����pHֵ������, ����ǰ�����C/Al������, ������Դ�����ܽ����ʧ�������ӡ�
��1 pHֵ�Գ���ǰ������C/Al��Ӱ��
Table 1 Effects of pH value on C/Al of precipitated precursor

��2����Ϊ��ͬpHֵʱ�ϳɵĵ�������ĩ�ıȱ�����͵��� �������� �ɱ�2���Կ���, ��pHΪ9ʱ, ����ǰ�����кϳɵĵ�������ĩ�ȱ�������, Ϊ4.26m2/g; ����pHΪ7��11ʱ, �ϳɵĵ�������ĩ�ıȱ������С�� �ڳ���������, pHֵ����Ӱ���������ĵ�ɷֲ�״��, ����һ��Ӱ�콺�����������ٺͿ����ž۳̶ȡ� ��ͬpHֵ��ҪӰ�����ǰ������Al(OH)3���ӵijߴ�, ����һ��Ӱ�쵪������ĩ�����ȡ�
��ȻpHֵ�Ժϳɵ�������ĩ��������Ӱ��, ���Է�ĩ��, ������Ӱ�첻��, ��1550�淴Ӧ4h��, ��ĩ�ĵ�����������33%, ����������1%����, ��˵������ǰ��������Դ�����Ȳ���Ӱ�쵪����Ӧ�Ĺؼ�����, ��ǰ������Դ���ڵ�״̬����Ӱ�쵪����Ӧ���ʵĹؼ����ء�
��2 pHֵ��AlN��ĩ���ܵĹ�ϵ
Table 2 Relationship between pH value and properties of AlN powders
2.3 ������Լ�������
��ʪ����ѧ��, ������Լ��Ƿ�ֹ��ĩ�ž۵�һ����Ҫ��ʩ�� �ڷ�Ӧ��ϵ�м�������������Լ���, һ���������Լ������������ӱ���, ʹ���Ӽ�����ݼ�������, ��С���ӵı�������; ��һ����, ������Լ��������������γɵ�ǰ��������Ϻ�, ���Լ������桪OH�ļ�������, ��������ķǼ����ǻ�������ˮ���θ���, ��Ч�ط�ֹ����Ԥ�չ�����������ˮ������ëϸ������ɵ�Ӳ�žۡ� ���, ����Һ�����������Լ���, �����ڽ��������γɱ�����������ռ�λ��ЧӦ, �Ӷ���߿����ķ�ɢ����, ���ӽ�����ȶ���, ʹ��������ϸС, ��ֹ�������žۡ� ����, ����̼��Ϊ��ˮ������, ��Al(OH)3����Ϊ��ˮ������, ̼����Al(OH)3�������Բ�ͬ, ���ߺ��ѽ�Ͻ���, ��Ҫ�����ڱ�����Լ������ÿ���ʵ�ֽ�����̼���Ľ��ܽ�ϡ� ������Լ�����ˮ�Ի���������Al(OH)3��������, ����ˮ����������̼������, ̼�������ڱ�����Լ�������, ����������Al(OH)3������Χ, �Ӷ�ʵ������Դ��̼Դ���ܽ������ȷ�ɢ��Ŀ�ġ� ͼ2��ʾ�ֱ�Ϊ�����ӱ�����Լ�����������ı�����Լ���ϳɵ�AlN��ĩ��SEM�� ��ͼ2���Կ���, û�����ӱ�����Լ��ϳɵĵ�������ĩӲ�ž���������, ������С������; �����ӱ�����Լ��ϳɵĵ�������ĩ����ϸС����, ��ɢ������, ����Ҫԭ�������ڱ�����Լ�������, ����˿����ķ�ɢ����, ʵ����ǰ��������Դ��̼Դ�ľ���ϸ��ɢ, �Ӷ��Ʊ������Ⱦ��Ⱥͷ�ɢ���õĵ�������ĩ���¡�
2.4 ��ҺŨ�ȵ�Ӱ��
��3����ΪAl(NO3)3��ҺŨ�ȷֱ�Ϊ0.1�� 0.4�� 0.8��1.2mol/Lʱ�ϳɵ�ǰ���ﵪ����Ӧ�����ɵĵ�������ĩ�����ʡ�
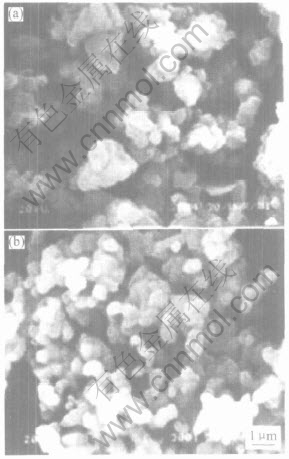
ͼ2 AlN��ĩ��SEM��
Fig.2 SEM images of AlN powders synthesized
without (a) and with (b) surface active agent
��3 Al(NO3)3��ҺŨ����AlN��ĩ���ܵĹ�ϵ
Table 3 Relationship between concentration of Al(NO3)3 solution and properties of AlN powders

�ɱ�3���Կ���, ��Ȼ��ͬŨ�ȵ�����Һ�ϳɵĵ�������ĩ�ĵ������ĺ�������, ����Al(NO3)3��ҺŨ��Ϊ0.4mol/Lʱ, �ϳɵĵ�������ĩ�ıȱ�������, ������ҺŨ�ȹ������ʱ, �ϳɵĵ�������ĩ�ıȱ��������С��
����Һ�г���������Al(OH)3���ӵĴ�С��Ҫȡ�����κ��ٶȺͳɳ��ٶ�, �������ٶ�������Һ�г������ʵĹ����Ͷ�������ء� ��Ȼһ����Ϊ��������ε�Ũ�ȿ���ʹ��Һ�Ĺ����Ͷ�����, ʹ�γɵ�Al(OH)3������ĿѸ������, ����δ��ֳ���ǰ, ����������ʧ, �����ڻ��ϸ������ĩ, ���ǵ�Ũ����ߵ�һ���̶Ⱥ�, �����κ�Ѹ��, ������, ����ϸС, ��������ͨ�������˶����ײ�������۽�, ʹС������������������, ͨ�����淴Ӧ�� ������ɢ�������ɢ���ܺϵ���������, �γ�һ���������������, �����ֲ��ܺ϶��γ�һ��������ž����ӡ� ���, ����ҺŨ�ȶ��γɿ������ȵ�Ӱ�����������, ��ҺŨ�ȹ��ߺ��Ͷ��������Ʊ�ϸ���ȵķ�ĩ�� ���о��������, ������ҺŨ��Ϊ0.4mol/Lʱ, �ϳɵĵ�������ĩ�ıȱ�������
2.5 ����������Ӱ��
ͼ3��ʾΪ����ǰ�����ڲ�ͬ������������ϵ�з�Ӧ4h��, ��Ӧ�����е������뵪�������Ĺ�ϵ�� ��ͼ3���Կ���, ����������Ϊ1~5L/minʱ, ���ŵ�������������, �����е�����������; ��������������5L/min��, ���������Ե�����Ӱ�첻�� ���������ڷ�Ӧ��ϵ��, ���ӵ����ķ�ѹ���ή��һ����̼�ķ�ѹ, �����ڷ�Ӧ���ҽ���, ���������������ӵ�һ���̶Ⱥ�, һ����̼Ũ���㹻��, ���������Է�ӦӰ�첻�� ��������������10L/min��, �ںϳɵĵ�������ĩ�п��Թ۲쵽��������ά����, �䳤�ȿɴ�200��m�� ����Forslund���о��������[12], ˵���ڵ�����Ӧ�����д������෴Ӧ, ���������ٹ���ʱ, �ص���������������������(��ͼ4)��
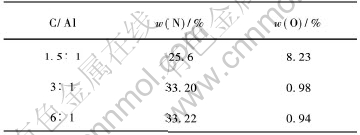
2.6 ̼����Ӱ��
��4����Ϊ����������ͬ, ��̼ͬ���ȵ�ǰ��������AlN��ĩ�����͵������� �ɱ�4���Կ���, ��C��AlĦ����Ϊ����ֵ(��1.5��1ʱ), ����̼������, ������Ӧ����ȫ, ��Ӧ���ﵪ�����ܵ�[CM(22](Ϊ25.6%), �������ܸ�(Ϊ8.23%); ����C��[CM)] AlĦ����Ϊ3��1��6��1ʱ, ̼�Ѿ�����, �ܹ���֤������Ӧ��ȫ����, �ϳɵ�AlN��ĩ�ĵ��������ɴ�33%����, �ӽ�����ֵ, ����������Ӧ���н�Ϊ��ȫ�� ��ǰ������C��AlĦ���ȴ���3��1ʱ, ��Ȼ������������Ӧ�̶�Ӱ�첻��, ���������γ�̼���յ�ʱ������������ ��˿�����Ϊ, ��C��AlĦ����Ϊ3��1ʱ, ��Ӧ�Ѿ���ȫ, Ϊ�ϼ�̼����, �ټ�������̼�����ӳ����γ�̼ʱ������ӳɱ���
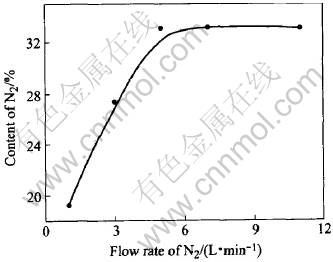
ͼ3 ���������뵪�����Ĺ�ϵ
Fig.3 Relationship between flow rate and content of nitrogen in products
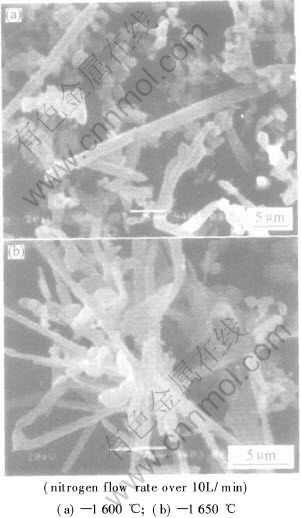
ͼ4 AlN�����SEM��
Fig.4 SEM images of AlN whiskers
��4 ̼����AlN��ĩ�е��� ��������Ӱ��
Table 4 Effects of carbon content on nitrogen and oxygen content of AlN powders
2.7 ��ĩ����
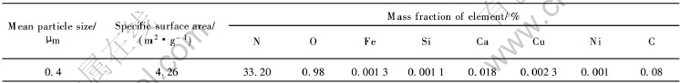
��������Ʒ۹���: ��0.4mol/L����������Һ�ͱȱ����Ϊ156m2/g��̼��Ϊԭ��, ����������Ӳ֬��(SA)�;��Ҷ���(PEG)��Ϊ������Լ�, ���Ƴ���������pHΪ9, ͨ�����������յõ���ɢ�Ժá� �ž۳̶�С��ǰ����, ������ǰ�����ڳ�ѹ�� ��������Ϊ5L/min��������, ��1550������4h, ���Ӧ������650��Ŀ����г�̼4h, �Ʊ���AlN��ĩ���������5���С� ͼ5��ʾΪ����ǰ����ϳɵĵ�������ĩ��SEM�� ��ͼ5�ɿ���, ���ó���ǰ������ϵ�Ʊ��ĵ�������ĩΪ��״�����Բ���ο���, ���ɢ������, ��ĩ������ϸС����, ƽ������ԼΪ0.4��m��

ͼ5 ����ǰ������ϵ�Ʊ���AlN��ĩ��SEM��
Fig.5 SEM image of AlN powders synthesized from precipitated precursor
��5 AlN ��ĩ������
Table 5 Properties of AlN powders
3 ����
��0.4mol/L����������Һ�ͱȱ����Ϊ156m2/g��̼��Ϊԭ��, ����ԭ����̼����(C/Al)Ϊ3��1, ����������Ӳ֬��(SA)�;��Ҷ���(PEG)��Ϊ������Լ�, ���Ƴ���������pH=9, ͨ�����������յõ���ɢ�Ժá� �ž۳̶�С��ǰ��� ����ǰ�����ڳ�ѹ�� ��������Ϊ5L/min��������, ��1550������4h, ���Ӧ������650��Ŀ����г�̼4h, �Ʊ���������Ϊ33.20%, ������Ϊ0.98%, �ȱ����Ϊ4.26m2/g��AlN��ĩ��
REFERENCES
[1]Mussler B H. Advanced materials & powders[J]. Am Ceram Soc Bull, 2000, 79(6): 45-47.
[2]Sheppard L M. Aluminum nitride: a versatile but challenge material[J]. Am Ceram Soc Bull, 1990, 69(11): 1801-1812.
[3]�ܺ�ƽ, ��ҫ��, ����. �������մɵ��о���Ӧ��[J]. ������ѧ��, 1998, 26(4): 517-522.
ZHOU He-ping, LIU Yao-cheng, WU Yin. Development of aluminum nitride ceramics[J]. Journal of the Chinese Ceramic Society, 1998, 26(4): 517-522.
[4]Pathak L C, Ray A K, Das S, et al. Carbothermal synthesis of nanocrystalline aluminum nitride powders[J]. J Am Ceram Soc, 1999, 82(1): 257-260.
[5]Hashimoto N, Yoden H, Nomura K. Preparation of aluminum nitride powder from aluminum polynuclear complexes[J]. J Am Ceram Soc, 1991, 74(6): 1282-1286.
[6]Cho Y W, Charles J A. Synthesis of nitrogen ceramic powders by carbothermal reduction and nitridation, Part 3: aluminum nitride[J]. Mater Sci Tech, 1991,7: 495-504.
[7]������, ��ѡ��, �ֽ���, ��. ̼�Ȼ�ԭ���ϳɵ�������ĩ���о�[J]. ���ϵ���, 2001, 15(7): 56-69.
QIN Ming-li, QU Xuan-hui, LIN Jian-liang, et al. Research on synthesis of AlN powders by carbothermal reduction method[J]. Materials Review, 2001, 15(7): 56-59.
[8]֣��Զ, �½�, ��ΰ. ʪ��ѧ�����ϳɼ�Ӧ��[J]. ���ϵ���, 2000, 14(9): 25-27.
ZHNEG Shi-yuan, CHEN Jian, PAN Wei. Compositing by wet-chemical method and its application[J]. Materials Review, 2000, 14(9): 25-27.
[9]����ΰ, ��ѧ��, ����. �ܽ�-�������Ʊ�PZT������Ӧ����[J]. �й���ɫ����ѧ��, 2003, 13(1): 127-131.
WU Xiang-wei, DUAN Xue-chen, CHEN Zhen-hua. Reaction mechanism of synthesizing PZT nano-crystalline powder by sol-gel process[J]. The Chinese Journal of Nonferrous Metals, 2003, 13(1): 127-131.
[10]������, ��ƽ, ������, ��. ���������о�����Ӧ����״[J]. ���ϵ���, 2000, 14(2): 47-49.
TIAN Yu-ming, HUANG Ping, LENG Shu-yan, et al. Current status of precipitation research and its application[J]. Materials Review, 2000, 14(2): 47-49.
[11]¦����, ���, Ф����. �ܽ����������Ʒ���Ӱ���ĩ���ȵ���Ҫ����[J]. �й����弼��, 2002, 8(1): 15-17.
LOU Yan-liang, LI Chun-hua, XIAO Jian-zhong. Influential factors on particle size of ZrO2 powder prepared by sol-coprecipitional method[J]. China Powder Science and Technology, 2002, 8(1): 15-17.
[12]Forsland B, Zheng J. Carbothermal synthesis of aluminum nitride at elevated nitrogen pressure, Part ��: effect of process parameters on conversion rate[J]. J Mater Sci, 1993, 28: 3125-3131.
������Ŀ: ���ҽܳ������ѧ����������Ŀ(50025412); �����ص�����о���չ�滮������Ŀ(G2000067203)
�ո�����: 2004-09-25; ������: 2005-01-21
�����: ������(1975-), ��, ��ʿ, ������
ͨѶ����: ������, ��ʿ; �绰: 010-62332727; E-mail: mlqin75@hotmail.com
[1]Mussler B H. Advanced materials & powders[J]. Am Ceram Soc Bull, 2000, 79(6): 45-47.
[3]�ܺ�ƽ, ��ҫ��, ����. �������մɵ��о���Ӧ��[J]. ������ѧ��, 1998, 26(4): 517-522.
[7]������, ��ѡ��, �ֽ���, ��. ̼�Ȼ�ԭ���ϳɵ�������ĩ���о�[J]. ���ϵ���, 2001, 15(7): 56-69.
[8]֣��Զ, �½�, ��ΰ. ʪ��ѧ�����ϳɼ�Ӧ��[J]. ���ϵ���, 2000, 14(9): 25-27.
[9]����ΰ, ��ѧ��, ����. �ܽ�-�������Ʊ�PZT������Ӧ����[J]. �й���ɫ����ѧ��, 2003, 13(1): 127-131.
[10]������, ��ƽ, ������, ��. ���������о�����Ӧ����״[J]. ���ϵ���, 2000, 14(2): 47-49.
[11]¦����, ���, Ф����. �ܽ����������Ʒ���Ӱ���ĩ���ȵ���Ҫ����[J]. �й����弼��, 2002, 8(1): 15-17.


