���±�ţ�1004-0609(2016)-03-0699-08
��þ�����ղ����Ż��������ˮ������ѧ����
�� ǿ1, 2, 3���κ�ƽ1, 2���� ��1, 2
(1. �й���ѧԺ ���ݵ���ѧ�о��� �й���ѧԺ����ѧ��ɿ�ѧ�ص�ʵ���ң����� 510640��
2. �й���ѧԺ ���ݵ���ѧ�о��� �㶫ʡ��������������о������ص�ʵ���ң����� 510640��
3. �й���ѧԺ��ѧ������ 100049)
ժ Ҫ��
��þ�����ղ�������ǵ��ز�����ԵĹؼ���������Լ�ˮ������ѧ�������ù����е���Ҫ���ԡ�����������鷽������þ�����ղ��������Ż�����������������Ż�����Ϊ�����¶�650 �棬����ʱ��90 min����������20 ��/min��������С42 ��m���ڴ��Ż������²���ˮ���ʴﵽ58.37%(70��ˮ��1 h)�������ղ����Բ�����Ե�Ӱ���ɴ�С��˳��Ϊ�����¶ȡ����ȴ�С������ʱ�䡢�������ʡ��Ż�����������þ������С���ᾧ�Ƚϵͣ��ȱ�����ϴ�(71.55 m2/g)�����Ż�����ˮ�������У������¶ȿ������ӿ�ˮ����Ӧ�Ľ��У�ˮ������ѧ�������ڻ�ѧ��Ӧ�������ͣ���Ӧ�ı��ۻ��Ϊ27.94 kJ/mol���ڽϸ��¶������£�����ѧ�����ɻ�ѧ��Ӧ����������ת��Ϊ����ɢ�������͡�
�ؼ��ʣ�
��þ�������ղ�����������鷽����ˮ������ѧ��
��ͼ����ţ�TD985���� ���ױ�־�룺A
��þ����һ����̼��þΪ��Ҫ������ɵĿ����Դ��ȫ��̽������þ����Դ��������100�ڶ֣���Ҫ�ֲ����й������ʡ�����˹��˹�工�˵ȹ��ҡ����У��ҹ�����þ�������Ĺ��ң�Լռȫ���ܴ�����31%[1]������þ������Դ���ù����У�����������Ҫ�Ĵ�������֮һ��������Ҫ��Ϊ���ۡ����ռ�����������[2]����������þ���ڵ�¯�����ں����ɵ���þ���������¶���2500~3000 ��֮�䣻��������1400~1700���¶ȷ�Χ�ڣ���̼��þ�ֽ��������þ�ս�ɽṹ���ܵ�����þ����õĵ���þ������þ��Ҫ�����Ʊ��ͻ���ϡ����յ��¶ȷ�Χ��700~1200��֮�䣬��õ�����þ���л��Ըߡ������ἰ��;����ص㣬���㷺Ӧ���ڽ��ġ�������ҽҩʳƷ��ũҵ����������ҵ��
��þ��������Ҫ����̼��þ�ֽ⼰����þ�ᾧ�������̣�ͨ������������ͬʱ���С��ɴ�������ķֽ⼰�ᾧ�̶ȵIJ�������ɲ�����Բ�����Ҫԭ�ӹ��սǶȷ��������ղ����������Ӱ�����չ�����̼��þ�ֽ⼰����þ�ᾧ�̶ȵ���Ҫ���ء���ˣ�ͨ���������ղ�������ʵ�ֶԲ�����Եĵ��ء�Ŀǰ���о���Ҫ�����ڶ������¶ȡ�����ʱ�估���ȴ�С�ȵ����ضԲ�������༰���Ե�Ӱ��[3-5]������Щ���ص��ۺ��뽻��Ӱ��ǶȽ���ϵͳ���о����١�
���ղ���������������ղ�����������Ҫָ�ꡣĿǰ��������Եı��������۷�����Ҫ�������ᷨ������������ˮ������[6]�����У������ᷨ�ζ��յ���ж�����þ��ԭ�����������ܳ���Ӱ��ϴ�������ʵ��������̷��ӣ�ʵ��Ӧ�ý��١�ˮ����ֱ�������˲�����ˮ��Ӧ�������仯����������Ļ��ԣ����Ը�ֱ�۵ط�ӳ����ķ�Ӧ���ԣ����м����ڲ������ŵ㡣��ˮ�������У���ѧ��Ӧ����ɢ������Ҫ�Ĺ��̡��������̵���Կ������ж�ˮ������ѧ�Ĺؼ����ڡ�Ŀǰ�����ڲ���ˮ������ѧ���̷�����Ȼ���ڽϴ�����顣����ѧ���о�������������ˮ������������ɢ����[7]������һЩѧ������Ϊ�ܻ�ѧ��Ӧ����[8-9]����ˣ�����ˮ������ѧ������Ȼ��Ҫ��������ķ�����̽����
������鷽����һ�ֻ���������۵ĸ�Чϵͳ�����Ż���Ʒ���[10]���÷�������ֱ������ư���������������������(Z)�ж���Ʒ��Ʒ��ָ�꣬����߶��������Ӱ�������µ�����Ч�ʣ�����������ƵĿ�ѧ�ԡ�ͬʱ��������鷽�����Ż������ʵ��Ӧ���о��нϺõ������ԣ���˱��㷺Ӧ�����ܽ� [11]�����Ϻϳ�[12-13]����������������Ż���Ȼ������Ӧ������þ�����ղ����Ż���������Ե��ص��о���δ��������������������������鷽������þ�����չ��̲���������ƣ���ˮ������Ϊָ���Ż������ղ����������Ż������ˮ������ѧ���̽�������ķ�����̽��������Ϊ��þ��Ŀ����Դ�����ṩ��������鼰�������ݡ�
1 ʵ��
1.1 ʵ��ԭ��
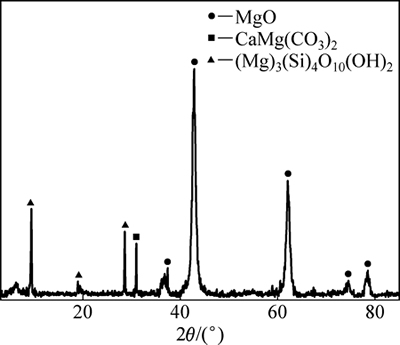
ʵ��������þ���������Ừʵҵ����˾�ṩ��X��������(XRD)���������ʾ����Ҫ����Ϊ̼��þ�����еĸơ������ʷֱ�����ʯ����ʯ�����(��ͼ1)������X����ӫ�����(XRF)�����ó��仯ѧ�ɷ֣�������1���С�

ͼ1 ��þ��XRD��
Fig. 1 XRD pattern of magnesite
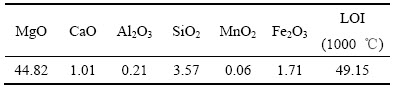
��1 ��þ����Ʒ��ѧ�ɷ�
Table 1 Chemical composition of magnesite (mass fraction, %)
1.2 ʵ�����
1.2.1 ��þ����������
��þ�������ĥ��ɸ��һ������������������鷽���趨�����ղ�������������¯(Carbolite RHF14/3)�н������գ���Ȼ��ȴ�������ղ�����Ʒ����þ�����շֽ������Ҫ�������·�Ӧ��
MgCO3��MgO+CO2�� (1)
1.2.2 �������
����X������������������Ҫ������ɣ�������������������Scherrer��ʽ�������е�����þ������С��ʹ�ó�����ɨ��羵(SEM)��������ı�����ò������N2���Ѹ�BET�ȱ�����������ⶨ����ıȱ������
1.2.3 ���ղ���ˮ�����Բⶨ
����ˮ����(70 ��)�������ղ���Ļ��ԡ�����Ʒ������������50��������и���30 min���ô�����ȷ����1 g��������(w0)������4 mL����ˮ�����Ƚ��������70 ��������б���60 min����������150����20 min����ȴ�����ˮ����Ʒ������(w1)������ˮ����Ӧ���£�
MgO+H2O��Mg(OH)2 (2)
���ղ���ˮ�����Կ������е�MgOˮ����(X)����ʾ������㹫ʽ��ʽ(3)��ʾ��
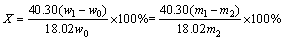 (3)
(3)
1.2.4 �Ż�����ˮ������ѧ����
��ȡ3.0 g�Ż����������װ��100 mL����ˮ���Ѿ�����(20��35��50��65 ��)����ƿ����һ���Ĵ�������������(0��300��600��900 r/min)ˮ��һ��ʱ��(0.5��1��1.5��2.0��2.5��3 h)����ˮ��������Һ���ˣ�����ˮ�Ҵ���ϴ���ٽ�ˮ����Ʒ����105 ��ķ�������к�ɡ�����������ˮ����Ʒ(m1)����������¯����500 ������1.5 h���������պ������m2���Ż������ˮ���ʰ���ʽ(3)���㡣
1.3 ������鷽��
������鷽�����������(Z)��������Ʒ����ָ��IJ����ԣ�������ָ����Ϊ��Ʒ�������Ե����۱�������������3�����͵�����ȣ�1) ��Ŀ���ԣ�������ָ��Խ�ӽ�Ŀ��ֵԽ�ã�2) ��С���ԣ�������ָ��Խ��������ֵԽ�ã�3) �������ԣ�������ָ��Խ��������ֵԽ��[14]���������е���������Ϊˮ�����ԣ�����������������ȣ�����㹫ʽ���£�
 (4)
(4)
ʽ�У�nΪʵ����ܴ�����yiΪ��i��ʵ�������µ�ָ��ֵ����ʾ��i��������������ˮ���ʡ�
2 ���������
2.1 ���ղ���������Ż�
��������ѡȡ�������¶ȡ�����ʱ�䡢�������ʼ����ȴ�С4�����ղ�����Ϊ�������ӣ��ֱ���A��B��C��D��ʾ��ÿ������ѡ��4��ˮƽ������������鷽����ѡ��L16(44) ֱ������ư����������飬�ֱ��ÿ��������������������顣��2����Ϊ����ˮƽ����������ư��ż�������3���С�
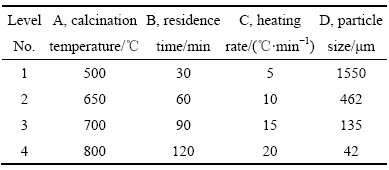
��2 ������鷽������ˮƽ��
Table 2 Factors and levels of Taguchi method
�������������������˲�ͬ���ز�ͬˮƽ������ȣ���ø�Ӱ�����ӵ�ƽ��ЧӦ(��ͼ2)�������ʾ�����������¶ȵ����ߣ�����ˮ����������ȳ�����������С�Ĺ��ɣ��������¶ȴ�500 ��������650 �棬��ƽ���������0.66������2.16���˺����������¶ȵ����ߣ�����ȳ��ֻ����½������ƣ��½���800��ʱ��2.00���汣��ʱ��ı仯����ȳ������Ƶı仯���ɣ�����仯�ķ��Ƚ�С����������ֵΪ1.76(����ʱ��90 min)������Сֵ(1.69)������0.7(����ʱ��30 min)��������������5 ��/min������20 ��/min���������1.70������1.75������������1550 ��m�½���42 ��m���������1.63������1.83�����ֵ�����ڽϴ���������ʡ���С�����������¡���������������鷽���ķ���������ȷ�����Ż�����������ΪA2 B3 C4 D4�����������¶�650 �棬����ʱ��90 min����������Ϊ20 ��/min�����ȴ�СΪ42 ��m��������鷽���ṩ�����Ż������²���ָ���Ԥ�ⷽ��[14]������Ԥ�ⷽ������õ��Ż�����ˮ����Ϊ58.61%����ʵ����֤�����У��Ż������ʵ��ˮ����ԼΪ58.37%����Ԥ��ֵ�Ͻӽ�(����4)����֤��������������鷽�������ղ��������Ż��������Ч�ģ���ʵ�������в�����Ծ��нϺõ������ԡ�
��3 �������鰲�ż����
Table 3 Arrangements and results of calcination experiments
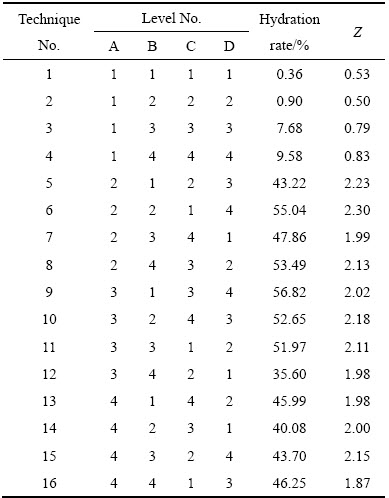
����������Լ���������ӶԻ��ԵĹ�����[15]���Ӷ��жϸ����ӶԲ���ˮ�����Ե�Ӱ���С���ɱ�4�ļ�������֪�������ӶԲ���ˮ������Ӱ���ɴ�С��˳�����£������¶ȡ����ȴ�С������ʱ�䡢�������ʡ����������¶ȵ�Ӱ����Ϊ�������乱����Ϊ98.14%����С��Ϊ�������ʣ��乱���ʽ�Ϊ0.07%��
2.2 �Ż������������
��þ�����չ��̷�������Ҫ��̼��þ�ֽ������þͬʱ�ͷų�CO2�Ĺ��̣�����һ�����ȷ�Ӧ���̡��ڷֽ�����У�̼��þ������[CO3]�ṹ��Ԫ��C��O���������ѣ��ͷų�CO2������Oԭ�ӣ�ʹ����Щλ�õĻ�ѧ��ɷ����˱仯���γ��˻�ѧ���[16]���ڴ�״̬�µIJ���ᾧ�ȵͣ��ṹ���ɣ��ȱ��������ṹȱ�ݶ࣬����仯ѧ���Ըߡ���̼��þ�ֽ������ɺ����������¶ȵ���������ʱ����ӳ�������ľ���ṹ����������ռ��������λ���������ⲿ�������������£��ṹ�зֽ����µ�Oԭ�ӷ���λ�ƣ�����Mg����γ�MgO���塣�˹���ʹ��MgO����ṹ���������ƣ�����ߴ�����ѧ��������[4,7]�����������¶ȹ��͡�����ʱ����̼����տ������Ƚϴ�ʱ�������������������ڲ���ʹ����ֽⲻ��֣��Ӷ���������ԡ�
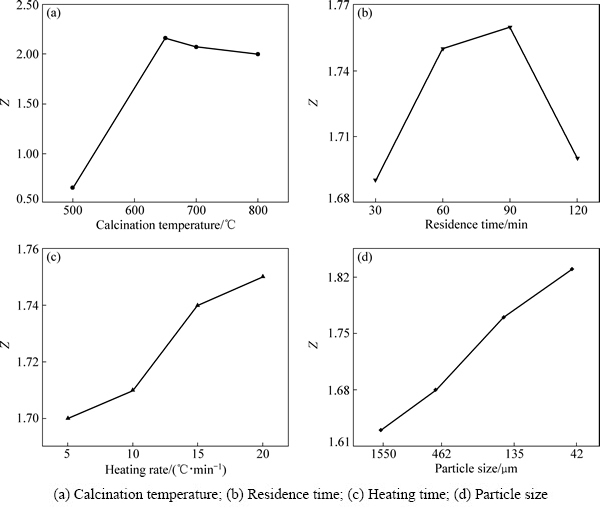
ͼ2 ����ƽ��ЧӦ
Fig. 2 Average of Z ratios
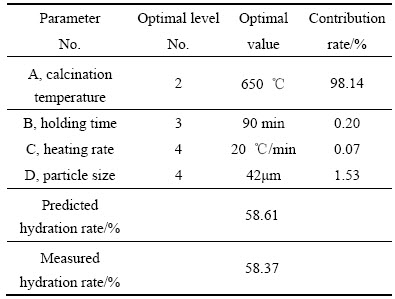
��4 �Ż�����ˮƽ��Ԥ��ˮ���ʼ����ӹ�����
Table 4 Optimum working conditions, predicted hydration rate and contribution rate of factors
�Ż������XRD����ͼ3��ʾ����ͼ3��֪������������鷽���Ż������ղ�����̼��þ������������Ѿ���ȫ��ʧ������������þ�������壬����̼��þ�Ѿ���ȫ�ֽ⡣����2��Ϊ42.7�㴦����þ(200)������������߿�����Scherrer��ʽ����õ��侧����СΪ13.8 nm����������ɵ�����þ����С������ᾧ�ȵ͡��������ò�۲�����ʾ(��ͼ4)�������������ܼ�С�������ǣ������䲼���˴�С��һ�����ף��������չ�����̼��þ�ķֽ⼰����þ�Ľᾧ�йء�
ͼ3 �Ż������XRD��
Fig. 3 XRD pattern of optimized calcined sample

ͼ4 �Ż������SEM��
Fig. 4 SEM image of optimized calcined sample
���Ż�������е�BET�ȱ�������������ʾ���Ż�����ıȱ����Ϊ71.55 m2/g����Щ������������������þ���о���С���ᾧ�ȵͼ��ȱ��������ص㣬�����Ż�������нϸ�ˮ�����Ե�ԭ��
2.3 �Ż�����ˮ������ѧ����
��þ�����ղ���ˮ��������Ҫ�Dz����е�MgO��H2O������Ӧ�Ĺ��̡�����ˮ�������IJ�ͬ��ˮ������ѧ���Է�Ϊ����ɢ���ơ�����ɢ���ƺͻ�ѧ��Ӧ����3������[7, 17]������ɢ���ƶ���ѧģ�Ϳ��Կ���������ʶ�����þˮ���ʵ�Ӱ������жϡ�����߽������ʿ����������ˮ����(40%~70%)����ˮ������Ϊ����ɢ����[18]��ʵ������ʾ(��ͼ5)���������߽������ʲ�δ��ýϴ�IJ���ˮ���ʣ��ɴ˿����ų��Ż�����ˮ������Ϊ����ɢ���ƵĿ����ԡ�
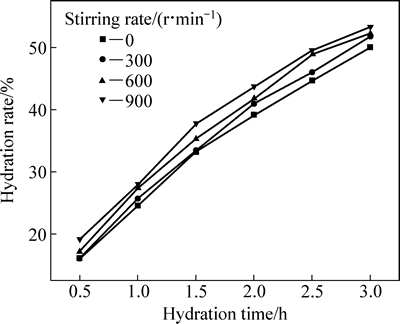
ͼ5 �Ż������ڲ�ͬ���������µ�ˮ��������
Fig. 5 Hydration rate curves of optimized calcined sample at different stirring rates
��һ���ж�ˮ������ѧ���̳���ˮ�������ݴ�������ɢ�Լ���ѧ��Ӧ�Ķ���ѧ���̽�����ϣ�ͨ�����ϵ����ȷ���䶯��ѧ���͡����¶��������Ż������ˮ���ʽ����ʾ(��ͼ6)��ˮ���¶ȶ�ˮ���ʵ�Ӱ��ϴ��¶�����������ˮ���ʵ���ߡ���20 �漰35 ��������ˮ��ʱ��ˮ��������ˮ��ʱ����ӳ����������ӣ����¶�������50 �漰65 ��ʱ��ˮ������ˮ��ʱ��0~2 h�����ӽϿ죬����2.0~3 h��ʱ���ˮ���ʵķ��Ƚ�С����ˮ��������ͬʱ��������ɢ����ѧ����[7]������þˮ����Ӧ����ѧ����[8]�����������ɢ����ѧ����
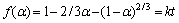 (5)
(5)
����þˮ����Ӧ����ѧ����
 (6)
(6)
ʽ�У�f (��)Ϊˮ���ʺ�������Ϊˮ���ʣ�kΪ���۷�Ӧ���ʳ�����tΪˮ��ʱ�䡣

ͼ6 �Ż������ڲ�ͬ�¶��µ�ˮ��������
Fig. 6 Hydration rate curves of optimized calcined sample at different temperatures
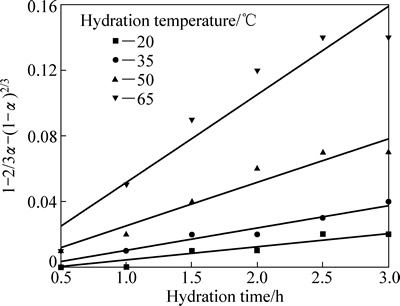
ͼ7 ����ɢ����ѧ������Ͻ��
Fig. 7 Fitting results of internal diffusion dynamics equation

ͼ8 ��ѧ��Ӧ����ѧ������Ͻ��
Fig. 8 Fitting results of chemical reaction dynamics equation
��ͬ�¶��µ�ˮ����������Ͻ����ʾ(��ͼ7��ͼ8����5)������ɢ���ƶ���ѧ���̵��������ϵ���Ȼ�ѧ��Ӧ����ѧ���̵��������ϵ��ҪС��20 �� ��35 ��������ˮ�������ݾ��Ϻõط���������þˮ����Ӧ����ѧ���̣������ϵ��������0.98�����������µ�����������ɢ����ѧ���̵�������ϵ����Ϊ0.868��0.952���ɴ˿��Գ����ƶ���ˮ�������ܻ�ѧ��Ӧ���ơ�����50 �漰65 ��ˮ��������ˮ��������������þˮ����Ӧ����ѧ������ϵ����ϵ�������½������ƣ��½���0.965��0.944(�ֱ��Ӧͼ8�����ֱ��C1��D1)����������ɢ����ѧ���̵�������ϵ����������0.954��0.943�����ִ��������Ҫԭ��������ˮ����Ӧ�Ľ��У����ɵ���ˮ������������þ������δˮ��������þ������Χ����ֹ�����γɵ�������þ����ɢ��ˮ���ӽ��뵽������þ����[9]����ʱ��ˮ�����̽���������ɢ���ƵĹ��̡�����ˮ����Ӧ����ѧ���̷ֱ��50 ��ˮ���¶ȡ�25 h��ˮ��ʱ�������¼�65 ��ˮ���¶ȡ�2.0 h��ˮ��ʱ�������µ�ˮ�������ݽ�����ϣ��õ����ֱ��C2��D2(��ͼ8)�������ϵ���ֱ�Ϊ0.995��0.986���������Ͻ���Ϻõط�����ˮ����Ӧ����ѧ���̡��ɴ˿����ж��ڽϸ�ˮ���¶������£�ˮ������ѧ��һ���ɻ�ѧ��Ӧ����������ɢ���ƵĹ��̡�
��5 ����ѧ������ϵ��
Table 5 Correlation coefficient of dynamics equations
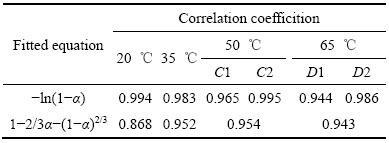
ѡȡ20 �棬35 �����Ͻ����50 ���C2�ߺ�65���D2����Ͻ�������ݰ�������˹���̣������������ˮ����Ӧ�Ļ�ܣ�
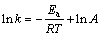 (7)
(7)
ʽ�У�EaΪ��Ӧ��ܣ�RΪĦ�����峣����TΪ����ѧ�¶ȣ�AΪָǰ���ӡ�
��ˮ���¶���ˮ�����ʳ���k�������(��ͼ9)��������ñ��۷�Ӧ���Ϊ27.94 kJ/mol�����ڻ�ѧ��Ӧ���(Ec)����ɢ���ƻ��(Ed)�о�[19]��Ed��25.12 kJ/mol��Ec�����Խ�һ��ȷ����������������Ż������ˮ����ӦΪ��ѧ��Ӧ�������͡����ڽϸߵ��¶������£�ˮ������ѧ�����ɻ�ѧ��Ӧ������ת��Ϊ����ɢ���ƵĹ��̡�
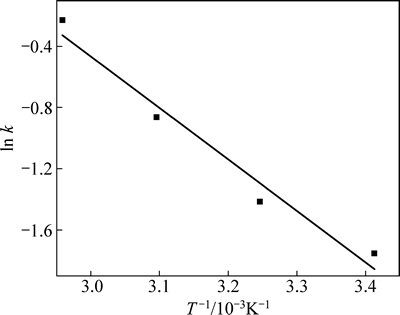
ͼ9 ��Ӧ���ʳ������¶ȵĹ�ϵ
Fig. 9 Relationship between k and temperature
3 ����
1) ����������鷽������þ�����ղ��������Ż����Ż����ղ������£������¶�Ϊ650 �棬����ʱ��Ϊ90 min����������Ϊ20 ��/min��������СΪ42 ��m�����Ż������²���70 ��ˮ��1 h��ˮ���ʴ�58.37%�������ղ����Բ�����Ե�Ӱ���ɴ�С��˳�����£������¶ȡ����ȴ�С������ʱ�䡢�������ʡ����������¶ȵ�Ӱ����Ϊ�������乱����Ϊ98.14%����������Ӱ����С���乱���ʽ�Ϊ0.07%���Ż�������̼��þ��ȫ�ֽ�ת��Ϊ����þ�����е�����þ������С���ᾧ�ȵ͡��Ż�����ȱ����71.55 m2/g��
2) �¶ȶ��Ż������ˮ������Ӱ��ϴ�����ˮ���¶ȿ������ӿ�ˮ����Ӧ�Ľ��С�ˮ����Ӧ���ڻ�ѧ��Ӧ�������ͣ��䷴Ӧ�ı��ۻ��Ϊ27.94 kJ/mol���ڽϸ�ˮ���¶������£�����ѧ�����ɻ�ѧ��Ӧ������������ɢ���ơ�������Ϊ��þ��Ŀ����Դ�����ṩ�˸�������鼰�������ݡ�
REFERENCES
[1] ������. �й���þ����״�뷢չ����[J]. �й��ǽ�����ҵ����, 2006, 57(5): 6-8.
WANG Zhao-min. Present situation and the development tendency of magnesite in China[J]. China Non-metallic Mining Industry Herald, 2006, 57(5): 6-8.
[2] �� ƽ, л ��, ������. ����þ������þ������þ������þ����ṹ��XRD����[J]. �й��ǽ�����ҵ����, 2004, 38(1): 31-33.
SUN Ping, XIE Yan, NIE Dong-rui. XRD analysis of magnesium oxide crystal structure in caustic burned magnesia, dead burnt magnesite and fused magnesite[J]. China Non-metallic Mining Industry Herald, 2004, 38(1): 31-33.
[3] �� �, ������. ��þ����չ���������þ�ս��뾧����������ѧ���о�[J]. ������ѧ��, 1989, 17(1): 64-69.
LI Nan, CHEN Rong-rong. Kinetics of sintering and grain growth of MgO during calcination of magnesite[J]. Journal of Chinese Ceramics Society, 1989, 17(1): 64-69.
[4] �� ��, �� ��. �����ƶȶ�MgO���Ե�Ӱ��[J].�Ͼ���ҵ��ѧѧ��(��Ȼ��ѧ��), 2008, 30(4): 52-55.
CUI Xin, DENG Min. Effects of calcined conditions on activity of MgO[J]. Journal of Nanjing University of Technology (Natural Science Edition), 2008, 30(4): 52-55.
[5] ����ϲ, Ѧ����, ����ΰ, ��ݼݼ, �ź첨, ������. ��þ��β���Ʊ�����MgO �����ܱ���[J]. ��������ѧ��, 2012, 6(4): 1315-1319.
HUANG Ming-xi, XUE Jian-jun, GAO Pei-wei, LUO Jing-jing, ZHANG Hong-bo, WU Ze-mei. Preparation and properties of high-active MgO from magnesite tailings[J]. Chinese Journal of Environmental Engineering, 2012, 6(4): 1315-1319.
[6] ������, ��췢, ������. ˮ�Ϸ��ⶨ����MgO���������������о�[J]. �κ��о�, 2012, 18(1): 38-41.
DONG Jin-mei, YU Hong-fa, ZHANG Li-ming. Study on experimental conditions of hydration methods of deternining active magnesium oxide content[J]. Journal of Salt Lake Research, 2012, 18(1): 38-41.
[7] ����ΰ, �� ��, �� ��, �� Ƽ, �� ƽ. ��þ���Ʊ���������þ����ˮ������ѧ�о�[J]. ���ϴ�ѧѧ��(��Ȼ��ѧ��), 2011, 42(12): 3912-3917.
LIU Xin-wei, FENG Ya, LI Hao, ZHANG Ping, WANG Ping. Preparation of light-burned magnesia from magnesite and its hydration kinetics[J]. Journal of Central South University (Science and Technology), 2011, 42(12): 3912-3917.
[8] Ǯ����, ����Ӣ, �� ��, ������. ��������þˮ������ѧ[J]. ����������ӹ�, 2007(12): 1-4.
QIAN Hai-yan, LI Su-ying, DENG Min, ZHANG Shao-ming. Hydration dynamic of light burned magnesia[J]. Industrial Minerals and Processing, 2007(12): 1-4.
[9] ��ѧ��, ������. ��������þˮ������ѧ�о�[J]. ���ι�ҵ, 2000, 32(4): 16-19.
ZHAI Xue-liang, YANG Yong-du. Study of hydration kinetics of activated MgO[J]. Inorganic Chemicals Industry, 2000, 32(4): 16-19.
[10] PHILLIP J R. Taguchi techniques for quality engineering[M]. New York: McGraw Hill Professional, 1996: 3-15.
[11] FATIH D, BUNYAMIN D. Optimization of the dissolution of magnesite in citric acid solutions[J]. International Journal of Mineral Processing, 2008, 87(1): 60-64.
[12] NITA S, JOONSOO B, AGUS P S. Optimization of operating parameters for liquid-cooled PEM fuel cell stacks using Taguchi method[J]. Journal of Industrial and Engineering Chemistry, 2012, 18(3): 1039-1050.
[13] AMIN B D, JAVAD M, AMIR M. An optimization study on the leaching of zinc cathode melting furnace slag in ammonium chloride by Taguchi design and synthesis of ZnO nanorods via precipitation methods[J]. Materials Research Bulletin, 2013, 48(10): 4235-4247.
[14] SANG M K, KI S P, KI D K. Optimization of parameters for the synthesis of bimodal Ag nanoparticle by Taguchi method[J]. Journal of Industrial and Engineering Chemistry, 2009, 15(6): 894-897.
[15] ղ־��, ���ҽ�, ���ļ�, ��۾�. ��ڷ���TiO2�п���ϳ��о�[J]. ���̹���ѧ��, 2006, 6(2): 302-305.
ZHAN Zhi-jie, ZHANG Zhong-jie, XU Wen-jia, ZHU Hui-juan. Synthesis of hollow TiO2 spheres by Taguchi method[J]. The Chinese Journal of Process Engineering, 2006, 6(2): 302-305.
[16] FU Da-xue, FENG Nai-xiang, WANG Yao-wu. Study on the kinetics and mechanism of grain growth during the thermal decomposition of magnesite[J]. Bulletin of the Korean Chemical Society, 2012, 33(8): 2483-2488.
[17] ZHAO Yu-na, Zhu Guo-cai. Thermal decomposition kinetics and mechanism of magnesium bicarbonate aqueous solution[J]. Hydrometallurgy, 2007, 89(3/4): 217-223.
[18] ���Ȼ, ������, ��С��, �����, ������. ʪ������ճ�����з��Ķ���ѧ[J]. ���ϴ�ѧѧ��(��Ȼ��ѧ��), 2008, 39(6): 1181-1184.
LI Hao-ran, FENG Ya-li, LUO Xiao-bing, WANG Hong-jie, DU Zhu-wei. Leaching kinetics of extraction of vanadium pentoxide from clay mineral[J]. Journal of Central South University (Science and Technology), 2008, 39(6): 1181-1184.
[19] SIDNEY W B. The foundations of chemical kinetics[M]. Toronto: McGraw-Hill, 1960: 183-196.
Parameters optimization of magnesite calcination and hydration dynamics of optimized sample
ZHANG Qiang1, 2, 3, HE Hong-ping1, 2, TAO Qi1, 2
(1. Key Laboratory of Mineralogy and Metallogeny, Guangzhou Institute of Geochemistry,
Chinese Academy of Sciences, Guangzhou 510640, China;
2. Guangdong Provincial Key Laboratory of Mineral Physics and Materials,
Guangzhou Institute of Geochemistry, Chinese Academy of Sciences, Guangzhou 510640, China;
3. University of Chinese Academy of Sciences, Beijing 100049, China)
Abstract: Parameters are important for activity controlling during magnesite calcination. The activity and hydration dynamics of calcined samples are crucial properties. Taguchi method was used to optimize the parameters in magnesite calcination. The results show that the optimized parameters are achieved at calcination temperature of 650 ��, with heating rate of 20 ��/min and residence time of 90 min, and the particle size is 42 ��m. The optimal hydration rate reaches 58.37% after hydrating at 70 �� for 1 h. The influences of parameters on activity decrease from high to low as calcination temperature, particle size, residence time, heating rate. The optimal sample contains small crystal of MgO with high specific surface area (71.55 m2/g). During hydration, elevated temperature accelerates significantly the hydration reaction. The apparent activation energy is 27.94 kJ/mol, indicating that the dynamics is controlled by hydration reaction. Hydration dynamics changes gradually from hydration reaction controlled towards internal diffusion controlled at higher temperature.
Key words: magnesite; calcination parameter; Taguchi method; hydration dynamics
Foundation item: Project (41372048) supported by the National Natural Science Foundation of China; Project (20111071010019) supported by Foshan-Chinese Academy of Sciences Cooperation, China
Received date: 2015-04-08; Accepted date: 2015-08-30
Corresponding author: TAO Qi; Tel: +86-20-85290252; E-mail: taoqi@gig.ac.cn
(�༭ ������)
������Ŀ��������Ȼ��ѧ����������Ŀ(41372048)����ɽ��Ժ�к�����Ŀ(20111071010019)
�ո����ڣ�2015-04-08�������ڣ�2015-08-30
ͨ�����ߣ��� �棬���о�Ա����ʿ���绰��020-85290252��E-mail��taoqi@gig.ac.cn
ժ Ҫ����þ�����ղ�������ǵ��ز�����ԵĹؼ���������Լ�ˮ������ѧ�������ù����е���Ҫ���ԡ�����������鷽������þ�����ղ��������Ż�����������������Ż�����Ϊ�����¶�650 �棬����ʱ��90 min����������20 ��/min��������С42 ��m���ڴ��Ż������²���ˮ���ʴﵽ58.37%(70��ˮ��1 h)�������ղ����Բ�����Ե�Ӱ���ɴ�С��˳��Ϊ�����¶ȡ����ȴ�С������ʱ�䡢�������ʡ��Ż�����������þ������С���ᾧ�Ƚϵͣ��ȱ�����ϴ�(71.55 m2/g)�����Ż�����ˮ�������У������¶ȿ������ӿ�ˮ����Ӧ�Ľ��У�ˮ������ѧ�������ڻ�ѧ��Ӧ�������ͣ���Ӧ�ı��ۻ��Ϊ27.94 kJ/mol���ڽϸ��¶������£�����ѧ�����ɻ�ѧ��Ӧ����������ת��Ϊ����ɢ�������͡�
[1] ������. �й���þ����״�뷢չ����[J]. �й��ǽ�����ҵ����, 2006, 57(5): 6-8.
[3] �� �, ������. ��þ����չ���������þ�ս��뾧����������ѧ���о�[J]. ������ѧ��, 1989, 17(1): 64-69.
[4] �� ��, �� ��. �����ƶȶ�MgO���Ե�Ӱ��[J].�Ͼ���ҵ��ѧѧ��(��Ȼ��ѧ��), 2008, 30(4): 52-55.
[6] ������, ��췢, ������. ˮ�Ϸ��ⶨ����MgO���������������о�[J]. �κ��о�, 2012, 18(1): 38-41.
[8] Ǯ����, ����Ӣ, �� ��, ������. ��������þˮ������ѧ[J]. ����������ӹ�, 2007(12): 1-4.
[9] ��ѧ��, ������. ��������þˮ������ѧ�о�[J]. ���ι�ҵ, 2000, 32(4): 16-19.
[15] ղ־��, ���ҽ�, ���ļ�, ��۾�. ��ڷ���TiO2�п���ϳ��о�[J]. ���̹���ѧ��, 2006, 6(2): 302-305.
[19] SIDNEY W B. The foundations of chemical kinetics[M]. Toronto: McGraw-Hill, 1960: 183-196.


