���������Ѷ�����ø���Ե���ǿЧӦ
˾ʿ�ԣ� �� ������������л����
(���ϴ�ѧ ��ѧ����ѧԺ������ ��ɳ��410083)
ժ��Ҫ���ֱ�������Ϊ5 nm��25 nm��2.4 ��m��TiO2��������ø����35 �棬pHΪ7�������²��õ�λ���ⶨ������TiO2�ϵ�����ø�Ļ��Ա仯����������TiO2Ĥ��pH��Ӧ���Ʊ�����ø/����TiO2����Ĥ�缫���о��������������TiO2������ø�Ļ��������Ե���ǿЧӦ��������ø��TiO2(�����ֱ�Ϊ5 nm��25 nm��2.4 ��m)����ø�����ϳ����ֱ�Ϊ0.45��0.22��0.28��0.31 mol/L���ø��ϵ缫�����صļ�ⷶΧΪ8.5��10-5~0.15 mol/L�����ϵ��Ϊ0.993 73�������Ϊ5��10-6 mol/L����ʹ��������35 d������ά��38����
�ؼ��ʣ�
����TiO2��ø����������ø�����ϵ缫��
��ͼ����ţ�O614.41+1 ���ױ�ʶ�룺A ���±�ţ�1672-7207(2007)04-0692-04
Enhancement of urease activity by TiO2 nanoparticles
SI Shi-hui, LI Sai, YANG Zheng-peng, XIE Ya-lin
(School of Chemistry and Chemical Engineering, Central South University, Changsha 410083, China)
Abstract: The urease was adsorbed on TiO2 with different particle sizes(5 nm, 25 nm, 2.4 ��m). Under conditions of 35 �� and pH=7, the activity of urease absorbed on TiO2 particles was measured by potentiometry. Based on the pH response of nano-TiO2 film, a urease/nano-TiO2 complex films electrode was developed. The results show that the activity of urease can be enhanced by being adsorbed on nanostructure materials, and the Michaelis-Menton constant of free and urease adsorbed on different particles sizes of TiO2 (5 nm, 25 nm, 2.4 ��m) are 0.45, 0.22, 0.28 and 0.31 mol/L, respectively. The complex films electrode is sensitive to urea in the linear range 8.5��10-5-0.15 mol/L, the correlation coefficient and the detection limit are 0.993 73 and 6��10-5 mol/L, respectively. The lifetime of the urease/nano-TiO2 complex films electrode can remain 38% after 35 d.
Key words: nano-titanium oxide; enzyme adsorption; urease; complex films electrode
���ײ���������ߴ��С���ṹ���⣬��˾���������ص�������ѧ���ԣ���С�ߴ�ЧӦ���ȱ������Ӧ���Ըߣ�����ЧӦ��[1-3]���������������������ķ�չ�����ײ��ϵ�����ЧӦ���������ǵĹ� ע[4-7]��Ŀǰ�������Ѷ�����TiO2��SiO2��̼���ܺ��������۵ȵ�����ЧӦ�������о�[8-11]��
����TiO2���бȱ������ѧ�ȶ��Ժõ��ŵ�һֱ�ܵ����ǵĹ�ע��Ŀǰ������TiO2��Ӧ��ʮ�ֹ㷺�����磺�ڻ�����ѧ�У�������TiO2��Ϊ��������ڷ�ˮ����������ˮ����[12]����ҽ�������У�����TiO2�����İ뵼�������ԣ�����ɱ�������Ͱ�֢����[13]���ڿ�ѧ�о��У���TiO2��Ϊ���в���Ӧ���ڴ��������Ʊ�[14]�������о�������TiO2���ײ��ϵ�����ЧӦ��ߴ�ЧӦ�й�[11]��Ϊ�ˣ���������������TiO2Ϊ������������ø���о���ͬ�ߴ�����TiO2������ø���Ե�Ӱ�죻���⣬��������TiO2��ΪpH����Ĥ�Ʊ�����ø/����TiO2����Ĥ�缫�����ڲⶨ���ص�Ũ�ȡ�
1��ʵ����
1.1���������Լ�
��Ҫ�����У�PHS-3C����pH��(�Ϻ��״�����������)����������ˮԡ(�Ϻ���������������)����������ϴ��(��ɽ�г�����������˾����)��78HW-3���´���������(���������������˾����)��800B���Ļ�(�Ϻ���ͤ��ѧ����������)��
��Ҫ�Լ��У�����ø(EC.3.5.1.5 type��Sigma��˾����)��TiO2(�����ֱ�Ϊ5 nm��25 nm��2.4 ?m�������ŵ����Ƽ�����˾����)����˿(ֱ��Ϊ������1 mm)����ˮ�Ҵ����״���1 mmol/L Na2HPO4-1 mmol/L NaH2PO4������Һ(PBS)�������Լ���Ϊ��������ʵ����ˮ��Ϊ��������ˮ��
1.2 ����������TiO2���������ø���ԵIJⶨ
�ܹ��£��ֱ�2 mg����Ϊ5 nm��25 nm�� 2.4 ?m��TiO2��������3 mL��0.125 mg/mL������ø��Һ�У���4 ����������12 h���ⶨʱ����35 �棬��0.1 mol/L��������ҺΪø������Ƚ�����ҺpHֵ��ø����pHֵ������ͬ���ⶨø��Ӧ��pHֵ��Ӧ�仯����¼��λ-ʱ��(E-t)���ߡ�
1.3 ����ø/����TiO2���ϵ缫�ⶨ����
������ϸɰֽ����˿�����ĥ�ɾ���Ȼ�ֱ���1 mol/L NaOH��Һ������ˮ��ϴ3�Σ����ɡ�������TiO2��������15 min���������õ���˿�缫������TiO2�����н���1 min��ȡ�������ɣ��ظ��������Σ���ò�ͬ��ȵ�TiO2Ĥ�缫��
��2 mg����ø����0.4 mL�����λ�����Һ�С�(1 mmol/L, pH=7.0)��ʹ��ǰ������4 ������С�TiO2Ĥ�缫������ȥ����ˮ�������������15 min����ϴ�������������ø��Һ��24 h(4 ��)���缫����ʱ�����䱣����4 ��������λ�����Һ�С�
�����£��ò�ͬŨ�ȵ�������Ϊø������ݵ�λ��������ø/����TiO2���ϵ缫�ⶨ���ص�Ũ�ȡ�
2 ��������
2.1 TiO2��������ø���Ե�Ӱ��
ͼ1��ʾΪ��ͬ������TiO2������ø���Ե�Ӱ�졣�ɼ���û��TiO2ʱ������ø��pHֵ��Ӧ�仯��С���ֱ����3�ֲ�ͬ������TiO2�̶�������ø��pHֵ��ӦѸ����ߣ���������Ϊ25 nm��5 nm�� TiO2������ø��pHֵ��Ӧ�������������������������ȱ�������������ܸߣ����������ϸߣ�ʹ�����ø��������������TiO2���档���⣬�����������ߴ��С��������ø�ڲ�����ˮ���ŷ������ã��Ӷ�����ø�����ϵı仯�����ֱ仯ʹ��ø�û������ĸ��ӽ���������ø�Ĵ�Ч�ʡ�
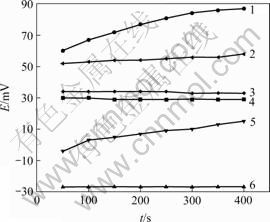
1������ø����������Ϊ25 nm��TiO2���棻2������ø����������Ϊ2.4 ��m��TiO2���棻3������Ϊ2.4 ��m��TiO2�ܽ���4������Ϊ25 nm��TiO2�ܽ���5������ø����������Ϊ5 nm��TiO2���棻6������Ϊ5 nm��TiO2�ܽ�
ͼ1 ��ͬ��������TiO2������ø���Ե�Ӱ��
Fig.1 Effect of difference size nano-TiO2 on activity of urease
������TiO2��Ũ�ȶ�����ø���Ե�Ӱ������о��������������35 �棬pHֵһ���������£���0.1 mol/L������ҺΪ��Һ���ں�0.125 g/L������ø��Һ�н�����TiO2(����25 nm)��Ũ�ȴ�6��10-2 g/L�ı���0.5 g/L��ø��Ӧ��pHֵ��ӦѸ�����ӣ�������������TiO2��Ũ�ȣ�pHֵ��Ӧ���½���
2.2 ���ϳ����IJⶨ
�ֱ�ⶨ����ø�������ڲ�ͬ����TiO2���������ø�����ϳ�����ʵ�����������ø��Ӧ���ֳ�Michaelis-Menton����ѧ������������������ϳ���(Km)��ø�����ﶯ��ѧ����������ֵ����Lineweaver- Burk�������[15]��

����˫������ͼ������1/[S]Ϊ�����꣬1/vΪ��������ͼ�����һ��ֱ�ߣ�����б��Km/V������ؾ�1/V�������Km��
���������������ø�����ϳ���Ϊ0.45 mol/L�������ֱ�Ϊ5 nm��25 nm��2.4 ��m��TiO2����������ø���ϳ����ֱ�Ϊ0.22��0.28��0.31 mol/L���ɼ��������Կ�����������TiO2����������ø���ϳ����ϵͣ�ø�Ļ��Դ�˵������TiO2������ø��������ǿЧӦ��

1������ø����������Ϊ2.4 ��m��TiO2���棻
2������ø����������Ϊ25 nm��TiO2���棻3����������ø��4������ø����������Ϊ5 nm��TiO2����
ͼ2 ����Ũ��������ø��Ӧ�ٶȵĹ�ϵ
Fig.2 Relationship between urea concentration and urease reaction velocity
2.3 ����ø/����TiO2����Ĥ�缫�ⶨ����
����ø������ϵͳ��һ����Ҫ��ø���������ش�ΪCO2��NH3����Ӧʽ���£�
![]()
�������TiO2����̬������Ĥ�Ʊ�����ø/����TiO2����Ĥ�缫���������������ص�Ũ�Ȳⶨ��ͼ3��ʾΪ����ø/TiO2����Ĥ�缫�ⶨ����Ũ�ȵ���Ӧ���ߡ���8 mL 5 mmol/L���ؼ��뵽15 mL 1 mmol/L PBS��Һ�缫��λ��ʱ�����½���������ȶ���ʵ���л��о��˲�ͬĤ��ȶԵ缫��λ��Ӧ��Ӱ�죬���������Ĥ��ȶ��ڸ��ϵ缫�����ص���Ӧû��Ӱ�졣������Ϊ����ʵ�����ֱ���������̶�����ø��ø��Ҫ�̶���TiO2Ĥ�缫������㣬Ĥ�ĺ�ȶ�����ø�Ĺ�����û�кܴ��Ӱ�졣��һ���棬���������Ĥ�������õ��ԣ�����ø���ڶ�ʱ������TiO2���Ĥ��ϡ�ʵ����50~300 s�ڵ�?EΪ����źš�
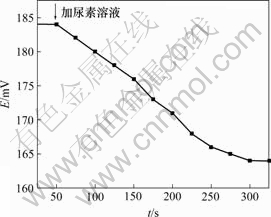
ͼ3 ������Һ�����缫��λ��Ӧ
Fig.3 Potential response of urease/TiO2 electrode after addition of urea
�ı�pHֵ��Ӱ��ø���������ϻ��ŵ����ȣ�ͬʱҲӰ���������ȣ��Ӷ�Ӱ��ø���ӶԵ�����ӵĽ�Ϻʹ���ʵ�����Ż���Na2HPO4/NaH2PO4������Һ��pHֵ�����ָõ缫��pHֵΪ7~8ʱ������øpHֵ��Ӧ���
��25~45 �淶Χ�ڲⶨ���¶ȶԵ缫��Ӧ��Ӱ�죬������֣������¶ȵ����ߣ��缫��Ӧ���������¶ȴ���35 ��ʱ��ø�����ȱ��ԣ��缫��Ӧ�������¶����߶����͡���ˣ��缫��������Ϊ��pHֵΪ7~8��PBS������Һ���¶�Ϊ35 �档��ʱ��Ӧ���
����ѹ��������²ⶨ����Ũ�ȶԵ缫��λ��Ӱ�죬�����ͼ4��ʾ���ɼ����缫��λ������Ũ�ȳ����Թ�ϵ�������Իع鷽��������ϵ��Ϊ0.993 73�����صļ�ⷶΧΪ8.5��10-5~0.15 mol/L���������Ϊ3ʱ(pH�Ƶ����Ϊ��1 mV)����ø÷����������صļ����Ϊ5��10-6 mol/L��
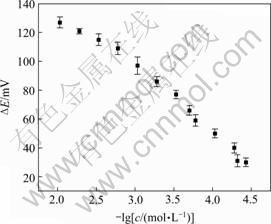
ͼ4 �缫��Ӧ������Ũ��c��ϵ
Fig.4 Dependence of potential response of urease/TiO2 electrode on concentration of urea
��35 �棬pH=7.0��PBS������Һ�У��ⶨ����ø/����TiO2����Ĥ�缫��ʹ������(��ͼ5)������������õ缫��λ��Ӧ�ɳ���35 d��35 d��缫��Ӧ��Ȼά������ø���л��Ե�38%���缫����ʱ��������PBS�У����ܹⱣ����4 ������С�

ͼ5 ����ø/TiO2����Ĥ�缫��ʹ������
Fig.5 Lifetime of urease/TiO2 complex films electrode
3 �� ��
a. ����TiO2�����ܹ���Ч���������ø�Ĵ����ԡ�������TiO2Ϊ���ػ����Ʊ�������ø/����TiO2����Ĥ�缫������������ø�缫��ȣ��ڲⶨ����Ũ��ʱ��һ���ĸĽ���
b. ������ø/����TiO2���ϵ缫���������������ȸߣ�ʹ�������������軯ѧ���Ρ�
�ο����ף�
[1] Agheli H, Malmstrom J, Hanarp P, et al. Nanostructured biointerfaces[J]. Materials Science and Engineering C, 2006, 26: 911-917.
[2] Keller N, Pietruszka B, Keller V. A new one-dimensional tungsten carbide nanostructured material[J]. Materials Letters, 2006, 60: 1774-1777.
[3] Yakovlev N, Kaveev A, Sokolov N, et al. Novel magnetic nanostructures: Epitaxial cobalt films in transparent fluoride matrix[J]. Current Applied Physics, 2006, 6: 575-578.
[4] Service R F. Nanomaterials show signs of toxicity[J] . Science, 2003, 300: 243.
[5] Brumfiel G. A little knowledge[J]. Nature, 2003, 424: 246-248.
[6] Teixeira A I, Mckie G A, Foley J D, et al. The effect of environmental factors on the response of human corneal epithelial cells to nanoscale substrate topography[J].Biomaterials, 2006, 27(21): 3945-3954.
[7] Kim J, Grate J W, Wang P. Nanostructures for enzyme stabilization[J]. Chemical Engineering Science, 2006, 61: 1017-1026.
[8] Yeates T O, Padilla J E. Designing supramolecular protein assemblies[J]. Current Opinion in Structural Biology, 2002, 12(4): 464-470.
[9] Woolley A T, Cheung C L, Hafner J H , et al .Structural biology with carbon nanotube AFM probes[J]. Chemistry & Biology, 2000, 7(11): R193-R204.
[10] Hafner J H, Cheung C L, Woolley A T, et al. Structural and functional imaging with carbon nanotube AFM probes[J]. Progress in Biophysics and Molecular Biology, 2001, 77(1): 73-110.
[11] Oberdorster G, Finkelstein J N, Johnston C. Acute pulmonary effects of ultrafine particles in rats and mice[J]. Res Rep Health Eff Inst, 2000, 96: 5-74.
[12] �� ��. ���������ѹ�������ڻ�����ѧ�е�Ӧ��[J]. ����ѧԺѧ��, 2006, 5(4): 57-60
ZHANG Ye. Application of nanometer TiO2 photocatalysis technique in environmental science[J]. Journal of Dali University, 2006, 5(4): 57-60.
[13] ������, �� ��, �����, ��. ����TiO2�IJ��Ӹ��Լ�Ӧ�ý�չ�о�[J]. ϡ�н����챨, 2005, 24(12): 6-10.
ZHANG Qing-long, SHEN Yi, WU Guo-you, et al. Modification of TiO2 photocatalyst and application[J]. Rare Metals Letters, 2005, 24(12): 6-10.
[14] �� ��, �� ��, ������. TiO2�����������о���չ[J]. ����������, 2005, 10(12): 6-9.
ZHAI Lin, ZHONG Fei, LIU Peng-yi. Advances in research of TiO2 gas sensors[J]. Sensor World, 2005, 10(12): 6-9.
[15] �� ��, �쾲��, �º�Ԩ. ����SiO2�������ӹ̶�������������ø�����ﴫ����[J]. �ߵ�ѧУ��ѧѧ��, 2004, 25(4): 614-617.
ZHANG Juan, XU Jing-juan, CHEN Hong-yuan. A biosensor based on immobilizing horseradish peroxidase on SiO2 nanoparticles[J]. Chemical Journal of Chinese Universities, 2004, 25(4): 614-617.
�ո����ڣ�2006-09-05
������Ŀ��������Ȼ��ѧ����������Ŀ(20475065)
����飺˾ʿ��(1967-)���У����Ϲ�ʼ�ˣ����ڣ���ʿ���������ײ��ϼ����ﴫ�������о�
ͨѶ���ߣ�˾ʿ�ԣ��У����ڣ��绰��0731-8836993��E-mail: sishihui@mail.csu.edu.cn
[4] Service R F. Nanomaterials show signs of toxicity[J] . Science, 2003, 300: 243.
[5] Brumfiel G. A little knowledge[J]. Nature, 2003, 424: 246-248.
" target="blank">[15] �� ��, �쾲��, �º�Ԩ. ����SiO2�������ӹ̶�������������ø�����ﴫ����[J]. �ߵ�ѧУ��ѧѧ��, 2004, 25(4): 614-617.ZHANG Juan, XU Jing-juan, CHEN Hong-yuan. A biosensor based on immobilizing horseradish peroxidase on SiO2 nanoparticles[J]. Chemical Journal of Chinese Universities, 2004, 25(4): 614-617.


