���±�ţ�1004-0609(2009)08-1511-06
EDTA��Ϸ��ϳ����ᱵ��
�� �������º�������������־�ˣ���������������
(���ϴ�ѧ ұ���ѧ�빤��ѧԺ����ɳ 410083)
ժ Ҫ��
����EDTA ��Ϸ��������ºϳ������ᱵ��������X��������(XRD)������Ҷ�������(FTIR)�Լ�ɨ���������(SEM)�о��˸����ᱵ���Ľṹ����ò���о���Ӧ���������ᱵ������ò��Ӱ�죬���㲻ͬpH ֵ��Ba-EDTA �����������ȶ����������������EDTA ����Ч�������ᱵ�����Ĵ�С����ò���ڸ��ַ�Ӧ�����У�pHֵ�Բ�����ò��Ӱ�����pHֵΪ9~10ʱ���õ������ᱵ�����������ҷ�ɢ�Ժã�SO42?�ļ����ٶȶ�BaSO4��������òӰ�첻����������Ba-EDTA����������Ba2+���ͷ��ٶȡ�FTIR�����ʾ���Ʊ���BaSO4��������������EDTA�Ĺ����š�
�ؼ��ʣ�
��ͼ����ţ�TQ 132.3 ���ױ�ʶ�룺 A
Synthesis of barium sulfate particles by complexation method in presence of EDTA
ZHANG Ming, LI Xin-hai, HU Qi-yang, WANG Zhi-xing, GUO Hua-jun, LIU Wan-rong
(School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China)
Abstract: Barium sulfate particles were synthesized in the presence of EDTA at room temperature. X-ray diffractometry (XRD), Fourier transform infrared resonance(FTIR) and scanning electron microscopy (SEM) were used to characterize the structure and morphology of BaSO4 particles. The effect of the preparation parameters on the particles size distribution and morphology were investigated. The complexation stability constant of Ba-EDTA at different pH values was calculated. The results show that the size and morphology of BaSO4 particles can be effectively controlled by additing EDTA in the precipitation process. Among all the operation conditions, the pH value has significant effect on the particle size. The obtained barium sulfate particles are spherical and well dispersed at pH=9?10. The feeding rate of SO42? has less effect on the morphology of BaSO4, the reason is that Ba-EDTA complex controls effectively the reactivty of Ba2+ in the solution. The FTIR result dacates that the surface of the prepared BaSO4 absorbs the functional group of EDTA.
Key words: EDTA; barium sulfate; complexation reaction
�����¹��������Ŀ������úͲ�����ҵ�����չ�����ᱵ��Ϊ�ڶ���ҵ����Ҫԭ�ϣ���Ӧ��������������������Ҫ��Ҳ�������[1?4]����ҽҩ����X����˫����Ӱ�����ķ�չ��Ҫ�߱��ߺ�������ճ�ȡ�����ϸ�������ŵ����ܵ����ᱵ[1]�������ϡ���ֽ��������ҲҪ��ϸ���ȵ����ᱵ��Ϊ�����������Ӽ������������������о���̽���µĺϳɷ����Ի�ú������Ⱥ���ò�����ᱵ����[5?12]��������[5]�����Ͱ�ˮ����Һ���Ʊ����������ᱵ���������о��˱�����Լ��Կ�����Ӱ�죬�õ�����ѹ�������Ϊ��55 mL�����顢30 mL���Ҷ������������ѡ�15 mL��������10 mL�Ȼ��������Һ��JIA��[6]�ڱ�Ĥ��Ӧ���кϳ��������ᱵ���ڷ�Ӧ�����У�Na2SO4��Һ��������Ĥ��������BaCl2��Һ�У���Ч������Һ�����Ͷȣ��Ӷ��õ�ϸС���ȵ�BaSO4������ZHAO��[13]�ڳ��������м���EDTA�õ�ֱ��Ϊ16 nm��BaSO4������������ƫ��������ɵõ�203 nm��BaSO4������Һ�෴Ӧ��Ȼ����õķ������������������žۣ��������ںϳ����������Ĺ����С����⣬��Щ�������ո��ӣ���Ӧʱ�䳤�����������ڷ�Ӧ��ϵ�������˴���������Լ���ʹ����Щ�л�����������Է���[13]������������ϳ�����Խ��Խ�ܵ��о��ߵĹ�ע���������ֺϳɷ������м�����С��ܺĵ��Լ�������ò���Ƶ��ŵ㣬��˱������ϳɽ���������[14]��������[15]�ȶ�������[16?17]��
�������߲���EDTA��ϳ��������������Ʊ�����BaSO4������ʹ��EDTA����ǿ��ϼ��������������ϣ�Ȼ���ٽ��г�����Ӧ�Ժϳ����ᱵ������������ϼ���pHֵ�ͼ��Ϸ�ʽ�ȷ�Ӧ���������ղ�����ò��Ӱ�죬���������������ȶ������������˽�EDTA�Բ�����ò����Ӱ����������ݡ�
1 ʵ��
��BaCl2��2H2O ��Na2SO4 Ϊԭ�ϲ��û�ѧ��������(25 ��)�����ºϳ�BaSO4�����岽�����£���һ������EDTA������(Na2H2Y��2H2O)(EDTA��Ba2+��Ħ����Ϊ1?1)�ܽ0.5 mol/L��BaCl2 ��Һ�У�����HCl ����NaOH ����pHֵ��һ����Χ���ٽ����ƺõ�0.5 mol/L Na2SO4 ��Һ�Բ�ͬ���ٶȼ��뵽������Һ�У�ͬʱ���衣��Һ���Dz��а�ɫ�������ɡ���������1 h��Ӧ���ܷ⣬����һ��ʱ�䡣�õ��ij�����ȥ����ˮ�Լ���ˮ�Ҵ�ϴ�����κ���80 ���¸���24 h�õ����ղ���BaSO4�����з�Ӧ���Ϊ��������
����Hitachi S530 ��ɨ���������(SEM)�۲������ò������RigakuX���������Ƿ�����������࣬Cu K������Դ��ɨ������Ϊ10?~70?���ܵ�ѹΪ50 kV���ܵ���Ϊ100 mA������NICOLET ����Ҷ�������(FTIR)�ǡ�KBr ѹƬ�������������к����������
2 ���������
2.1 EDTA��BaSO4��ò��Ӱ��
��������������̿��Էֳɾ��˵��γɺͳ������������ᱵ���ܶȻ�������С(Ksp=1.1��10?10)���������̷dz�Ѹ�١���Ba2+��SO42?��������������˲ʱ���ɣ��������������������ھ���ϸС���ȱ�����������žۣ��ϳɵ�BaSO4��ò��ͼ1(a)��ʾ��ͼ1(b)��ʾΪ��Ӧ�����м���EDTA�����Ż���Ӧ������õ������ξ���ɢ��BaSO4 ��������ͼ1(b)�ɿ�������������ԼΪ1 ��m��˵��EDTA ������Ч�ظ��ƺͿ���BaSO4 ����ò��ͼ2��ʾΪ���Ż������²���EDTA�������BaSO4�����XRD�ס���ͼ2���Կ������Ʊ���BaSO4����Ϊ������ϵ�������������Ƭ(JSCDX?1035)���Ӧ��

ͼ1 ����EDTA����ʱBaSO4 ������SEM��
Fig.1 SEM images of BaSO4 particles obtained in absence (a) and presence (b) of EDTA
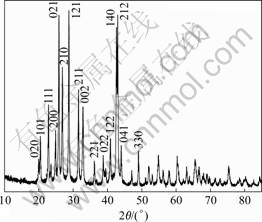
ͼ2 ���Ż������²���EDTA��ϵõ�BaSO4 ������XRD��
Fig.2 XRD pattern of BaSO4 particles obtained with EDTA under optimum reaction conditions
ͼ3 ��ʾΪ���Ż������²���EDTA�������BaSO4������FTIR�ס���ͼ3��֪��λ��3 450 cm?1������ƽ�������մ��Ƿ��Ӽ������ˮ�����е�O��H�������壻2 500~3 000 cm?1��������Ϊ��Ƶ��������COOH���ŵ���������1 635 cm?1����COO?�������壻1 408 cm?1��OH?�������壻λ��1 173��1 110��982��610 cm?1�ļ������շ������SO42?�������壻λ��633 cm?1���������շ�����Ba��O����ɵġ�FTIR�Ľ��˵������BaSO4�����в���EDTA���ʡ�
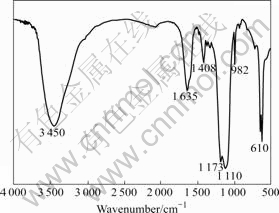
ͼ3 ���Ż������²���EDTA�������BaSO4 ������FTIR��
Fig.3 FTIR spectrum of BaSO4 particles obtained with EDTA under optimum reaction conditions
EDTA��һ�ֳ��õ���ϼ������ķ�������������������4���Ȼ�����������������γ���λ����EDTA����������ӵ������ṹʽ��ͼ4 ��ʾ����EDTA���뵽BaCl2 ��Һ�к�Ba2+Ѹ����EDTA����γ�Ba2+-EDTA����Ba2+-EDTA����SO42?��������BaSO4��������Ӧʽ���£�
Ba2++EDTA![]() Ba2+��EDTA (1)
Ba2+��EDTA (1)
Ba2+��EDTA+SO42?![]() BaSO4+EDTA (2)
BaSO4+EDTA (2)
����Ba-EDTA�������һ�����ȶ��ԣ���ˣ�������BaSO4���������У��൱�ڿ�����Ba2+���ͷ��ٶȣ�ʹ���ɵľ�����ʱ���ֳ���
2.2 pHֵ��BaSO4������ò��Ӱ��
��ˮ��Һ�У�EDTA�������·�ʽ������⣺
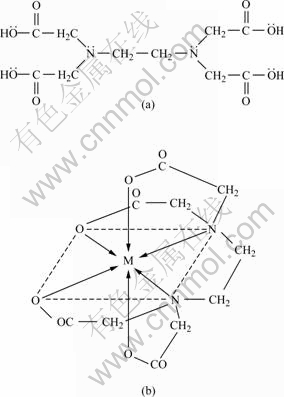
ͼ4 EDTA ��EDTA����������γ������ķ��ӽṹʽ
Fig.4 Molecular structural formula of EDTA (a) and M-EDTA complex (b)
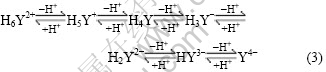
![]()
ʽ�У�M��ʾ�������ӣ�Y��ʾEDTA�����ӡ�
������������Y֮�䷢������Ӧ����ʹEDTA �μ�����Ӧ�������½�����ЧӦϵ����Y(H)��ʾ��һ��pH ֵ�£�δ�μ���λ��Ӧ��EDTA�ĸ��ִ�����ʽ����Ũ��[Y��]���ܲμ���Ϸ�Ӧ��Y4?��ƽ��Ũ��[Y]֮�ȣ���
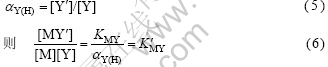
��ʽ(6)ȡ����������
![]()
ʽ�У�KMYΪ�ȶ���������Y(H)Ϊ��ЧӦϵ���� Ϊ�����ȶ�����������˵������Һ���Ӱ����������ʵ���ȶ��̶ȣ�[M]ΪEDTA��ϵĽ�������Ũ�ȡ���1����ΪBa-EDTA ������ڲ�ͬpH ֵʱ���ȶ�������
Ϊ�����ȶ�����������˵������Һ���Ӱ����������ʵ���ȶ��̶ȣ�[M]ΪEDTA��ϵĽ�������Ũ�ȡ���1����ΪBa-EDTA ������ڲ�ͬpH ֵʱ���ȶ�������
�ɱ�1���Կ���������pHֵ������ Ҳ����������pHֵ������Ba-EDTA �����Խ��Խ�ȶ�����SO42?���뵽��ϵ�У�Ba2+�ͷ��ٶȻ������Ӷ��õ���BaSO4 ����������(��ͼ5(a)~(c))����pH��10ʱ��BaSO4 ������ʼ��С�����ҿ�ʼ�ž�(��ͼ5(d)~(e))�������������ʵ������м����NaOH �ƻ���Na2H2Y��ˮ��ƽ�⣺
Ҳ����������pHֵ������Ba-EDTA �����Խ��Խ�ȶ�����SO42?���뵽��ϵ�У�Ba2+�ͷ��ٶȻ������Ӷ��õ���BaSO4 ����������(��ͼ5(a)~(c))����pH��10ʱ��BaSO4 ������ʼ��С�����ҿ�ʼ�ž�(��ͼ5(d)~(e))�������������ʵ������м����NaOH �ƻ���Na2H2Y��ˮ��ƽ�⣺
Na2H2Y![]() 2Na++H2Y2? (4)
2Na++H2Y2? (4)
��1 ��ͬpHֵʱBa-EDTA������lgKBaY, lg��Y(H)�� lg
Table 1 lgKBaY, lg��Y(H), lg of Ba-EDTA complex at different pH values
of Ba-EDTA complex at different pH values
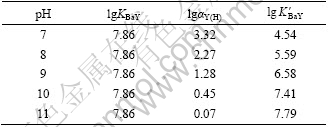
���SEM����Կ�������pHֵΪ9~10ʱ���õ���BaSO4 ���������Σ���С���ȣ���ɢ�Ժá�
2.3 ��Ӧ������ٶȶ�BaSO4������ò��Ӱ��
��������ѡ�����ַ�ʽ��Ba-EDTA ��ϵ�еμ�Na2SO4 �����鷴Ӧ������ٶȶ�BaSO4 ��ò��Ӱ�죬��һ�ַ�ʽΪ��μ��룬�μ��ٶ�Ϊ3 mL/min���õ���BaSO4 ������ͼ6(a)��ʾ���ڶ��ַ�ʽΪ��Na2SO4 ���ٵ���Ba-EDTA ��ϵ�У��õ���BaSO4������ò��ͼ6(b)��ʾ����ͼ6���Կ��������ּ��Ϸ�ʽ�õ���BaSO4 ��ò����������е�һ�ּ��Ϸ�ʽ�õ��IJ������ȷֲ����Ӿ��ȡ�������EDTA��Ba2+�����һ����Ȼ��ϵ��SO42?˲ʱ�������࣬��EDTA ��������ϵ��Ba2+��Ũ�ȣ���ˣ���Ӧ��μ��ٶȶ�BaSO4��ò��Ӱ�첢���Ǻܴ�

ͼ5 ��ͬpHֵʱ����EDTA ��Ϸ��Ʊ�BaSO4 ������SEM��
Fig.5 SEM images of BaSO4 particles obtained at pH value of
7 (a), 8 (b), 9 (c), 10 (d) and 11 (e) in presence of EDTA

ͼ 6 pHֵΪ9ʱ����EDTA�������BaSO4������SEM��
Fig.6 SEM images of BaSO4 particles obtained with EDTA at pH=9: (a) Drop by drop; (b) Poured int
3 ����
1) ����EDTA ��������������ºϳ������ξ���ɢBaSO4 ����������ԼΪ1 ��m��
2) ͨ��EDTA ��������ÿ�����Ч������ϵ��Ba2+�Ĺ����Ͷȣ�ʹ�þ�����ʱ���ֳ��Ӷ����һ���Ժá���ɢ���ȵ�����BaSO4 �������ڸ��ַ�Ӧ�����У�pH ֵ��Ӱ����Ϊ���ԡ�pHֵΪ9~10ʱ�õ���BaSO4���������Σ���С���ȣ���ɢ�Ժá�
3) ͨ������Ba-EDTA�ڲ�ͬpHֵ�µ������ȶ�������pHֵԽ��Ba-EDTA�����Խ�ȶ�����SO42?���뵽��ϵ�У�Ba2+�ͷ��ٶȱ仺���Ӷ��õ���BaSO4��������pH��10ʱ��������С�������žۣ���������NaOH�ļ����ƻ���Na2H2Y��ˮ��ƽ�⡣
[1] ������, ������, ������. ����CTɨ���Ƿ�����ͬ����BaSO4��X���ߵ�˥������[J]. ɽ��ʦ����ѧѧ��: ��Ȼ��ѧ��, 2007, 22(2): 66?68.
LIU Ji-hua, XU Dong-bin, XIN Yin-chang. Study on different types of barium sulfate attenuation to X-ray by CT scanner[J]. Journal of Shandong Normal University(Nature Science), 2007, 22(2): 66?68.
[2] VINK A P, VANDER K E, DORENBOS P, van EIJK C W E. Luminescent properties of Ce3+ in MSO4 (M: Ca, Sr and Ba) and the effect of Na+ co-doping[J]. Optics Commuications, 2002, 210: 277?284.
[3] NAGARAJA B M, ABIMANYU H, JUNG K D, YOO K S. Preparation of mesostructured barium sulfate with high surface area by dispersion method and its characterization[J]. J Colloid Interf Sci, 2007, 316: 645?651.
[4] GONZALEZ P R, FURETTA C, CALVO B E, GASO M I, CRUZ-ZARAGOZA E. Dosimetric characterization of a new preparation of BaSO4 activated by Eu ions[J]. Nucl Instrum Meth B, 2007, 260: 685?692.
[5] �� ��, �����, �� ��, ������. ���Ͱ�ˮ����Һ���Ʊ���ϸ���ᱵ����[J]. �廪��ѧѧ��: ��Ȼ��ѧ��, 2002, 42(12): 1594?1597.
WANG Min, WANG Yu-jun, GUO Lin, ZHU Shen-lin. Preparation of ultrafine barium sulfate particle using a water/oil microemulsion[J]. Journal of Tsinghua University: Science & Technology, 2002, 42(12): 1594?1597.
[6] JIA Z Q, LIU Z Z. Synthesis of nanosized BaSO4 particles with a membrane reactor: effects of operating parameters on particles[J]. J Membr Sci, 2002, 209(1): 153?161.
[7] BALA H, FU W Y, ZHAO J Z. Preparation of BaSO4 nanoparticles with self-dispersing properties[J]. Colloids and Surfaces A: Physicochem Eng Aspects, 2005, 252: 129?134.
[8] CHEN Q D, BAO H Y, SHEN X H. Radiolytic synthesis of BaSO4 microspheres[J]. Radiat Phys Chem, 2008, 77: 974?977.
[9] GUO Z, JONES A G, LI N. The effect of ultrosound on the homogeneous nucleation of BaSO4 during reactive crystallization[J]. Chemical Engineering Science, 2006, 61: 1617?1626.
[10] ������, ���ƽ, Ա��ʤ, ����˨. ���ᱵ���������Ʊ������о�[J]. Ӧ�û����빤�̿�ѧѧ��, 2001, 9(2/3): 141?145.
LIU You-zhi, LI Jun-ping, YUAN Ru-sheng, LIU Lai-shuan. Study on the preparation methods of nano BaSO4 particles[J]. J Basic Science and Engineering, 2001, 9(2/3): 141?145.
[11] Ԭ��, Ҧ ��, ������, ʯ�һ�, ������. P(St-co-Ma)ˮ���Ծۺ�������ᱵ������ò�ĵ���[J]. ���ܸ߷���ѧ��, 2007, 19/20(1): 49?52.
YUAN Jin-fang, YAO Li, GUO Bao-lin, SHI Jia-hua, GAO Qing-yu. Control of barium sulfate crystal morphology with water soluble copolymer P(St-co-Ma)[J]. J Functional Polymers, 2007, 19/20(1): 49?52.
[12] UCHIDA M, SUE A, YOSHIOKA T, OKUWAKI A. Hydrothermal synthesis of needle-like barium sulfate using a barium(��)-EDTA chelate precursor and sulfate ions[J]. J Mater Sci Lett, 2002, 19: 1373?1374.
[13] ZHAO Y H, LIU J R. Effect of EDTA and phosphate on particle size during precipitation of nanosized BaSO4 particles[J]. Chem Lett, 2006, 35(9): 1040?1041.
[14] WANG L X, ZHANG Q T. The effect of pH values on the phase formation and properties of BaFe12O19 prepared by citrate-EDTA complexing method[J]. J Alloys and Compounds, 2008, 454: 410?414.
[15] MA L, CHEN W X, ZHENG Y F, XU Z D. Hydrothermal growth and morphology evolution of CePO4 aggregates by a complexing method[J]. Mater Res Bull, 2008, 43: 2840?2849.
[16] WANG X J, WAN F Q, LIU J, GAO Y J, JIANG K. Synthesis and characterization of Cu3P hollow spheres by a facile soft-template process[J]. J Alloys and Compounds, 2008, doi:10:1016/j.jallcom.2008.06.052.
[17] ZHU R H, YU R B, YAO J X, WANG D, KE J J. Morphology control of hydroxyapatite through hydrothermal process[J]. J Alloys and Compounds, 2008, 457: 555?559.
������Ŀ�������ص�����о���չ�ƻ�������Ŀ(2007CB613607)
�ո����ڣ�2008-09-24�������ڣ�2009-02-09
ͨѶ���ߣ����º������ڣ���ʿ���绰��0731-88836633��E-mail: xhli@mail.csu.edu.cn
ժ Ҫ������EDTA ��Ϸ��������ºϳ������ᱵ��������X��������(XRD)������Ҷ�������(FTIR)�Լ�ɨ���������(SEM)�о��˸����ᱵ���Ľṹ����ò���о���Ӧ���������ᱵ������ò��Ӱ�죬���㲻ͬpH ֵ��Ba-EDTA �����������ȶ����������������EDTA ����Ч�������ᱵ�����Ĵ�С����ò���ڸ��ַ�Ӧ�����У�pHֵ�Բ�����ò��Ӱ�����pHֵΪ9~10ʱ���õ������ᱵ�����������ҷ�ɢ�Ժã�SO42?�ļ����ٶȶ�BaSO4��������òӰ�첻����������Ba-EDTA����������Ba2+���ͷ��ٶȡ�FTIR�����ʾ���Ʊ���BaSO4��������������EDTA�Ĺ����š�


