���±��: 1004-0609(2006)05-0904-05
O2/Ar��������������ȷֽ��Ʊ���
WO3����ֽ�ˮ��������
������1, 2, ����Ԫ1, ������1, �ܽ���1, �� ��1
(1. ���ϴ�ѧ ��ѧ����ѧԺ, ��ɳ 410083;
2. �������մ�ѧԺ ���Ͽ�ѧ�빤��ѧԺ, ������ 333001)
ժ Ҫ��
�ڲ�ͬ���O2/Ar�������������, ��700�潫������識��ȷֽ��Ʊ�WO3������ ����XRD�� XPS�� DRS�ȼ����Դ������б���, ��������ڵ��ӽ�����Fe3+��Һ��ϵ�µĹ���ֽ�ˮ�������ԡ� �������: Ar��������, WO3������������λ����, ���������������, ��Ar���������õ�WO3�����������������ߡ� �о���Fe2+�Թ���ֽ�ˮ�������Ե�Ӱ��, ��Fe3+������Ϊ���ӽ�����Ĺ���ֽ�ˮ������Ӧ��, һ��Ũ�ȵ�Fe2+��������������WO3����������, ��Fe2+���Ӻ�Fe3+���ӵ�Ũ���൱ʱ, WO3������ȫʧȥ����������ԡ�
�ؼ���: WO3; O2/Ar����; ����λ; ���; �ֽ�ˮ ��ͼ�����: O612.6; O643.36
���ױ�ʶ��: A
Photocatalytic activity for O2 evolution of WO3 prepared through pyrolysis of ammonium paratungstate under O2/Ar atmosphere
GAO You-liang1, 2, CHEN Qi-yuan1, YIN Zhou-lan1, ZHOU Jian-liang1, LI Jie1
(1. School of Chemistry and Chemical Engineering, Central South University,Changsha 410083, China;
2. School of Materials Science and Engineering, Jingdezhen Ceramic Institute,Jingdezhen 333001, China)
Abstract: A series of WO3 catalysts were obtained through pyrolysis of ammonium paratungstate under different O2/Ar at 700��. The catalysts were identified by XRD, XPS, DRS measurements, and the photocatalytic activity of WO3 for O2 evolution was studied. The results indicate that with the increasing content of Ar, the oxygen vacancies of WO3 catalysts are increased, the photocatalytic activity for O2 evolution is advanced and the photocatalytic activity of WO3 obtained in pure Ar is the highest. The influence of Fe2+ on photocatalytic activity for O2 evolution was also investigated. The results show that the activity of WO3 is restrained by Fe2+ in the photocatalytic reaction with Fe3+ as electron acceptor.
Key words: WO3; O2/Ar atmosphere; oxygen vacancy; photocatalytic; water splitting
����������Ϊ���ܲ���, �ѹ㷺Ӧ���ڹ��±�ɫ[1-3]�� ���±�ɫ[4, 5]�Լ����崫����[6, 7]�ȷ��档 ����, ����������Ϊ�뵼��Ӧ���ڹ��ˮ���о������ࡣ Gratian��[8]�����о������������ڿɼ����յ��µ��������; Sayama��[9]������Fe3+/Fe2+������WO3��ɵ�������ԭϵͳ, ��ϵͳ��WO3��Fe3+���ڵ�������, ���ڿɼ����²�������, ��Fe3+���ϱ�����, ͬʱFe2+�����ֺ�������������±�������ΪFe3+����, ����������, ʵ������ѭ��; Bamwenda��[10]�о������Ƶ�WO3, Ce4+/Ce3+ϵͳ�� ��������ϵ��������WO3������, ʵ�ֲַ��������⡣
����������뵼�������������ȱ���������[11], ��λ(����Ԫ�ؿ�λ������λ)�ǽ����������г����ĵ�ȱ��, �ڻ�ԭ�������жԽ�������������ȴ�������ɽ�����������ɵ�������, �����������λ�� ���Ƕ�WO3�뵼����Ϊ����������˳����о�, ����WO3������λ���������ܵ�Ӱ����о�δ���б����� �������߲��ò�ͬ��ɵ�O2/Ar��������������什����ȷֽ��, �õ�һϵ�к���ͬ����λ��WO3����, �����������Խ������о�; ����, ����Fe2+��WO3����ֽ�ˮ�������Ե�Ӱ��������о���
1 ʵ��
1.1 WO3�������Ʊ�
�ֱ�ȡһ�������������(AR, �㶫̨ɽ������)�ڴ�����, ���ڹ�ʽ¯, ͨ��ͬ���Ar/O2�������, ͬʱ������700��, ����4h��, ������ȴ�����¡� ��ͬ���Ar/O2�������(����60mL/min)�������Ƶõ�WO3��Ʒ�ֱ����ڱ�1��
��1 ��ͬ���O2/Ar��������������Ƶõ�WO3��Ʒ
Table 1 WO3 prepared under different atmosphere of O2/Ar

1.2 WO3�����ı���
�����ձ���ѧD/max 2250ȫ�Զ�ת��X���������Ǽ����Ʒ�ľ���, ��������Ϊ: ������ѹ40kV, ��������300mA, Cu��K������(��=0.154056nm), ʯī��ɫ���� ����Ӣ��Kratos��˾XSAM800���������Dzⶨ��Ʒ�ı������, ���������Ϊ: ����ԴΪMgK��, ����Ϊ1253.6eV, 16mA, 12kV, ������ģʽΪFRR, �зֱ�, ��������ն�����5��10-7Pa, ���ӽ������ֵ������Ⱦ̼(C1s, BE: 284.7eV)У�� ���ñ�������ͨ��TU-1901 ����ɼ��ֹ��ȼ�(��IS19-1������, BaSO4Ϊ�αȱ��װ�)�Դ����������������(DRS)������ WO3����ָ��������Ӳ�ʺϽ�������˾�����������IJ���, ��������: 1) ȷ��ȡ0.1g���Ҵ�����Ʒ����250mL��ƿ��, ��20mLˮ, 10mL KOH(100g/L)��Һ, 10mL K3[Fe(CN)6](0.25mol/L)��Һ, ����ҡ��, ʹ��Ʒ��ȫ�ܽ�; 2) ����10mL H3PO4(��=1.68g/mL), 5mL H2SO4(5mol/L)��Һ, ����, ��ȴ������; 3) ��KMnO4(0.02mol/L)����Һ�ζ������ֺ�ɫ, ��(0.5~1.0)min�ڲ���ʧ��Ϊ�յ㡣 ����, ȷ��ȡ����Ʒ�����Ķ������ٻ�����250mL��ƿ��, Ȼ��ͬ��������1)�� 2)��3)���С� ��ʽ1)������ָ��(X)��ֵ:
X=3-V/V0(1)
ʽ�� V0Ϊ�ζ��������ٻ���������KMnO4(0.02mol/L)����Һ�����, mL; VΪ�ζ�������Ʒ������KMnO4(0.02mol/L)����Һ�����, mL��
����SP-2305 ������ɫ����(�ȵ��ؼ������ ���Ϊ������ �̶���Ϊ5A����ɸ)�������Ӧ���
1.3 ������Լ��
��Ӧװ�ò������Ƶ����ù�Դ�пռ���ʽʯӢ��Ӧ��(Լ560mL), ��Դ��250W��ѹ����, ��������Ϊ365nm�� ��Ӧǰ��560mL������ˮ���10min�Ծ�����ȥ��Ӧ��ϵ�е�����, ������ȴ�����º���뵽��Ӧװ����, ͬʱ����4.48g WO3����, ���Ʒ�Ӧ��pHΪ2.0�� �¶�Ϊ32�桢 ���ӽ�����Fe3+��Ũ��Ϊ32.0mmol/L�� ���ô���������ʹ������������, ����������ͨ������ɫ������
2 ���������
2.1 WO3������X���������ͱ���������
ͼ1��ʾΪWO3��ƷWO3(A0)�� WO3(A1)�� WO3(A2)�� WO3(A3)��X���������ס� ��ͼ1���Կ���4�ִ�����Ϊ��������, ��������識��ȷֽ������, û��������������������IJ�ͬ���ı侧��ṹ��

ͼ1 WO3������X����������
Fig.1 XRD patterns of WO3 catalysts
ͼ2��3��ʾ�ֱ�ΪWO3(A3)��WO3(A0)��XPS�ס� ��ͼ2��֪, ����WO3(A3)����W���ִ���2�ּ�̬, 35.500eV��37.670eV�ֱ��Ӧ��W6+��4f7/2��4f5/2, ռ73.33%; 34.300eV ��36.470eV�ֱ��Ӧ��W5+ ��4f7/2��4f5/2, ռ30.50%�� ��ͼ3��֪, ����WO3(A0)����W���ִ���3�ּ�̬, 35.500eV��37.670eV�ֱ��Ӧ��W6+��4f7/2��4f5/2, ռ65.87%; 34.200eV ��36.370eV�ֱ��Ӧ�ڵ�4f7/2��4f5/2, ռ22.38%; 32.800eV��34.800eV�ֱ��Ӧ��W4+ ��4f7/2��4f5/2, ռ11.74%�� �����������֪, �������Ƚϳ��(������е��������ӽ�)ʱ, ��������ȷֽ������WO3(A3)�������W6+��, �����ٲ���W5+, ���ڴ�Ar������, ��������ȷֽ������WO3(A0)���治����W6+��W5+, ���в���W4+, ��W5+��W4+֮����ռ��������, W6+��ռ��������, ��Ӧ������λ����֮���ࡣ
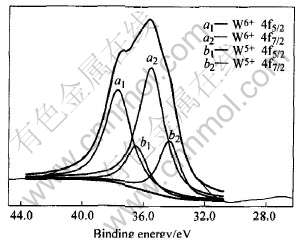
ͼ2 WO3(A3)��XPSͼ
Fig.2 XPS spectra of WO3(A3)
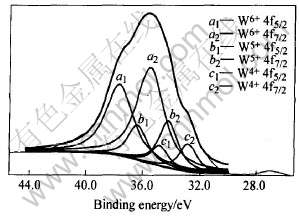
ͼ3 WO3(A0)��XPSͼ
Fig.3 XPS spectra of WO3(A0)
2.2 WO3���������������(DRS)
��200~700nm��Χ��������-�ɼ���������ײ���, �����ͼ4�� ��ͼ4��֪, ��200~420nm��Χ��, ��WO3�����ķ����ʻ�����ͬ, �����������������Ĺ��������ܲ��, ����420~700nm��Χ��, WO3(A0)�� WO3(A1)�ķ���������С��WO3(A2)�� WO3(A3), ��WO3(A0)�ķ�������С�� �����ʵļ�С��ζ�ŶԿɼ������յļ�ǿ, ��ǰ�ߵĹ��������ܵ������Ը���, ��Կɼ����������ܴ�С˳��Ϊ: WO3(A3)��WO3(A2)��WO3(A1)��WO3(A0)�� ������[11]ָ��, �ڻ�ԭ�������д�������������ʱ, ���������з�Ӧ:
![]()
![]() ,
, ![]() �ǽ����������е�����λ, ����������, ��������������λ�����ĵ���, �����ױ�����������, �������λ��ʩ��������, ���ǵ��ܼ�ED�ڽ����д��ڵ�����EC����, ��ͼ5��ʾ�� ˵������������ȷֽ�(������ԭ������NH3)������, ����Ar����������, ������Բ���, ����λ����Ӧ����, ���������ĵ�������Ӧ����, �����420~700nm��Χ��, WO3��������������������λ���������ǿ��
�ǽ����������е�����λ, ����������, ��������������λ�����ĵ���, �����ױ�����������, �������λ��ʩ��������, ���ǵ��ܼ�ED�ڽ����д��ڵ�����EC����, ��ͼ5��ʾ�� ˵������������ȷֽ�(������ԭ������NH3)������, ����Ar����������, ������Բ���, ����λ����Ӧ����, ���������ĵ�������Ӧ����, �����420~700nm��Χ��, WO3��������������������λ���������ǿ��
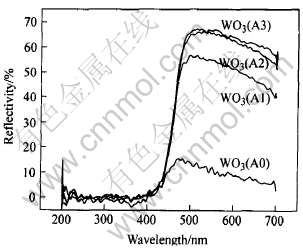
ͼ4 WO3����������-�ɼ����������
Fig.4 UV-Vis diffusion reflectance spectra of WO3
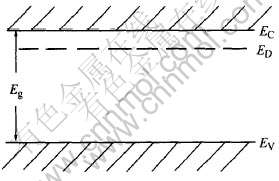
ͼ5 ��������λ��WO3���ܴ�ͼ
Fig.5 Band structure of WO3 with oxygen vacancies
2.3 ����WO3����ָ��
��2����Ϊ��������ָ���� �ӱ�2��֪, ��ʵ������������������ȷֽ����Ƶõ�WO3����ָ����������3, ����С��3, ˵��W���ֲ�������W6+, ���еͼ�̬W, ������Ar����������, ��O2�����ļ���, ��ָ����С, ˵���ͼ�̬W�ı���������, ����XPS�������һ�¡�
��2 ����WO3����ָ��
Table 2 Oxygen indexes of catalysts

2.4 �������
2.4.1 ����λ��WO3�������Ե�Ӱ��
ͼ6��ʾΪ4�ִ������������뷴Ӧʱ��Ĺ�ϵ�� ͼ6�������: ��250W, ������Ϊ365nm�ĸ�ѹ����������, WO3(A0)�������Ļ������, ��������������ȷֽ������O2����������, ���ƵõĴ���������λ����, ����������������С�� ���ڹ������������Ĺ����������� ��ɷ���Ч�ʺ������ӵ�ת�����ʵ���������Ҫ��ϵ[12], ͼ6��ʾ�Ĺ���������Դ�С˳����ͼ4��ʾ����420~700nm��Χ�ڵĹ��������ܴ�С˳����ȫһ��, ˵������������λ���Ը��ƴ����Կɼ������������, �Ӷ���ߴ������������ԡ�
2.4.2 Fe2+��Ũ�ȶ�WO3�������Ե�Ӱ��
ͼ7��ʾΪ��ͬ��ʼŨ��Fe2+ʱ, WO3(A1)�������������뷴Ӧʱ��Ĺ�ϵ�� ͼ7�������: �ڹ����Ӧ��ʼʱ, Fe2+���ӵĴ��ڶԹ����ӦӰ��ܴ�, ������Fe2+������ʼŨ�ȵ�����, ����ͬʱ��������������, ��Fe2+��Ũ����Fe3+��Ũ���൱ʱ, WO3������ȫʧȥ�������ԡ� ����Teruhisa��[13]��ʵ����, Fe2+��Fe3+��WO3�������һ��������, ����Fe3+��WO3����������ȸ���, ����, Fe3+ /Fe2+��Եĵ缫��λ��O2/H2O��, Fe2+��H2O�����ױ�����, ����, ������WO3����������һ����Fe2+��, WO3�ܹ��ղ����Ŀ�Ѩ����������Fe2+, ��ʹH2O�������ܵ�һ���̶ȵ�����, ����Fe2+��Ũ����Fe3+��Ũ���൱ʱ, WO3�Ĺ������������ȫ�����ơ�

ͼ6 WO3�������������뷴Ӧʱ��Ĺ�ϵ
Fig.6 Dependence of photocatalytic O2 evolution on irradiation time
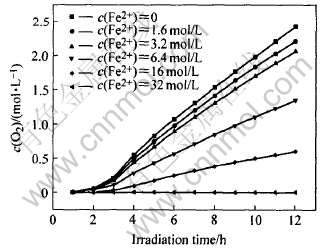
ͼ7 Fe2+������WO3(A1)������
�������뷴Ӧʱ��Ĺ�ϵ
Fig.7 Time course of photocatalytic O2 evolution as function of Fe2+
3 ����
�ڲ�ͬ���O2/Ar�������������, ��700�潫������識��ȷֽ�, �õ�һϵ�о��в�ͬ����λ�Ĵ���, ����������˹���ֽ�ˮ�������Լ�⡣ ʵ��������: ��Ar��������������ȷֽ����õ���WO3�����������������ߡ� ��������ȷֽ�(������ԭ������NH3)������, ����Ar����������, ������Բ���, ����λ��һ����Χ������, ���Ը��ƴ����Կɼ������������, �Ӷ��������WO3�����Ĺ���������ԡ� ����, ��Fe3+������Ϊ���ӽ�����Ĺ���ֽ�ˮ������Ӧ��, һ��Ũ�ȵ�Fe2+��������������WO3�Ĺ����������, �ҵ�Fe2+��Ũ����Fe3+��Ũ���൱ʱ, WO3�Ĺ������������ȫ�����ơ�
REFERENCES
[1]Srinivasa R K, Madhuri K V, Uthanna S, et al. Photochromic properties of double layer CdS/MoO3 nano-structured films[J]. Mater Sci Eng B, 2003, B100: 79-86.
[2]Avellaneda C O, Bulhoes L O S. Photochromic properties of WO3 and WO3��X(X=Ti, Nb, Ta and Zr) thin films[J]. Solid State Ionics, 2003, 165: 117-121.
[3]SU Lian-yong, ZHANG Lin-gang, FANG Jing-huai, et al. Electrochromic and photoelectrochemical behavior of electrodeposited tungsten trioxide films[J]. Solar Energy Materials & Solar Cells, 1999, 58: 133-140.
[4]Pehlivan E, Tepehan F Z, Tepehan G G. Comparison of optical, structural and electrochromic properties of undoped and WO3-doped Nb2O5 thin films[J]. Solid State Ionics, 2003, 165: 105-110.
[5]Bonhote P, Gogniat E, Gratzel M, et al. Novel electrochromic devices based on complementary nanocrystalline TiO2 and WO3 thin films[J]. Thin Solid Films, 1999, 350: 269-275.
[6]Aguir K, Lemire C, Lollman D B B. Electrical properties of reactively sputtered WO3 thin films as ozone gas sensor[J]. Sensors and Actuators B, 2002, 84: 1-5.
[7]Lee D S, Han S D, Huh J S, et al. Nitrogen oxides-sensing characteristics of WO3-based nanocrystalline thick film gas sensor[J]. Sensors and Actuators B, 1999, 60: 57-63.
[8]Bamwenda G R, Arakawa H. The visible light induced photocatalytic activity of tungsten trioxide powders[J]. Applied Catalysis A, 2001, 210: 181-191.
[9]Sayama K, Yoshida R, Kusama H, et al. Photocatalytic decomposition of water into H2 and O2 by a teo-step photoexcitation reaction using a WO3 suspension catalyst and an Fe3+/Fe2+ redox system[J]. Chem Phy Lett, 1997, 277: 387-391.
[10]Bamwenda G R, Arakawa H. The photoinduced evolution of O2 and H2 from a WO3 aqueous suspension in the presence of Ce4+/Ce3+[J]. Solar Energy Materials & Solar Cells, 2001, 70: 1-14.
[11]��ع��. �������뻯����뵼�����[M]. ����: �������ӿƼ���ѧ������, 1991. 49.
XU Yu-long. Semiconductor Basis on Oxides and Compounds[M]. Xi��an: Xi��an University of Electronic Sciencs and Techenology Press, 1991. 49.
[12]����, ���¾�, ���, ��. WOx/TiO2������Ŀɼ�������Ի���̽��[J]. ������ѧѧ��, 2004, 20(5): 507-511.
ZHANG Qi, LI Xin-jun, LI Fang-bai, et al. Investigation on visible-light activity of WOx/TiO2 photocatalyst[J]. Acta Phys-Chim Sin, 2004 , 20(5): 507-511.
[13]Teruhisa O, Fumihiro T, Kan F, et al. Photocatalytic oxidation of water on TiO2-coated WO3 particles by visible light using Iron(��) ions as electron acceptor[J]. Journal of Photochemistry and Photobiology A, 1998, 118: 41-44.
������Ŀ: ���Ҹ����о���չ�ƻ�������Ŀ(2002AA327140)
�ո�����: 2005-07-14; ������: 2006-01-13
ͨѶ����: ������, ����; �绰: 0798-8499678; E-mail: gaocsu@163.com


