���±�ţ�1004-0609(2011)04-0927-05
�����͵���ʶ���Һ�絼�ʵ�Ӱ��
���ٷ�1, 2���ΰ��3�����緼1, 2��������2��ʷ��÷2������ϼ2����־��2��������2������ΰ2
(1. �����Ƽ�ʦ��ѧԺ ����ʡ���ϱ��湤���ص�ʵ���ң��ϲ� 330013��
2. �����Ƽ�ʦ��ѧԺ ���Ͽ�ѧ�빤��ѧԺ���ϲ� 330013��
3. �����Ƽ�ʦ��ѧԺ ��������Ա�����칫�ң��ϲ� 330013)
ժ Ҫ��
�ں������Ƶļ��Ի�����Һ�У��о�ֲ��(C6H18O24P6)Ũ�ȶ���Һ�絼�ʵ�Ӱ�졣������������ˮƽ����ʵ�飬�о������͵��������������(NaOH)��������(Na2SiO3?9H2O)������(H3BO3)��������(Na2WO4?2H2O)��������(NaAlO2)��̼����(Na2CO3)����Һ�絼�ʵ�Ӱ����ɡ��������������ֲ�������Ũ�����ӣ���Һ�絼�ʼ�С������NaOH��Na2SiO3?9H2O��Na2WO4?2H2O��Na2CO3��NaAlO2Ũ�����ӣ���Һ�絼������
�ؼ��ʣ�
��ͼ����ţ�TG146.2���� ���ױ�־�룺A
Influence of environmentally friendly electrolytes on solution conductivity
ZHANG Rong-fa1, 2, LIAO Ai-di3, ZHANG Shu-fang1, 2, LI Ming-jie2, SHI Xing-mei2,
WANG Hai-xia2, JIA Zhi-xiang2, WANG Li-jun2, LIU Li-wei2
(1. Jiangxi Key Laboratory of Surface Engineering, Jiangxi Science and Technology Normal University, Nanchang 330013, China;
2. College of Material Science and Engineering, Jiangxi Science and Technology Normal University, Nanchang 330013, China;
3. Office of Retirement, Jiangxi Science and Technology Normal University, Nanchang 330013, China)
Abstract: In an alkaline basic solution containing sodium silicate, the influence of phytic acid (C6H18O24P6) concentration on the solution conductivity was studied. The influence regularities of environmentally friendly electrolytes, such as NaOH, Na2SiO3?9H2O, H3BO3, Na2WO4?2H2O, NaAlO2 and Na2CO3, on the solution conductivity were systematically studied by the orthogonal experiment with four factors and three levels. The results show that the solution conductivity decreases with the increase of phytic acid and boric acid, but increases with the increase of Na2SiO3?9H2O, NaOH, Na2WO4?2H2O, Na2CO3 and NaAlO2 concentrations.
Key words: magnesium alloys; micro arc oxidation; electrolyte; conductivity
þ�ǵ����ϴ�����ḻ��Ԫ��֮һ������˵��ȡ֮��������֮����[1]��þ�Ͻ������ܶ�С����ǿ�ȸߡ����ȵ����Ժã�ͬʱ���ڼӹ����ͣ���Ϊ�ִ����������ӡ�ͨѶ����ҵ����ѡ����[1-2]����þ�Ͻ���ʴ�Ժ���ĥ�Բ��Լ����㷺Ӧ�á������������������������Ϸ�չ�����Ը���þ�Ͻ�������ܵ�һ����Ч���������õ������ɺ�Ũ�Ⱦ�����Һ�ĵ絼 ��[3-5]��������þ�Ͻ�����������ʹ�õĵ���ʾ���Ϊ������õ��й�����[3-8]��������[8-9]������[9]��������[6]��̼����[7]��������[5, 8]�ȡ��л�����������������ĵ���ʣ��ѱ������к��ǻ�����������Ȼ��Ͱ����ȹ����ŵ����ʣ������[8]����������[9]�ȡ���Щ�л������Ϊ���Ӽ����뵽��Һ�У���Ҫ��ֻ������ֲ���Ǵ���ʳ����������ȡ����Ȼ���л����ữ����㷺Ӧ���ڹ���ũ��ʳƷ��ҽҩ���ջ��ͽ��������ȸ�������[10]�����ֲ����Ϊһ����Ҫ�����������þ�Ͻ�������[11-12]����������Ĥ��ʴ�����ڹ���������Ĥ��[12]����Һ�絼����������ʱ��Һ��ϵ��һ����Ҫ����������������ѹ���մɲ������ٶȡ��մɲ�����ò�Լ��մɲ����ʴ���й�[13]���ڿ�������������������ʱ����ȷ������ʶ���Һ�絼�ʵ�Ӱ����ɲ�ѡ��ǡ������ַdz���Ҫ����Ȼ�Ѳ�������������ʶ���Һ�絼�ʵ�Ӱ��[3-5, 11-12]��������ʸı���Һ�絼�ʵ����ô�Сδ��ϵͳ�о������������о�ֲ��Ũ�ȶ���Һ�絼�ʵ�Ӱ�죬����������ʵ��ϵͳ�Ա��������ơ������ơ����ᡢ�����ơ������ƺ�̼���ƶ���Һ�絼�ʵ�Ӱ����ɡ�
1 ʵ��
������1 g/L NaOH��5 g/L Na2SiO3?9H2O�Ļ�����Һ�У��ֱ����1��2��3 ��4 g/Lֲ�ᣬ�ⶨֲ�����ǰ������Һ�ĵ絼�ʡ�Ȼ�������������ˮƽ����ʵ���о��������ơ������ơ����ᡢ�����ơ������ƺ�̼���ƶ���Һ�絼��Ӱ����ɡ�ʵ������ֲ�ᴿ�Ȳ�С��70%�������Լ�Ϊ����������Һ������ˮ���á�ʹ��Sartorius������ƽ(����0.01 mg)�����Լ���������DDS-307�絼���Dz�����Һ�絼�ʡ�
2 ���������
��1 g/L NaOH+5 g/L Na2SiO3?9H2O������Һ�У��ֱ���벻ͬŨ��ֲ�ᣬ��Һ�絼�ʱ仯��ͼ1��ʾ(�����¶�18 ��)��
��ͼ1�ɼ�������ֲ��Ũ�����ӣ���Һ�絼����С��ֲ������к���12��������ԭ�ӣ���ǿ�� �ԣ���������볣�������Լ���1[10]����Ϊһ�ֶ�Ԫǿ�ᣬֲ����ˮ��Һ�з������룬���뷽��Ϊ[14]
RH12+H2O![]() RH11-+H3O+ (1)
RH11-+H3O+ (1)

ͼ1 ֲ��Ũ�ȶ���Һ�絼��Ӱ��
Fig.1 Influence of phytic acid concentration on solution conductivity in base solution containing 1 g/L NaOH and 5 g/L Na2SiO3?9H2O
RH11-+H2O![]() RH102-+H3O+ (2)��(R=C6H6O6(PO3)6)
RH102-+H3O+ (2)��(R=C6H6O6(PO3)6)
��ֲ�������Ի�����Һ�У�H3O+���������Һ�е�OH-������Ӧ������ˮ������ֲ��ǰ��������Һ�е�������ΪSiO32-��OH-��ÿ����һ��ֲ����ӣ���Һ�оͼ���һ��OH-������һ��ֲ�����ӡ�����ֲ�����ӱ�OH-��ö࣬��ˮ��Һ���ƶ��ٶ�������˼���ֲ�����Һ�絼�ʼ��١�
��1 ֲ�����ⳣ��������[10]
Table 1 Ionized constant and acidity of phytic acid[10]

������������ѹ����Һ�絼��������أ�����絼�ʵ����Ӷ���С[5, 15]���ڻ�����Һ�м���ֲ�����Һ�絼�ʼ��٣����������ʱ������ѹ���ߣ�����������ǰ��ʵ������һ��[11]��
�������о��ĵ�������������ơ������ơ����ᡢ�����ơ������ƺ�̼���ƣ���˱�ʵ������ʹ����������ˮƽ����ʵ�飬�ֱ��о����Ƕ���Һ�絼�ʵ�Ӱ�졣
��ʹ������ʵ��Ƚ��������ơ������ơ�����������ƶ���Һ�絼��Ӱ�졣����ʵ������ˮƽ����2��
��2 ����ʵ��ĸ����غ�ˮƽ
Table 2 Factors and levels of orthogonal experiment

ѡ��L9(34)����ʵ������������������η���������ͷ���ʵ�λ����[16]������ʵ����Լ�ʵ��������3��
����ʵ�����ݷ���ʹ��ֱ�۷���������3��K1��K2��K3�ֱ�Ϊ�����ص�һˮƽ���ڶ�ˮƽ�͵���ˮƽ�ĵ絼�ʵļӺ�ֵ��k1��k2��k3�ֱ�Ϊ��������Ӧˮƽ��ƽ��ֵ������K1��K2��K3��ֵ����3������(R)Ϊ��������Ӧˮƽ��ƽ��ֵk1��k2��k3�����ֵ����Сֵ֮����Ĵ�С��Ӧʵ���и��������õĴ�С����������������ض�ָ���Ӱ���ͨ��Ϊ��Ҫ���ء��ӱ�3���������ɼ���Ӱ����Һ�絼�ʵ����شӴ�С����ΪNaOH��Na2SiO3?9H2O��Na2WO4?2H2O��H3BO3��
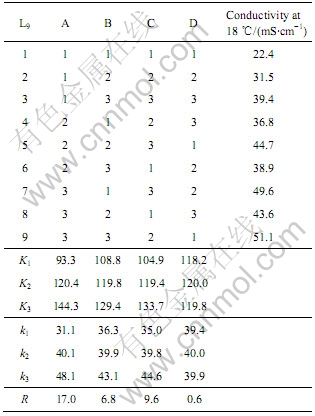
��3 �絼������ʵ����
Table 3 Results of orthogonal experiment about conductivity

�Ը����ص�ˮƽ�������ָ꣬��ļӺ�ֵΪ�����꣬�ɻ���������ָ���ϵͼ(��ͼ2)����ͼ2�ɼ�����Һ�絼����NaOH��Na2SiO3?9H2O��Na2WO4?2H2OŨ�����Ӷ�������H3BO3�����Ӷ���С��
�������������ΪA3B3C1D3ʱ����NaOH����Ϊ0.15 mol/L��Na2SiO3?9H2OΪ0.15 mol/L��H3BO3Ϊ0.05 mol/L��Na2WO4?2H2OΪ0.15 mol/Lʱ����Һ�絼������������������ΪA1B1C3D1ʱ����NaOH����Ϊ0.05 mol/L��Na2SiO3?9H2OΪ0.05 mol/L��H3BO3Ϊ0.15 mol/L��Na2WO4?2H2OΪ0.05 mol/Lʱ����Һ�絼����͡���3��û������������ϣ���˻��밴��A3B3C1D3��A1B1C3D1��������������Һ����������Һ�絼�ʣ���������4����������2����ϵõ�����Һ�絼��ȷʵ�ȱ�3��9������е���һ����ϵ絼�ʷֱ�Ҫ���С��
���ձ�2��ͬ��ʹ������ʵ��Ƚ�NaOH��NaAlO2��Na2CO3����Һ�絼��Ӱ�졣����ʵ������ˮƽ�Լ�ʵ�����ֱ����5��6��
�ӱ�6�ɼ���Ӱ����Һ�絼�ʵ����شӴ�С����ΪNaOH��Na2CO3��NaAlO2��3�����ȡ��ˮƽʱ���絼�ʾߣ�ȡ��ˮƽʱ���絼�ʾ͵͡�

ͼ2 �����ض���Һ�絼�ʵ�Ӱ��
Fig.2 Effect of factors on electrolytic conductivity: (a) NaOH; (b) Na2SiO3?9H2O; (c) H3BO3; (d) Na2WO4?2H2O
��4 ������С�絼��ʱ��Һ���
Table 4 Electrolyte compositions with maximum and minimum conductivities

��5 ����ʵ��ĸ����غ�ˮƽ
Table 5 Factors and levels of orthogonal experiment

��6 �絼������ʵ����
Table 6 Results of orthogonal experiment about conductivity
����������ˮ��Һ�н��еģ���Һ�絼�ʶ����������Լ�����Ĥ����Ӱ��ܴ����ȣ��絼���������ѹ(UB)�йء�������Ĥ�����ŵ��γɣ��ŵ������ԭ����ʩ�ӵĹ�����ѹ���ڵ��Һ�Ļ�����ѹ��������ѹ����Һ������(��)�ľ��鹫ʽΪ[15]
UB=aB+bBlg �� (3)
ʽ�У���һ���Ľ����͵��Һ�����˵��aB��bBΪ ������
�絼���ǵ����ʵĵ���������ʽ(3)��֪��������ѹ����Һ�絼�ʵ����Ӷ���С������Һ�ĵ絼�ʺܴ��������ѹ�ܵͣ�����ʹ�õĹ�����ѹ��Ӧ�ܵͣ��෴�أ�����Һ�絼�ʺ�С���������ѹ�ܴ�����ѹҲ�ܸߣ���ʱ������ѹҲ���ܸ��ڵ�Դ���ѹ��������������ֹͣ���缫����δ��������������������Ĥ��[17]��
��Σ���Һ�絼�ʾ�������Ĥ���ܡ���������������һ����ϵ����Һ���մɲ�ɿ����Ǵ����ڸõ�·ϵͳ�е���������[13]����ˣ���Һ�絼��Խ���մɲ�������ٶ�ҲԽ�죬����Ĥ�������Խ���մɲ����ʴ�Խ���[13]��
�絼������Һ��������Ŀ�Ķ��ٺ����ӱ���������Ĵ�С�й�[18]���ڱ�ʵ���У���ͬ�����3��ˮƽ������ͬ����������7�ֵ���ʣ����Է�Ϊ3�ࣺ1) �������ơ������ơ�̼���ƺ�������Ϊһ�࣬����Ϊ��������ǿ����ʡ�����Щ����ʼ��뵽������Һ�У���Һ�絼��������������Ӷ������Ҷ���Һ�絼��Ӱ���2) ֲ�������Ϊһ�࣬���dz��� �ԡ�ֲ���ǿ���ԣ���������һԪ���ᣬ������������������ȱ����ԭ�ӣ��Ӻ�������ˮ�����е�OH-���ͳ�H+���������ֵ���ʼ��뵽���Ի�����Һ�У����ڷ�������кͷ�Ӧ����Һ�絼������Ũ�ȵ����Ӷ����١����⣬H3BO3�����ᣬ�����Ӱ��Ч����NaOH��Na2SiO3?9H2O��Na2WO4?2H2O��С��3) ������Ϊһ�࣬����������ʣ�ʵ������Һ�в���������������ӣ��������������������ڼ����ɵ�������Һ�д������ڵ���������[Al(OH)4]-��[Aln(OH)4n+2](n+2)- [19-20]����ˣ��������ƺ�������ʱ����Һ�絼�ʲ�û�д��������[20]������Һ�絼��Ӱ������С�������йص���ʶ���Һ�絼��Ӱ��Ĺ��ɣ���Ϊ���þ�Ͻ������������ṩ��Ҫ���������ݡ���ѡ�����ӵ����ʱ����Ҫ�����������Ĥ���ܵ�Ӱ�죬ͬʱ��Ҫ��˸����֮�������ã�ʹ��Һ�絼�ʱ�����һ�����ʵķ�Χ���Ӷ����ǡ�������������ա�
3 ����
1) �������ơ������ơ�̼���ƺ������Ƴʼ��ԣ�����ǿ����ʣ����Ƕ���Һ�絼��Ӱ�������Һ�絼��������������Ӷ����ߡ�
2) ֲ�����������ԣ�������뵽���Ի�����Һ�У���Һ�絼������Ũ�ȵ����Ӷ��½���
3) ��������������ʣ��������ƺ�������ʱ����Һ�絼�ʲ�û�д�������ӡ�
REFERENCES
[1] ʦ����, ����, ������, ������, ������. �����ҹ�����þ��ҵ��չ�Ľ���[J]. ���ϵ���, 2001, 15(4): 5-7.
SHI Chang-xu, LI Heng-de, WANG Dian-zuo, LI Yi-yi, ZUO Tie-yong. A proposal on accelerating development of metallic magnesium industry in China[J]. Material Review, 2001, 15(4): 5-7.
[2] TSAI H K, LIAO C C, CHEN F K. Die design for stamping a notebook case with magnesium alloy sheets[J]. Journal of Materials Processing Technology, 2008, 201: 247-251.
[3] LI W P, ZHU L Q, LIU H C. Effects of silicate concentration on anodic films formed on AZ91D magnesium alloy in solution containing silica sol[J]. Surface & Coatings Technology, 2006, 201: 2505-2511.
[4] LIANG J, HU L T, HAO J C. Characterization of microarc oxidation coatings formed on AM60B magnesium alloy in silicate and phosphate electrolytes[J]. Applied Surface Science, 2007, 253: 4490-4496.
[5] DING Jun, LIANG Jun, HU Li-tian, HAO Jing-cheng, XUE Qun-ji. Effects of sodium tungstate on characteristics of microarc oxidation coatings formed on magnesium alloy in silicate-KOH electrolyte[J]. Transactions of Nonferrous Metals Society of China, 2007, 17: 244-249.
[6] GHASEMI A, RAJA V S, BLAWERT C, DIETZEL W, KAINER K U. The role of anions in the formation and corrosion resistance of the plasma electrolytic oxidation coatings[J]. Surface & Coatings Technology, 2010, 204: 1469-1478.
[7] ZHANG Y J, YAN C W, WANG F H, LOU H Y, CAO C N. Study on the environmentally friendly anodizing of AZ91D magnesium alloy[J]. Surface & Coatings Technology, 2002, 161: 36-43.
[8] WU D, LIU X D, LU K, ZHANG Y P, WANG H. Influence of C3H8O3 in the electrolyte on characteristics and corrosion resistance of the microarc oxidation coatings formed on AZ91D magnesium alloy surface[J]. Applied Surface Science, 2009, 255: 7115-7120.
[9] WU C S, ZHANG Z, CAO F H, ZHANG L J, ZHANG J Q, CAO C N. Study on the anodizing of AZ31 magnesium alloys in alkaline borate solutions[J]. Applied Surface Science, 2007, 253: 3893-3898.
[10] ףȺӢ, �� ��. �����ɫʳƷ���Ӽ���ֲ��[J]. ��ʳ�ӹ�, 2004, 6: 57-61.
ZHU Qun-ying, LIU Jie. A multifunctional green food additive��phytic acid[J]. Grain Processing, 2004, 6: 57-61.
[11] ZHANG R F, ZHANG S F, DUO S W. Influence of phytic acid concentration on coating properties obtained by MAO treatment on magnesium alloys[J]. Applied Surface Science, 2009, 255: 7893-7897.
[12] ZHANG R F, XIONG G Y, HU C Y. Comparison of coating properties obtained by MAO on magnesium alloys in silicate and phytic acid electrolytes[J]. Current Applied Physics, 2010, 10: 255-259.
[13] ������, ���ȷ�. ��ͬ�絼����Һ��þ�Ͻ��������մɲ���������ɼ���ʴ��[J]. ϡ�н��������빤��, 2005, 34(3): 393-396.
JIANG Bai-ling, ZHANG Xian-feng. Growth rhythm and corrosion resistance of ceramic coatings formed by micro-arc oxidation on magnesium alloys in different conductivity solutions[J]. Rare Metal Materials and Engineering, 2005, 34(3): 393-396.
[14] ֣���, ���ɺ�, �� ��. AZ91Dþ�Ͻ�ֲ��ת��Ĥ�������ʴ�����о�[J]. ����������ѧѧ��, 2006, 46(1): 16-19.
ZHENG Run-fen, LIANG Cheng-hao, SHAO Lin. Study of composition and corrosion protection afforded by phytic acid conversion coatings applied to AZ91D magnesium alloy[J]. Journal of Dalian University of Technology, 2006, 46(1): 16-19.
[15] BURGER F J, WU J C. Dielectric breakdown in electrolytic capacitors[J]. Journal of The Electrochemical Society, 1971, 118: 2039-2042.
[16] �� ��. ������Ƶļ����뷽��[M]. �Ϻ�: �Ϻ���ͨ��ѧ������, 1987: 12.
LUAN Jun. The technology and method of experiment design[M]. Shanghai: Shanghai Jiaotong University Press, 1987: 12.
[17] �²���, ������, ����ϲ, �� ��. ���ҺŨ�ȶ�þ�Ͻ���������Ĥ��Ӳ�ȵ�Ӱ��[J]. ������ѧѧ��: ��Ȼ��ѧ��, 2008, 27(2): 86-88.
CHEN Chang-hua, LIU Xiao-lie, SUN Li-xi, PAN Hui. Effect of electrolyte concentrations on anode film��s hardness for magnesium alloy[J]. Journal of Xihua University: Natural Science, 2008, 27(2): 86-88.
[18] ��Ӣ��. ������ѧ[M]. ����: ұ��ҵ������, 1983: 287.
LIANG Ying-jiao. Physical chemistry[M]. Beijing: Metallurgical Industry Press, 1983: 287.
[19] YEROKHIN A L, LEYLAND A, MATTHEWS A. Kinetic aspects of aluminium titanate layer formation on titanium alloys by plasma electrolytic oxidation[J]. Applied Surface Science, 2002, 200: 172-184.
[20] GUO H F, AN M Z. Growth of ceramic coatings on AZ91D magnesium alloys by micro-arc oxidation in aluminate-fluoride solutions and evaluation of corrosion resistance[J]. Applied Surface Science, 2005, 246: 229-238.
������Ŀ������ʡ����������������Ŀ(GJJ08363��GJJ09573)
�ո����ڣ�2010-03-12�������ڣ�2010-08-12
ͨ�����ߣ����ٷ������ڣ���ʿ���绰��0791-3831266��E-mail: rfzhang-10@163.com


