�й���ɫ����ѧ�� 2004,(10),1658-1665 DOI:10.19476/j.ysxb.1004.0609.2004.10.007
AZ91Dþ�Ͻ��ں�SO2���������еij��ڸ�ʴ��Ϊ
�����Ƽ���ѧ���Ͽ�ѧ�빤��ѧԺ��ʴ���������,�����Ƽ���ѧ���Ͽ�ѧ�빤��ѧԺ��ʴ��������� ����100083 ,����100083�й���ѧԺ�����о���������ʴ����������ص�ʵ��������110016
ժ Ҫ��
�������ڼ��ٵķ���,���ý���������ɨ��羵��X����������ֶζ�AZ91Dþ�Ͻ��ں���SO2��ҵ��Ⱦ�����еij��ڸ�ʴ����ò�Լ���ʴ��������˷������о����������:SO2����þ�Ͻ�ĸ�ʴ,����SO2��������,þ�ĸ�ʴ���ʼӿ졣þ�Ͻ�ij��ڸ�ʴ���оֲ���ʴ����������ʴ���ȴӦ�����忪ʼ,��ʴ�����ڲ��ϱ�������һ�㱣���Եĺ���MgO��Mg(OH)2�ı�Ĥ��SO2�����˱�Һ���pHֵ,��ǿ�ܽ����,�ٽ�������MgSO3��6H2O��MgSO4��6H2O��ʴ���������,ʹ����Ĥʧȥ��������,����þ�Ͻ�ĺ��ڸ�ʴ��
�ؼ��ʣ�
��ͼ����ţ� TG172.3
����飺�ִ�(1976),Ů,��ʿ�о���.��ʿ;�绰:01062333975;Email:lincwi@sohu.com;
�ո����ڣ�2004-03-03
�����Ƽ����������ص�ר�����������Ŀ(2001DEA30038);
Initial corrosion of AZ91D magnesium alloy in atmosphere containing SO2
Abstract��
The initial surface morphology of corrosion layer, corrosion products and structure of rust layer for AZ91D magnesium alloy in SO2 industrial polluted atmosphere were analyzed by metallographic observation, SEM and XRD. The results show that corrosion rate increases with increasing SO2 content in the atmosphere. The initial attack has the characteristics of localized corrosion. Corrosion starts from �� phase, and MgO and Mg(OH)2 form at first, which provide a protective layer. SO2 decreases pH in the electrolyte layer, accelerates dissolution process, and promotes the formation of MgSO3��6H2O and MgSO4��6H2O. These soluble corrosion products result in the loss of protection function and the acceleration of corrosion. Meanwhile, cracks appear with continuation of corrosion, which provide the paths for oxygen and other corrosion pollutants filtering into matrix, further resulting in severe localized corrosion.
Keyword��
SO2; atmosphere; AZ91D magnesium alloy; corrosion;
Received�� 2004-03-03
þ�dz��õĽ����ṹ�����������һ�֡� ����þ�Ͻ��ǿ�ȡ� �ȸնȸ�, �����Ժ�, ���������õ������ӹ�����, ���þ�Ͻ��ں��չ�ҵ�� ������ҵ�͵���ͨѶ��ҵ�����ڵõ�����㷺��Ӧ��
ĿǰԽ��Խ���þ�Ͻ��Ʒ��Ӧ��������Ⱦ���յĴ���������, ����þ�Ͻ��ڴ�����Ⱦ�����и�ʴ�������о�����, ��˶������ϵͳ���о���̽��, ��Ϊþ�Ͻ�ʵʩ������ʩ�ṩ����, ��������������Ӧ�÷�Χ��
����������Ҫ�������ڼ��ٵķ���, ����SEM�� XRD���ֶη������о�AZ91Dþ�Ͻ���SO2��ҵ��Ⱦ���������еij��ڸ�ʴ��Ϊ�������
1 ʵ�鷽��
��������AZ91Dþ�Ͻ�, �仯ѧ���(��������, %)Ϊ: Al 8.89, Zn 0.78, Mn 0.24, ����ΪMg�� �ߴ�Ϊ40 mm��20 mm��3 mm��
1.1 ���ڼ���ʵ��
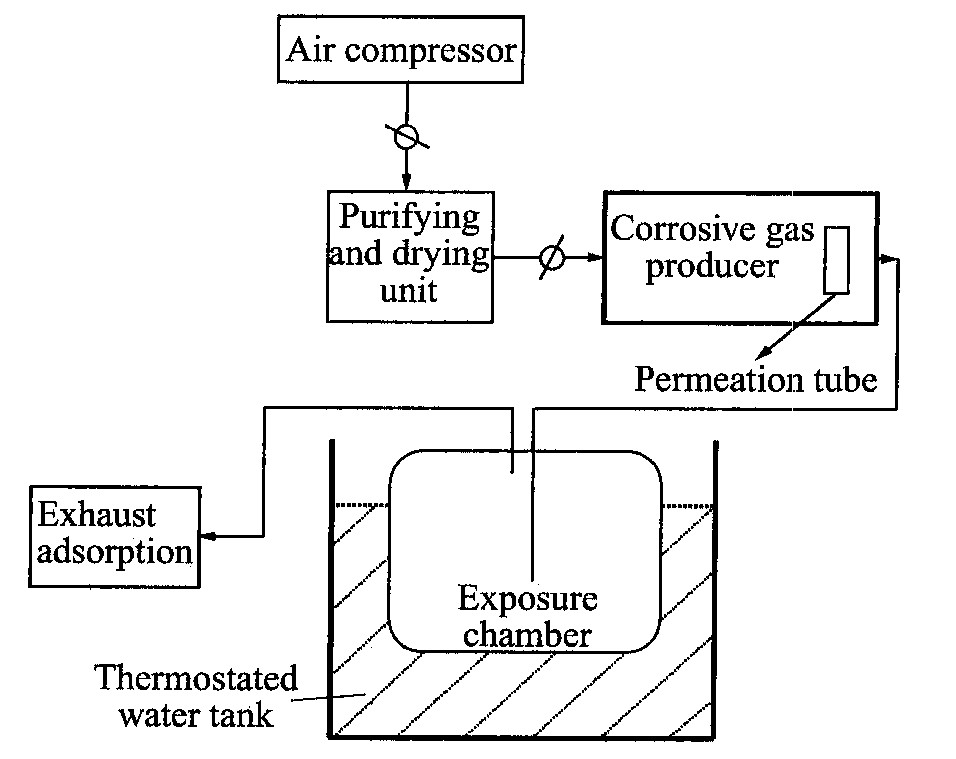
���������Ϳ�ѹ���� ���徻��ǰ����װ�á� ����ʴ���巢��װ�á� ����ˮԡ�ۡ� ��Ʒ�ҡ� �������װ�ù���ģ����Ⱦ������ʴϵͳ, ��ʾ��ͼ��ͼ1�� ��ϵͳ������������ģ�ҵ��Ⱦ�Ĵ�������, ���ص�����:
ͼ1 ģ����Ⱦ�����н������ϳ��ڸ�ʴ��Ϊװ��ͼ
Fig.1 Schematic diagram of experimental set-up of atmospheric corrosion
1)�����ľ�������ϵͳ
ͨ����ʯ�ޡ� �轺�� ����ɸ�� �������Ƶȴ����������, �Ӷ��õ�һ�������Ĵ�������Ŀ�����
2)����ʴ���巢��װ��
�ò��ֺ������ܼ����İ뵼������Ӧ����װ��, �����ɹ��ұ������о����������ͱ궨�� װ�ÿ����������ߴ���Ũ�ȵ���Ⱦ����, ��SO2�� NO2��, Ҳ�ɶ�̨����ʴ���巢��װ������, ͬʱ�������������塣
3)��ʴʵ���
�ú���ˮԡ�ۿ����¶�, ��ʵ��۵ײ�����һ�����ĸ���ˮ��Һ, �ɿ���ʵ�������ʪ�ȡ�
4)������ղ���
�������ʴ�����õĸ�ʴ�������Ϊ��������, �ʿ��ü���Һ����л��ա� β����10%�������������մ�����ֱ���������⡣
���ú���ˮԡ�ۿ�����Ʒ���¶�Ϊ25 ��, �����ʵ�Ũ�ȵĸ���ˮ��Һ������Ʒ����, ʹ��Ʒ��ʪ�Ⱥ�Ϊ95%, ����ͨ�뺬5 mg/m3��50 mg/m3 SO2�Ŀ�����
SO2������Ũ�ȿ�ͨ�����ڿ���������������, �ɰ�ʽ(1)���м���:
ʽ�� ��(SO2)������ʴ���������Ũ��, mg/m3; M����ʴ�����Ħ������, g/mol; p0��������ѹǿ, Pa; V0����ʴ�����Ħ�����, L/mol; T0�����¶�, K; p����������ѹǿ, Pa; T������, K; R�����ܵ�����, ��g/min; Q��ϡ����������, mL/min��
��������Ϊ1.64 ��g/min��SO2����, ��ʵ���¶ȿ���Ϊ308 K�� ����Ϊ0.120 L/min��0.012 L/minʱ, ��������Ⱦ����SO2�ĺ���Ϊ5��50 mg/m3��
1.2 ��ʴ���ʲⶨ
���Ƚ�������200��1 000��ˮĥɰֽ��ĥ������, �ƾ���ϴ, ����ˮ��ϴ, ��紵��, �������� Ȼ����������ʵ������, ��ʴһ��ʱ���, ȡ������, ��CrO3(180 g/L)ˮ��Һ(80 ��, 10 min)ȥ��þ�Ͻ�ʴ����, ����ˮ��ϴ������ˮ�Ҵ���ϴ, ��紵��, ���ø�������24 h, Ȼ������� ����ʽ(2)����ƽ����ʴ����:
V=(m0-m1-m2 ) /��A (2)
ʽ�� V�Ǹ�ʴ���, mm; ���ǽ������ϵ��ܶ�, g/cm3; m0Ϊ����ԭʼ����, g; m1Ϊ���������ʴ����������, g; m2Ϊ�����ʴ����ʱͬ����ʴ�ߴ硢 ͬ�ֲ��ϵĿհ�������У��������ʧ, g; A�Ǹ�ʴ�����ı����, m2; t�Ǹ�ʴʱ��, h��
1.3 ��ò��ʴ����ļ��
���ձ���ѧDMAX-RB(Cu K��)XRD��VG ESCALAB MK2(MgK��)����������Ƿ�����ʴ��� ��Cambridge stereoscan 360ɨ��羵�۲����������۸�ʴ��ò�仯�� ��MET�ͽ��������۲첻ͬʱ���������������
2 ʵ����
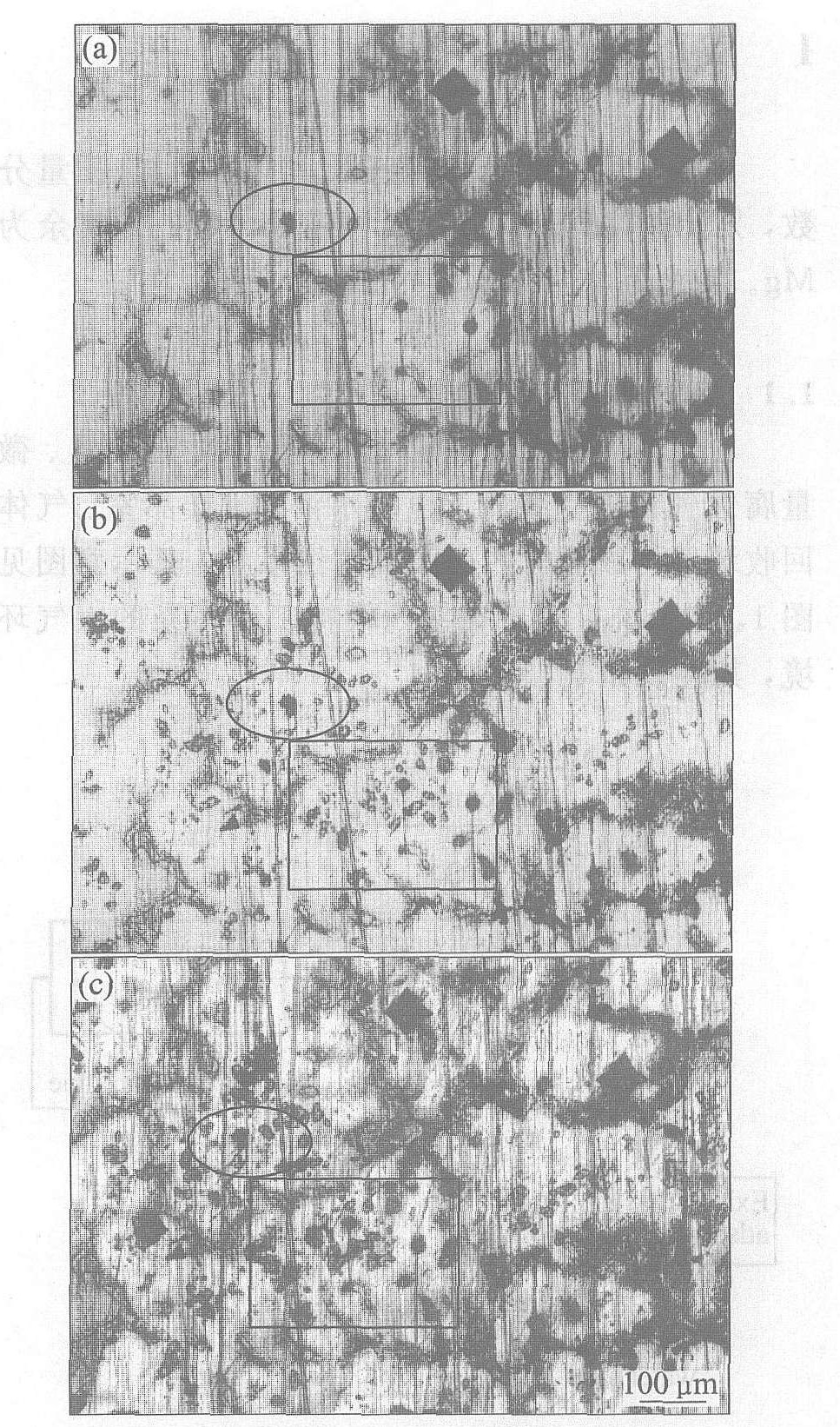
ͼ2��ʾ��AZ91Dþ�Ͻ�Ľ�����֯, ���п��Կ���, ������������������(Mg17Al12)��ɵĶ���Ͻ�
ͼ2 AZ91Dþ�Ͻ�Ľ�����֯
Fig.2 Microstructure of AZ91D alloy
2.1 ���ڸ�ʴ��Ϊ�۲�
������Ӳ�ȼ�������������ϱ��, ��ʴһ��ʱ���ȡ��, �ڽ��������¹۲���ͬ����ĸ�ʴ��ò�仯, ͬʱ��ɨ��羵�¹۲�����ò�ı仯��
1)�������еĸ�ʴ
�ڴ�������, 34 h�������ֻҺ�ɫ�ߵ�, �港ʴʱ����ӳ�, �Һ�ɫ�ߵ������ࡣ ͼ3�е�ԲȦ�ͷ������ڹ۲��������ѡȡ�ļ����仯�Ƚ����Ե�С���� �Ҵ�ͼ4�п����Է��ָ�ʴ��Ҫ������������塣 ��ɨ��羵�¹۲췢�ָ�ʴ�����Բ��״��
2)��SO2��Ⱦ�����еĸ�ʴ
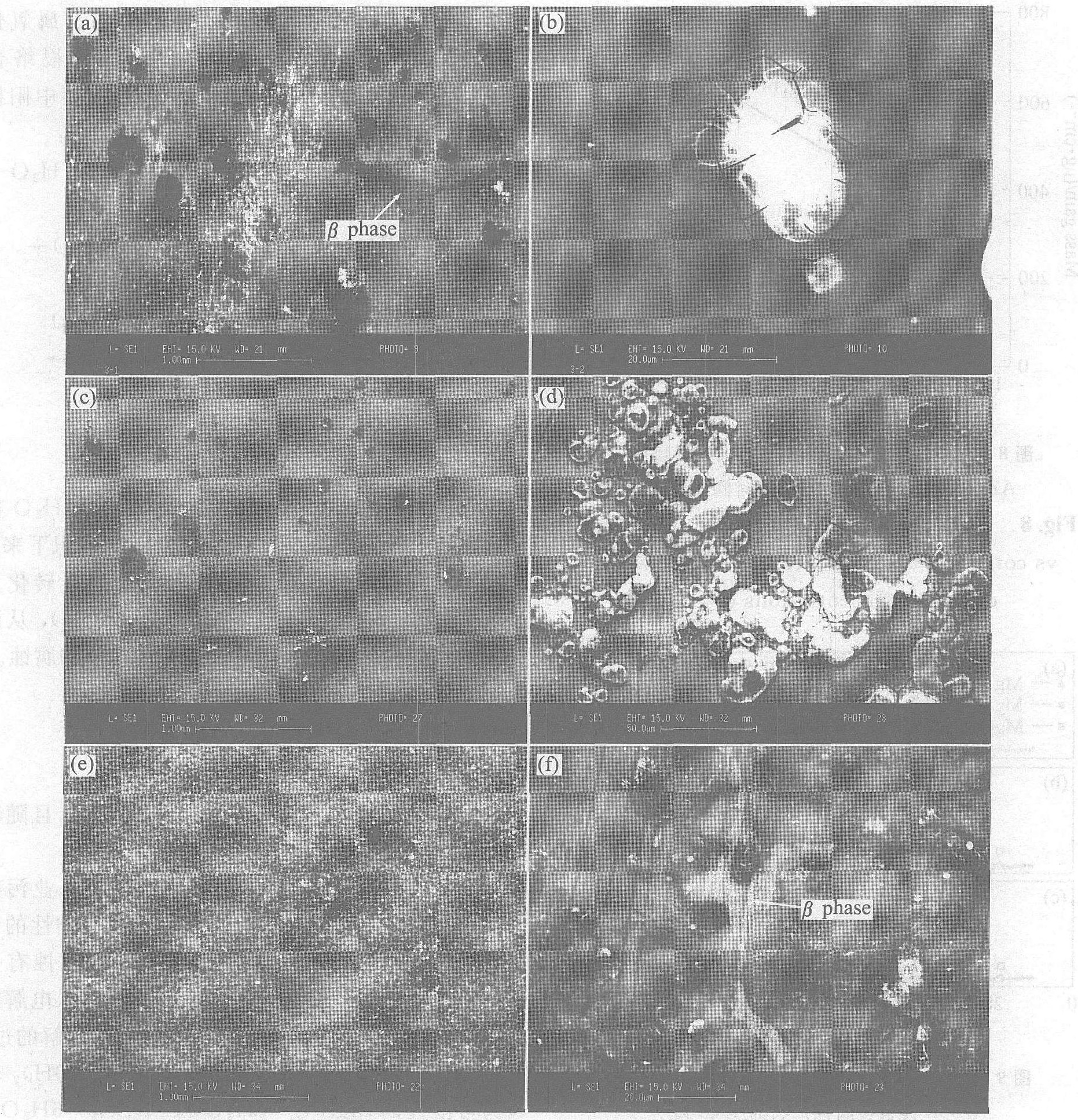
�ڽ��������¹۲췢��, ����������������ְߵ�״��ʴ����, �港ʴ�IJ��Ͻ���, �ߵ�״��ʴ���ﲻ�ϵ���������, ���������졣 ��ͨ��5 mg/m3 SO2ʱ, AZ91Dþ�Ͻ�ʴ24 h��, ����ֲ�������ʴ, ���ֻҺ�ɫ�ߵ�, ������û��ʧȥ��������, 48 h����淢����ʴ��������������, �����лҺ�ɫ�ߵ����Ŀ��������, 72 h������ʴ�������������, ���������аߵ��ø����ܼ��� ����ͨ��50 mg/m3 SO2ʱ(ͼ5), 9 h������ѷ�����ʴ, ���ֻҺ�ɫ�ߵ�, 34 h��ʴ��������, ��ʴ���Լӿ�, 178 h����2/3��ȫ����һ�㸯ʴ��, ��ʵ�������Է���50 mg/m3 SO2������þ�Ͻ��ͨ��5 mg/m3 SO2�����еĸ�ʴ�������ء� ͼ5�е�ԲȦ�ͷ������ڹ۲��������ѡȡ�ļ����仯�Ƚ����Ե�С����
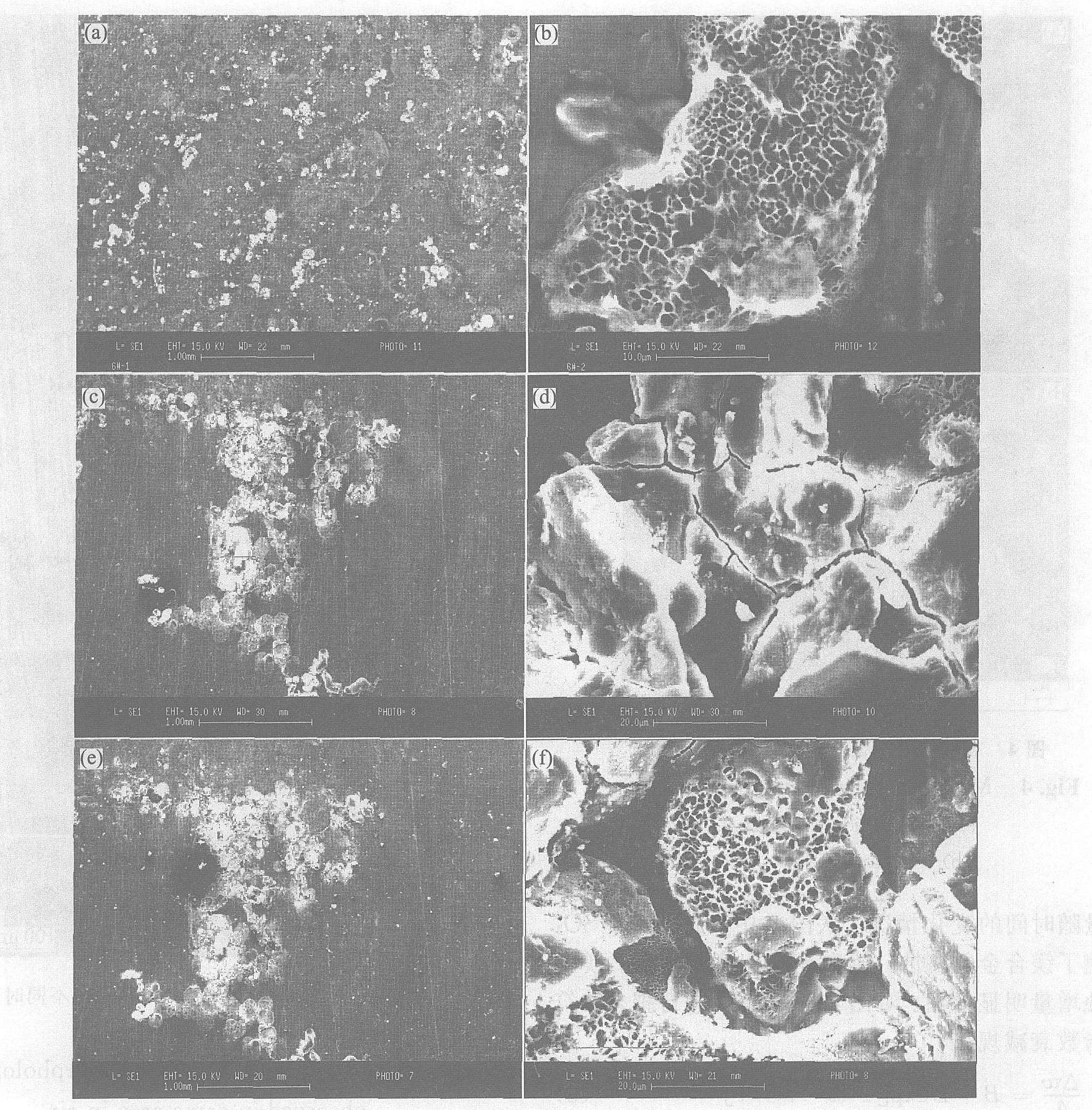
��ɨ��羵�¹۲�, ��ͨ��5 mg/m3 SO2ʱ(ͼ6), ��ʴ120 h, ����ʴ����Ŵ�����������, 240 h��, ���120 h�ı�����ò, ���ָ�ʴ����ľ����Ѿ�����, ���������ƺͷ�϶����, 360 h���ָ�ʴ��������, ��1 500���¹۲����ڲ��ṹ, �������ڲ��Ŀ��ṹ��ø����ܼ��� ͼ7������50 mg/m3 SO2�����б�����ò�仯�Ľ���� 120 h������ѷ��������Եĸ�ʴ����, �Ŵ��ͬ�����ָ�ʴ�����п������� 360 h��ʴ��չ, ��ʴ��������, ���ұ�ø����ܼ��� ��ʴ���ȴ�������忪ʼ, ���港ʴ�IJ��Ͻ���, Խ��Խ��ĸ�ʴ������������ı߽�����(��ͼ7 (f))��
ͼ3 �ڴ������в�ͬʱ�����ͬһ����ʴ����仯
Fig.3 Variation of corrosion morphologies observed in same area in pure air
(a)��Before weathering; (b)��58 h; (c)��130 h
2.2 ���ڸ�ʴ���ʲⶨ
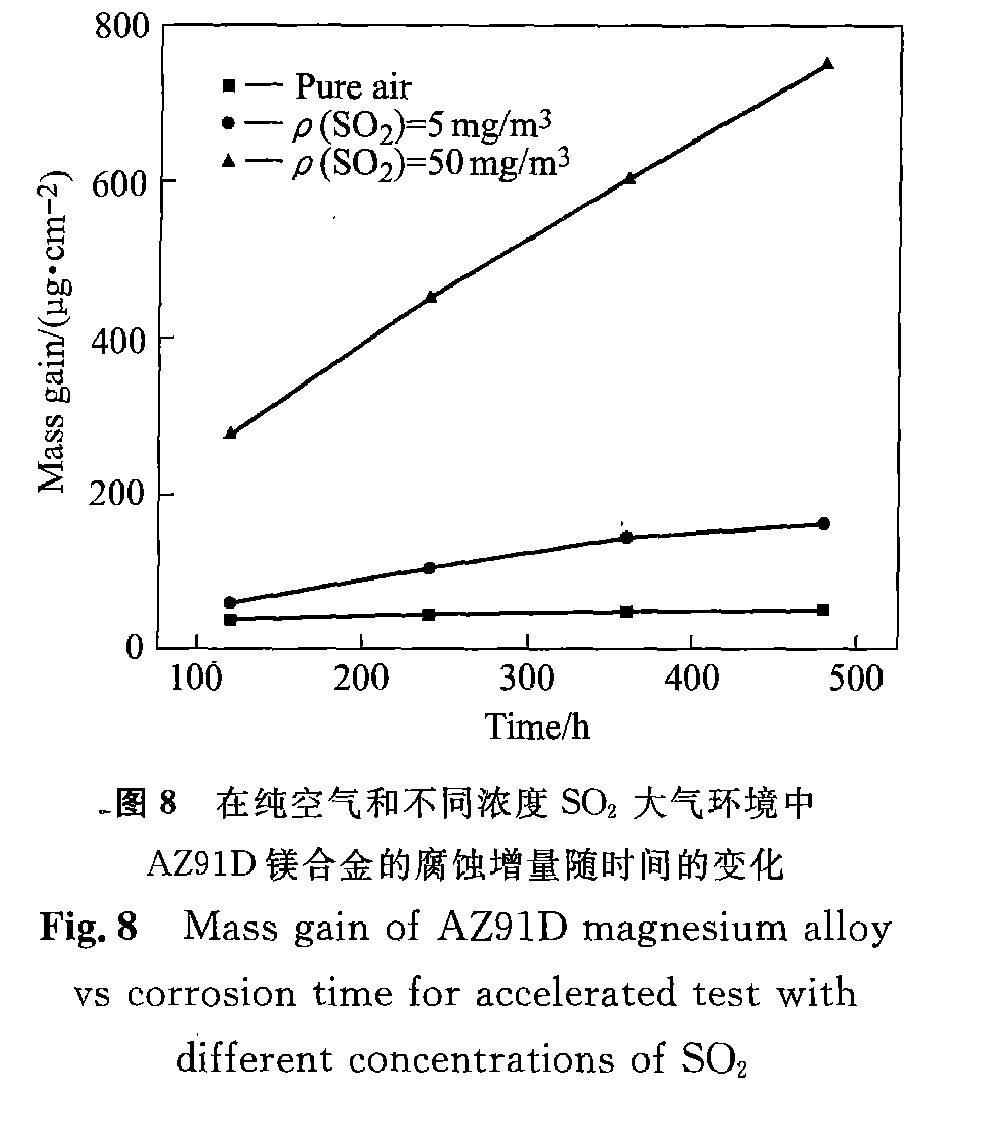
ͼ8��ʾ��ͨ�벻ͬŨ�ȵ�SO2����������������ʱ��ı仯����� ��ͼ8�п��Է���: SO2������þ�Ͻ�ĸ�ʴ, ����SO2Ũ�ȵ�����, þ�ĸ�ʴ�����������ӡ� ��ͼ8�е����߽������, ����ָ��˥������:
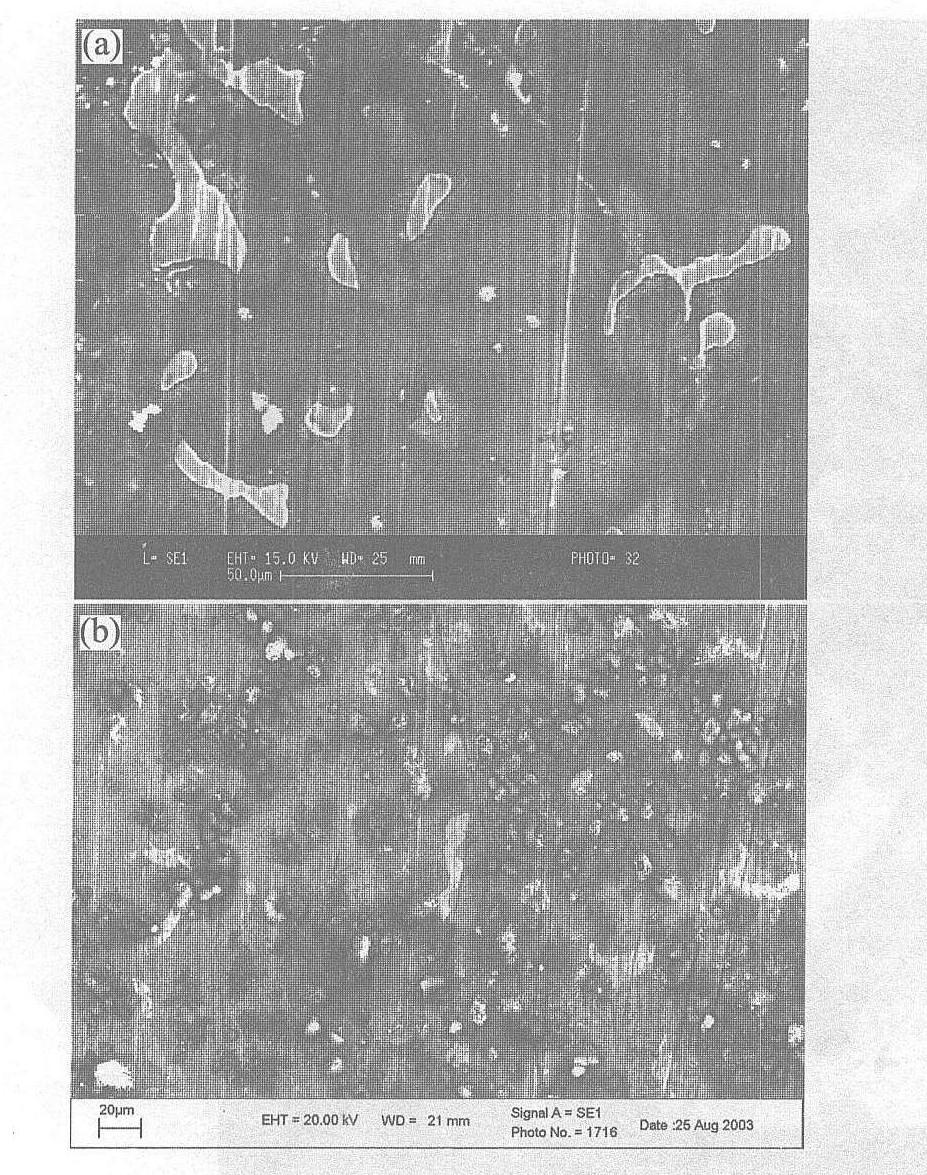
ͼ4 �ڴ�������þ�Ͻ���������ò
Fig.4 Morphologies of magnesium alloy
(a)��Corrosion after 120 h; (b)��Corrosion after 720 h
������õ�B�� D��kֵ����1�� ����Ͻ�����Կ���, SO2ʹ��ʴ����Ĥ�ı��������½���
��1 ��ʽ(3)�������B�� D�� kֵ
Table 1B, D, k values calculated by using Eqn.(3) to correlate experimental data
Environment |
B | D | k |
Pure air |
55.65 | -27.11 | 237.03 |
��(SO2)=5 mg/m3 |
220.82 | -228.55 | 339.82 |
��(SO2)=50 mg/m3 |
2 507.80 | -2 414.76 | 1 514.23 |
2.3 ��ʴ�������
��ʴ�����EDXS��������: ��������, ���港ʴ��������ҪԪ����Mg�� O��������Al, �ں�SO2��ҵ��Ⱦ����������, ����ĸ�ʴ�����г���Mg�� O�� Al, ������SԪ��, ����SO2Ũ�ȵ�����, ��ʴ������S�ĺ���Ҳ����������(����2)��
ͼ5 �ں�50 mg/m3SO2���������в�ͬʱ�� ����ͬһ����ʴ����仯
Fig.5 Variation of corrosion morphologies observed in same area in air containing 50 mg/m3 SO2
(a)��Before weathering; (b)��9 h; (c)��34 h
��2 AZ91Dþ�Ͻ���港ʴ�����EDXS���
Table 2 EDXS results of corrosion products on surface of AZ91D magnesium alloy(mass fraction, %)
Environment |
Mg | O | S | Al |
Pure air |
51.29 | 46.69 | 2.02 | |
��(SO2)=5 mg/m3 |
32.14 | 65.32 | 0.98 | 1.56 |
��(SO2)=50 mg/m3 |
36.18 | 60.74 | 1.60 | 1.48 |
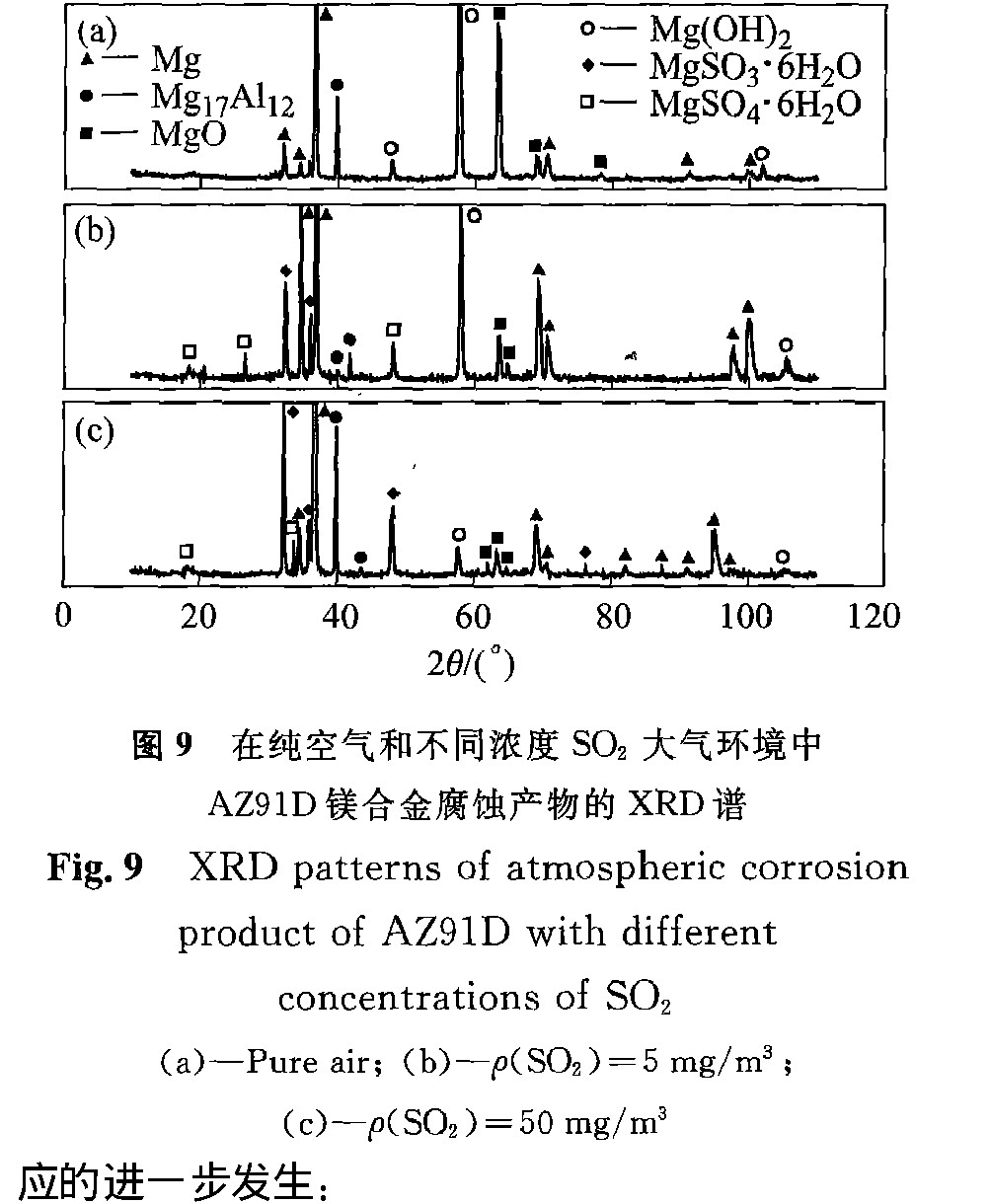
����XRD����þ�Ͻ����ĸ�ʴ��������ͼ9�� �ڴ���������Ҫ��ʴ����Ϊ: MgO�� Mg-(OH)2�� Al(OH)3; ���ں�SO2��ҵ��Ⱦ����������, ��Ҫ������MgO�� Mg(OH)2�� MgSO3��6H2O��MgSO4��6H2O��
ͼ6 �ں�5 mg/m3 SO2����������AZ91Dþ�Ͻ������ò�ı仯
Fig.6 Morphologies of AZ91D magnesium alloy for accelerated test with 5 mg/m3 SO2
(a)��120 h; (b)��20 h (magnified); (c)��240 h; (d)��240 h (magnified); (e)��360 h; (f )��360 h (magnified)
3 ����������
þ�Ͻ��ڹ����е�Ӧ���ܵ����Ƶ���Ҫԭ�����䵯��ģ����, �����Բ�, ��������ʴ���ܲ�
1)ˮ�����ڽ��������ϵ�����
þ�Ͻ�ı��������������ˮ���ӵ�����, ����������γ�һ��ܱ���ˮĤ�� þ�Ͻ��ڳ���ʱ��Ҫ����������������, ������������Ҫ���, ���������Ƕ���Ӳ��, ���������������Ƚӽ���ˮ��������, ��H2O(g)��H2O(l), �������̵��ʱ�Ϊ:
��H=��H (H2O, l )-��H(H2O, g )
=-285.83-(-241.82)
=-44.01 kJ��mol-1
ͼ7 �ں�50 mg/m3 SO2����������AZ91Dþ�Ͻ������ò�ı仯
Fig.7 Morphologies of AZ91D magnesium alloy for accelerated test with 50 mg/m3 SO2
(a)��120 h; (b)��120 h (magnified); (c)��240 h; (d)��240 h (magnified); (e)��360 h; (f )��360 h (magnified)
2)SO2����������ܽˮĤ��, ��ˮĤ�����������
SO2���ӵļ��Լ�ǿ, ������ˮ, ���³�ѹ�±���ˮ��Һ�����ܽ�SO2�����������ˮ�������Ϊ32��
SO2(g)��SO2(aq)
�������ɺܲ��ȶ���������, ��ˮ��Һ�д����������ƽ��:
SO2(aq)+H2O��HSO-3(aq)+H+(aq)
K1=1.3��10-2
HSO-3��H++SO
K2=6.1��10-8
����ⳣ����֪, ����ˮ�е�SO2��������ˮ�Ϸ�����ʽ����, ͬʱHSO-3���ӵ�Ũ�ȴ��SO
3)�绯ѧ��Ӧ
�����������γ��������Һ����ʱ, �Ϳ�ʼ�˵绯ѧ��ʴ����
Mg(s)��Mg2+(aq)+2e-
þ��������Ӧͨ������Ϊ�����Ļ�ԭ:
O2(g)+2H2O+4e-��4OH-(aq)
������������������, ������������������þ(�ǻ�����������), �γɿ�״��ʴ����:
Mg2+(aq)+2OH-��Mg(OH)2(s)
��G=-63.19 kJ��mol-1
SO2��ˮĤ��������������ɵ�����������������������ƶ�, ���������ǻ����Ľ���������(Mg��OH)�����γɽ���-������������(SO-3),SO2�������ܽ�ʹ���ҺĤ��������pHֵ����, �Ӷ���ǿ�������ܽ�Ĺ���:
MgO(s)+HSO-3(aq)+H+(aq)+5 H2O��MgSO3��6H2O
Mg(OH)2(s)+HSO-3(aq)+H+(aq)+4H2O��MgSO3��6H2O
HSO-3(aq)+1/2O2��SO
MgO(s)+SO
Mg(OH)2(s)+SO
����MgSO3��6H2O��MgSO4��6H2O��ˮ�п���, ��˲�����Ϊ���帯ʴ������������� ��ʴ������б����Ե�MgO��Mg(OH)2ת��Ϊ�����Ե�MgSO3��6H2O��MgSO4��6H2O, �Ӷ�ʧȥ�˱���Ĥ�ı�������, ������þ���ڵĸ�ʴ��
4 ����
1)SO2��ͨ�������þ�Ͻ�ĸ�ʴ, �����Ŷ�������Ũ�ȵ�����, þ�ĸ�ʴ���ʼӿ졣
2)AZ91Dþ�Ͻ��ں�SO2��ģ�ҵ��Ⱦ������, ��ʴ�����ڲ��ϱ�������һ�㱣���Եĺ���MgO��Mg(OH)2�ı�Ĥ, �˱�Ĥ�Ը�ʴ��һ�����谭���á� ������SO2�Ĵ���, ��������ҺĤ��, ʹ������pHֵ����, �Ӷ���ǿ���ܽ�Ĺ��̡� ��ʴ����Ҳ���б����Ե�MgO��Mg(OH)2ת��Ϊ�����Ե�MgSO3��6H2O��MgSO4��6H2O��
3)�ڴ���������Ҫ��ʴ����Ϊ: MgO�� Mg-(OH)2�� Al(OH)3; ���ں�SO2��ҵ��Ⱦ����������, ��ʴ������Ҫ��MgO�� Mg(OH)2�� MgSO3��6H2O��MgSO4��6H2O��
4)���ڴ�����ʴ���оֲ���ʴ�������� ��ʴ���ȴ�������忪ʼ, ��SO2����������, ���ɵĸ�ʴ����Ĥ���з�϶�����Ʋ���, ��������ٽ���ˮ��������Ⱦ�����ڸò�λ������, �Ӿ��˸ò�λ�Ľ�һ����ʴ, ��þ�Ͻ�Ĵ�����ʴ��һ�ֲ����ȵľֲ���ʴ��
�����
[13] ��GhaliE.Corrosionandprotectionofmagnesiumalloys[J].MaterialsScienceForum,2000,350351:261272.