���±�ţ�1004-0609(2011)06-1348-11
�������������մɵ�ǿ���ս������θ�ʴ��Ϊ
�ܿƳ�������ǿ�������գ���־��
(���ϴ�ѧ ��ĩұ������ص�ʵ���ң���ɳ 410083)
ժ Ҫ��
���������ս᷽���Ʊ�NiFe2O4�������մɲ��ϣ�������960 �������ⸯʴʵ�顣ͨ�������ս�������ṹ��������ɡ���������ı�����ò��ɷ��Լ�����ʺ������������ʺ����ȣ��о�BaO��Yb2O3��CoO�������Լ����������ɶ�NiFe2O4�������մ��ս����ܵ�Ӱ�죻�����˸ý����մ�ǿ���ս�����Ϊ�������������ĵ�ⸯʴ���ܣ����Բ���ǿ���ս���ƺ����θ�ʴ��Ϊ����̽�֡�����������ս�����У�BaO��Yb2O3��ý����մ��е��մ��෴Ӧ�����µ����࣬CoO���մ����γɹ����壬���ӿ��ս����ܻ����̣���Cu-Niȡ����Cu�ʹ�Ni��Ϊ�����մɵĽ����࣬����߲��ϵ�����ܶȣ�NiFe2O4�������մɵĸ����ܶȿ����Ƶ������н��������ʧ���մ���ĸ�ʴ����������Ҳת��Ϊ���ܵ�NiFe2O4�ࡣ
�ؼ��ʣ�
����������������������մ���NiFe2O4����ⸯʴ��
��ͼ����ţ�TF 821���� ���ױ�־�룺A
Enhanced sintering and molten salt corrosion behavior of nickel ferrite based cermets
ZHOU Ke-chao, TAO Yu-qiang, LIU Bao-gang, LI Zhi-you
(State Key Laboratory of Powder Metallurgy, Central South University, Changsha 410083, China)
Abstract: NiFe2O4 based cermets were prepared by sintering method under controlled atmosphere, and their electrolysis corrosion in aluminum electrolysis at 960 �� was examined. Based on the studies of the microstructure and phase composition after sintering, surface morphology and composition after electrolysis, impurity content in electrolyte and cathode aluminum, the effects of BaO, Yb2O3 and CoO additive and metal composition on the sintering properties of NiFe2O4 based cermets were analyzed. The electrolysis corrosion property of highly sintered cermets as inert anode was characterized. The enhanced sintering mechanism and molten salt corrosion behavior were also discussed. The results show that the doped BaO, Yb2O3 and CoO react with the ceramic matrix, and then accelerate the process of sintering densification. The substituting of pure Cu and pure Ni by Cu-Ni as metal phase of cermets can increase the relative density of NiFe2O4 based cermets. The high relative density of NiFe2O4 based cermets is benefit to inhibit metal loss and ceramic-phase corrosion, and the anode surface will change to NiFe2O4 dense layer.
Key words: inert anode; aluminum electrolysis; cermets; NiFe2O4; electrolysis corrosion
����������Ƿ�����940~960 ���ǿ��ʴ��Na3AlF6-Al2O3�����еĵ绯ѧ��Ӧ���̣������Դ���ĺͻ�������������Լ����ҵ�Ŀɳ�����չ�����ڶ��Ե缫��������¹��ս����ױ������ҵ��ʵ�ֵ����������������ŷźʹ���Ƚ���Ŀ��[1-3]����20����80���������������Ҫ��ҵ��˾�������ڶ��Ե缫��������¹�����Ϊ21��������ҵ�����ļ����ؼ���������Դ��2003�꽫�ù�����Ϊ�� ��20�������ȵ��з����⣬�й���ҵ��˾������Ϊ10������з�����֮�ס�������ҵ��˾[4-5]����ʿMoltech��˾[6-7]������˹��ҵ��˾[8-9]�����ô���ҵ��˾[10]��������������ʵ����[11]��Ų���Ƽ���ѧ[12-18]���������¿�����ѧ[19]�����ϴ�ѧ[20-24]�Ͷ�����ѧ[25-27]�ȶԶ�������������ʪ�����������µ���ʵȹؼ����ϼ�����¹��ս�����ϵ���о���
�����������ϼ�����������¹��յĺ����뼼���ѵ㡣��Ϊ�����������ϣ�Ӧ�����ܵ���ʵĸ�ʴ������̬������ʴ���������õ����ԺͿ�������ǿ�����ڼӹ����ͼ�����������������ӡ����Ͳ��ϰ����������մ�[17]������/�Ͻ�[8, 12-13]�ͽ����մ�[15-16]�ȡ������մɼ���������մɵ���ʴ�ԡ��������ȶ��ԡ��������Ժͽ��������õ����Լ����ȳ���Ե��ŵ㣬��Ϊ�����Ӧ��ǰ���Ķ����������ϡ����͵Ľ����մɲ����Ǽ⾧ʯ���������մ���Ͻ�ĸ��ϲ��ϣ��մ�����NixFe3-xO4��NiFe2O4+NiO��ZnFe2O4+ZnO��NixFe2yZnzO(3y+x+z)��NiAl2O4���������������Cu��Ni��Fe����Ͻ����У�NiFe2O4�������մ����ھ����մ����ڵ���������е��ܽ�ȵ͡�����¶������õĵ������ܡ��մ���������������Ժõ��ŵ㣬һֱ�ǹ�������о��ص�[15-16, 20-23, 26-27]��������ҵ��˾����ŵ�Ƚ�����˾�Ȼ����Ը�����Ͻ�����25 d��6 kA���������[28]�����ϴ�ѧ���й���ҵ�ɷ�����˾����28 d��4 kA��960~980 �������顣���͵������Ҳ����һЩ���⣬�����Ч�ʵ���̼��������������ʴ���ء�����Ԥ��-�����͵����������ѡ�����������������˼��ȹ��������Ѷ������������䡢���������ֲ������ȡ�ԭ�������ʺ���ƫ�ߣ�����������ʴ������Ϊ�ؼ������������ص��о��ս������ͽ�������ɶ�NiFe2O4�������մɵ��ս����ʴ���ܵ�Ӱ�죬��̽�ֲ��ϵ�ǿ���ս���ƺ����θ�ʴ��Ϊ��
1 ʵ��
��Fe2O3��NiOΪԭ�ϣ������ȷ�Ӧ�ϳɷ��� (1 200 ������6 h)�Ʊ�NiFe2O4���մɡ������ĺϳɲ������һ�����Ľ��������Ӽ��ͳ��ͼ�������ģѹ����Ⱦ�ѹ���͡�ѹ��������ѹ1��10-4~5��10-4��N2�����У���1 150~1 350 ���½����սᡣ
XJP-6A�ͽ���������JSM-6360LV��ɨ��羵��������֯������ò������JSM-6360LV��ɨ��羵�� EDX-GENESIS�������ǽ�������֯�����ɷַ��������õ¹����ȹ�˾HZG4/B-PC��X�����Ƿ���������ɡ�ASTM C373-88(1999)�ⶨ�ܶȣ��Ķ˵缫�������ڿ�����Ar�����µĵ����ʣ������¶ȷ�ΧΪ25~1 100 �档���ʵ�����õ�������Ϊ78.07%Na3AlF6-9.5%AlF3-5.0%CaF2- 7.43%Al2O3 (��������)������ʷ��ӱ�Rc(�������NaF��AlF3��Ħ����)Ϊ2.3�������¶�Ϊ947 �棬����¶�960 �棬Բ���������ײ����Ϊ2.5 cm2�������ܶ�Ϊ1.0 A/cm2������Philips8424 TW2424��X����ӫ�����(XRF)������ʺ�ԭ���е����ʺ�����
2 ��������
��Cu/NiΪ�������NiFe2O4�������մ���һ�������IJ�����ϵ������WC-Co�Ͻ�������ͨ��WC��Co����ܽ�����ʵ���ս����ܻ���Ҳ����Al2O3/Ni����������ջ�ԭ���ս����սᡣNiFe2O4������ �մɵ��ս���̼�Ҫ��ֹ�մ������ʧ�����µĻ�ԭ����Ҫ������������������������֮�䲻���������ܽ��������սᷴӦ��NiFe2O4�������մɵ��ս� �����ϸ������������ѹ�£�ͨ���մ����ս��� �ɡ��ս����ܶ�������������������NiFe2O4�������մɵĺ��IJ�����ֱ��Ӱ����ϵ���ѧ���������ʴ���ܡ�NiFe2O4�������մɵĸ����ܶ��ս��ǽ���������е�����ؿ��������Լ��ɴ˴����������ͺͱ��������������Ч������
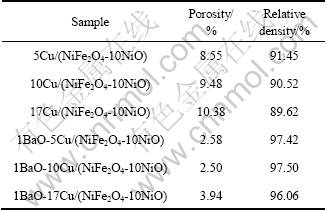
�����ս�������ǿ���ս�ij����ֶΡ�NiFe2O4�������մɵ��ս�������ѡ���豣֤�丯ʴ�ܽ����ֻ�������ʶ�������������Һ���������մ������һ���̶ȵķ�Ӧ����ǿ�մ��౾�����ս���ϵ����ɢ����������1 273 K��BaO�ķֽ��ѹ(2.224 V)�Ը���Al2O3��(2.188 V)[29]��������ѧ������Fe2O3����ϵ�в���о����֣�����1%��BaO�ɵõ��Ϻõ��ս�Ч������1����Ϊ��1 200 ���ս�4 h�������ܶȵĶԱȡ�����1%��BaOʹxCu/(NiFe2O4-10NiO)�����մɵ�����ܶ���������������ຬ��Ϊ5%��10%��17%ʱ���������մɲ���1%BaO��Ʒ������ܶȷֱ�Ϊ97.42%��97.50%��96.06%����δ������Ʒ������ܶȷֱ�ֻ��91.45%��90.52%��89.62%���ֱ������5.97%��6.98%��6.44%��
��1 1 200 ���ս�ʱCu/(NiFe2O4-10NiO)�����մɵ�����ܶ�
Table 1 Relative density of Cu/(NiFe2O4-10NiO) based cermets sintered at 1 200 ��
ͼ1��ʾΪ�����ຬ��17%�����ĶϿ���ò��δ���������մ���ľ����ߴ粻��10 ?m������ͨ״̬���ԣ�1% BaO������ʹ��������20 ?m�� �ң������Ŀ���Ҫ�Թ����ıտ���ʽλ���մ���ľ��紦�����������������1% BaO��������߲��ϵ��ս����ܡ�

ͼ1 1 200 ���ս�����մɵĶϿ�SEM��
Fig.1 SEM images on fracture surface of cermets samples sintered at 1 200 ��: (a) 17Cu/(NiFe2O4-10NiO); (b) 1BaO- 17Cu/(NiFe2O4-10NiO)
Ϊ��ʾ�ս�����п��ܷ����ķ�Ӧ���Ʊ���BaO��NiFe2O4-10NiO����ɢż��������������մ��ս���ͬ�Ĺ��̡�NiFe2O4-10NiO�մɻ�����BaO����X���������������(��ͼ2)�����������BaFe2O4��Ba2Fe2O5��NiBa3O4�������ࡣ��ս�Ч��������Դ����Щ������IJ������䵼�µ�NiFe2O4���NiO��ṹ�ı仯����������մ��е�NiFe2O4���NiO��ʵ�����Ƿǻ�ѧ����������ֱ�Ϊ��Fe2+��Ni(1-x)FexFe2O4��ͬʱ��Fe2+��Fe3+��Ni(1-x)Fex��O (x��x��)(����5�����������)���������ӵ�BaO����������߷������·�Ӧ������ȱFe3+��O��Ni(1-x)FexFe(2-2y)O(4-3y)��ȱNi��O��Ni(1-x-y)Fex��O(1-y)������x ?1��y?1(��ͬ)��
Ni(1-x)FexFe2O4+yBaO=
Ni(1-x)FexFe(2-2y)O(4-3y)+yBaFe2O4 (1)
Ni(1-x)FexFe2O4+2yBaO=
Ni(1-x)FexFe(2-2y)O(4-3y)+yBa2Fe2O5 (2)
Ni(1-x)Fex��O+3yBaO=Ni(1-x-y)Fex��O(1-y)+yNiBa3O4 (3)
����Fe2O3-BaO��NiO-BaO��Ԫ��ͼ��3���������ڱ�ʵ����ս��¶��¾�Ϊ���࣬�ս���ϵ�в�����Һ���ս������ս����ܵĸ��ƿ���Դ��NiFe2O4���NiO������п�λŨ�ȵ���ߡ�NiFe2O4��Ϊ���⾧ʯ�ṹ��Ni2+ռ�ݾ����е�Bλ��Fe3+ռ�ݾ����е�Aλ�Ͳ���Bλ��NiFe2O4��NiO������ܿ�λ������ǿ��1 300 ���������λŨ�ȸߴX���ٷֵ�ʱ�Բ��ᷢ���ṹ�ϵķֽ⡣��Ӧ(1)��(2)����ʹ�þ����е�A��B��Oλ�Ŀ�λŨ��ͬʱ��ߣ�����������ɢ���DZ�����ɢ���߿�λŨ�ȴٽ���������������Ӧ�Ŀ�λ��ɢ���ƽ��е���ɢǨ�ƣ��ӿ�NiFe2O4������ս���̣�������������ʧ�������ij�����������ͬ��������NiO������С�ʵ��ͬʱ���֣���һ�����BaO�ĺ���������BaFe2O4��Ba2Fe2O5��NiBa3O4������������Ŀռ�λ�����ü�ǿ�Ͷ���NiFe2O4��ľ���Ǩ�ƣ����ս�ĸ���Ч����ǿ��
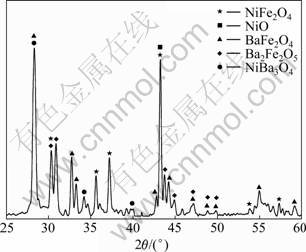
ͼ2 BaO��NiFe2O4-10NiO�����XRD��
Fig.2 XRD pattern of interface of BaO and NiFe2O4-10NiO composite ceramics
ͼ3��4��ʾ�ֱ�Ϊ��������960 ����10 h���������ò��ͼ����ʾ������1%BaOʹ�����еĽ�����ʧ��ĺ�ȷֱ���300~350 ?m���͵�100~ 200 ?m(��10%Cu��Ʒ��ͼ3��ʾ)��400~500 ?m ���͵�Լ300~400 ?m(��17%Cu��Ʒ��ͼ4��ʾ)���ý�������������մ��ս����ܶȵ���߿ɷ�ֹ�ڲ���������������������ֱ�ӽӴ�����Ч���Ƶ������н������ѡ�����ܽⸯʴ���Ӷ���ֹ���ڽ��������ʧ���µĵ���������Լ��ɴ˴�����������������

ͼ3 �����մ�960 ����10 h�������SEM��
Fig.3 SEM backscattered images of cermets after electrolyzed at 960 �� for 10 h: (a) 10Cu/(NiFe2O4-10NiO); (b) 1BaO- 10Cu/(NiFe2O4-10NiO)

ͼ4 �����մ�960 ����10 h������������Ƭ
Fig.4 OM images of cermets after electrolyzed at 960 �� for 10 h: (a) 17Cu/(NiFe2O4-10NiO); (b) 1BaO-17Cu/(NiFe2O4-10NiO)
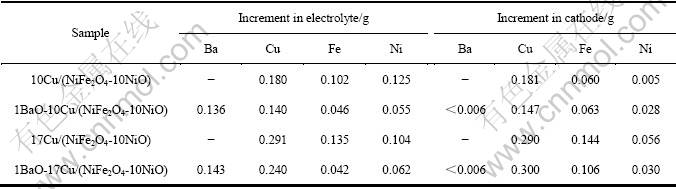
��2����Ϊ���10 h�����ʺ���������������ʴԪ�ص���������BaO����ܽ�������ʣ���δ��������������������������Fe��Ni��CuԪ�ؽ������ʺ��������ܺ���������Ч�����ƽ����մ��и�����ĵ�ⸯʴ��
��2 �����մɵ��10 h�����ʺ���������������ʴԪ�ص�������
Table 2 Net increments of elements of anode distributed in electrolyte and aluminum cathode after electrolyzed at 960 �� for 10 h
����մ��ྦྷ�����ԣ��侧������ʴ��������С���������������ף�ǿ�������ϣ�����Ч��߽����մɲ��ϵ���ʴ���ܡ������о�֤ʵ���մɲ���������ϡ��������ɷ��Ͳ��ϵ��ս����ܡ������ֽ��ѹ[29]���ܽ��ڵ�����еĽ���̬Al��ϡ��������ͷ�����ķ�Ӧ����ѧ������ѡȡCeO2��Y2O3��Yb2O3 3�����������NiFe2O4�������մɵIJ����о���������֣�����0.5%~1.0% Yb2O3���������Ʋ��ϵ��ս��ʴ���ܡ�
ͼ5��ʾΪ1 300 ���ս��δ������2.0% Yb2O3����17Cu/(NiFe2O4-10NiO)��Ʒ����SEM��Yb2O3����ʹ���ߴ��С��NiFe2O4��(���ɫ)�ľ��硢NiFe2O4����NiO��(dz��ɫ)������ø�ƽ ֱ��ͼ5(a)��ʾ��NiFe2O4��ľ��紦������ɫ�ĵ�״���ӣ�ijЩ��������ɵ�״�������ļ�����Cu���NiO�������Ե����Щ���ӵijߴ������ȼ�ǿ����˵����ɫ������NiFe2O4��Ľ��������Ժã�����NiFe2O4�ྦྷ����չ������Cu���NiO��������� ��ž۳ɽϴ������Ϊ�������������ڽ��洦�ž۳�Ĥ�����¶Բ�����ѧ�͵����������̫��Ӱ�죬Yb2O3�IJ���Ӧ������

ͼ5 1 300 ���ս�δ������2.0%Yb2O3����17Cu/ ( NiFe2O4-10NiO)��Ʒ��SEM��
Fig.5 SEM images of 17Cu/(NiFe2O4-10NiO) samples sintered at 1 300 ��: (a) Without Yb2O3; (b) With 2.0% Yb2O3
��ͼ5(a) ��������������Cu��NiO��NiFe2O4 3����û�м���YbԪ�أ�ͼ5(b)����ɫ����1��2�к���һ������YbԪ��(��ͼ6(b))��2���Yb�����Ըߣ��������������ʱѡ����Ӱ�졣
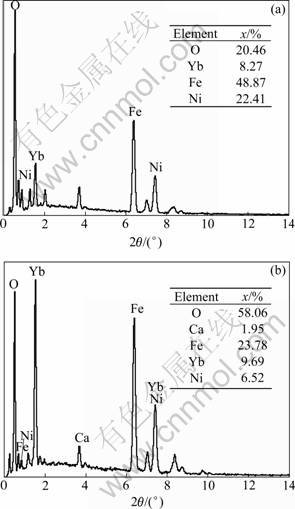
ͼ6 ͼ5(b)�����������EDX��
Fig.6 EDX analysis of product in Fig.5(b): (a) Point 1; (b) Point 2
ͼ7��ʾΪ1 300 ���ս�IJ���3.0%Yb2O3��Ʒ��XRD�ס�������������Ʒ�г�Cu��NiO��NiFe2O4 3���⣬�������������ࡣΪ�����ر����������࣬�Ʊ��˸߲��Ӻ�����������XRD�����ʾ����ԭ����3�������⣬ֻ�����������廯����YbFeO3��һ������(��ͼ8)����˵��ͼ7��������ΪYbFeO3�࣬����Yb2O3��NiFe2O4��NiO��ͨ����Ӧ(4)��(5)���ɡ�YbFeO3������ɲ��ɱ����ʹNiFe2O4���NiO�������������ӵĿ�λŨ�����ӣ���������BaO���������ƣ�Yb2O3������ͬ�������˲��ϵ��ս����ܻ����̡�
Ni(1-x)FexFe2O4+yYb2O3=
Ni(1-x)FexFe(2-2y)O(4-3y)+2yYbFeO3 (4)
Ni(1-x)Fex��O+yYb2O3=Ni(1-x)Fe(x��-2y)O(1-y)+2yYbFeO3 (5)
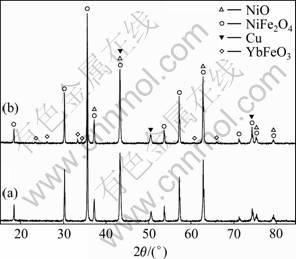
ͼ7 δ���������3.0%Yb2O3��10Cu/(NiFe2O4-10NiO) XRD��
Fig.7 XRD patterns of 10Cu/(NiFe2O4-10NiO) samples sintered at 1 300 ��: (a) Without Yb2O3; (b) With 3.0%Yb2O3
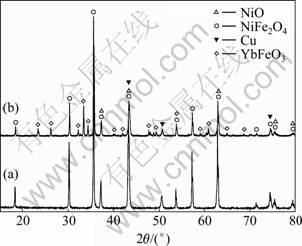
ͼ8 δ���������10%Yb2O3 10Cu/(NiFe2O4-10NiO)��XRD��
Fig.8 XRD patterns of 10Cu/(NiFe2O4-10NiO) samples: (a) Without Yb2O3; (b) With 10%Yb2O3
ͼ9��ʾΪ�Աȵ��10 h����Ʒ�ײ���SEM��
��ͼ9��֪��δ������Ʒ������һ�����100~120 ��m��Cu��ʧ�㣻0.5% Yb2O3������Ʒֻ�ھֲ�����30~50 ��m����Cu�㣬һЩ����û�����ԵĽ����������ʧ�ļ��������0.5%Yb2O3�IJ�����Ч�����˽����մɵĽ�����������е���ʧ�����ʵ��Ե���ʺ������������ʺ���������ʾ(����3)��0.5%Yb2O3������δ������Ʒ��ȣ�Cu��Ni��Fe������������������1�����ϣ�������Fe������������δ����ʱ��0.522 g(����ʺ�������������֮��)���͵����Ӻ��0.111 g�������������0.5%Yb2O3���������˽����մ��н������ڵ������е���ʧ��������������մ�������NiFe2O4�����ʴ���ܡ�������Ϊ���Ӽ����մɻ���ķ�Ӧ������YbFeO3�����ھ�/����棬����������ܶ�(��ͼ9)��Ҳǿ�����մ���(����NiFe2O4��)���������ϣ������˾�����ͨ���ף������˽�������������ܽ���մ���ľ��縯ʴ��

ͼ9 ���10 h����Ʒ�ײ���SEM��
Fig.9 SEM images of 10Cu/(NiFe2O4-10NiO) samples after electrolyzed for 10 h: (a) Without Yb2O3; (b) With 0.5%Yb2O3
��3 ��1 300 ���ս�����մ���960 ����10 h�����ʺ���������������ʴԪ�ص�������
Table 3 Net increments of elements from anode distributed in electrolyte and aluminum cathode after electrolyzed at 960 �� for 10 h of ceramic sintered at 1 300 ��
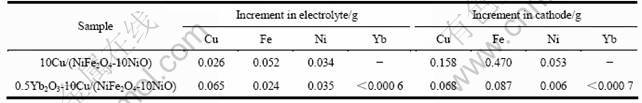
Ba2+��Yb3+�����Ӱ뾶ԶԶ����Ni2+��Fe3+�����Ӱ뾶����BaO��Yb2O3��Ϊ���Ӽ������߲�����������е�NiFe2O4���NiO���γɹ����壬�������ս���������䷴Ӧ�����µ����ࡣCo2+��Ni2+�����Ӱ뾶�������CoO��Ϊ���Ӽ�����������е��մ����γɹ����塣ͼ10��ʾΪ1 300 ���ս��δ���ӺͲ���10%CoO�����մɵ�XRD�ף���ͼ10���Կ���, ����10%CoO��15(20Ni-Cu)/(10CoO-NiFe2O4)�����մ��в�û�г����µ����࣬��˵�����ӵ�CoO��ȫ��NiFe2O4��NiO���γ��˹����塣
ͼ11��ʾΪ1 300 ���ս��15(20Ni-Cu)/ [10(CoO-NiO)-NiFe2O4]�����մɵ�����ܶ��治ͬCoO�������ı仯���ߡ���ͼ11���Կ���, ��Ʒ������ܶ�����CoO�����������Ӷ�����������10%CoO����Ʒ����ܶȴﵽ97.8%����δ������Ʒ������ܶ����������0.7%����˵������CoO�����ڸò��ϵ��ս����ܻ���
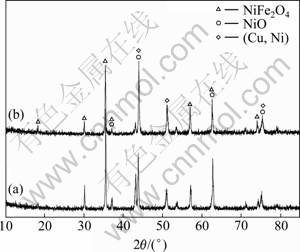
ͼ10 1 300 ���ս��10%CoO�����մɵ�XRD��
Fig.10 XRD patterns of samples sintered at 1 300 ��: (a) 15(20Ni-Cu)/(10NiO-NiFe2O4); (b) 15(20Ni-Cu)/(10CoO- NiFe2O4)
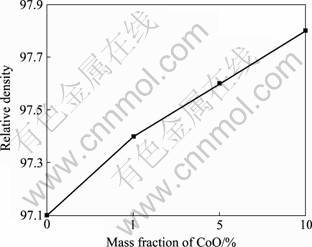
ͼ11 CoO��������15(20Ni-Cu)/(NiO-NiFe2O4)�����մ�����ܶȵ�Ӱ��
Fig.11 Effect of CoO content on relative densities of 15(20Ni-Cu)/(NiO-NiFe2O4)cermets
ͼ12��ʾΪCoO����15(20Ni-Cu)/(NiO-NiFe2O4)�����մɵĵ絼�����¶ȵı仯���ߡ���ͼ12���Կ��������ɷֽ����մɵ絼�ʾ����¶����߶������ϰ뵼�嵼����ɡ�����ͬһ�¶��£�����CoO�����������ӣ���Ʒ�ĵ絼�ʲ���������960 ���£�����10%CoO�����մɵĵ絼�ʴﵽ��53.04 S/cm����δ����CoO��Ʒ�絼�ʵ�43.35 S/cm�����22%������Ҫ�����ڿ�Ѩ��Co2+��Co3+����Ծ�ļ��ʴ�������Ni2+��Ni3+����Ծ�ļ�������ģ����⣬���Ӻ���Ʒ����ܶȵ����С�˵��ӺͿ�Ѩ����ɢ��������һ���������Ʒ�ĵ絼�ʡ�
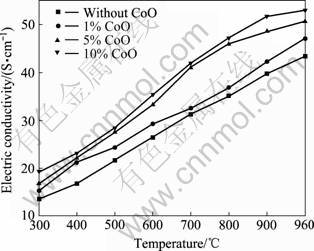
ͼ12 CoO����15(20Ni-Cu)/(NiO-NiFe2O4)�����մɵĵ絼�����¶ȵĹ�ϵ
Fig.12 Relationship between electric conductivity of CoO doped 15(20Ni-Cu)/(NiO-NiFe2O4) and temperature
ͼ13��ʾΪ��ͬCoO��������15(20Ni-Cu)/ (NiO-NiFe2O4)�����մ���960 ���µ��12 h�������ײ���SEM��ͼ13�о�����ɢ�İ�ɫ��״��Ϊ(Cu,Ni)���Ͻ����ࡣδ����CoO��Ʒ�ĵײ���һ��Լ100 ��m�ĸ�ʴ�㣬�ø�ʴ���ڽ������ѱ���ȫ��ʴ�����½϶�������ϱ���������ɡ�����1.0%CoO����Ʒ�ײ���ʴ����Լ��80 ��m����ʴ�����н϶�Ŀ���������˵������1%CoO���ں����ϵͣ���δ����Ч�ֵ�����ʵ���ʴ����Ʒ����ʴ������Ȼ�ϲ����5%CoO��Ʒ�������һ�����Լ40 ��m�Ľ�������ʧ�㣬�ò��ڿ�����Ʒо�����٣��Ƚ����ܣ����������ʧ��δʹ���ϳ������ظ�ʴ�������������CoO���Ӻ���Ʒ�ս�����ܶ���ߣ����������մ������ʪ���������ƣ���ʴ�������С�Ķ��ο���NiFe2O4����NiO��Ĺ�����������ͣ������С���γɵ����ܲ㣬������Ч�ֵ�����ʶԽ����մɵĽ�һ����ʴ����������Ϊ10%ʱ�������ײ�����һ�����ԼΪ130 ��m�Ľ�������ʧ�㣬�ò����ɶ�ף������������������ͨ����Щ�������������ڲ�����˵����������CoO�ᵼ�²��ϵ���ʴ�����½���
��4����Ϊδ���������Ͳ���5%CoO�������12 h�����ʺ���������������ʴԪ�ص����������ӱ�4�п��Կ���������5%CoO�����������ʺ��������е�Cu��Ni��Fe���ʺ������Խ��ͣ����������������CoO������Ч���ƽ����մ��и�����ĵ�ⸯʴ��
NiFe2O4�������մ��н������������Ϊ����߲��ϵĵ�����������ܡ�������Բ������ܵ�Ӱ�������Ҫ�������ս��ʴ�����������档�ս�ʱ������̬�Ĵ�Cu��������žۺ�����������¶��ο��IJ�������̬Ni��������ܾ��ȵطֲ����մɻ����У�������״�������մ�������ս���Ҫ������Ӧ�ĵ�����ͬ�������ڲ��ϵ��ս����ܻ����ڵ������У�Cu�����ʴ��������Ni��ģ��α����Cu����ת��Ϊ�������ٸ�ʴ��Ni ���������һֱ����ѡ�����ܽ�[30]����ˣ��Ż��������Cu/Ni��ȿɻ�ýϺõ��ۺϽṹ�����ܡ�
ͼ14��ʾΪһ���������Ϊ17%��������ĩ��ʼƽ�������൱(Լ8 ��m)��1 300 ���ս������Ľ�����Ƭ��17%Ni����Ʒ�Ʊ������г��ֽ���������ž۳���Ƭ״��������Ϊ���αտף�˵���ս����һֱΪ�����Ni�������ڲ������մɻ�����սᣬ������������17%Cu��Ʒ��Ҳ�϶࣬�϶���ܼ��ֲ���Cu������������˵���ս������Cu��Ǩ���ž۲������ο��������ڲ��ϵ����ܻ�������Cu��Ni��Ϸ�Ϊ���������Ʒ�У�������������ͬ�����ֽϴ������Ni��Cu�۵���ʽ����ʱ����Ʒ�ս�ṹ���Ը��ƣ����ijߴ��������������Ʒ������ �ͣ��������Cu���м���������մ���ʪ�Ժõ�NiԪ�ؿɸ���Cu����NiO��NiFe2O4�����ʪ�ԣ������ս���������ڽ��������������Ǩ�ƣ����ٶ��ο����γɣ�ͬʱ���ڽ����������ò�����������մɻ����ս�ĸ���Ӱ��̶Ƚ��͡��մɻ���������ս�Ԥ�ڽ������õ���ʴ���ܡ�
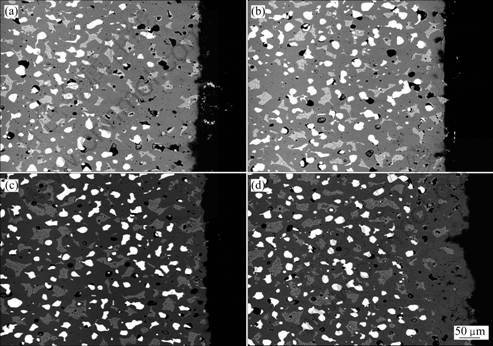
ͼ13 �����մɵ�������ײ���ʴ�����SEM��
Fig.13 SEM images of electrolyzed samples: (a) Without CoO; (b) With 1.0% CoO; (c) With 5.0% CoO; (d) With 10.0% CoO
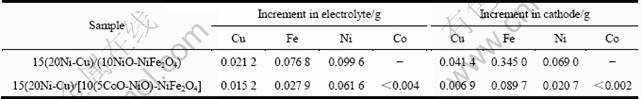
��4 1 300 ���ս�����մ�960 ����10 h�����ʺ���������������ʴԪ�ص�������
Table 4 Net increments of elements from anode distributed in electrolyte and aluminum cathode after electrolysis at 960 �� for 10 h

ͼ14 �����ຬ��Ϊ17%ʱ10NiO-NiFe2O4�����մɵĽ�����Ƭ
Fig.14 OM photographs of 10NiO-NiFe2O4 cermets with 17% metal phase added by Ni(a), Cu(b), Cu-10Ni mixture(c) and 10Ni coated Cu(d)
��17(10Ni-Cu)(10NiO-NiFe2O4)��960 ����40 h�������SEM����(��ͼ15)���Կ������������������漰����ʽ��յIJ����Ե�ֱ����Լ140 ��m��60 ��m�Ľ�������ʧ�㣬��NiO��Ҳ��ʧ�ˣ����ò���ת��Ϊ�����ܵġ�3������������ʴ��NiFe2O4�࣬�Բ��ϵ��͵�ⸯʴ���ܸ�������
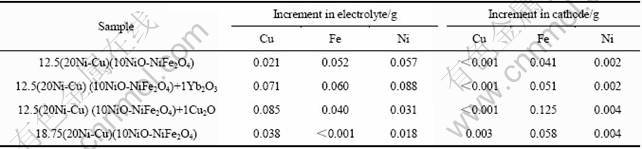
���ڽ�����ΪCu-Ni�Ͻ��NiFe2O4������մɵ��ʱ���ڱ����γ����ܵ�NiFe2O4��㣬��960 ���½���һ����Ʒ10 h���ʵ�飬������������������Ԫ�ĸ�ʴ�������5����Ϊ����ʺ������ڵ��������������ʺ��������2��3��������Աȣ���������ΪCu-Ni�Ͻ�ʱ��������Cu�������ʺ�����������������������������������͡�ͬʱ������������Ni����Ҳ���Լ��١�Fe������һ���̶ȵĽ��͡��ɴ˿ɼ��������������ѡ�����ܽ��ܵ����õ����ƣ��մ�����ܽ�����Ҳ�в�ͬ�̶ȵĽ��ͣ���Ӧ����ڽ����մ��ս����ܵ���ߡ�

ͼ15 17(10Ni-Cu)/(NiFe2O4-10NiO)�����մ�960 ���µ��40 h���SEM��
Fig.15 SEM images of 17(10Ni-Cu)/(NiFe2O4-10NiO) cermets after electrolyzed at 960 �� for 40 h: (a) Bottom; (b) Side face
��5 Cu-Ni��������Ʒ��960 ����10 h�����ʺ���������������ʴԪ�ص�������
Table 5 Net increments of elements in electrolyte and aluminum cathode after electrolyzed at 960 �� for 10 h
3 ����
1) NiFe2O4�������մ���ϵ����������BaO��Yb2O3ʱ���ս���������Ӽ����մɻ����෴Ӧ����������BaFe2O4��Ba2Fe2O5��NiBa3O4��YbFeO3�������������������մ�����ս���ԣ������˽����մɵ��ս����ܻ����̡�
2) NiFe2O4�������մ���ϵ����������CoO,�����մɻ����γɹ����壬���ٽ����մɲ��ϵ��ս����ܻ����̣���Ч��߲��ϵĵ������ܺ���ʴ���ܡ�
3) �����Cu��Ni�����࣬��Cu-Ni�Ͻ���NiFe2O4�������մɵĽ�������Ԫʱ���������������Ǩ�Ƶ����ơ��������ʪ�Ե���ߡ�������ò���ڵ��������������ڼ����ս�����ж��ο����γɣ���ø����ܶȵ��ս��塣
4) �����ܶ��ս��NiFe2O4�������մɵ������б���������ɸ���ʴ����NiFe2O4��ɵ����ܲ㣬�������������������ܽ��������ĵ�����������������������ĸ�ʴ���ʡ�
REFERENCES
[1] KENIRY J. The economics of inert anodes and wettable cathodes for aluminum reduction cells[J]. JOM, 2001, 53(5): 43-47.
[2] SADOWAY D R. Inert anodes for the Hall-H��roult cell: The ultimate materials challenge[J]. JOM, 2001, 53(5): 34-35.
[3] LI Jie, LAI Yan-qing, ZHOU Ke-chao, LI Zhi-you, LIU Ye-xiang. Preparation and preliminary testing of cermet inert anode for aluminum electrolysis[J]. Transactions of Nonferrous Metals Society of China, 2003, 13(3): 663-670.
[4] ROBERT L K, SIBA P R, ROBERT K D, ALFRED F L. Corrosion of cermet anodes during low temperature electrolysis of alumina[R]. Washington: Alcoa technical center, 1997.
[5] JOHN Y. Inert anode metal life in low temperature aluminum reduction process[R]. Washington: Goldendale Aluminum Company, 2003.
[6] PAWLEK R P. Inert anodes: an update[C]//Wolfgang Schneider. Light Metals 2002. Warreudale PA. USA: TMS, 2002: 449-456
[7] PAWLEK R P. Inert anodes: an update[C]//ALTON T. Tabereaux. Light Metals 2004. Warreudale PA. USA: TMS, 2004: 283-287.
[8] ANTIPOV E V, BORZENKO A G, DENISOV V M, FILATOVET A Y, IVANOV V V, KAZAKOV S M, MAZIN P M, MAZIN V M, SHTANOV V I, SIMAKOV D A, TSIRLINA G A, VASSILIEV S Y, VELIKODNY Y A. Electrochemical behavior of metals and binary alloys in cryolite-alumina melts[C]// TRAVIS J G. Light Metals 2006. Warreudale PA: TMS, 2006: 403-408.
[9] PAWLEK R P. Aluminum wettable cathodes: An update[C]// PETERSON R D. Light Metals 2000.Warrendale PA: TMS, 2000: 449-454
[10] CHIN P C, SIDES P J, KELLER R, The transfer of nickel, iron, and copper from Hall cell melts to molten aluminum[J]. Canada Metall Q, 1996, 35: 61.
[11] YANG Y H, JOHN N H, GREG K K. Aluminum electrolysis tests with inert anodes in KF-AlF3-based electrolytes[C]//Travis Galloway. Light Metals 2006. Warrendale PA. USA: TMS, 2006: 421-424
[12] NGUYEN T, DE NORA D V. Oxygen evolving inert metallic anode[C]//TRAVIS J. Galloway, Light Metals 2006. Warrendale PA, USA: TMS, 2006: 385-390.
[13] KAENEL R, NORA D V. Technical and economical evaluation of the de NORA inert metallic anode in aluminum reduction cells[C]//TRAVIS J. Light Metals 2006. Warrendale PA, USA: TMS, 2006: 397-402.
[14] SEKHAR J A, NORA V, LIU J, WANG X. TiB2/colloidal alumina carbon cathode coating in Hall-Heroult and drained cells [C]//WELCH B. Light Metals 1998. Warrendale PA, USA: TMS, 1998: 605-615.
[15] OLSEN E, THONSTAD J. The behaviour of nickel ferrite cermet materials as inert anodes[C]//HALE W. Light Metals 1996. Warrendale PA, USA: TMS, 1996: 249-257.
[16] OLSEN E, THONSTAD J. Nickel ferrite as inert anodes in aluminum electrolysis (Part��): Material fabrication and preliminary testing[J]. Journal of Applied Electrochemistry, 1999, 29(3): 293-299.
[17] ISSAEVA L, YANG Jian-hong, HAARBERG G M, THONSTAD J, AALBERG N. Electrochemical behavior of tin species dissolved in cryolite-alumina melts[J]. Electrochimica Acta, 1997, 42(6): 1011-1018.
[18] THONSTAD J, SOLHEIM A. The use of strongly acid low melting bath in aluminium electrolysis[J]. Aluminium, 1986, 12: 938-941.
[19] MARK G, MARGARET H. Cu-Al alloy as an anode for aluminum electrowinning[J]. Corrosion Science, 2006, 48: 2457-2469.
[20] ������, �� ��, �� ��, �� ��, ��Ծ��, �Ʋ���, ��ҵ��. CaO���Ӷ�10NiO-NiFe2O4�����մ��ս����ܻ���Ӱ��[J]. �й���ɫ����ѧ��, 2006, 16(8): 1355-1360.
LAI Yan-qing, ZHANG Yong, ZHANG Gang, LI Jie, HE Yue-hui, HUANG Bai-yun, LIU Ye-xiang. Effect of CaO doping on densification of 10NiO-NiFe2O4 composite ceramics[J]. The Chinese Journal of Nonferrous Metals, 2006, 16(8): 1355-1360.
[21] LAI Yan-qing, TIAN Zhong-liang, LI Jie, YE Shao-long, LI Xin-zheng, LIU Ye-xiang. Results from 100 h electrolysis testing of NiFe2O4 based cermet as inert anode in aluminum reduction[J]. Transactions of Nonferrous Metals Society of China, 2006, 16: 970-974.
[22] HE Han-bing, ZHOU Ke-chao, LI Zhi-you, HUANG Bai-yun. Effect of BaO addition on electric conductivity of xCu/10NiO-NiFe2O4 cermets[J]. Transactions of Nonferrous Metals Society of China, 2008, 18(5): 1134-1138.
[23] �� ��, �ܿƳ�, ��־��, ����Ӿ. ���ն�NiFe2O4�մ��ս����ܻ���Ӱ��[J]. �й���ɫ����ѧ��, 2004, 14(6): 1002-1006.
ZHANG Lei, ZHOU Ke-chao, LI Zhi-you, ZHANG Xiao-yong. Effect of atmosphere on densification in sintering nickel ferrite ceramic for aluminum electrolysis[J]. The Chinese Journal of Nonferrous Metals, 2004, 14(6): 1002-1006.
[24] LI Jie, L? Xiao-jun, LAI Yan-qing, LI Qing-yu, TIAN Zhong-liang, FANG Zhao. Effect of carbon fibre on properties of TiB2/C composite cathode coating for aluminum electrolysis[J]. Jounal of Central South University of Technology, 2008, 15: 526-530.
[25] ʯ����, �����, ������, �淽ϼ. �����������Cu-Ni-Cr�������������о�[J]. ��ұ����, 2004, 24(6): 45-47.
SHI Zhong-ning, XU Jun-li, QIU Zhu-xian, SHU Fang-xia. Research on the properties of Cu-based metal anodes for aluminum electrolysis cell at low temperature[J]. Mining and Metallurgical Engineering, 2004, 24(6): 45-47.
[26] ������, �� ��, Ҧ�㴺, ���˺�. NiFe2O4������TiO2�ļ⾧ʯ���ս����[J]. ������ѧ��, 2004, 32(9): 1150-1153.
JIAO Wan-li, ZHANG Lei, YAO Guang-chun, LIU Yi-han. Sintering process of NiFe2O4 spinel with and without TiO2 adding[J]. Journal of the Chinese Ceramic Society, 2004, 32(9): 1150-1153.
[27] ϯ����, Ҧ�㴺, ���˺�. ������������⾧ʯ���������۽ṹ�����ܵ�Ӱ��[J]. ������ѧѧ��: ��Ȼ��ѧ��, 2005, 26: 574-577.
XI Jin-hui, YAO Guang-chun, LIU Yi-han. Effect of additives on microstructure and properties of inert anode of NiFe2O4 spinel[J]. Journal of Northeastern University: Natural Science, 2005, 26: 574-577.
[28] ALCORN T R, TABEREAUX A T, RICHARDS N E. Operational results of pilot cell test with cermet "inert" anodes[C]//CHRISTIAN M B. Light Metals 1993. Warrendale PA. USA: TMS, 1993: 433-445.
[29] ��Ԫ��, �����, �Ŵ���. �绯ѧ�����ֲ�[M]. ��ɳ: ���Ͽ�ѧ����������, 1985: 338-339.
ZHU Yuan-bao, SHEN Zi-chen, ZHANG Chuan-fu. Electrochemical data handbook[M]. Changsha: Hunan Science and Technology Press, 1985: 338-339.
[30] STRACHAN D M, KOSKI O H, MORGAN L G, WESTERMAN R E, PETERSON R D, RICHARDS N E, TABEREAUX A T. Results from a 100-hour electrolysis test of a cermet anode: material aspects[C]//CHRISTIAN M B. Light Metals 1990. Warrendale PA, USA: TMS, 1990: 395-401.
(�༭ ������)
������Ŀ�����Ҹ����о���չ�ƻ�������Ŀ(2008AA030501)�������ص�����о���չ�ƻ�������Ŀ(2005CB623703)��������Ȼ��ѧ�����Ŷ�������Ŀ(51021063)
�ո����ڣ�2010-06-18�������ڣ�2010-09-20
ͨ�����ߣ��ܿƳ������ڣ���ʿ���绰��0731-88836264��E-mail: zhoukechao@mail.csu.edu.cn


