���±�ţ�1004-0609(2010)09-1716-08
Mg2Cu������Ͻ�ı��渴�����
����1, 2, ������1, �ּξ�1, �� ��1
(1. �����ѧ ���Ͽ�ѧ�빤��ѧԺ������ 400044��
2. �����ѧ ����þ�Ͻ���Ϲ��̼������ģ�����400044)
ժ Ҫ��
���û�е��ĥ���Ʊ�Mg2Cu�Ͻ𣬲��ԸúϽ�Ϊ������������������Ϊ5%�ĵ���(C��Co��Ni��Cu)��������(Cr2O3��Fe3O4��TiO2��V2O5)��ͨ����е��ĥ�ԺϽ���б��渴����ԡ�����p��c��T�����Dzⶨ�Ͻ�Ĵ������ܣ��о����Ӳ�ͬ���ʺ��������Mg2Cu�Ͻ������ܵ�Ӱ�졣�����������200 ���300 ���£�����C��Fe3O4�ܹ���Ч���Mg2Cu�Ͻ�Ļ��ԣ�ʹ������������Ӧ������������ʱ�䣬���������������Ʒ���Ч������400 ���£�����Co��Ni��TiO2��Fe3O4�ܹ���Ч��������ʱ�䣬���ƺϽ���ۺϴ������ܡ�
�ؼ��ʣ�
����Ͻ���Mg2Cu����е��ĥ�����渴�����������������
��ͼ����ţ�TG146.2��TB34��TK91 ���ױ��룺A
Multi-phase surface modification of
Mg2Cu-based hydrogen storage alloys
CHEN Yu-an1, 2, YANG Li-ling1, LIN Jia-jing1, CHENG Ji1
(1. College of Materials Science and Engineering, Chongqing University, Chongqing 400044, China;
2. National Engineering Research Center for Magnesium Alloys, Chongqing University, Chongqing 400044, China)
Abstract��Mg2Cu alloys were prepared by mechanical grinding. In order to modify the surface performance of the alloys, 5%(mass fraction) of simple substances such as C, Co, Ni and Cu or oxides such as Cr2O3, Fe3O4, TiO2, V2O5 were added into Mg2Cu alloys by mechanical grinding. The hydrogen storage properties of the alloys were determined by p��c��T apparatus. The effects of simple substances and oxides on the hydrogen storage properties of the alloys were investigated. The results show that the addition of C or Fe3O4 into Mg2Cu alloys can improve the reactivities of the alloys at 200 �� and 300 ��. At those temperatures, the alloys containing C or Fe3O4 can react easily with hydrogen, resulting in that the hydriding times of the alloys can be shortened and the hydriding/dehydriding capacities of the alloys can be improved. The hydrogen absorption times of Mg2Cu alloys with Co, Ni, TiO2 or Fe3O4 can be effectively shortened and the comprehensive hydrogen storage properties of the alloys can be improved at 400 ��.
Key words��hydrogen storage alloy; Mg2Cu; mechanical grinding; multi-phase surface modification; hydrogen storage property
þ������Ͻ���������ᡢ�������ߡ���Դ�ḻ���ŵ㣬������Դ������Ӧ������ǰ��������������Ͻ��������¶Ƚϸߣ��������ٶȽ����Լ�ѭ���ȶ��Բ�������Ӱ��������ʵ��Ӧ��[1-2]��
�о�������þ������Ͻ����ͨ������;�������䴢�����ܣ�1) �����µķ����Ʊ��Ͻ𣬼�̽����ͳ���������µIJ��Ϻϳɻ��Ʊ�����������������[3-4]��2) ���洦�����ԣ��������л��ܼ���������Ͻ���棬ʹ֮���иߵĴ����Լ�����ʴ���ܣ��ӿ��������ٶ�[5]��3) Ԫ��ȡ�����ԣ���ͨ������Ԫ�������ͺϽ��⻯��ķֽ��¶ȣ�ͬʱ���ֽϸߵ����� ��[5-6]��4) �뵥�ʡ���������л�����ɸ�����ϵ���Ը������������ѧ������ѧ����[7-9]��
�����꣬���û�е��ĥ�����кϽ���渴����Ա���Ϊ��һ�ָ���þ������Ͻ����ܵ���Ч������OELERICH��[10]��MgH2��TiO2��V2O5��������һ�������ĥ����ָ���봿������ṹ������ȣ�һЩ�������ӿ�Ͻ�����ʱ�Ĵ����ã��ر�������0.2%Cr2O3(Ħ������)ʱ����0.84 MPa��300 ��������£��Ͻ�ķ�������2 min�ڼ��ɴﵽ6.7%��SAKIN- TUNA��[11]ָ����Ԫ�ػ�ʹ�⻯��ķֽ��¶Ƚ���50~150 �棬������ѭ�����������ӣ������ʧ��Ԫ�ط��������ӺϽ�Ĵ������⣬�����ѵ���һ��������ֹ�����������������á���������������V2O5��Cr2O3�ȣ��������MgH2�Ķ���ѧ���ܣ�������ߵ����ºϽ��γ��⻯������ܡ���Щ�������������������ĥ����þ�ı�����������ȱ������ʹ��ԭ��ͨ�������⣬Cr2O3�ɼӿ����ⷴӦ�Ľ��У���V2O5��Fe3O4���ܴٽ����⣬TiO2Ҳ�����þ�⻯�����ܣ���ӿ��ٶȣ������¶ȣ���ֹ�����ȣ���Ϊ������ϵĽ�һ���о��춨�˻�����
VIJAY��[12]�û�е��ĥ���Ʊ���Mg-x% Cr2O3(xΪ����������x=5, 10, 15, 20)���״�����ϣ�����100��200��300 ����¶��½�������Ӧ�����ܲ��ԡ������ʾ����200 ���300 �桢3 MPa��ʵ�������£���Cr2O3�ĺ���Ϊ5%ʱ�����ϲ��ϴ������ﵽ���ֵ���ֱ�Ϊ5.67%��6.01%����100 ��ʱ�������������Ǻ���15% Cr2O3�ĺϽ���ֵΪ3.80%����ͬ�����¶ȷ�Χ��0.1 MPa�½��з���ʵ��ʱ����Cr2O3�ĺ�����5%���ӵ�15%ʱ������Cr2O3����������ͬ�¶��µķ������������ӵ����ƣ��������Ҳ�ɴﵽ���ֵ��Ϊ4.02%������Cr2O3�ĺ�����15%���ӵ�20%ʱ���Ͻ�ķ������ֻ���١���ˣ�Cr2O3��Mg���������ܾ��нϴ�Ĵ����ã�������������ܵ�Ӱ�첻�Ǻܴ�
�������о���һ��ѡ�õĶ���Mg��Mg2Ni�������塣�ڴˣ���������ͨ����е��ĥ���Ʊ�Mg2Cu�Ͻ�ͨ��XRD����ȷ������ȫ�γɺ��Դ�Ϊ������������Ϊ5%�ĵ��ʻ���������ԺϽ���б��渴����ĥ���������о��Ͻ��ڲ�ͬ�¶��µĴ������ܣ��Ա�Ϊ����Ͻ��һ���ķ�չ�ṩ�ο���
1 ʵ��
�����Ȳ�����99%��Mg��Cu��ĩ�����ʵ�����2?1����Ϻ����ڲ���ֹ��ڣ�Ȼ��װ��¹�FRITSCH��˾������Pulverisett-5����ĥ���У�����������½�����ĥ����ĥ��ת��Ϊ600 r/min������������Ϊ20?1������ĥ������ÿ��2 hȡ�������Ͻ��ĩ����XRD�������Լ��Mg2Cu���γɹ��̲�ȷ������ȫ�γɡ����Ʊ��õ�Mg2Cu����Ͻ���ϴ���ڳ���������ܷ���б��á���������觹��ж�Mg2Cu+5%M(M=C, Co, Ni, Cu, Cr2O3, Fe3O4, TiO2, V2O5)���б��渴����ĥ��������ĥ������Ϊ�������ĥ��ת��Ϊ600 r/min�� ���ϱ�Ϊ10?1�� ��ĥʱ��Ϊ1 h��
�����ò��ϵ�����ṹ������Rigaku D/max2500PC X�����������Ͻ��С���ʵ���������£�Cu K�����䣬ʯī��ɫ����������ѹΪ40 kV����������Ϊ150 mA����Ǿ���Ϊ0.02?��ɨ���ٶ�Ϊ4.00 (?)/min��ɨ�跶ΧΪ20?~120?��
�Ͻ���������������Ĵ���ѧ���Ƶ�p��c��T�������Ͻ��в��ԡ���������Ϊ99.999%����ʼ��ѹΪ3 MPa������ÿ���Ͻ�������200��300��400 �� 3���¶��µ������ѧ���ߺͷ���p��c��T���ߡ�
2 ��������
ͼ1��ʾΪMg��Cu��Ϸ�ĩ��2~8 h��ĥ���XRD�ס����Կ�������ĥ2 h��(��ͼ1(a))����ĩ�������ɵ���Mg��Cu���ɣ�Mg2Cu�������ǿ�Ⱥ�����˵��ֻ�Ǻ��ٵ�һ�����γ���Mg2Cu�ࡣ��ĥ4 hʱ(��ͼ1(b))��������Mg��Cu�⣬Mg2Cu�������������࣬��ǿ��Ҳ�������� ����6 h��ĥ��(��ͼ1(c))��Cu���������Ŀ�����Լ��٣�Mg����

ͼ1 ��е��ĥ���Ʊ���Mg2Cu��XRD��
Fig.1 XRD patterns of Mg2Cu prepared by mechanical grinding: (a) 2 h; (b) 4 h; (c) 6 h; (d) 8 h
�����ȫ��ʧ����ʱMg2Cu����������۴������ϻ��Ǵ�ǿ�����������������������������ĥ8 h��(��ͼ1(d))������ΪMg��Cu��ĩ����ȫ�ϳ�ΪMg2Cu��������ĥʱ����ӳ����Ͻ�������������˵����ĩ������ϸ��������[13]��Ϊ��������ĥ���Ʊ�Mg-Cu��Ԫ�Ͻ�ʱ�����ȷ�������Mg��Cu�еĹ��ܣ�����γɹ���������������࣬������Cuԭ�Ӿ�����䣬�Ӷ���������ԭ���ںϽ��е���ɢ��
ͼ2��ʾΪ��е��ĥMg2Cu�Ͻ���400 ����������XRD�ף��ɼ��úϽ���������Mg2Cu��MgCu2��MgH2��3�����ࡣһ����˵��Mg��Cu�ܹ��γ�2�ֽ����仯����Mg2Cu��MgCu2������Mg2CuΪ�����࣬��300 �桢2 MPa�������±��ܹ����⣬��MgCu2�����������������Ӧ[14]���ڱ���ʵ���У���Mg2Cu��400 �������ⷢ����Ӧʱ����������MgH2��MgCu2���䷴ӦʽΪ��2Mg2Cu+3H2![]() 3MgH2+MgCu2���������ڷ�Ӧ����ȫ�������IJ�������������������Mg2Cu��
3MgH2+MgCu2���������ڷ�Ӧ����ȫ�������IJ�������������������Mg2Cu��
���ܣ�6ͼ3��ʾΪ���渴����ĥ������Mg2Cu+5%M (M=C, Co, Ni, Cu)ϵ�кϽ��ڲ�ͬ�¶��µ������ѧ���ߺͷ���p��c��T���ߡ�����ͼ3(a)��(b)��(c)
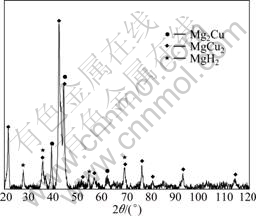
ͼ2 ��е��ĥ���Ʊ���Mg2Cu��400 ��������XRD��
Fig.2 XRD pattern of Mg2Cu prepared by mechanical grinding after absorbing hydrogen at 400 ��
�DZ��渴����ĥ�����Ͻ�ֱ���200��300��400 ���µ������ѧ���ߣ�ͼ3(d)��(e)��(f)���ڶ�Ӧ�¶��µķ���p��c��T���ߡ���1����Ϊ��ϵ�кϽ�����������ܵIJ��Խ����
����ͼ3�ͱ�1��ʵ������֪����200 ��ʱ������C��Co��Ni���б��渴�ദ����Mg2Cu����������Ӧ������Mg2Cu+5%C��������ʱ����̣�������Cu�ĺϽ��������������ڴ��¶�������
��1 Mg2Cu+5%M(M =C, Co, Ni, Cu)����Ͻ���渴����ĥ�����������������
Table 1 Absorption/desorption properties of Mg2Cu+5%M(M=C, Co, Ni, Cu) synthesized by multi-phase surface modification of ball milling at different temperatures
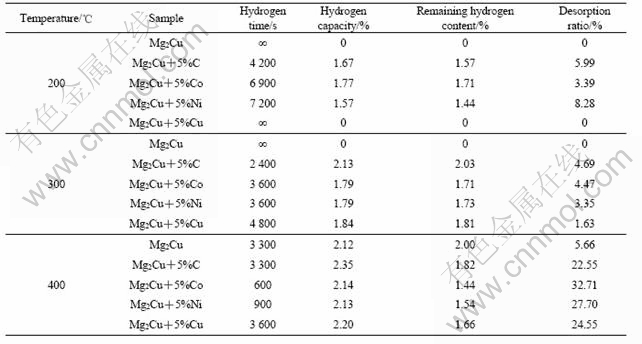
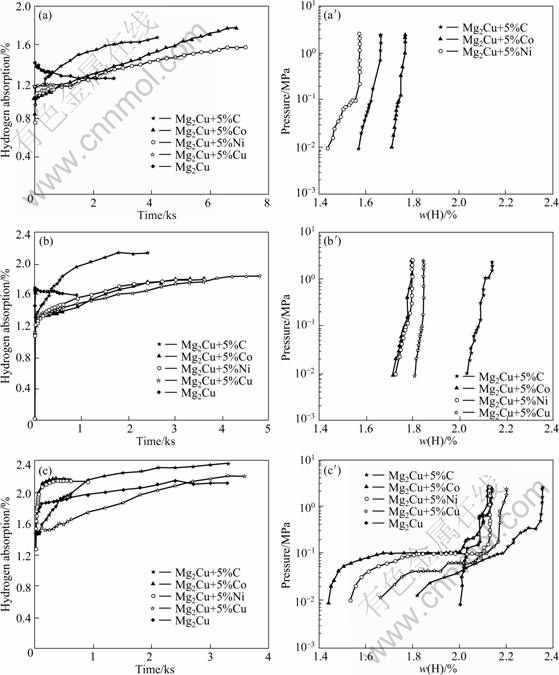
ͼ3 ���渴����ĥ������Mg2Cu+5%M(M=C, Co, Ni, Cu)ϵ�д���Ͻ��ڲ�ͬ�¶��µ������ѧ���ߺͷ���p��c��T����
Fig.3 Hydrogen absorption kinetic curves and desorption p��c��T curves of Mg2Cu+5%M(M=C, Co, Ni, Cu) synthesized by multi-phase surface modification of ball milling at different temperatures: (a), (a��) 200 ��; (b), (b��) 300 ��; (c), (c��) 400 ��
�Ͻ����������ѣ���Mg2Cu+5%Ni�з��⼣���������¶���300 ��ʱ��Mg2Cu+5%M(M=C, Co, Ni, Cu)����������������Ӧ��������ʱ���200 ��ʱ���̣�������Ҳ������������C�ԺϽ������ܵĸ�����Ϊ���ԡ������ӵ��ʵĺϽ����С����¶�(200~300 ��)�·����Ժ����ѡ����¶�������400 ��ʱ���������кϽ�����ֳ��ϺõĴ������ܣ��������ﵽ���ͬʱ�����Եķ�������������������̼�ĺϽ��ڸ�ϵ�кϽ��о�����ߵ������������ﵽ2.35%��
ֵ��ע����ǣ�δ�����渴����ĥ������Mg2Cu�Ͻ���200 ���300 ����С����¶��¾������⣬400 ��ʱMg2Cu����������Ϊ2.12%��ͬʱ�Ͻ��ڸ��¶��·����ʽ�Ϊ5.66%���ҷ���ƽ̨��խ������Ϊ���������⡣���������渴����ĥ������Mg2Cu�Ĵ������ܵõ��˽����Եĸ��ƣ����������¶ȵ����ߣ����������������ʲ���������ƽ̨������������200 ���300 ��ʱ������̼�ĺϽ������Խϸߣ�����Ϊ����������Ӧ������ʱ��϶̣������������������ӡ�400 ��ʱ��Co��Ni����ߺϽ�ı�����������Ե�Ч������Ч�������˺Ͻ������ʱ�䣬����˷����ʣ�Ҳ��һ���̶�������˺Ͻ����������
�ɴ˿ɼ�����Mg2Cu��������C��Co��Ni��Cu�ı��渴����ĥ���ܹ���һ���̶��ϸ��ƺϽ�Ĵ������ܡ�
ͼ4��ʾΪMg2Cu�зֱ�����5%��Cr2O3��Fe3O4��TiO2��V2O5��������ĥ��������200��300��400 ���µ������ѧ���ߺͷ���p��c��T���ߡ���2����Ϊ��ϵ�кϽ��ڶ�Ӧ�¶��µĴ������ܡ�
��ͼ4�ͱ�2��֪����200 ��ʱ��������Cr2O3��Fe3O4�ĺϽ��⣬����Ͻ�δ����������������Ӧ��ͬʱ�ڸ��¶��£����кϽ�ķ���p��c��T�����Ͼ�û�����Եķ���ƽ̨�������⼣����300 ��ʱ���Ͻ��������������200 ��ʱ�����ƣ������������������¶�������400 ��ʱ�����кϽ�����������ﵽ�������ʱ��Ҳ��̣�ͬʱ��Mg2Cu�⣬����������ĺϽ�������Եķ��������ڷ���p��c��T�����Ͽ��Թ۲쵽�Ͽ��ķ���ƽ̨(��ͼ4(c��))��˵�������������Mg2Cu���и�����ĥ�����Ͻ�Ĵ������ܵõ��˸��ơ�
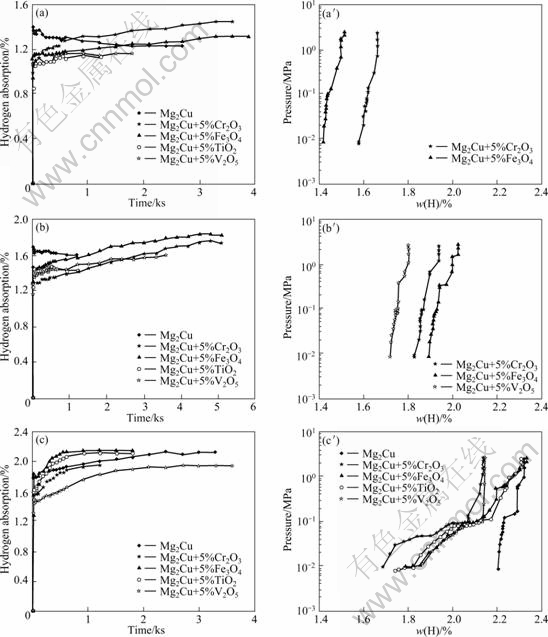
ͼ4 ���渴����ĥ������Mg2Cu+5%M(M=Cr2O3, Fe3O4, TiO2, V2O5)ϵ�д���Ͻ��ڲ�ͬ�¶��µ������ѧ���ߺͷ��� p��c��T����
Fig.4 Hydrogen absorption kinetic curves and desorption p��c��T curves of Mg2Cu+5%M(M=Cr2O3, Fe3O4, TiO2, V2O5) synthesized by multi-phase surface modification of ball milling at different temperatures: (a), (a��) 200 ��; (b), (b��) 300 ��; (c), (c��) 400 ��
��2 Mg2Cu+5%M(M=Cr2O3, Fe3O4, TiO2, V2O5)ϵ�д���Ͻ���渴����ĥ�����������������
Table 2 Absorption/desorption properties of Mg2Cu+5%M(M=Cr2O3, Fe3O4, TiO2, V2O5) synthesized by multi-phase surface modification of ball milling at different temperatures
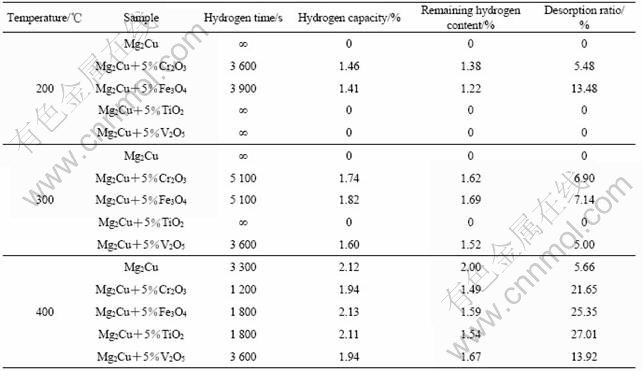
�ԱȺϽ�Ĵ������ܿ��Է��֣���200��300 ��ʱ������Fe3O4�ĺϽ������Խϸߣ�����������Ӧ������ʱ��϶̣��������ϸߣ�������Ҳ�ϴ���400 ��ʱ���кϽ���н����Եķ������������˵������TiO2��Fe3O4�ĺϽ���нϸߵ����������ܡ�
3 ����
��������ʵ�����������֪�����û�е��ĥ���Ʊ���Mg2Cu����Ͻ�û�����õĴ������ܣ�ֻ��400 ��ĸ����²������⣬������ʱ��ϳ����������ͷ����ʶ��ϵͣ����е��¶��� (200��300 ��)����������������ơ��������벻ͬ����������б��渴����ĥ���䴢�����ܵõ��˲�ͬ�̶ȵĸ��ơ�
���ȣ���Mg-Ni������C���и�����ĥ������������Ӳ�Ƚϴ�þ������Ӳ�Ƚ�С��̼�����Ĵ��Խϴ�ʹ�ø���������ĥ�����е��Գ����ĥ[15]���Ӷ�����Ͻ��������Ӵ��ı����������ʵ�����������̼���и�����ĥ�Ͻ��������ͷ����ʾ�����Mg2Cu�����������۶ϡ�
�ܿ��Խ��ͺϽ�������������еľ�������[16]���Ӷ����ƺϽ�ľ�������仯����˾��кܸߵĴ����ԡ�������������ĥ�����е���ĥ�������⣬���д��������ã��Ͻ�����ʱ��������������������Ϊ��ԭ�ӣ�������þ�������MgH2���Ӷ��������⻯��Ӧ�Ļ�ܣ�Ҳ�����ڸ��ƺϽ�Ĵ�������[17]����Ҳ�Ǽ���Co��Ni���и�����ĥ�Ͻ������ʱ�����̣����������ӵ���Ҫԭ��
SEDER��[18]�ڶ�Mg2Cu���澭XPS��AES�����������Mg2Cu�����þ����������ʹͭ�Խ���̬����ʽ�����ڱ��棬��������ӵĻ�ѧ���룬����˷�Ӧ�ٶȡ���ʵ��Ҳ�������Ͻ�������ͭ��Mg2Cu�Ͻ��������¶Ƚ��͡���������ߡ�ֻ��������C��Ni��Co�ĺϽ�������ȣ����������ķ�����Խ�С��
KANDAVEL��RAMAPRABHU [17]��Ϊ������Ͻ�������������侧��������Ͻ�����ԭ�������Ԫ��֮��ĵ��ת�Ƶ����ص�Ӱ�졣�������������и�����ĥ��������ߺϽ��������֮��ĵ��ӽ�����Ӧ���ӿ���-�̷�Ӧ�Ľ��У��Ӷ����ƺϽ�Ĵ������ܡ�ͨ������¶��̬�Ĺ���������Ĵ��������ڵ�һ��̬��[19]����Ȼ���пɱ仯�ϼ۵IJ�ͬ�����������þ������Ͻ�ľ���Ӱ�첻ͬ������Ч�����DZȽ����Ե�[20]��������Mg2Cu�Ͻ���������������б��渴����ĥ�Ľ��������Fe3O4��Cr2O3���ƺϽ����ܵ����ý����ԡ�
�ۺ������о���������ӵ��������н���Ԫ�ؾ��пɱ�Ķ��̬����̬�Ľ������ӵõ���ԭ���ṩ��һ�����ӿɱ���ԭ�ɵͼ�̬�������ں��ߵIJ��ȶ����ֿ����������ɸ�̬�Ľ������ӣ���㹹����һ�ֶ�̬ƽ�⣬�����ڽ����������֮�����ݵ��ӵ����ã������Ч�ظ����˺Ͻ�Ĵ������ܡ�
4 ����
1) ���û�е��ĥ���Ʊ�Mg2Cu����Ͻ�Mg��Cu���ʷ�ĩ�ڲ���ֹ�����ĥ8 h����ȫ�γ�������Mg2Cu��Mg2Cu��200 ���300 ���µĴ������ܲ��ѣ�400 ��ʱ������Ч���⣬������ʱ�䳤������Ч���ϲ
2) �������Ӳ�ͬ���ʻ��������Mg2Cu���и�����ĥ�����Ͻ�Ĵ������ܵõ����ơ���200 ���300 ���£�����C��Fe3O4�ĺϽ���Խϸߣ�����������Ӧ������ʱ��϶̣�����������������Ч���Ϻã���400 ��ʱ������Co��Ni��TiO2��Fe3O4���ƺϽ�������ܵ����ý����ԡ�
REFERENCES
[1] ����ӱ, ����ѧ, ����, ����Ӫ, ����. ��ĥʱ���þ̼���ϴ�����Ͻṹ�����ܵ�Ӱ��[J]. ���ܲ���, 2008, 39(3): 424-425.
HU Xiu-ying, ZHOU Shi-xue, WANG Zhen-hua, MA Huai-ying, LEI Gui-qin. Effect of ball milling time on the structure and properties of Mg-C composites for hydrogen storage [J]. Functional Materials, 2008, 39(3): 424-425.
[2] �� ��, �� ��. ������������ϵ��о���չ[J]. �й����Ͻ�չ, 2009, 28(5): 2-10.
CHEN Jun, ZHU Min. Progress in research of hydrogen storage materials with high capacity[J]. Materials China, 2009, 28(5): 2-10.
[3] ������, �� �D, VARIN R A, ������, ����, ������. ��ĥ��ʽ������Mg2FeH6������Ϻϳ���������ܵ�Ӱ��[J].�й���ɫ����ѧ��, 2008, 18(1): 42-47.
LI Song-lin, LIU Yi, VARIN R A, LIU Huai-fei, CUI Jian-min, CHEN Shi-qi. Effect of ball milling methods on synthesis and desorption properties of nanocrystalline Mg2FeH6 hydrogen storage materials [J]. The Chinese Journal of Nonferrous Metals, 2008, 18(1): 42-47.
[4] ����ΰ, ������, ����. La-Mg-Niϵ����Ͻ���о���չ[J]. �������ܲ���, 2009, 16(2): 46-50.
WANG Li-wei, JIN Zi-li, ZHANG Yang-huan. Recent research on La-Mg-Ni system hydrogen storage alloys[J]. Metallic Functional Materials, 2009, 16(2): 46-50.
[5] Ǯ����, �ƹ�ǿ, �� ��. Mg-Niϵ����Ͻ�ĸ���[J]. ϡ�н���, 2008, 32(1): 107-114.
QIAN Xiao-jing, HUANG Guo-qiang, LIN Bo. Improvement on Mg-Ni-based hydrogen storage alloy[J]. Chinese Journal of Rare Metals, 2008, 32(1): 107-114.
[6] YOO J H, SHIM G, YOON J S, CHO S W. Effects of substituting Al for Cr in the Ti0.32Cr0.43V0.25 alloy on its microstructure and hydrogen storage properties[J]. International Journal Of Hydrogen Energy, 2009, 34: 1463-1467.
[7] �ܵ���, ����ˮ, ¬Զ־, �ų���. þ��������ϵ�����������[J]. ��е���̲���, 2008, 32(4): 5-9.
ZHOU Dian-wu, LIU Jin-shui, LU Yuan-zhi, ZHANG Chu-hui. Hydriding and dehydrogenating properties of magnesium-based hydrogen storage materials[J]. Materials for Mechanical Engineering, 2008, 32(4): 5-9.
[8] �� ��, Ԭ����, ���־�, �� ǿ. Mg0.9M0.1Ni(M=Cr, Al, Ti, Zr)��Ԫþ������Ͻ���Ʊ�����绯ѧ���ܵ��о�[J]. �Ͽ���ѧѧ��, 2005, 38(2): 74-79.
FENG Yan, YUAN Hua-tang, QIAO Lin-jun, LIU Qiang. Preparation and electrochemical characteristics of Mg0.9M0.1Ni(M=Cr��Al��Ti��Zr)[J]. Acta Scientiarum Naturalium Universitatis Nankaiensis, 2005, 38(2): 74-79.
[9] �����, ���и�, �Ʋ���. Mg-Ni������Ͻ���о���չ[J]. ���ϵ���, 2003, 17(12): 9-11.
XU Yi-jun, TANG You-gen, HUANG Bo-yun. The research of Mg-Ni based hydrogen storage materials[J]. Materials Review, 2003, 17(12): 9-11.
[10] OELERICH W, KKASSEN T, BORMANN R. Metal oxides as catalysts for improved hydrogen sorption in nanocrystalline Mg-based materials [J]. Journal of Alloys and Compounds, 2001, 315(1/2): 237-242.
[11] SAKINTUNA B, LAMARI-DARKRIM F, HIRSCHER M. Metal hydride materials for solid hydrogen storage: A review[J]. International Journal of Hydrogen Energy, 2007, 32: 1121-1140.
[12] VIJAY R, SUNDARESAN R, MAIYA M P, SRINIVASA MURTHY S. Hydrogen storage properties of Mg-Cr2O3 nanocomposites: The role of catalyst distribution and grain size[J]. Journal of Alloys and Compounds, 2006, 424: 289-293.
[13] ������, ������, ��ѧ��, ���춫. ��ĥ���Ʊ�Mg-Cu�Ǿ�̬�Ͻ��ĩ[J]. ��ĩұ����, 2005, 23(1): 36-39.
WANG Xiao-jun, WANG Xiao-li, CHEN Xue-ding, XIA Tian-dong. On Mg-Cu amorphous alloy powders produced by ball milling[J]. Powder Metallurgy Technology, 2005, 23(1): 36-39.
[14] REILLY J J, WISWALL R H Jr. Reaction of hydrogen with alloys of magnesium and nickel and the formation of Mg2NiH4 [J]. Inorg Chem, 1968, 7(11): 2254-2256.
[15] �����, ����ѧ, ����, ��Ӣ��. ����þ̼���ϴ���������ܵ�Ӱ��[J]. ��ұ����, 2008, 28(4): 105-107.
WU Jun-qing, ZHOU Shi-xue, WANG Zhen-hua, L? Ying-hai. Effect of Ni on properties of Mg/C composites for hydrogen storage[J]. Mining and Metallurgical Engineering, 2008, 28(4): 105-107.
[16] PAN H G. Studies on the electrochemical properties of MlNi4.3-xCoxAl0.7 hydride alloy electrodes[J]. Journal of Alloys and Compounds, 1999, 648: 293-295.
[17] KANDAVEL M, RAMAPRABHU S. Correlation between hydrogen storage properties and amount of alloy particles in Mg-based composites [J]. Journal of Alloys and Compounds, 2007, 438: 285-292.
[18] SEILER A, SCHLAPBACH L, von WALDKIRCH T, SHALTIEL D, STUCKI F. Surface analysis of Mg2Ni-Mg, Mg2Ni and Mg2Cu[J]. Less-Common Met, 1980, 73 (1): 193-199.
[19] �� ��, �� �, ���Ʒ�, ����Ȫ. ������þ��������ϴ�������Ӱ����о���չ[J]. ���ϵ���, 2008, 22(11): 115-119.
CAI Hao, GU Hao, ZHU Yun-feng, LI Li-quan. Research progress in the influence of catalysts on hydrogen storage property of magnesium-based hydrogen storage materials[J]. Materials Review, 2008, 22(11): 115-119.
[20] OELERICH W, KIASSEN T, BORMANN R. Metal oxides as catalysts for improved hydrogen sorption in nanocrystalline Mg-based materials[J]. Journal of Alloys Compounds, 2001, 315(1/2): 237-242.
������Ŀ����������Ȼ��ѧ����������Ŀ(CSTC 2006BB4197)�������ѧ���������豸���Ż���������Ŀ
�ո����ڣ�2009-11-15�������ڣ�2010-02-20
ͨ�����ߣ����������ڣ���ʿ���绰: 13996300268������: 023-65127306�� E-mail: chenyuan@cqu.edu.cn


