������La9.33Si6O26/Ce0.85Bi0.15O1.925
�����ӵ�������Ʊ����䵼������
�ܺ��Σ��� �裬��־��
(���ϴ�ѧ ���Ͽ�ѧ�빤��ѧԺ������ ��ɳ��410083)
ժ Ҫ��
ժ Ҫ�����Ծ���ϩ��Ϊ�ۺϼ��Ŀռ����ϳɷ��빲�����������Ʊ�85% La9.33Si6O26-15% Ce0.85Bi0.15O1.925�����������ӵ����塣ͨ��X�������䷽����������������ɺ;����ߴ磬���ý����迹�����о����ϵ������ӵ����ԡ��о�������������úϳɷ������Ʊ�La9.33Si6O26 ��Ce0.85Bi0.15O1.925�����������ϲ��ϣ������Ϸ����ƽ�������ߴ�Ϊ35 nm���������ս������ϵ�ƽ�������ߴ�Ϊ70 nm��ͨ�������ϼ�����������߲��ϵ������ӵ����ԣ���600 ��ʱ�������ϲ��ϵ������ӵ����Աȴ�La9.33Si6O26�ĵ��������2��������������
�ؼ��ʣ�
La9.33Si6O26�մ��������ӵ������������ϲ��������������ϳ���
��ͼ����ţ�TB33 ���ױ�ʶ�룺A ���±�ţ�1672-7207(2009)05-1265-05
Preparation and conductivity of nano-composite
La9.33Si6O26/Ce0.85Bi0.15O1.925 oxygen ionic conductor
ZHOU Hai-tao, ZHANG Hong, LI Zhi-cheng
(School of Materials Science and Engineering, Central South University, Changsha 410083, China)
Abstract: 85% La9.33Si6O26-15% Ce0.85Bi0.15O1.925 nano-composite oxygen-ionic conductors were fabricated by combining with the steric-entrapment-synthesis method polymerized by polyvinyl alcohol and the co-precipitation process. The phase component and grain size of the prepared samples were analyzed by X-ray diffractrometry, and the oxide-ionic conductivities were measured by AC impedance measurement. The results show that the nano-composite materials compose of La9.33Si6O26 and Ce0.85Bi0.15O1.925 were successfully obtained, the average grain size of the as-calcined powder is 35 nm and the one of as-sintered bulk is 70 nm. The oxide-ionic conductivity is enhanced obviously by nanocomposite technology. The conductivities of nanocomposite increase by two orders in magnitude compared to that of the pure La9.33Si6O26 ceramic at 600 ��.
Key words: La9.33Si6O26 ceramic; oxygen ionic conductor; nano-composite; conductivity; synthesis
�����Դ������ز��ϵ��о��뿪���ǵ�ǰ����ʮ�ֹ�ע����Ҫ����[1-4]��ȼ�ϵ��(FC)�ǿ�����������Դ����Ҫ;��֮һ������ʲ��ϵ����ʶ�FC���ۺ�������ؼ����ã���ˣ��Ե���ʲ��ϵ��о�����Գ�Ϊ��������о��ȵ㡣������ʯ�ṹ��La9.33Si6O26���������������ӵ����Ժͽϸߵ�����Ǩ����������Ϊ�����¹���������ȼ�ϵ����߿���DZ���ĵ���ʲ���[5]��La9.33Si6O26�ļ�϶��ԭ����������C�᷽���La1/O3ͨ������Ǩ�ƣ������ӵ����Գʸ�����������[6]�����������La9.33Si6O26�ྦྷ�մɵ絼�ʽ�һ����ߡ�
��20�����������ϼ������������ǵļ�����Ȥ��������ʵ�ֲ�ͬ�ɷ������׳߶��ϵij����Ч���ϣ���������ϵ�ʹ��Ҫ��[7]�������������ǶԸ������ӵ���������˴����о�����Sata��[8]���ֲ�״�������е����ʽṹ���ӵ�����ĵ���������������ߣ�Maier��[9]�����׳߶����ӵ��������������������������������ʵ���о���Ŀǰ��δ�����������ϼ����о�La9.33Si6O26�����ϵ�����ı�����ͬʱ������өʯ�ṹ��CeO2���մ������������¾��нϸߵ絼�ʣ��侧�����������������ж����������Ǩ�Ʒ���[10]����������������о����֣�Bi���ӵ�CeO2���б��������ӷ�ʽ���õ������ӵ�������[11]���ڴˣ����������ϼ����Ʊ�������Ce0.85Bi0.15O1.925��La9.33Si6O26�������ϲ��ϣ��о������ӵ����ԡ�
1 ʵ ��
�����Ծ���ϩ��(PVA)Ϊ�ۺϼ��Ŀռ����[12]�Ʊ��������ȡ���ɢ�Ժõ�La9.33Si6O26�������ӡ���La2O3 (����Ϊ99.9%)��������������õ���Һ�������뵽�����ȵ������������Ҵ���Һ�У�����һ������PVAˮ��Һ�����ڴ���������ϼ��Ƚ��裬ʹ����ȫ��Ͼ��ȣ����Ƚ���ֱ������Ϊֹ��������850 ������1 h�Ƶ�����La9.33Si6O26��ĩ��
ȡһ�������Ʊ���La9.33Si6O26���ۣ���ĥ���顢������ˮ�Ҵ�����ɢ��������ɢ30 min �õ���ɫ����Һ��Ȼ����60 �����ˮԡ�;��ҽ����£������������أ���������Һ�м��백ˮ��ȥ����ˮ�����ƻ����ϵ��pHֵ��8���ҡ���La9.33Si6O26��Ce0.85Bi0.15O1.925������Ϊ85?15����Ce0.85Bi0.15O1.925����ԭ����Ce(NO3)4��Bi(NO3)3 (����Ϊ99%)�����������Ce(NO3)4��Bi(NO3)3�Ļ��ˮ��Һ��Ȼ����������La9.33Si6O26����Һ�С��ڴ˹����У���25%�İ�ˮ���ƻ����ϵ��pHֵ��8���ҡ��������Һ�μ���Ϻ���ˮԡ���ºͽ���5 h��Ȼ�����³»�24 h����ϳ�������˻��յõ�dz��ɫ��ǰ���塣��ǰ�����ڿ�������750 ������1 h����La9.33Si6O26/ Ce0.85Bi0.15O1.925���Ϸ��塣
�����Ϸ���ѹ�Ƴ�ֱ�������Ϊ15 mm��3 mm������ԲƬ������1 500 ��/1 h�սᡣ����X��������(�ձ���ѧD/MAX 2500�ͣ�Cu K��Դ)�������� ��ɡ�
�ս������������Ⲣ������Ϳ�������缫����550 ��/30 min�̻������õ绯ѧ����վ (EG&G Princeton, Model 263A)������Ʒ�Ľ����迹������Ƶ�ʷ�ΧΪ10 mHz��100 kHz��
2 ���������
2.1 X�����������
ͼ1��ʾΪLa9.33Si6O26/Ce0.85Bi0.15O1.925���շ�����ս�����XRD�ס����Կ�������Ʒ��������JCPDS 49-0443����Ƭ��¼��La9.33Si6O26����ʯ�ͽṹXRD����ȫһ�¡�ͼ�м�ͷ��dz��ķ���ʯ�ṹ�������ǡ����CeO2өʯ�ṹ��������Ӧ����û�й۲쵽�������ʷ塣��˵�������պ��ս�����У�La9.33Si6O26��Ce0.85Bi0.15O1.925֮��û�з�����Ӧ���������ࡣ����Debye-Scherrer��ʽ����ͨ������Jade5+pdf2003�����ó�La9.33Si6O26/Ce0.85- Bi0.15O1.925���շ����ƽ�������ߴ�Ϊ35 nm���ս����ƽ�������ߴ�Ϊ70 nm���Ա�JCPDS 34-0394��¼��CeO2өʯ�ṹ��XRD���֣�ʵ���õ������λ��������ƫ������Jade5+pdf2003�������о���������ó�Ce0.85Bi0.15O1.925������a=0.544 25 nm���Դ��ڱ���CeO2������(0.541 13 nm)����������Bi3+���뵽CeO2�ľ����к�������ЧӦ����ġ�
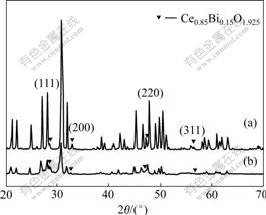
(a) �ս�������(b) ���շ���
ͼ1 La9.33Si6O26/Ce0.85Bi0.15O1.925���պ��սḴ�ϲ��ϵ�XRD��
Fig.1 XRD patterns of La9.33Si6O26/Ce0.85Bi0.15O1.925 composite materials
�������Ϸ�����֪��������PVAΪ�ۺϼ��Ŀռ����ϳɷ�������Ϲ����������Ʊ���La9.33Si6O26/ Ce0.85Bi0.15O1.925�������塣
�ڿռ����ϳɹ����У�����PVA�����еĴ����ǻ����Ի�������������γ����õĻ�ѧ������ʹ����������PVA�߷��������о������Ϸֲ��������������γɷ�ɢ���õķ��塣������ȷֽ�����γɵ�������ԭ�����ʹPVA�����ֽ⣬�ͷŴ���������������Ҳ���������ɷ�����γɡ������������ڻ�÷�ɢ�ԽϺõ���������ϡ�
�ڹ����������У�ʹ�ð�ˮ�����أ�������60 ��ɻ���ˮ�������������ˮ��Һ�����������OH-��Ce4+��Bi3+��OH-�����ֱ����Ce(OH)4��Bi(OH)3���������ڳ���������La9.33Si6O26������������Һ�н��У��Ǿ���ɺ˵�������Ҫ���ھ���ɺ˵�������[13]��La9.33Si6O26�������ӿ��ܳ�ΪCe(OH)4��Bi(OH)3���ӵijɺ˺��������ģ�Ce(OH)4��Bi(OH)3 ���Ӷ��������La9.33Si6O26���ӱ��棬ʹ�����պ��γɵ�Ce0.85Bi0.15O1.925����������La9.33Si6O26�������Ӿ��ȸ��ϡ�
��ͨ������£��մɲ������ս�����лᷢ������֮��Ļ�ѧ�ɷ����ɢ��Ǩ�ƣ�ʵ�־��������ᡢ����Ǩ�ƺ;�������La9.33Si6O26��Ce0.85Bi0.15O1.925�ֱ�����������ʯ�ṹ������өʯ�ṹ������ṹ���ͺ;����������ںܴ�IJ��졣���ս�����У����ߺ����γɹ����壻���⣬Ҫ�ƻ�2�����еĽṹ�������µ���ṹҲ��Ҫ���ĸ�������������ԣ����ս�����У�La9.33Si6O26/Ce0.85Bi0.15O1.925��������ϵ�е�2��������ֱܷ���ڶ����ᷢ�����Ե�����֮��ԭ����ɢ�뻯ѧ��Ӧ��ͬʱ��������La9.33Si6O26/ Ce0.85Bi0.15O1.925��������ϵ�У�Ce0.85Bi0.15O1.925��La9.33Si6O26�����������Χ�Ǿ�̬�κ��ָ����������ã����ԣ����ս�������ṩͬ����֮��ľ������ᡢ����Ļ�����Ժ��١���ˣ��ս����������������ԣ���Ȼ�����ž���ϸС�������ϲ���������
2.2 ��������
���ý����迹���Է����õ���Ʒ�����������и����¶ȵ���迹���ٸ�����ʽ�����������ͬ�¶��µ缫���ϵĵ絼�ʣ�

����lg ����103/T�ɻ�����ϵ絼�ʡ��¶ȵ�Arrhenius��ϵͼ�Σ���ͼ2��ʾ������LSO��ʾ��ʵ�����Ʊ��Ĵ�La9.33Si6O26��Ʒ��LSO/CBO��ʾLa9.33Si6O26/Ce0.85Bi0.15O1.925�������壬LSO-RΪ����[14]�����Ĵ�La9.33Si6O26���ϵĵ����ԡ�
�����Ͻ�����Կ����������������ĵ����Եõ��������ӡ��봿La9.33Si6O26��������ȣ����ϲ��ϵĵ絼����600 ��ʱ�����2��������������һ���棬ͨ��������������Ч������La9.33Si6O26����������ԶԲ��ϵ������ܵ�Ӱ�졣La9.33Si6O26Ϊ������ʯ�ṹ����ṹ����[SiO4]�����弰���϶��La3+����c���O2-����(��ͼ3��ʾ[15-16])������Si��O����Ϊ0.161 4 nm��O��Si��O�Ƕ�Ϊ109.4?�����е�ԭ��λ�Ʋ�������0.000 14~0.000 26 nm2֮�䡣��O3λ���ϵ����������⣬����λ�Ʋ����쳣��(0.000 53)����ռ��C�᷽���ϵ�ͨ������La��Χ���ɼ���϶������ֻ����C�᷽���ƶ����ྦྷ�մ��������ھ�����ȡ���������ԣ����ֵ���ĸ�������ʹ�������Ӵ�1������Ǩ����ȡ�����ϴ�����ھ���ʱ�ܵ�Լ���������ھ��紦��ʹ���ϱ��ֳ��ϵ͵ĵ絼�ʡ���өʯ�ṹ��Bi����CeO2����������λǨ�ƻ���ʵ�ֵ��磬������Ǩ�ƿ����ض����������С�������Ce0.85Bi0.15O1.925������2����ͬȡ���La9.33Si6O26���������˴��������ӵ����ã����������La9.33Si6O26�����ϵ������ӵ絼�ʡ�ͬʱ������XRD���������֪�����������ϵķ����Ʊ��ĸ��ϵ������ƽ�������ߴ�ֻ�� 70 nm�������ϲ��Ͼ��и߽����ܶ����ԣ��������ռ�ı����ܴ������������������ĸ߽����ܶȼ������ȱ�������ڽ�һ������La9.33Si6O26�����ϸ������Եĵ����ԣ�ʹ�ò��ϵĵ������ܼ�ǿ��
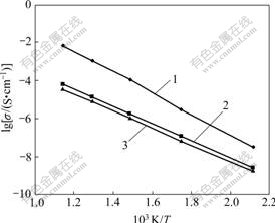
1��LSO/CBO; 2��LSO-R; 3��LSO
ͼ2 3�ֵ���ʲ��ϵĵ絼�ʡ��¶ȵ�Arrhenius��ϵ����
Fig.2 Arrhenius plots of conductivity��temperature of three kinds of electrolyte materials
���⣬���ϲ��Ͻ��洦���ڿռ���ЧӦҲ�����ڴٽ����ϵĵ����ԡ�ͼ3�б�dz���La9.33Si6O26��O3λ������ԭ�Ӻ������γɼ�϶�����ӣ�����O3ͨ����Ǩ��[2]��ȱ�ݻ�ѧʽ����Ϊ��
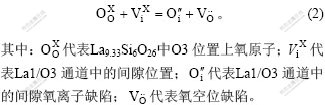
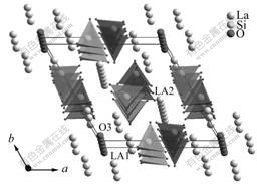
ͼ3 La9.33Si6O26����ṹʾ��ͼ
Fig.3 Sketch map of La9.33Si6O26 crystal structure
�������������Ce0.85Bi0.15O1.925���д��ڴ���������λȱ�ݣ�����������La9.33Si6O26��Ǩ�ƹ����ļ�϶�����ӣ�����O��i������洦����ƫ��������γ�![]() ����������ռ�����ʹ�ü�϶�����ӵ�Ǩ�Ƹ������ס�ͼ4��ʾΪ������渽������ȱ�ݷֲ�ʾ��ͼ��ͼ�У���ΪBi3+��������CeO2�е������ӿ�λŨ�ȣ���ֵ����Ce1-xBixO2-���еĦ�=x/2�ó�������Ϊ����洦�ľ��룬����Ϊ��ȱ��Ũ�ȣ�LSO��CBO�ֱ��ʾLa9.33Si6O26��Ce0.85Bi0.15O1.925���������洦�����ӵ�Ũ���������ӣ���������ӵ絼�ʡ����⣬�����ϲ��ϵĽṹЧӦҲ�Բ��ϵĵ������ؼ����á�2�ֲ�ͬ����������֮�䣬ԭ�ӵĶѶ����ɡ��ر�����ʯ�ṹ��La9.33Si6O26��өʯ�ṹ��Ce0.85Bi0.15O1.925����֮�䲻�����κξ���ṹ�������ԣ����������ȫ����������档����ھ����ڲ����ý��洦ԭ�ӵĶѻ��������ɣ��������ڷǾ�̬��ʽ������ԭ�Ӽ�������Ҳ��ͬ��ֱ�ӵ�����紦��������Ǩ�ƵĻ�ܽ��ͣ�����ʹ������������Ӱ����������˲�������ĵ絼�ʡ�
����������ռ�����ʹ�ü�϶�����ӵ�Ǩ�Ƹ������ס�ͼ4��ʾΪ������渽������ȱ�ݷֲ�ʾ��ͼ��ͼ�У���ΪBi3+��������CeO2�е������ӿ�λŨ�ȣ���ֵ����Ce1-xBixO2-���еĦ�=x/2�ó�������Ϊ����洦�ľ��룬����Ϊ��ȱ��Ũ�ȣ�LSO��CBO�ֱ��ʾLa9.33Si6O26��Ce0.85Bi0.15O1.925���������洦�����ӵ�Ũ���������ӣ���������ӵ絼�ʡ����⣬�����ϲ��ϵĽṹЧӦҲ�Բ��ϵĵ������ؼ����á�2�ֲ�ͬ����������֮�䣬ԭ�ӵĶѶ����ɡ��ر�����ʯ�ṹ��La9.33Si6O26��өʯ�ṹ��Ce0.85Bi0.15O1.925����֮�䲻�����κξ���ṹ�������ԣ����������ȫ����������档����ھ����ڲ����ý��洦ԭ�ӵĶѻ��������ɣ��������ڷǾ�̬��ʽ������ԭ�Ӽ�������Ҳ��ͬ��ֱ�ӵ�����紦��������Ǩ�ƵĻ�ܽ��ͣ�����ʹ������������Ӱ����������˲�������ĵ絼�ʡ�
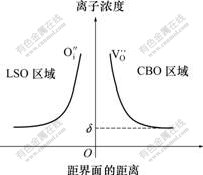
ͼ4 ���Ͻ���������ȱ�ݷֲ�ʾ��ͼ
Fig.4 Sketch map of oxygen-defect distribution near composite interface
3 �� ��
a. ���ռ����ϳɷ����빲�����ϳɷ����ϣ��Ʊ���ƽ�������ߴ�Ϊ35 nm��La9.33Si6O26/ Ce0.85Bi0.15O1.925�����Ϸ��塣
b. ���ս�����У�������ʯ�ṹ��La9.33Si6O26������өʯ�ṹ��Ce0.85Bi0.15O1.925֮��û�з�������֮������Ӧ�����˶Ծ����������Լ�����ã��Ӷ������ƽ�������ߴ�Ϊ70 nm��La9.33Si6O26/ Ce0.85Bi0.15O1.925�����������ӵ����塣
c. La9.33Si6O26�������ϲ��ϵ����ӵ������봿La9.33Si6O26�մɵ����ӵ絼�����������ߣ���600 ��ʱ���2��������������
d. �������ϵĸ߽����ܶȺ߽���ȱ���Լ������ṹLa9.33Si6O26����֮��������ߵ�����Ce0.85Bi0.15O1.925�Ĵ��ڣ���������������Ǩ�ƺ����La9.33Si6O26�����ϵ����ӵ������ܡ������ϼ�����������߲��ϵ����ӵ������ܡ�
�ο����ף�
[1] Weber A, Ivers-Tiff��e E. Materials and concepts for solid oxide fuel cells (SOFCs) in stationary and mobile applications[J]. J Power Sources, 2004, 127(1/2): 273-283.
[2] ZHANG Hong, WANG Jian, WANG Shenicun, et al. Conductivity investigations of cerium oxides doped by trivalent cations[J]. Trans Nonferrous Met Soc China, 2007, 17(1): S565-S569.
[3] �ռ���, ����, ���ǹ�, ��. ����ӵ����������LiNi0.3Co0.4Mn0.3O2���Ʊ�������[J]. ���ϴ�ѧѧ��: ��Ȼ��ѧ��, 2008, 39(1): 18-22.
SU Ji-tao, SU Yu-chang, LAI Zhi-guang, et al. Synthesis and properties of LiNi0.3Co0.4Mn0.3O2 cathode material for Li-ion batteries[J]. Journal of Central South University: Science and Technology, 2008, 19(1): 18-22.
[4] LIU Rong-hui, MA Wen-hui, WANG Hua, et al. Preparation and properties of Ce0.8Ca0.2O1.8 anode material by glycine-nitrate process[J]. Trans Nonferrous Met Soc China, 2007, 17(4): 874-879.
[5] Nakayama S, Kageyama T, Aono H, et al. Ionic conductivity of lanthanoid silicates, Ln10(SiO4)6O3(Ln = La, Nd, Sm, Gd, Dy, Y, Ho, Er and Yb)[J]. J Mater Chem, 1995, 5(2): 1801-1805.
[6] Julian R T, Saiful M, Peter R S. Defect chemistry and oxygen ion migration in the apatite-type materials La9.33Si6O26 and La8Sr2Si6O26[J]. J Mater Chem, 2003, 13(8): 1956-1961.
[7] Zhong C J, Maye M M. Core-shell assembled nanoparticles as catalysts[J]. Adv Mater, 2001, 13(19): 1507-1511.
[8] Sata N, Jin-Phillipp N Y, Eberl K, et al. Enhanced ionic conductivity and mesoscopic size effects in heterostructures of BaF2 and CaF2[J]. Solid State Ionics, 2002, 154/155(2): 497-502.
[9] Maier J. Ionic Transport in nano-sized systems[J]. Solid State Ionics, 2004, 175(1/4): 7-12.
[10] Mogens M, Nigel M, Sammes B, et al. Physical, chemical and electrochemical properties of pure and doped ceria[J]. Solid State Ionics, 2000, 129(1/4): 63-94.
[11] Li Z C, Zhang H, Bergman B. Synthesis and characterization of nanostructured Bi2O3-doped cerium oxides fabricated by PVA polymerization process[J]. Ceram Inter, 2008, 34(8): 1949-1953.
[12] Li Z C, Zhang H, Bergman B, et al. Synthesis and characterization of IT-electrolyte of La0.85Sr0.15Ga0.85Mg0.15O3-�� by steric entrapment synthesis method[J]. J Euro Ceram Soc, 2006, 26(12): 2357-2364.
[13] �ٽ���, �˻���, �� ά, ��. �Խ�������Ϊģ���Ʊ���-������������[J]. ��ѧ��չ, 2004, 16(3): 327-334.
GUAN Jian-guo, DENG Hui-yong, WANG Wei, et al. Preparation of well-defined core-shell nanocomposite particles based on colloidal templates[J]. Prog Chem, 2004, 16(3): 327-334.
[14] Panteix P J, Julien I, Bernache A D, et al. Synthesis and characterization of oxide ions conductors with the apatite structure for intermediate temperature SOFC[J]. Mater Chem Phys, 2006, 95(2/3): 313-320.
[15] Okudera H, Masubuchi Y, Kikkawa S, et al. Structure of oxide ion-conducting lanthanum oxyapatite, La9.33(SiO4)6O2[J]. Solid State Ionics, 2005, 176(15/16): 1473-1478.
[16] Zhang H, Li Z C, Bergman B, et al. Investigation of La9.33Si6O26 oxygen ionic conductor[J]. J Mater Sci Tech, 2007, 23(5): 629-632.
�ո����ڣ�2008-10-28�������ڣ�2008-12-29
������Ŀ����������ѧ�ع���Ա������������������Ŀ(2006331��20071108)����У��ʿ��ר����л���������Ŀ(20070533119)
ͨ�����ߣ���־��(1969-)���У�����ȫ���ˣ���ʿ�����ڣ����¹����մɲ����о����绰��0731-88877740��E-mail: zhchli@mail.csu.edu.cn
[9] Maier J. Ionic Transport in nano-sized systems[J]. Solid State Ionics, 2004, 175(1/4): 7-12.
" target="blank">[16] Zhang H, Li Z C, Bergman B, et al. Investigation of La9.33Si6O26 oxygen ionic conductor[J]. J Mater Sci Tech, 2007, 23(5): 629-632.


