���±�ţ�1004-0609(2009)03-0576-07
��ͬ�������������������ȶ�п���ཬ���ŵĸ�ʴ��Ϊ
�� ��1���Ŵ�ޱ1����۱�2��������1
(1. �����Ƽ���ѧ ��ʴ��������ģ����� 100083��
2. �Ϻ���ɽ�����о�Ժ ��������漼���о������Ϻ� 201900)
ժ Ҫ��
ͨ���ڲ�ͬ�����������ж������ȶ�п������ཬ�������飬����ɨ��羵��X���߹���������������ֶΣ��о��ڼ�ЪͨO2��ͨN2����������ö�п��ĸ�ʴ��Ϊ������������ڼ�ЪͨO2������£�п��ֱ���ʴ�������ڻ�������һЩ����ͺ����������п�����ĸ�ʴ��������Ų����ȵ���״����ڼ�ЪͨN2ʱ����п���п������������٣�������û�в������⣬��ʴ����ʴ��״���ڼ�ЪͨO2��ͨN2������£���п��ĸ�ʴ������������200 hʱ��ǰ�ߵĸ�ʴ������ʧ�����Ǻ��ߵ�2�����ң���п�帽�ſ�����ཬʱ�ĸ�ʴ��������ȥ�������̿��ơ�
�ؼ��ʣ�
�ȶ�п���������ཬ����������ʴ��Ϊ��
��ͼ����ţ�TG 172.4���� ���ױ�ʶ�룺A
Influence of content of oxygen on corrosion behavior of automotive hot-dip galvanized steel under alkaline mud adhesion
ZHANG Hong1, DU Cui-wei1, QI Hui-bin2, LI Xiao-gang1
(1. Corrosion and Protection Center, University of Science and Technology Beijing, Beijing 100083, China;
2. Institute of Welding and Surface Technology, Shanghai Baoshan Iron & Steel Group Corporation,
Shanghai 201900, China)
Abstract: In environments of different oxygen contents, the corrosion behaviors of hot-dip galvanized (HDG) steel sheet used in automobile under mud adhesion were investigated by scanning electronic microscopy, X-ray photoelectron spectroscopy and Raman spectroscopy. The results show that the zinc coating is eroded mostly, and some red rust and black rust appear on the substrate in the environment of oxygen supplied intermittently. The corrosion products on the galvanized steel sheet are needle-like objects. While in the environment of nitrogen supplied intermittently, a little area of the zinc coating is erode, and no red rust appears on the substrate. Corrosion products form on the blocks. With time prolongs, the corrosion rates of mass loss increase firstly whereas then decrease, and the corrosion rate of mass loss with oxygen supply is about two times greater than that with nitrogen supply under the mud adhesion up to 200 h. The corrosion processes of the galvanized steel sheet under alkaline mud adhesion are controlled by oxygen depolarization reactions.
Key words: hot-dip galvanized steel; alkaline mud; adhesion; corrosion behavior
����ȫ���������ö�п�������������������ֹ��ʴ�����;�����ʧ���ӳ������ķ�������������ʹ�ù���������п��ĸ�ʴ�о����ӹ�ע�����ܶԶ�п����NaCl��Һ��[1?2]����ˮ[3]�ʹ�����[4?6]�ĸ�ʴ��Ϊ����ҪӰ�����ؼ���ת�е�������ĸ�ʴ����[7]����������˴������о���ȡ���������о��ɹ���Ȼ�����ȶ�п���������ཬ��������µĸ�ʴ�о�����ȴ��չ�ý��١������������У����ڻ��������͵���λ�õȵ�Ӱ�죬�������ཬ����ѩ�εȵķɽ��ͳ���������������ʱ��ϴ�������һ���ĸ�ʴ����ˣ�����������п���ڽϸ�Cl?�������ཬ״̬�еĵ绯ѧ��ʴ��Ϊ��һ��ֵ��̽�ֵ����⡣�ҹ�����������Ϊ���������������������������ԵĿ���������ͳɵ��ཬΪ�������о�������յ���ԭΪ�ź��ף�Cl?������Խϴ��Һ�ɰ���ϴ����ԽϺã������ۺ�Ӱ�����أ����ཬ����һ���Ĵ����ԡ�
��п�帽���ཬ�Ժ�������ɢ��������������Ҫ����;��������������ɢ�ٶ�ȡ�����ཬ�ĺ�Ⱥ�ʪ�ȡ�����������������ɢ�����У�Ҫͨ����������������ëϸ��϶���γɵĵ��Һ�㼰��ʴ����㡣��Ũ�ȶԶ�п���ཬ���ŵĸ�ʴ״���кܴ��Ӱ�졣������п�����ཬ���ŵ�����£���Ũ�ȵIJ�ͬ������ĸ�ʴ������ò�ı仯��ʴ��Ϊ��������δ����ϸ�о��ı������������߲����ཬ���ŵ�ʵ�鷽�����Զ�п������Ũ�Ȳ�ͬ�Ļ����еĸ�ʴ��Ϊ�ͻ������г������о���
1 ʵ��
ʵ�����Ϊ������������˫���ȶƴ�Zn(GI)�����壬����0.7 mm����Zn����ƽ��Ϊ14 ��m������ΪIF�֡�����п�����и��3 cm��3 cm��������Ȼ������������ˮ����ͪ���ƾ���ϴ�������������ܷ⽺��������һ��ͺ�����ܷ⣬���á�
ʵ�����ཬ���ÿ�����������ƣ���ʵ�ʲ�õ���Ҫ�������ݼ���1����������Ȼ�����ĥ������С��850 ��m��Ȼ����105 ����6 h����������ȴ����ȥ����ˮ��������Ⱥͳ�ճ��״��������Һ���ཬ����ˮ��Ϊ15%(��������)��
��1 �������������Ҫ��������
Table 1 Main physical and chemical data of soil in Ku��erle city, China

�����Ƶ��ཬ���ȵ�ͿĨ���������棬���Ϊ8 mm���Ѹ����ཬ��������ֱ������ͬ�����л����������У��������Ϊ0.027 m3��ÿ�������ж�����3��ƽ��������ʵ��װ�ü�ͼ1���ڽ����ںͳ����ڶ�������£��ֱ��ЪͨO2��N2��������Ϊ60 mL/min��ÿ��22 hͨ��2 h��Ȼ�����ںͳ����ڶ���ա�ʵ���ڳ����½��С�
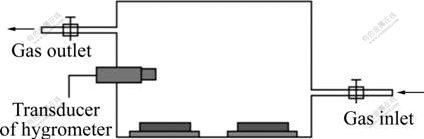
ͼ1 �ڼ�ЪͨO2��N2������¶�п�帽���ཬʾ��ͼ
Fig.1 Schematic diagram of mud adhesion on hot-dipping galvanized steel sheet under supplying O2 or N2 intermittently
ʵ�����48��100��150��200��250 h��ֱ�ȡ������ʵ���ཬ��������������������ȥ����ˮ��ϴ���پ���������ϴ�ɾ������ɣ����ཬ����250 h����������ĸ�ʴ�������������������SEM �۲�(��ѹΪ20 kV)�����Ը�ʴ�������XPS������Raman������
��ȡ����ĸ�����������ϴ��ȥ����ʴ��������������丯ʴ������ʧ���ʡ�
2 ʵ����
2.1 ��ʴ���п�����ĺ����ò
���л����������У��ֱ�ͨ��O2��N2���ڲ�ͬȡ��ʱ��õ���п������ཬ���Ÿ�ʴ��ĺ����Ƭ�������ͼ2��ʾ�����Կ�������ͨO2��N2�Ļ����У������ཬ�Ķ�п����涼���������ԵIJ����ȸ�ʴ���������������ߵĻ����У����港ʴ�����ء���ͨO2�Ļ�����(��һ��)����п����������ϴ�200 hʱ���ѿ�ʼ������������ͺ��⣻��ͨN2�Ļ�����(�ڶ���)����п������������С����250 hʱ����û�к���������ɼ���������Ũ�ȽϸߵĻ����У��ཬ�����µĶ�п�巢����ʴ�ij̶��뻷���������ĺ����кܴ��ϵ��

ͼ2 ��п�帽�ſ�����ཬʱ��ЪͨO2��N2������������ĺ����ò
Fig.2 Macro-photographs of galvanized steel sheet for different time interval of mud adhesion by supplying O2 ((a)?(e)) and N2 ((a��)?(e��)) intermittently: (a), (a��) 48 h; (b), (b��) 100 h; (c), (c��) 150 h; (d), (d��) 200 h; (e), (e��) 250 h
2.2 ��п����港ʴ���������ò
��ͨO2��N2������£�������ཬ���ŵĶ�п����港ʴ���������ò�кܴ���졣��ͨO2������£���п����港ʴ���������ò��ͼ3(a)��ʾ����ͼ�ɼ���п����港ʴ����ʲ����ȵ���״��ֲ�����ͨN2������£���ʴ����ʴ��״��������ɢ������������״���ͼ3(b)��ʾ��

ͼ3 ��ЪͨO2(a)��N2(b)��������ཬ����250 h��Ķ�п������ɫ��ʴ�����SEM��
Fig.3 SEM micrographs of corrosion products on samples with mud adhesion for 250 h under supplying O2 (a) and N2 (b) intermittently
��ȥ����ʴ����������ı���״��Ҳ���ںܴ�����ͨO2������£���ʴ����ѻ��ĵط����������Ļ��������γ��˺ܶ�ĸ�ʴ�ӣ��ܶȽϴ�ͼ4(a)�����ڼ�ЪͨN2������£�������ཬ����ʱ�Ķ�п���������Ȼ�оֲ�����Ķ�п���Ѿ����䡢���𣬵����廹û�в�����ʴ����ͼ4(b)��ʾ��

ͼ4 ��ЪͨO2(a)��N2(b)�����������������������ĸ�ʴ״��SEM��
Fig.4 SEM micrographs of surfaces of samples after cleaning corrosion products under supplying O2 (a) and N2 (b) intermittently
2.3 �ཬ�еĺ�ˮ�ʺͻ����е����ʪ�ȱ仯
�ڼ�ЪͨO2��N2������£���ͬȡ��ʱ������õ��ཬ�еĺ�ˮ����ͼ5��ʾ�����Կ�������������µ��ཬ��ˮ�ʶ����½������ڼ�ЪͨO2������µĺ�ˮ�ʱ��ڼ�ЪͨN2������µĺ�ˮ�ʽ��͵ÿ�һЩ��

ͼ5 �ڼ�ЪͨO2��N2����²�ͬȡ��ʱ���õ��ཬ�еĺ�ˮ��
Fig.5 Water contents of mud after different times under supplying O2 and N2 inter mittenly
ͬʱ���ڲ�ͬ��ȡ��ʱ�䣬�������м�ЪͨO2��N2�Ļ������������ʪ�ȵIJ����������ͼ6��ʾ����������µĻ������ʪ�ȶ����������ƣ����ڼ�ЪͨO2������µ������ٶ��Դ�һЩ��
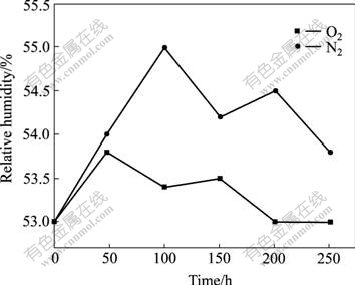
ͼ6 ��ͬȡ��ʱ���õĻ����е����ʪ��
Fig.6 Relative humidity of environment after different times
2.4 �ཬ����ʵ��������ĸ�ʴ����
�ڼ�ЪͨO2��N2������£��Բ�ͬʱ�������������ϴ�������������Եõ�������ཬ���Ų�ͬʱ���ĸ�ʴ������ʧ���ʣ������ͼ7��ʾ���������Կ������ڼ�ЪͨO2����µĸ�ʴ�������Դ��ڼ�ЪͨN2����µĸ�ʴ���ʣ���������µĸ�ʴ������200 h ���ﵽ���ֵ��ǰ��Ϊ���ߵ�2�����ҡ�

ͼ7 ��ЪͨO2��N2�����������ڿ�����ཬ����250 h���ƽ����ʴ������ʧ����
Fig.7 Average corrosion rates of mass loss of samples under supplying O2 and N2 intermittently
2.5 ��ʴ����ɷַ���
�ڼ�Ъͨ���Ļ����У�������ཬ��ʴ�����������ĸ�ʴ�������XPSȫ��ɨ������������ͼ��ʾ����ͼ8���Կ�������п���������ĸ�ʴ�����к���Zn��Fe��Cl��O��Ԫ�أ�п����2p3/2��2p1/2�����ܼ��壬��ѧλ��Ϊ22.97 eV��˵������ZnO[8]��������2p3/2��2p1/2�����ܼ��壬��ѧλ��Ϊ13.6 eV��˵������Fe2O3�����������ܼ���1sΪ531.0 eV��˵�����ܴ���Fe2O3��Fe3O4[9?10]���ȴ���2p3/2��2p1/2�����ܼ��壬��ѧλ��Ϊ1.60 eV��˵�����ڼ�ʽ�Ȼ���[11]��

ͼ8 ��Ъͨ���������ཬ����250 h��Ķ�п�����ĸ�ʴ����XPS��
Fig.8 XPS plot of corrosion products on surface of sample with mud adhering up to 250 h under supplying O2
�Զ�п�������ཬ���ź�����ĺ���ͺ������Raman���ײ����������ͼ9��ʾ����ͼ��֪������ͺ������Ҫ�ɷ�Ϊ����-FeOOH��Fe3O4�����⣬���Ц�-FeOOH����-Fe2O3�ͦ�-Fe2O3[12?13]��
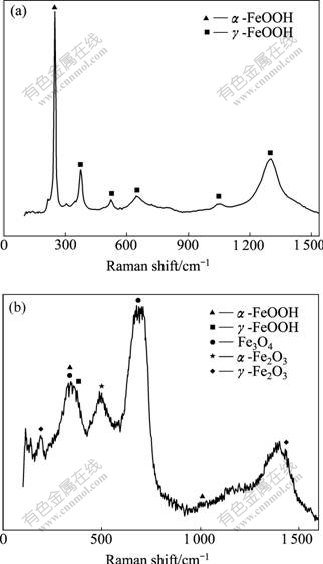
ͼ9 �ཬ����250 h��Ķ�п���������ĺ���ͺ����Raman��ͼ
Fig.9 Raman plots of red rust(a) and black rust(b) on samples with mud adhering 250 h under supplying O2
������ʵ�������Կ������ཬ���Ÿ�ʴ���ڱ��港ʴ�IJ������ԣ����Ҹ�ʴ���ʵĴ�С��Ҫ�ܻ����е�O2������Ӱ�졣
�ཬ�еĺ�ˮ���仯��Ҫ����Ϊ��ѧ��Ӧ�����ġ��������е���������ͨ��ʱ�����������һ���֡�����������£��ཬ�����ˮ��������������������ʧ��Ӧ��������ġ��ڼ�ЪͨO2����£��ཬ��ˮ����ʧ��Խϴ�������Ϊ��ѧ��Ӧ�ٶȽϿ죬���ڼ�ЪͨN2������£���ѧ��Ӧ�ٶȽ�����ˮ��������Խ�С�����⣬�����е����ʪ���ڼ�ЪͨO2�����������Խ�СҲ˵������һ�㡣
�ཬ���Ÿ�ʴ��һ�ֵ绯ѧ��ʴ����п���ڿ�����ཬ�е�����������Ҫ������ȥ�������á�ʵ�鿪ʼʱ�����������ڳ�ʪ���ཬ���������谭������Һ�и�ʴ�Ƚ����ƣ����Ż�������Ũ�ȵ�����ʴ�ٶ��������ڸ�ʴ���ڣ����ܻ�������Ũ��������(ͨO2)����С(ͨN2)���������ཬ��ˮ�����٣�����������ۻ������ӻ����ѳ��ֽϴ������⣬���ڸ�ʴ���η�Ӧ�������Ը�ʴ��������ճ���γɽ��ܲ㣬�����������á���ˣ�����ʱ����ӳ���ʹ��ʴ�����м�С�����ơ�
�������̰��������������裬���������������������ӻ���������Ӧ�����������������̱Ƚϸ��ӣ��ڶ���ṹ���ཬ�а�������Һ��Ķ�����������ɢ���ַ�ʽ�����ͨ��ëϸ��϶���γɵ����ʴ�����[14]��
��������ѧԭ�������ཬ�з��������缫��Ӧ����缫��λ����[15?16]��
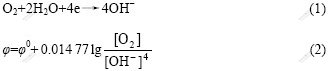
����ʽ�ɼ����ཬ�е��ܽ���Ũ��Խ�ߣ����缫��λ��Խ�����ཬ�ĸ�ʴ��Խǿ����һ������Ϊȥ�����������������̣���һ������Խ�Fe2+ ����ΪFe3+�����¸�ʴ���٣����ཬ�����㹻������Fe2+��Fe3+�����ٶȸ���Fe��Fe3+��
���⣬������ཬ�е�Cl?�����ϴԸ�ʴ�ٶȵ�Ӱ�첻�ɺ��ӡ�Cl?�Ǽ�ǿ�������������Cl?�����ھֲ��ۻ�Ĥʱ����ͨ���ֲ��ữ���ã��ƻ�������Χ�ĸ��Ի�����ʹ���������pHֵ���ͣ��Ӷ��ܽ�ۻ�Ĥ��Ȼ���ڳ����O2��H2O�������������п��ͻ���ľֲ���ʴ¶���Ľ���������Ϊ������������ۻ�Ĥ������Ϊ�������γɻ?�ۻ���ʴ��ء�ֻ�е�������Ӧ��������Ӧͬʱ�Ƚ���ʱ��������ʴ��Ӧ���ܽ��С�����ʴ��Ӧ���������������������ܵ��谭����û���ʱ��п�ĸ�ʴ��Ӧ�ͻ����[17]��
��ˣ��ڱ�ʵ���У�����������ʴ�ij�ʼ������ͬ�������ڻ�������Ũ�ȵIJ�ͬ���������������صı仯���Ը�ʴ�����нϴ��Ӱ�졣��ʴ�������ܱջ�������Ũ�ȡ��ཬ�еĺ�ˮ�ʺ�Cl?���ۺ����á�
��п���ڿ�����ཬ���Ÿ�ʴ�����У���п���ں���O2��H2O�Ļ����лᷢ����ʴ��ط�Ӧ���ڸ�ʴ�����У����ɵ�Zn2+��OH?�������Zn(OH)2�������ཬ�д��ڽ϶��Cl?����ʴ������һ����Ӧ����Zn5(OH)8Cl2��H2O���������ֻ��������ɵظ����� �Ʋ���棬��е�������ý�Ϊ���ޣ������ʴ���ܽ���̷���������У��Ʋ�����ʴ��Zn5(OH)8Cl2��H2O��ʴ����ij����ǵ��������������¶�п����ʴ���ܲ��ߵ�һ����Ҫԭ���ݱ�������õ��ཬ���������������й�����ȷ�ϣ�����״��ΪZn5(OH)8Cl2��H2O�����ڸ�ʴ����Ϊ�ᾧ���õļ�ʽ�Ȼ�п��������ܺܺõ���ֹ�Ʋ�Ľ�һ����ʴ[18?19]��
�ɴˣ����Ʋ��п���ڿ�����ཬ�еĸ�ʴ�������¡�

п�Ʋ㸯ʴ��һ���̶��Ժ��忪ʼ��ʴ����������ͺ��⡣
�ڼ�ЪͨO2����£������ڿ�����ཬ�������ȷ��������ܽ⣬����Fe2+�����ˮ�Ⲣ�ڸ��������ת��Ϊ��ɫ�����⣬���ij����������ཬ�д���Cl?��������ϵ����ɫ�����ں����Ļ�ѧ�����͵绯ѧ�����У�ת��Ϊ�����ķǾ��������Ħ�-FeOOH�Լ���-FeOOH������еĦ�-FeOOH�ɦ�-FeOOHת����������-FeOOHҲ�����ٽ�һ��ת��Ϊ��-FeOOH�����ڷǾ�̬��Fe�Ģ�ۺ͢��������ľ�������ת������е�Fe3O4��ͬʱ����-FeOOH�ͦ�-FeOOH����ͨ���绯ѧ�������̱���ԭΪFe3O4[20]��
��п��ͻ����������Ӧ��Ϊ��ȥ�������̣���ʴ��������ȥ�������ƣ�
![]()
4 ����
1) �����ö�п���ڿ�����ཬ���Ź����У������˲����ȸ�ʴ���ڲ�ͬ�������Ļ����У�п��ͻ���ĸ�ʴ�̶��кܴ�����𣬸�ʴ������ֲ�ͬ������ò��
2) �ڲ�ͬ�����������У���п�����ཬ���Ÿ�ʴ�µĸ�ʴ���ʶ��������������ƣ���п���ڼ�ЪͨO2�Ļ����еĸ�ʴ������ʧ���ʱȼ�ЪͨN2�ĸ�ʴ������ʧ���ʴ�ö࣬������200 hʱ��ʴ��������1�����ҡ�
3) �ڼ�ЪͨO2��N2������£���п�帽�ſ�����ཬ�ĸ�ʴ��������ȥ�������̿��ơ������е��������Զ�п���ཬ��ʴ��Ӱ��dz�������
[1] WORSLEY D A, MCMURRAY H N, SULLIVAN J H, Williams I P. Quantitative assessment of localized corrosion occurring on galvanized steel samples using the scanning vibrating electrode technique[J]. Corrosion, 2004, 60(5): 437?447.
[2] BARRANCO V, FELIU S, FELIU J S. EIS study of the corrosion behavior of zinc-based coatings on steel in quiescent 3% NaCl solution. Part 1: Directly exposed coatings[J]. Corrosion Science, 2004, 46(9): 2203?2220.
[3] �� ��, ���ٻ�, �� ��, κ����. �Ƚ��Ʋ����ൺվ�ĺ�ˮ��ʴ��Ϊ�Ա�(��)�����ɽ���[J]. �й���ɫ����ѧ��, 2007, 17(9): 1527?1535.
LI Yan, XING Shao-hua, LI Xin, WEI Xu-jun. Seawater corrosion behavior of hot dip coatings at Qingdao test station (��)����Splash zone[J]. The Chinese Journal of Nonferrous Metals, 2007, 17(9): 1527?1535.
[4] NEUFELD A K, COLE I S, BOND A M, FURMAN S A. The initiation mechanism of corrosion of zinc by sodium chloride particle deposition[J]. Corrosion Science, 2002, 44(6): 555?572.
[5] ODNEVALL W, LEYGRAF C. Atmospheric corrosion of zinc based materials: runoff rates, chemical speciation and eco~toxicity effects[J]. Corrosion Science, 2001, 43(5): 809?816.
[6] CHUNG S C, LIN A S. EXAFS study of atmospheric corrosion products on zinc at the stage[J]. Corrosion Science, 2000, 42(9): 1599?1610.
[7] COLOMBAN Ph, CHERIFI S, DESPERT G. Raman identification of corrosion products on automotive galvanized steel sheets[J]. Journal Raman Spectroscopy, 2008, 39(3): 881?886.
[8] WEI X Q, MAN B Y, LIU M, XUE C S, ZHUANG H Z, YANG C. Blue luminescent centers and microstructural evaluation by XPS and Raman in ZnO thin films annealed in vacuum, N2 and O2[J]. Physica B, 2007, 388(1/2): 145?152.
[9] ZHAGN X, SLOOF W G, HOVESTAD A, VAN WESTIGN E P M, TERRYN H, DE WIT J H W. Characterization of chromate conversion coatings on zinc using XPS and SKPFM[J]. Surface and Coatings Technology, 2005, 197(1): 168?176.
[10] ������. X���߹��������Ӧ�ý���[J]. ����ʱ��, 2006, 20(8): 54?56.
WEN Mei-lan. Introduction of x-ray photoelectron spectroscopy application[J]. Chemical Industry Times, 2006, 20(8): 54?56.
[11] ARAMAKI K. XPS and EPMA studies on self-healing mechanism of a protective film composed of hydrated cerium(��) oxide and sodium phosphate on zinc[J]. Corrosion Science, 2003, 45(1): 199?210.
[12] �����, ���Ԫ, ���Ķ�, ֣��ΰ, ���ʰ�. 3.4%NaCl����������ʴ��Ϊ�ı����������׳����о�[J]. ����ѧ�������, 2000, 20(6): 800?802.
CAO Pei-gen, XU Hao-yuan, CAO Wen-dong, ZHENG Jun-wei, GU Ren-ao. Two-dimensional surface Raman imaging of a roughened iron electrode in saline solution[J]. Spectroscopy and Spectral Analysis, 2000, 20(6): 800?802.
[13] ����÷. �ִ�����ʴ���ĺ��⡢���������о�[J]. ����ѧ�������, 2006, 26(12): 2247?2250.
YANG Xiao-mei. Study on the infrared spectra and Raman spectra of steel rusty layer with atmospheric corrosion[J]. Spectroscopy and Spectral Analysis, 2006, 26(12): 2247?2250.
[14] LINGSTROM R, SVENSSON J E, JOHANSSON L G. The atmospheric corrosion of zinc in the presence of NaCl, the influence of carbon dioxide and temperature[J]. Electrochemical Soc, 2000, 147(5): 1751?1757.
[15] ʩ����, �� ��, �ż���, �ܳ���. п����Ͻ�Ĵ�����ʴ�о���״[J]. �й���ʴ�����ѧ��, 2005, 25(6): 373?379.
SHI Yan-yan, ZHANG Zhao, ZHANG Jian-qing, CAO Chu-nan. Review of atmospheric corrosion of zinc and zinc alloy[J]. Journal of Chinese Society for Corrosion and Protection, 2005, 25(6): 373?379.
[16] ������, ֣�ҟ�, Ҧ����, �� ��. �꾮�ཬ��̼�ֵĸ�ʴ�ͷ���[J]. ʯ����Ȼ������, 2000, 29(5): 257?263.
FU Zhao-yang, ZHENG Jia-shen, YAO An-lin, LI Jian. Corrosion and protection of carbon steel in drilling mud[J]. Chemical Engineering of Oil & Gas, 2000, 29(5): 257?263.
[17] ����Ƽ, �½���. ��п�����۸��ۻ�Ĥ��ʴ��Ϊ���о�[J]. ���ϱ���, 2007, 40(2): 7?10.
REN Yan-ping, CHEN Jin-hong. Corrosion behavior of passivation on hot-dipping galvanized steel prepared from trivalent chromium[J]. Materials Protection, 2007, 40(2): 7?10.
[18] ʯ����, κ��, �� ��, ³ ��. �ȶ�п��п���Ͻ�Ʋ������֯��������ʴ��Ϊ[J]. ���ϱ���, 2002, 35(3): 35?36.
SHI Huan-rong, WEI Wu-ji, DING Yi, LU Gang. Microstructures and salt spray corrosion behaviors of hot-dip Zn and 55Al-Zn coatings[J]. Materials Protection, 2002, 35(3): 35?36.
[19] SERE P R, ZAPPONI M, ELSNER C I, DI SARLI A R. Comparative corrosion behavior of 55 aluminum-zinc alloy and zinc hot-dip coatings deposited on low carbon steel substrate[J]. Corrosion Science, 1998, 40(10): 1711?1723.
[20] REFAIT P H, ABDELMOULA M, GENIN J M R. Mechanisms of formation and structure of green rust one in aqueous corrosion of iron in the presence of chloride ions[J]. Corrosion Science, 1998, 40(9): 1547?1560.
������Ŀ��������Ȼ��ѧ����������Ŀ(50571022)�����ҿƼ���������ƽ̨����������Ŀ(2005DKA10400)
�ո����ڣ�2008-08-21�������ڣ�2008-11-17
ͨѶ���ߣ��� �죬������ʦ����ʿ���绰��010-62333931��E-mail: hongzhang0523@163.com
(�༭ ������)


