�й���ɫ����ѧ�� 2003,(03),631-634 DOI:10.19476/j.ysxb.1004.0609.2003.03.019
���ں�SO2ʪ��/���ﻷ���еĸ�ʴ����
�й���ѧԺ�����о���������ʴ����������ص�ʵ����,�й���ѧԺ�����о���������ʴ����������ص�ʵ����,�й���ѧԺ�����о���������ʴ����������ص�ʵ����,�й���ѧԺ�����о���������ʴ����������ص�ʵ���� ����110016 ,����110016 ,����110016 ,����110016
ժ Ҫ��
�������帯ʴ�����䡢�������ɨ��羵�о������ں�SO2 ��ʪ�����ա�����SO2 �ĸ�������ѭ���ļ������������µĸ�ʴ���ɡ���������δ��SO2 ����������������ͬ�ĶԱ����顣���鹲�ֱ���� 5������ (12 0h) ������ʱ���ӳ� , SO2 �ĸ�ʴ���������Լ�ǿ , ���ĸ�ʴ���ֳ���ָ���仯���� , �����ĸ�ʴ������ʱ���ӳ��������ӡ��������ʾ�����ں�SO2 �ij�ʪ�����к����γɱ����Ժõ�Al2 O3 Ĥ , ���ڴ����黷���еĸ�ʴ����ΪAl2 (SO4 ) 3 ��18H2 O����δ��SO2 �ĶԱ����黷�������ĸ�ʴ�� , 5�������ۼ��������ӽ�Ϊ 0 .0 43g/m2 , ��ʴ������ʧ����С�ڼ�SO2 ʱ�ĸ�ʴ������ʧ ;���������Ժܹ�����
�ؼ��ʣ�
��ͼ����ţ� TG172
�ո����ڣ�2002-08-23
���������ص�����о���չ�滮������Ŀ (G19990 6 5 0 );
Corrosion of aluminum in wet/dry environment containing SO2
Abstract��
The corrosion of aluminum in wet/dry enviroment containing SO 2 was studied by using IR and SEM. The compared test without SO 2 was also carried out. The test went on for 5 cycles (120 h) .The corrosive effect of SO 2 became strong during the test.The corrosion of aluminum followed a function of positive exponent. It shows that the corrosion rate of aluminum increases with time. The results also indicate that, a protect film of Al 2O 3 can not form on aluminum in wet environment containing SO 2. The main corrosion product in the test environment is Al 2 (SO 4) 3��18H 2O. The aluminum was corroded lightly in the compared test environment, and the mass increase was only 0.043 g/m 2. The corrosion mass loss was smaller obviously than that in accelerate corrosive environment containing SO 2. The surface of specimens was still shiny compared with that with SO 2.
Keyword��
aluminum; atmospheric corrosion; SO 2;
Received�� 2002-08-23
���Ǵ����й㷺ʹ�õ�һ�ֳ�����ʴ���ϡ� ���Ź�ҵ�ִ������̼ӿ�, ���д�����Ⱦ����Ӿ硣 ���Թ�ҵ������ ����β����ȼ�������ȵ���Ⱦ��SO2����ʹ���н�����ʴ����, ��SO2��Ⱦ�Ĵ����Ǹ�ʴ����ǿ�Ĵ�������
1 ʵ��
�������ΪL4������ �����ʺ��� (��������) ΪFe 0.27%, Si 0.2%�� �����ߴ�Ϊ20 mm��20 mm��2 mm�� �����ý���ɰֽ��ĥ��600#, ��ˮ��ϴ��ƾ���ˮ�� ��ͪ���͡� ��� ��SO2�ļ��ٸ�ʴ���鰴����GB9789��88��GS-3C�����帯ʴ��������������н��С� �����¶ȿ�����40 ��, ʪ�Ƚӽ�98% �� ÿ������������ͨ��0.2 L SO2����, ���������ˮ�� �����������ڱ�¶8 h, Ȼ�������ڴ������� (�¶�Ϊ19 ��, ʪ��Ϊ56%) �б�¶16 h, �����ظ��γ�ʪ��������ѭ���� ÿ24 h (1������) ȡ��һ������, �������������ͱ�������� ����ͬ������������δ��SO2����ĶԱ����顣 ��ɨ��羵�¹۲츯ʴ��ò, ��X�������估�������ⸯʴ��� ���鹲����5�����ڡ�
2 ʵ����������
���ڴ������кܺõ���ʴ��, ��Ϊ����¶�ڴ����п�Ѹ������һ��ܱ��������Զ�����������, ������������ܡ� �����Ժ��Ҿ��б�����
2.1 ��ʴ��̬�븯ʴ����
������SO2Ϊ���ټ��ļ��ٸ�ʴ���黷����, ��1���ں�ʴ��������, �����������, ��ʴ����, �������汻�Ұ�ɫ��ʴ���������ǡ� ��5��������������ܵ�ƽ����������Ϊ39.63 g/m2, ����SO2�Ա������921���� ͼ1��ʾΪ�����ڸ�ʴ��������������港ʴ��̬��ɨ��羵�� �ɼ�1���ڼ��ٸ�ʴ�������������ȽϹ⻬, δ�����Եĸ�ʴ��ֲ���ʴ (ͼ1 (a) ) �� ��2���������������������ȫ������״�ĸ�ʴ����������, ��ʴ����Ĥ�ֲ�¡��, �ʹ���״ (ͼ1 (b) ) �� ��������ʱ���ӳ�, ��ʴ����Ĥ�Ĺ�������������չ, ���ѵ��������, ���ѵĸ�ʴ����ĤƬ֮���϶�ӿ�, һЩ��ʴ����ĤƬ�Ѿ��ɶ�, ������ƽ״ (ͼ1 (c) , (d) ) �� ����Oesch��
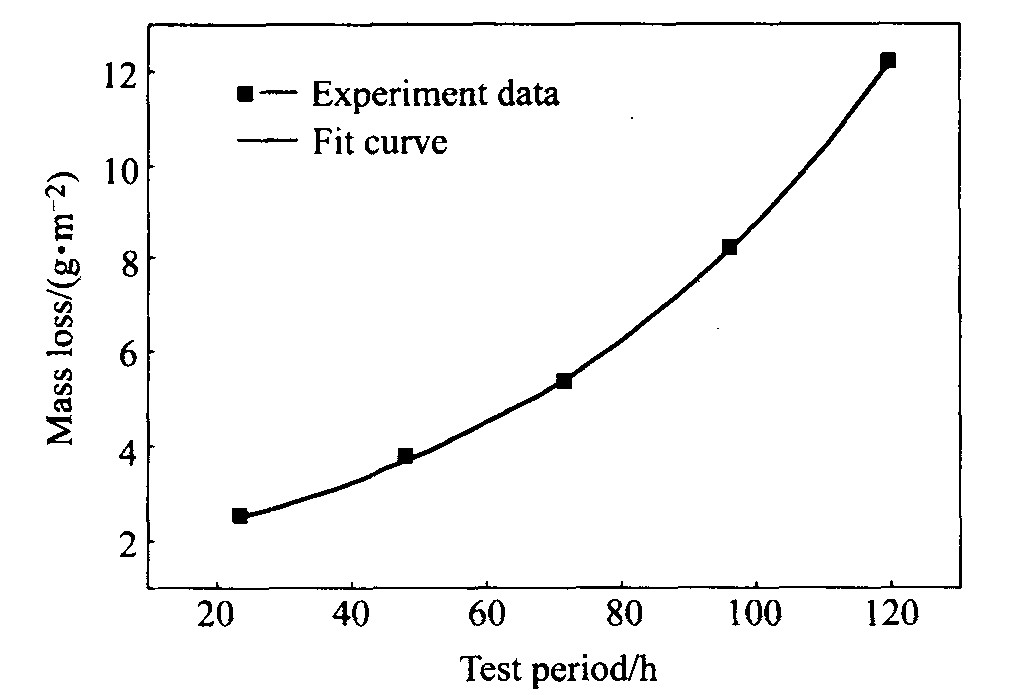
ͼ2��ʾ������SO2���ٸ�ʴ���黷���и�ʴ������ʧ��ʱ��ı仯���ߡ� ������, ʵ������������������غ�, ����ʴ������ʧ��ʱ���ӳ�����ָ���仯���ɡ� ������߷���Ϊ��m=0.129+1.203exp (0.016 9t) �� ˵��������SO2Ϊ���ټ��ļ��ٸ�ʴ���黷����, ��ʴ������ʧ��ʱ���ӳ�����ָ������, ����ʴ������ʧ�����ٶ��������졣 ��������塢 ����ͳ��й�ҵ������������ʵ�������µĸ�ʴ���ʻ����϶����ɸ���͵ݼ����, ��ʴ����Ҳ�dz���, ��Ȼ�����еĸ�ʴ���ʡ�0.79 ��m/a
2.2 ��ʴ�������
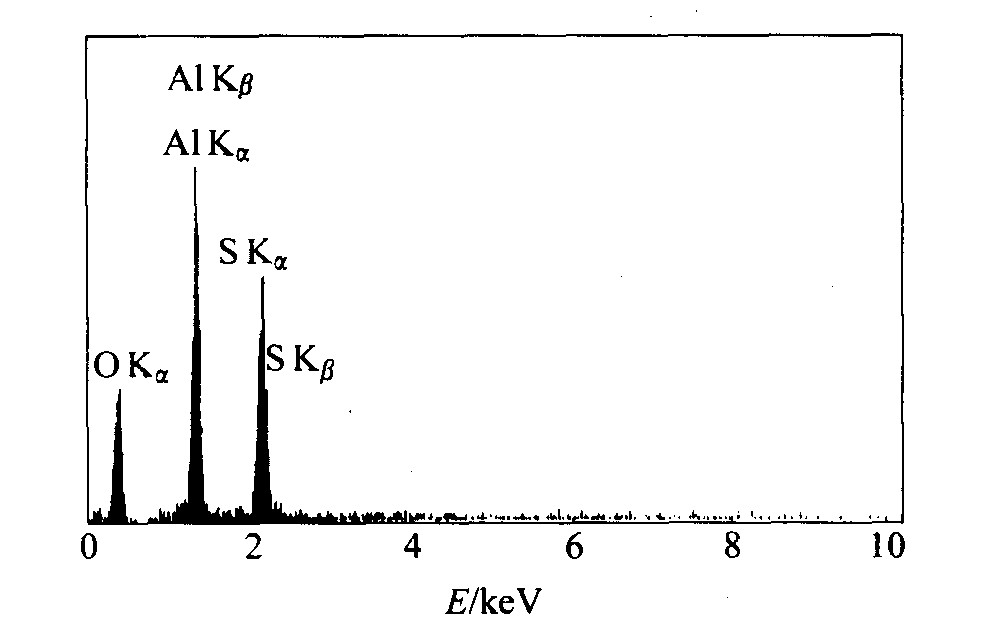
ͼ3��ʾΪ��5���ڼ��ٸ�ʴ�������������ɨ��羵����EDX��������� �ɼ���ʴ����������, �����3��Ԫ�ء� �����ڼ��ٸ�ʴ���������������ⷴ�����չ���ͼ4�� �������շ���ʾ��
ͼ1 ������������������ɨ��羵�� Fig.1 SEM micrograghs of surface of aluminum after exposure in test environments (a) ��24 h; (b) ��48 h; (c) ��72 h; (d) ��120 h
ͼ2 �������黷���еĸ�ʴ������ʧ Fig.2 Mass loss for aluminium in test environment
ͼ3 5���ڼ��ٸ�ʴ����� ��������ɨ��羵����EDX���� Fig.3 Result of EDX after 5 cycles in acceleration corrosive test
���ٸ�ʴ������������港ʴ����Ĥ�ijɷ���ҪΪAl2 (SO4) 3��18H2O�� ����SO2��ˮ�кͳ�ʪ�����о��иߵ�ˮ���Ժ�������, SO2�ڽ�������������������ʪ�������������ӡ� ��������п��ͬ, �����ʪ�ȴ���90%ʱ, SO2���и�ʴ���︲�ǵ��������������Ϊ������������������ļ���������ʮ��
SO2 (g) ��SO2 (aq)
SO2 (aq) +H2O��H++HSO-3
2HSO-3+O2��2H++2SO
��λ��pHͼ��ʾ��ˮ���γɵ���������Ĥ��pH<4��pH>8.5�Dz��ȶ���
ͼ4 �����ڼ��ٸ�ʴ����� ����������ⷴ�����չ��� Fig.4 IR spectrum of aluminum after every cycle accelerate corrosive test
���������β���Ĥ�� �����黷��������ʴ����, ˵��SO2������ʴ����Ҫ����, ���ĸ�ʴ������ҪΪ���������Ρ�
3 ����
��SO2ʪ��/����ѭ���ļ��ٸ�ʴ������, ���ĸ�ʴ������ʱ���ӳ���������, ���ֳ���ָ���仯����: ��m=0.129+1.203exp (0.016 9t) �� �������ʾ�����ں�SO2��ʪ�����б����γ����Խ��ʺ�����γɱ����Ժõ�Al2O3Ĥ, �ڴ����黷�������ĸ�ʴ������ҪΪAl2 (SO4) 3��18H2O�� ��δ��SO2�ĶԱ����黷�������ĸ�ʴ��, 5�����������ۼ����ӽ�Ϊ0.043 g/m2, ��ʴ������ʧ����С�ڼ�SO2ʱ�ĸ�ʴ������ʧ; ���������Ժܹ�����
�����