DOI��10.19476/j.ysxb.1004.0609.2018.06.13
�������������ʪ���ܽ������������Ĥ����Ϊ�����
������1, 3��������1��������2���̳���1��������1
(1. ���ݴ�ѧ ���Ͽ�ѧ�빤��ѧԺ������ 350118��
2. ���ݴ�ѧ ��е���̼��Զ���ѧԺ������ 350118��
3. ��������ѧԺ ���Ͽ�ѧ�빤��ѧԺ������ 350118)
ժ Ҫ��
Ӧ������ɨ���Ъϵͳ�����Ӷ���ѧģ��;ۺ�ʵ�飬�о�A356��м��������Ĥ�Ľṹ�����������������ۼ���ʪ���ܽ������Ĥ����Ϊ����̽����м���ۼ��еľۺϻ����������������Ħ��NaCl-KCl�ۼ�������NaF��Na3AlF6������Al2O3��ʪ��������AlF3���ۼ���Al2O3����ʪ�����ӷ�����ĵ�Ħ��NaCl-KCl�ۼ������ܽ�����Ĥ����ʹ��м�ۺ�Ϊ��������NaF��Na3AlF6�Դٽ��ۺϵ�Ч������������AlF3Ч���ϲ�ۺϻ������������������ۼ��е�����F-����м�ۺϵ�ǰ���������ۼ���Al2O3���õ���ʪ�Կ����������Ĥ���ܽ�̶ȡ�����Ĥ�ܽ�����������Һ�ο����Է��ؾۺϳɴ�������ۼ�����Һ�IJ���ʪ����������Һ�εľۺϣ�������Na3AlF6���Ƚ���������ۼ��ȣ��谭ϸС����ľۺϡ�
�ؼ��ʣ�
��м���ۺ���Ϊ�����Ӷ���ѧģ�������������������ʪ����
���±�ţ�1004-0609(2018)-06-1182-09���� ��ͼ����ţ�TG146.2���� ���ױ�־�룺A
�����������еͳɱ������ܺġ����ŷŵ��ص㣬�о�����[1-2]�����������������ĵ���������ԭ����5%�������Ĺ������(��������)�����������10%��CO2�����ŷ�Ҳ��Ϊ�������5%������������࣬��ͬ���͵ķ����������кܴ��𣬱ȱ���������״��Ƭ״���������ʱȽϵͣ�����м�ɻ����ʽ�Ϊ84.3%[3]���������յ���Ҫ�ѵ����������������ڱ����γ����ܵ�����Ĥ������ʱ��Һ������Ĥ�����������ͷų��������⣬�����еĸ�������������Ԫ��Ҳ��Ҫȥ����Ŀǰ��Է��������������о���Ҫ�����ڳ�����þ����������Ԫ��[4-6]����������ܽ��ƻ���������Ĥ����߷��������ʻ�ȱ�������о����������շ�ʽ��Ҫ�����֣�һ������ת¯�ォ�����������ۼ���ϣ�ͨ���ۼ��ܽ������������Ĥ��ʹ����������Һ�ͷų���[7-8]�����ǽ�������һ������ԭ�������ۣ�����������Ӵ�����һ����������ͨ���ۼ��ܽ��������Ĥ��ʹ����������Һ�����������У��ɻ�ýϸߵĻ�����[9-11]��
�ۼ��ijɷ����ܽ�����Ĥ�Ĺؼ���ͨ���ۺ�ʵ����Լ����ۼ��ܽ�����Ĥ������[12-13]��������������һ�����������ۼ��У�����ɢ�ķ����ۺ�Ϊһ��������ʱ����������������Ĥ�ѱ���ȫ�ܽ⡣��ͬ���ۼ��ɷ��ܽ�����Ĥ��������ͬ�������ۺ������ʱ�䡢�¶�Ҳ��ͬ��ROY��[14]�о�����������Ƭ���ۼ��еľۺϣ�̽���˷��������ࡢʱ����¶ȶԾۺ���Ϊ��Ӱ�죬��û�п��Ƿ�����Ũ�ȵ�Ӱ�졣���⣬���ڷ������ۼ��еľۺϻ���Ҳ��û���γ�һ�µĹ۵�[15]����ѧ����Ϊ�ۼ����Ⱥ��ۼ���Al2O3���������ʪ�Զ��ۼ��ܽ�����Ĥ�����������[16]��Ҳ��ѧ����Ϊ������������Ĥ������ѧ��Ӧ��ʹ������Ĥ�ܽ�[17]��Ҳ��ѧ����Ϊ����������Һ��Ӧ�����ۼ��������������Na�������Ӧ����ʹ����Ĥ����[12]��
�������߲��û��ھ�����ѧ�ķ��Ӷ���ѧģ���о��ۼ�������Ĥ����Һ����ʪ�ԣ�ͨ���ۺ�ʵ�飬��Ũ�ȽǶ��о�������������ܽ�����Ĥ����������̽�ֺ��������ۼ���ʪ�ܽ�����Ĥ�Ļ�����
1 ʵ��
1.1 �ۼ�������Ĥ����Һ��ʪ�Եķ��Ӷ���ѧģ��
����Materials Studio ������Forciteģ������ۼ���Al2O3���������Һ����ʪ���̷��Ӷ���ѧģ�⡣ͼ1��ʾΪ�ۼ�-Al2O3��������ۼ�-��Һ��ԭ�ӽṹģ�ͣ�����Al2O3��Al�ľ���ṹ�����������ݿ⣬��ʪ�涼ѡ(1 0 0)���棬ȡ6��ԭ�Ӳ��ȡ��������ľ����ߴ�Ϊa=71 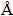 ��b=130
��b=130 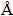 ��c=308
��c=308 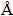 ��������ղ���Ϊ300
��������ղ���Ϊ300 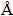 ���ۼ�ģ�����Ϊ��״��ֱ��Ϊ40
���ۼ�ģ�����Ϊ��״��ֱ��Ϊ40 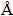 ���ۼ����Ϊ��Ħ��NaCl-KCl���Լ��ֱ�������������Ϊ10%��NaF��Na3AlF6��AlF3�����ۼ�����������������1���С���������ΪCOMPASS[18]����������������Al2O3�������ܡ����νṹ�ȷ��Ӷ���ѧ�о�[19-20]��ģ���¶�Ϊ1023 K����NVTϵ���Բ���2 fs����ԥ1.5 ns�����·�����NHL����ѹ������Andersen��
���ۼ����Ϊ��Ħ��NaCl-KCl���Լ��ֱ�������������Ϊ10%��NaF��Na3AlF6��AlF3�����ۼ�����������������1���С���������ΪCOMPASS[18]����������������Al2O3�������ܡ����νṹ�ȷ��Ӷ���ѧ�о�[19-20]��ģ���¶�Ϊ1023 K����NVTϵ���Բ���2 fs����ԥ1.5 ns�����·�����NHL����ѹ������Andersen��
1.2 ��м�������ۼ��еľۺ�ʵ��
ʵ�����ΪA356��м������PHI-700����ɨ���Ъϵͳ������м��������Ĥ�ijɷ����ȣ�����ͬ��ɨ����Ar+����ǹ������Ϊ������SiO2 /Si����������Ϊ2 nm/min��
�ۼ�������ԪΪ��Ħ��NaCl-KCl��������Ԫ�ֱ�ѡ��NaF��Na3AlF6��AlF3��ͨ���ۺ�ʵ��ȽϺ���ͬ��������ۼ��ܽ�����Ĥ�����������ƻ���ۼ�50 g�����뻡�������������в����ȵ�750 �棬�ۼ���ȫ�ۻ������A356��м10 g������20 min��ȡ��������ȴ����ˮ�ܽ��ۼ���ȡ���ۺϺ����������м�ڲ�ͬ�ۼ��еľۺ�Ч����
2 ���������
2.1 �������ۼ����Ӿ������̷���
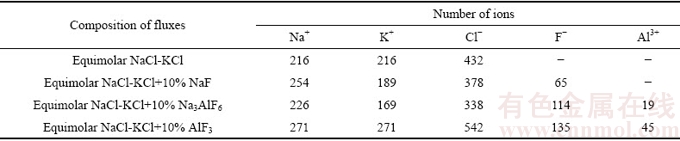
ͼ2��ʾΪ�������ۼ����Ӿ�������ʾ��ͼ���������̿ɷ�Ϊ3���Ρ���һ�Σ������ۼ���ʪ����Ĥ��ʹ�ۼ�����������Ĥ�ϣ��ڶ��Σ��ۼ��ܽ������������Ĥ���ƻ��������ԣ�ʹ����������Һ�������������У������Σ����ܽ���������ӱ������������ۼ��ϣ����ۼ��ϸ�����������棬��ͨ���������ۼ�������������ȥ������һ���У��ۼ�������ij�ֽӴ�����ʪ�����������أ��ڶ����У��ۼ��ܽ�����Ĥ���������������أ��������У��ۼ�����Һ�ķ��������������ء���ˣ�Ҫ��ַ����ۼ�����3���ε����ã��б�Ҫ�����о��ۼ�������Ĥ����Һ����ʪ�Ժ��ܽ��ԡ�
ͼ1 ��ʪ��ģ���ԭ�ӽṹģ��
Fig. 1 Atom structures of wetting simulations
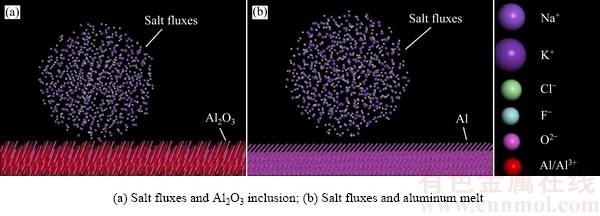
��1 ����ۼ�����������
Table 1 Ions number of mixture fluxes
2.2 �ۼ���Al2O3��ʪ�Եķ��Ӷ���ѧģ����
ͼ3��ʾΪ��Ħ��NaCl-KCl�ۼ�������NaF��Na3AlF6��AlF3����Al2O3����ʪ��Ϊģ���������Կ�������Ħ��NaCl-KCl�ۼ�������NaF��Na3AlF6�������Al2O3��ȫ��ʪ(��ͼ3(a)~(c))������ʱ���ӳ������������ۼ�����Al2O3��������չ��������AlF3����ۼ���Al2O3����û����ʪ���һ����ų⡣��15 psʱ�����Կ����ۼ���Զ��Al2O3���棬����û�нӴ�(��ͼ3(d))��
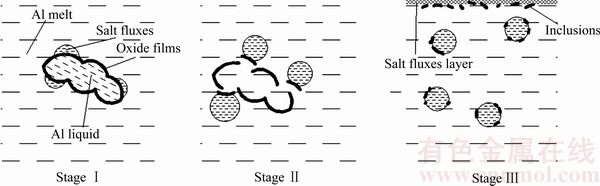
ͼ2 �������ۼ����Ӿ�������ʾ��ͼ
Fig. 2 Schematic diagram of purification process of Al chips by salt fluxes
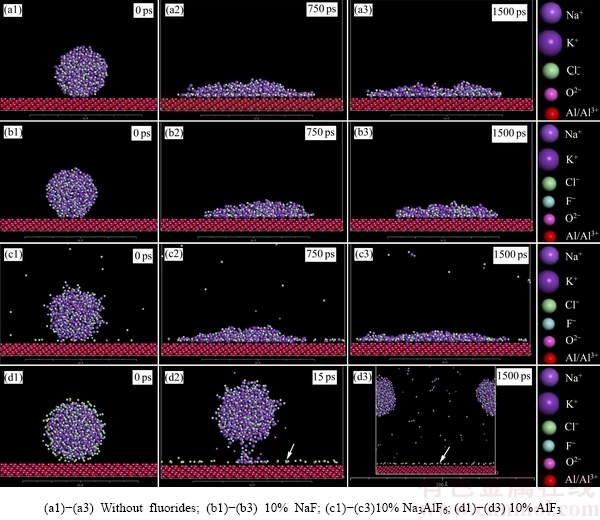
ͼ3 ��Ħ��NaCl-KCl�ۼ����ӷ��������Al2O3����ʪ��Ϊ
Fig. 3 Wetting behaviors between Al2O3 and equimolar NaCl-KCl fluxes
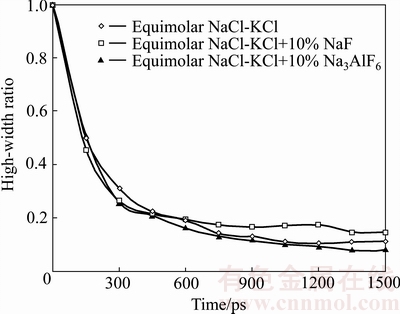
ͼ4 �����ۼ���Al2O3��ʪ��ĸ߿���
Fig. 4 Height-width ratio of molten fluxes after wetting with Al2O3
�ۼ���Al2O3�������ʪ�̶ȿ������ۼ��ĸ߿��ȱ仯���з����������ͼ4��ʾ�����Կ���������ʪAl2O3��3���ۼ���300 ps�ھͿ���չƽ��Al2O3�����ϣ�����Ϊ�߿�����1�����½���0.3����3���ۼ�����չ�����൱�����չƽ�ٶ���С��900 ps֮��߿�����ֵ�������䣬�����������ʪ����������ʪ�̶ȿ�������10%Na3AlF6���ۼ���Al2O3����ʪ����ã���ʪ����ۼ��߿���Ϊ0.08����Ħ��NaCl- KCl�ۼ���֮����ʪ���ۼ��ĸ߿���Ϊ0.11����NaF��ʹ��ʪ�����н��ͣ���ʪ����ۼ��߿���Ϊ0.15��
2.3 �ۼ�����Һ��ʪ�Եķ��Ӷ���ѧģ����
ͼ5��ʾΪ�ۼ�����Һ��ʪ�Եķ��Ӷ���ѧģ���������Կ�������Ħ��NaCl-KCl�ۼ�������NaF��Na3AlF6��AlF3������Һ����ʪ���ۼ�����������״�������ۼ�����Һ�Dz����ڵģ���������Һ�����ۼ��е��˶��������Һ���ۼ��ķ����ԡ��Ҹ����������ۼ�����Һ����ʪ��û�����Ե�Ӱ�졣
2.4 ��м��������Ĥ�ɷ����ȷ������
ͼ6��ʾΪ��������ɨ���Ъϵͳ�ⶨ����м����ɷֺ�����Ĥ��ȡ���ͼ6(a)���Կ�����A356��м�ı���ɷ���Ҫ��C��O��Al��Mg������C��Ҫ���Ի��ӹ������е���ȴ��Һ��O��Al��Mg�����Ա��������Ĥ������Al2O3������MgO����ͼ6(b)���Կ��������Ŷ�Ъ���ӽ�����ȵ����ӣ�OĦ���������ͣ�AlĦ�����������ӣ��������ı�����Al2O3Ϊ����Խ�����Al2O3����Խ�ͣ�����ԼΪ80 nm��
2.5 ��м�ۺ�ʵ����
ͼ7��ʾΪA356��м��750�������ۼ��еľۺϽ������ͼ7���Կ�����ԭʼΪƬ״����м(��ͼ7(a))�ڵ�Ħ��NaCl-KCl�ۼ��м���û�оۺϣ���Ȼ������ɢ����״�����״(��ͼ7(b))��������Һ������Ĥ��������ϵ����ͬ����м�ۻ�������������Ĥ����Ӧ���������³����ѷ죬��Һ������Ĥ�ѷ촦��������������Һ�ξۺϡ�������Ĥ�ڸ��������нϸߵ�ǿ�ȣ��谭��Һ��ȫ�ۺϳ�Բ��������ROY��[14]��ʵ����Ҳ���֣�����������Ƭ�ڵ�Ħ��NaCl-KCl���ۻ�������96 h����δ�ۺϣ�������Ħ��NaCl-KCl�ۼ������ƻ���ȥ����м��������Ĥ��

ͼ5 ��Ħ��NaCl-KCl�ۼ����ӷ����������Һ����ʪ���
Fig. 5 Wetting behaviors between aluminum melt and equimolar NaCl-KCl fluxes
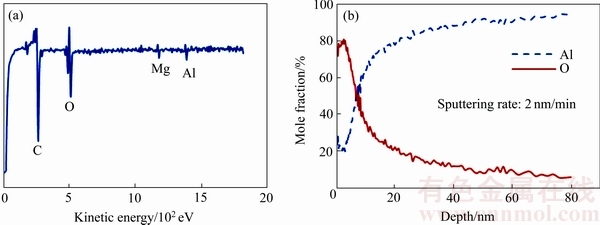
ͼ6 ��м����ɷ�������Ĥ���
Fig. 6 Surface constituents (a) and oxide film thickness(b) of aluminum chips

ͼ7 A356��м�ڲ�ͬ�����ۼ��еľۺ�Ч��
Fig. 7 Coalescence behavior of A356 aluminum chips in different molten salt fluxes
��Ħ��NaCl-KCl�ۼ�����NaF��Na3AlF6��AlF3����������ٽ�A356��м�ľۺ�(��ͼ7(c)~(e))����������������Ϊ0.1%ʱ����м��ʼ�ۺϳ�ϸСԲ������״�����ں�Na3AlF6���ۼ��У�����ߴ���Խϴ������ܽ�����Ĥ������Ҳ��ǿ�������������Ϊ0.3%ʱ������AlF3�������ۼ��е���м���ۺ�Ϊ������ֻ������û�оۺϡ�������������ﵽ0.5%ʱ����м�ں�NaF���ۼ����Ѿۺϳɵ��������ں�Na3AlF6���ۼ��л�������ϸС����δ�ۺϡ����֮�£���м�ں�AlF3�ۼ��еľۺ�Ч���ϲ�������ﵽ0.8%�������ȫ�ۺ�Ϊ��������
2.6 ��м�ں��������ۼ��еľۺϻ���̽��
2.6.1 ��м��������Ĥ���ܽ����
������м�е���Һ�����Լ80 nm��Al2O3����Ĥ����(��ͼ6(b))��Ҫ��Ч������м��������ȥ���������Ĥ��������ѧ��������[12, 15]����������Ĥ��ȥ�����̲������Է����У���Ҫͨ����ѧ��Ӧ���е�����ò���ȥ����
1) ����F-�������������Ĥ�����û���
����F-��Al2O3����Ĥ�����û�����һ����Ϊ������F-�İ뾶(0.136 nm)��Al2O3�����е�O2-�뾶(0.12 nm)�ӽ������ۼ�������O2-���ۼ��е�����F-���Ա˴���λ�������м�̬������������ӡ����м�̬������ӿ��Խ���Al2O3������ܽ��ܣ��ٽ�Al2O3������ܽ�[21]�����⣬�м�̬�������ӵ����ɵ���Al2O3�������������ȣ�ʹAl2O3���澧����������ѣ���������Ĥ��ǿ�Ƚ��ͣ�����ۼ������ɵ�F-��Ӱ������Ĥ�ܽ�̶ȵĹؼ�����֮һ��
��м���ۼ��еľۺ�ʵ�������������������������ĵ�Ħ��NaCl-KCl�ۼ���Ȼ���Խϳ�ֵ���ʪAl2O3��������Ч�ܽ�����Ĥ(��ͼ7(b))������NaF��AlF3��Na3AlF6���ۼ���������״̬�¶�����������F-�������������ﰴʽ(1)��ʽ(3)������⣬��ÿ100 g��Ħ��NaCl-KCl�ۼ���Ӳ�ͬ����������������F-Ũ����ͼ8��ʾ����ͼ8���Կ�����������ͬ���������ķ����AlF3������F-Ũ����ߣ������NaF��Na3AlF6���٣�����Щ���ɵ�F-�Ǵٽ�����Ĥ�ܽ�Ĺؼ���
���У���AlF3���ۼ���Ȼ������ʪAl2O3����Ҳ��ֽ��Cl-��F-����������Al2O3������(��ͼ3(d3)��ͷ����)��Na3AlF6�ܽ�Al2O3��������NaF�൱�����ܸ���ʽ(3)����������F-Ũ����ͣ�������һ������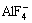 ��Al2O3�е�O2-Ҳ�������Ϸ�Ӧ������
��Al2O3�е�O2-Ҳ�������Ϸ�Ӧ������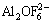 [22]���䷴Ӧʽ��ʽ(4)��ʾ���Ӷ��ٳ���Al2O3�ں�Na3AlF6�ۼ��еĿ����ܽ⡣
[22]���䷴Ӧʽ��ʽ(4)��ʾ���Ӷ��ٳ���Al2O3�ں�Na3AlF6�ۼ��еĿ����ܽ⡣
NaF=Na++F- (1)
Na3AlF6=3Na++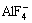 +2F- (2)
+2F- (2)
AlF3=Al3++3F- (3)
O2-+2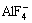 =
=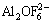 +2F- (4)
+2F- (4)
2) ��ʪ�Զ��ۼ��ܽ������������Ĥ��Ӱ��
�Ƚ�ͼ7��8���Կ�������NaF��AlF3��Na3AlF6���ۼ��ܽ�����Ĥ��������δ������F-Ũ�ȶ�Ӧ�����������ۼ���Al2O3����Ĥ����ʪ�Զ�����Ĥ�ܽ����Ŵٽ����á���ȻAlF3������F-Ũ����ߣ������ں�AlF3���ۼ���Al2O3����ʪ(��ͼ3(d))������ʹ���ɵ�F-��Al2O3��ֽӴ���ֻ��ͨ����������������F-�������ϣ�����ܽ�����Ĥ�����ñȽ����ޡ���ȻNaF��F-Ũ�Ƚϵͣ�����Al2O3������ȫ��ʪ(��ͼ3(b))��Ϊ����F-��Al2O3�ĽӴ����������������ܽ�����ĤЧ���Ϻá�
2.6.2 ��Һ�εľۺ�
ͼ9��ʾΪ��м�б�����Ĥ��������Һ�ξۺϹ���ʾ��ͼ����Һ�α��������Ĥ�����ұ�ȥ��֮��������Һ��������Ĥ���Ѵ��Ӵ����γ�����Һ����Һ��ֱ�ӽӴ�������ѧ�ڶ����ɱ����������Է����̶��dz��������ܽ��͵ķ�����У���Ӵ�����Һ�����ۼ���Ϊ���ֽ�������ͣ����Է��ؾۼ��ɸ����������վۺ�Ϊ�������������ù��̰����ű��������С�ͱ����ܽ��ͣ�����ǿ����Է����еġ�
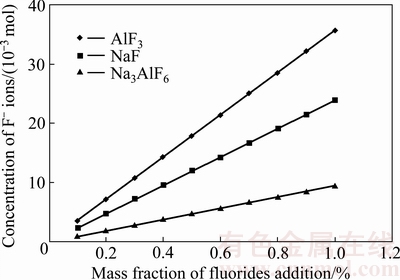
ͼ8 ���Ӳ�ͬ�����������100 g��Ħ��NaCl-KCl�ۼ�������F-Ũ��
Fig. 8 Concentration of free F- ions in 100 g equimolar NaCl-KCl fluxes with different fluorides contents
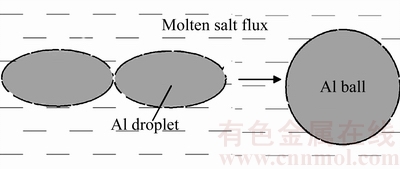
ͼ9 ��Һ�ξۺϹ���ʾ��ͼ
Fig. 9 Coalescence of aluminum droplets
������Һ�ξۺϹ��̿����Է����У������Ǵ���������������Ҫ�����ۼ�����Һ����ʪ�Ժ��ȡ����Ӷ���ѧģ�����ѱ��������о���4���ۼ�����Һ������ʪ(��ͼ5)����ˣ������谭��Һ�εľۺ��˶������ۼ���Խ����Һ�ε��˶�����Խ����ϸС����Һ�θ������Ծۺϳɸ��������о�����[23-24]��Na3AlF6����ۼ��ȵ����ñȽ���������ˣ������ۼ��е�Na3AlF6�������ﵽ0.3%֮����м�ͻ����ۺ�Ϊ�������壬������һЩϸС����δ�ۺϣ���ʹNa3AlF6��������ߵ�0.8%��Ҳ���ٽ���ЩС�������ȫ�ۺ�(��ͼ7(d))��
3 ����
1) �ۼ���Al2O3��ʪ�Եķ��Ӷ���ѧģ������������Ħ��NaCl-KCl�ۼ�������NaF��Na3AlF6������Al2O3��ʪ�����к�Na3AlF6���ۼ���ʪ����ã�����������Ĥ���ܽ⡣������AlF3���ۼ���Al2O3����ʪ������������Ĥ���ܽ⡣
2) A356��м��������Ĥ���ԼΪ80 nm���ۺ�ʵ��������������������ĵ�Ħ��NaCl-KCl�ۼ����ܽ�����Ĥ�������������������ۼ������ܽ�����Ĥ��ʹ��м�б���������Һ�����ۺϡ�����NaF��Na3AlF6�Դٽ���Һ�ۺϵ�Ч������������AlF3Ч���ϲ
3) �����ۼ��е�����F-����Al2O3�е�O2-����������ӣ��ٳ�����Ĥ���ܽ⣬������м�ۺϵ�ǰ���������ۼ���Al2O3���õ���ʪ�Կ������Al2O3���ܽ�̶ȡ���мȥ������Ĥ�����е���Һ�ο����Է��ؾۺϳɸ��������ۼ�����Һ�IJ���ʪ����������Һ�εľۺϣ������������������ۼ��ȣ��谭ϸС����ľۺϡ�
REFERENCES
[1] �� ��, �� ��, ��־��, ������. ԭ�����������������ܺĺ����������ŷŶԱ�[J]. �й���ɫ����ѧ��, 2012, 22(10): 2909-2914.
DING Ning, GAO Feng, WANG Zhi-hong, GONG Xian-zheng. Comparative analysis of primary aluminum and recycled aluminum on energy consumption and greenhouse gas emission[J]. The Chinese Journal of Nonferrous Metals, 2012, 22(10): 2909-2914.
[2] CUI J, ROVEN H J. Recycling of automotive aluminum[J]. Transactions of Nonferrous Metals Society of China, 2010, 20(11): 2057-2063.
[3] XIAO Y, REUTER M A, BOIN U D O. Aluminium recycling and environmental issues of salt slag treatment[J]. Journal of Environmental Science and Health, 2005, 40(10): 1861-1875.
[4] ̷ϲƽ, ֣����, �ζ���, ������. Al-3B�м�Ͻ��������������������Ͻ���������������Ӱ��[J]. �й���ɫ����ѧ��, 2014, 24(6): 1401-1407.
TAN Xi-ping, ZHANG Kai-hong, SONG Dong-fu, ZHANG Xin-ming. Effects of Al-3B master alloy addition on impurity iron content of recycled casting aluminum alloy[J]. The Chinese Journal of Nonferrous Metals, 2014, 24(6): 1401-1407.
[5] �����, ������, �� Խ. �ۼ���ȥ������������þ�������о�[J]. ��Ͻ�ӹ�����, 2015, 43(12): 23-27.
SUN De-qin, DAI Guo-hong, XU Yue. Study on the Mg element removing technology from Al slag melts by fluxing technology[J]. Light Metal Fabrication Technology, 2015, 43(12): 23-27.
[6] �����, ������, �� Խ. ����������ȥ��CrԪ�ص������о�[J]. ��Ͻ�ӹ�����, 2016, 44(1): 24-28.
SUN De-qin, DAI Guo-hong, XU Yue. Experiments of removing Cr from waste Al slag melts[J]. Light Metal Fabrication Technology, 2016, 44(1): 24-28.
[7] KHOEI A R, MASTERS I, GETHIN D T. Design optimization of aluminium recycling processes using Taguchi technique[J]. Journal of Materials Processing Technology, 2002, 127(1): 96-106.
[8] ZHOU B, YANG Y, REUTER M A, BOIN U M J. Modeling of aluminium scrap melting in a rotary furnace[J]. Minerals Engineering, 2006, 19(3): 299-308.
[9] BUTNARIU I, BUTNARIU I, BUTNARIU D. Technological researches concerning a decrease in the losses due to the oxidation of remelted scrap from aluminium alloys[J]. Materials Science Forum, 2010, 630: 71-74
[10] MOLOODI A, AMINI H, KARIMI E Z V, GOLESTANIPOUR M. On the role of both salt flux and cold pressing on physical and mechanical properties of aluminum alloy scraps[J]. Materials and Manufacturing Processes, 2011, 26(9): 1207-1212.
[11] XIONG B, ZHANG X, LI F, HU H, LIU C. Recycling of aluminum A380 machining chips[C]// HYLAND M. Light Metals. New Jersey: TMS, 2015: 1011-1015.
[12] YE J, SAHAI Y. Interfacial behavior and coalescence of aluminum drops in molten salts[J]. Materials Transactions, 1996, 37(2): 175-180.
[13] XIAO Y, REUTER M A. Recycling of distributed aluminium turning scrap[J]. Minerals Engineering, 2002, 15(11): 963-970.
[14] ROY R R, SAHAI Y. Coalescence behavior of aluminum alloy drops in molten salts[J]. Materials Transactions, 1997, 38(11): 995-1003.
[15] ZHOLNIN A G, NOVICHKOV S B. About the coalescence mechanism of aluminum, the analysis of the recent conceptions[C]// KVANDE H. Light Metals. Pennsylvania: TMS, 2005: 1197-1202.
[16] SYDYKOV A, FRIEDRICH B, ARNOLD A. Impact of parameters changes on the aluminum recovery in a rotary kiln[C]// SCHNEIDER W. Light Metals. Washington: TMS, 2002: 1045-1052.
[17] MASSON D B, TAGHIEI M M. Interfacial reactions between aluminum alloys and salt flux during melting[J]. Materials Transactions, 1989, 30(6): 411-422.
[18] SUN H. COMPASS: An ab initio force-field optimized for condensed-phase applications overview with details on alkane and benzene compounds[J]. The Journal of Physical Chemistry B, 1998, 102(38): 7338-7364.
[19] YEH I C, LENHART J L, RINDERSPACHER B C. Molecular dynamics simulations of adsorption of catechol and related phenolic compounds to alumina surfaces[J]. Journal of Physical Chemistry C, 2015, 119(14): 7721-7731.
[20] CHEN C F, LI H Y, HONG C W. Molecular dynamics analysis of high-temperature molten-salt electrolytes in thermal batteries[J]. CMC: Computers, Materials and Continua, 2015, 46(3): 145-163.
[21] �����. NaF-AlF3��������������ܽ�����о�[D]. ����: �����Ƽ���ѧ, 2015: 104-115.
ZHANG Ya-nan. Study on dissolution process of alumina in NaF-AlF3-based melts[D]. Beijing: University of Science and Technology Beijing, 2015: 104-115.
[22] �� ��, ��ӽ÷, ������. ����ʯ-�����������е������ ϵ[J]. ������ѧѧ��(��Ȼ��ѧ��), 2000, 21(1): 63-65.
XU Ning, GUO Yong-mei, QIU Zhu-xian. The acid & alkali system in cryolite-alumina melts[J]. Journal of Northeastern University(Natural Science) , 2000, 21(1): 63-65.
[23] ROY R R, YE J, SAHAI Y. Viscosity and density of molten salts based on equimolar NaCl-KCl[J]. Materials Transactions, 1997, 38(6): 566-570.
[24] TENORIO J A S, ESPINOSA D C R. Effect of salt/oxide interaction on the process of aluminum recycling[J]. Journal of Light Metals, 2002, 2(2): 89-93.
Behaviors and mechanism of alkali fluorides wetting and melting oxide films on aluminum chips surface
WANG Huo-sheng1, 3, FU Gao-sheng1, SUN Ze-tang2, CHENG Chao-zeng1, SONG Li-li1
(1. School of Materials Science and Engineering, Fuzhou University, Fuzhou 350118, China;
2. School of Mechanical Engineering and Automation, Fuzhou University, Fuzhou 350118, China;
3. School of Materials Science and Engineering, Fujian University of Technology, Fuzhou 350118, China)
Abstract: Nano scanning auger system, molecular dynamics simulations and coalescence experiments were employed to study the oxide film structure of A356 alloy chips and the behaviors of salt fluxes containing alkali fluorides wetting and melting oxide films. Moreover, the coalescence mechanism was discussed. The results show that equimolar NaCl-KCl with addition of NaF or Na3AlF6 wetted well with Al2O3 inclusions but addition of AlF3. Eequimolar NaCl-KCl containing alkali fluorides can melt oxide film and promote the coalescence of wrapped aluminum droplets in molten fluxes. The effects of NaF and Na3AlF6 on coalescence are more significant than that of AlF3. The coalescence mechanism analysis results show that free F- ions are the premise for chips coalescence and the wetting between fluxes and Al2O3 inclusions improve the coalescence degree. Aluminum droplets can coalesce spontaneously in molten fluxes and the non-wetting between fluxes and aluminum liquid is benefit for the coalescence, but the improvement of fluxes viscosity by Na3AlF6 will resist the coalescence of small aluminum droplets.
Key words: aluminum chip; coalescence behavior; molecular dynamics simulation; alkali fluoride; wetting
Foundation item: Project(2015DFA71350) supported by International Cooperation Project of Science and Technology Ministry of China; Project(2012H0006) supported by Important Science and Technology Programs of Fujian Province, China
Received date: 2017-04-06; Accepted date: 2018-01-02
Corresponding author: FU Gao-sheng; Tel: +86-13600809853; E-mail: fugaosheng@fzu.edu.cn
(�༭ ����)
������Ŀ�����ҿƼ������ʺ�����Ŀ(2015DFA71350)������ʡ�Ƽ��ƻ��ص���Ŀ(2012H0006)
�ո����ڣ�2017-04-06�������ڣ�2018-01-02
ͨ�����ߣ������������ڣ���ʿ���绰��13600809853��E-mail: fugaosheng@fzu.edu.cn
ժ Ҫ��Ӧ������ɨ���Ъϵͳ�����Ӷ���ѧģ��;ۺ�ʵ�飬�о�A356��м��������Ĥ�Ľṹ�����������������ۼ���ʪ���ܽ������Ĥ����Ϊ����̽����м���ۼ��еľۺϻ����������������Ħ��NaCl-KCl�ۼ�������NaF��Na3AlF6������Al2O3��ʪ��������AlF3���ۼ���Al2O3����ʪ�����ӷ�����ĵ�Ħ��NaCl-KCl�ۼ������ܽ�����Ĥ����ʹ��м�ۺ�Ϊ��������NaF��Na3AlF6�Դٽ��ۺϵ�Ч������������AlF3Ч���ϲ�ۺϻ������������������ۼ��е�����F-����м�ۺϵ�ǰ���������ۼ���Al2O3���õ���ʪ�Կ����������Ĥ���ܽ�̶ȡ�����Ĥ�ܽ�����������Һ�ο����Է��ؾۺϳɴ�������ۼ�����Һ�IJ���ʪ����������Һ�εľۺϣ�������Na3AlF6���Ƚ���������ۼ��ȣ��谭ϸС����ľۺϡ�
[5] �����, ������, �� Խ. �ۼ���ȥ������������þ�������о�[J]. ��Ͻ�ӹ�����, 2015, 43(12): 23-27.
[6] �����, ������, �� Խ. ����������ȥ��CrԪ�ص������о�[J]. ��Ͻ�ӹ�����, 2016, 44(1): 24-28.
[21] �����. NaF-AlF3��������������ܽ�����о�[D]. ����: �����Ƽ���ѧ, 2015: 104-115.
[22] �� ��, ��ӽ÷, ������. ����ʯ-�����������е������ ϵ[J]. ������ѧѧ��(��Ȼ��ѧ��), 2000, 21(1): 63-65.


