���±�ţ�1004-0609(2013)08-2296-06
���̼�Ȼ�ԭ�Ѱ���ȡ����þ�Ĺ���
�� ��1, 2, 3, 4�����ų�1, 2, 3, 4����ɲ�1, 2, 3, 4���� ��1, 2, 3, 4���� ��1, 2, 3, 4��
����1, 2, 3, 4��������1, 2, 3, 4��������1, 2, 3, 4
(1. ����������ѧ ���ұ����ҹ���ʵ���ң����� 650093��
2. ����������ѧ ����ʡ��ɫ�������ұ���ص�ʵ���ң����� 650093��
3. ����������ѧ ����ʡ������ɫ������Դ������ù����ص�ʵ����(��������)������ 650093��
4. ����������ѧ ұ������Դ����ѧԺ������ 650093)
ժ Ҫ��
������������þ��ԭ�ʡ�XRD��SEM���ֶ��뷽���о�����������Ѱ�̼�Ȼ�ԭ�¶ȡ�������ȡ�̼�Ȼ�ԭ����ʱ��ȶ�̼�Ȼ�ԭ�Ѱ���ȡ����þ���յ�Ӱ�졣�����������30~100 Paʱ��̼�Ȼ�ԭ�¶ȸ���1 623 K������þ�Ļ�ԭ���������ӣ�������̼�Ȼ�ԭ��Ӧ�Ľ��С����Ž�ú��ԭ��������þĦ���ȵ������Լ�̼�Ȼ�ԭʱ����ӳ���̼�Ȼ�ԭ��Ӧ��Ӧ���ʼӴ�ԭ����ߣ���̼�Ȼ�ԭ�¶�Ϊ1 623 K����ԭʱ��Ϊ4 h����̼��Ϊ1.6ʱ������þ��ԭ�ʳ���99%����ˣ�ѡ���ʵ��Ľ�ú��ԭ��������þĦ����ֵ�Լ�̼�Ȼ�ԭʱ�䣬���¶ȸ���1 623 K�����£���������̼�Ȼ�ԭ����þ���̵�˳������������þ��ԭ�ʵ���ߡ�
�ؼ��ʣ�
��ͼ����ţ�TF131��TF822 �� �� ���ױ�־�룺A
Process of magnesium production by calcined dolomite carbothermic reduction in vacuum
TIAN Yang1, 2, 3, 4, WANG Yu-chao1, 2, 3, 4, YANG Cheng-bo1, 2, 3, 4, YANG Bin1, 2, 3, 4, QU Tao1, 2, 3, 4,
LIU Da-chun1, 2, 3, 4, DAI Yong-nian1, 2, 3, 4, LIU Hong-xiang1, 2, 3, 4
(1. National Engineering Laboratory for Vacuum Metallurgy, Kunming University of Science and Technology, Kunming 650093, China;
2. Key Laboratory for Nonferrous Vacuum Metallurgy of Yunnan Province, Kunming University of Science and Technology, Kunming 650093, China;
3. State Key Laboratory Breeding Base of Complex Nonferrous Metal Resources Clear Utilization in Yunnan Province, Kunming University of Science and Technology, Kunming 650093, China;
4. Faculty of Metallurgical and Energy Engineering, Kunming University of Science and Technology, Kunming 650093, China)
Abstract: The temperature of calcined dolomite carbothermic reduction, molar ratio and carbothermic reaction time by calcined dolomite carbothermic reduction in vacuum were investigated by MgO reduction rate, XRD and SEM. The results show that the reduction rate of MgO clearly increases when temperature is higher than 1 623 K at 30-100 Pa, which is beneficial to MgO carbothermic reaction. The carbothermal reduction reaction rate increases with the increase of the molar ratio of coking coal reductant and magnesium oxide and carbon thermal reduction time at the carbon thermal reduction temperature of 1 623 K, the reduction time of 4 h and carbon ratio of 1.6, the magnesium oxide reduction rate is over 99%. Therefore, selecting the appropriate molar ratio of coking coal reductant and magnesium oxide and carbon thermal reduction time is beneficial to carbothermal reduction process for magnesium smelting going smoothly and magnesium oxide reduction rate increasing at the temperature higher than 1 623 K.
Key words: calcined dolomite; carbothermic reduction; metal magnesium; vacuum metallurgy
þ�ǽ����ڸ��������ĵ���������ṹ���ϣ�Ҳ�ǹ���Ӧ����������Ľ����ṹ���ϡ��ܶȽ��൱������64%��Zn��25%���ֵ�23%������þ��þ�Ͻ���Ϊ21���͵���ɫ���̲���[1]��2011���й�ԭþ �����ﵽ67��t��ռȫ��þ������86%������þ����þ��ز�Ʒ����Լ40.02��t��ר��Ԥ���ڽ��10�꽫��һ����������[2]��Ŀǰ��������80%���ϵĽ���þ����Ƥ���������ģ���Ƥ������þ�ܺĸߡ�ԭ������������������ͷ����ŷ�����[3-4]�����⣬���ڻ�ԭ�����Բ��㣬���»�ԭ�����ڽϳ���һ����12 h���ң���ԭ������ԭ��SiO2����Ӱ��ϴ�����Ч�ʽϵ�[5-7]�����ǵ�ʹ��̼��Ϊ��ԭ���ڳɱ�������߱���DZ�����ƣ���19����30�����ʼ������ܶ�ѧ�߷ֱ��ڳ�ѹ��������������¶�̼�Ȼ�ԭ����ȡ����þ������һϵ�еĴ���С���о�[8-10]���������ڼ����ϵ�һЩ���⣬������û��ʵ�ֹ�ҵ����������20����������������ѧ���ұ����ҹ���ʵ���Ҷ�����þ���̼�Ȼ�ԭ����þ��չ�˽϶�ϸ��������о�����[11-13]����������þ���̼�Ȼ�ԭ������ѧ������ѧ����������չ��һϵ�е���С��ʵ�飬ȡ�������õ�Ч����������þ��̼�Ȼ�ԭ��������������˽⡣Ȼ����ʵ����þ������ʹ�õ�ԭ�����Ѱף������Ѱ�̼�Ȼ�ԭ���̵��о����������롣Ϊ�ˣ��������߾����ض����������̼�Ȼ�ԭ�Ѱ���ȡ����þ�Ĺ���Ӱ�����ϵͳ���죬����Ϊ̼�Ȼ�ԭ����ȡ����þ����Ӧ���ṩ�����������ݡ�
1 ʵ��
1.1 ʵ��ԭ��
�Ѱ����̼�Ȼ�ԭ����þ���̰����²�����У�
MgO(s)+C(s)=Mg(g)+CO(g) (1)
CaO(s)+3C(s)=CaC2(s)+CO(g) (2)
MgO(s)+CaC2(s)=Mg(g)+CaO(s)+C(s) (3)
1.2 ʵ��ԭ�ϼ�����
ʵ��ԭ�ϣ�ɽ��ij���ṩ���Ѱ�(��ɷּ���1)����ú(C������63.58%����������)��������(CaF2 ��ѧ������)�����岽�����£�ʵ��ǰ����ȡһ��Ħ����(n(MgO):n(C)Ϊ1:1~1:2)�Ľ�ú������þĥϸ����74 ��m���ٳ�ȡ��ú������þ��������5% CaF2(��������)����Ͼ��ȣ���2~12 MPa��ѹ�����Ƴ�d 20 mm��15 mm�ſ顣ʵ��ʱ������õ��ſ�ȷ���������ʯī�����У���ʢ�����ϵ������������¯�������¯�ܷ����ȴˮ���أ�����ձó���գ���¯��ѹǿ����30 Pa����ʱͨ�����£�������������Ϊ11 K/min���ң�����������ѽ����¶�(800 ��)������һ��ʱ���(20 min)���ټ���������1 473~1 873 K���趨�¶Ȳ���ʼ��ʱ���£��ں��������±���2~5 h��������Ȼ�ԭ��Ӧ��ʹ��ԭ�����Ľ���þ�������������������ᾧ��������ʱ�������ͣ�罵�£���¯�½�������ʱ�ر�ˮ��ϵͳ����¯ȡ������ȡ��������¼��ȡ���ͷ�����
��1 �ѰĻ�ѧ�ɷ�
Table 1 Chemical compositions of calcined dolomite (mass fraction, %)

1.3 ��������
����Rigaku D/max-3B��X���������Ƿ�����Ӧ������������������࣬Cu Ka����Դ��ɨ������Ϊ10��~100�㣬�ܵ�ѹΪ50 kV���ܵ���Ϊ100 mA������Philips XL30ESEM-TMP��ɨ����������۲������������ò����������(EDAX��PHOENIXTM)���������������Ԫ�غ���������EDTA�ζ�����ⷴӦ������þ�ĺ��������ݽ���þ�Ļ�ԭ�ʦ�����������ض�����þ̼�Ȼ�ԭ���̵�Ӱ�죺
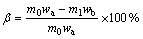 (4)
(4)
ʽ�У��±�ʾ��ԭ�ʣ�%��m0��ʾ��Ӧǰ����������g��m1��ʾ��Ӧ������������g��wa��ʾ��Ӧǰ�����е�MgO������%��wb��ʾ��Ӧ������е�MgO������%��
2 ���������
2.1 �Ѱ����̼�Ȼ�ԭ�¶ȶ�����þ��ԭ�ʵ�Ӱ��
��30~100 Pa��ϵͳѹ����n(C)/n(MgO)Ϊ1.6��2~5 h�Ļ�ԭ����ʱ�������£�������1 523~1 723 K���Ѱ�̼�Ȼ�ԭ�¶ȶ�����þ��ԭ�ʵ�Ӱ�죬�����ͼ1��ʾ��
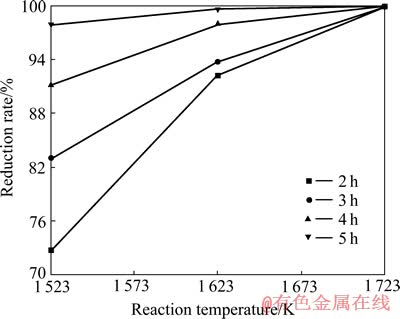
ͼ1 ̼�Ȼ�ԭ�¶�������þ��ԭ�ʹ�ϵ
Fig. 1 Relationship between reduction temperature and reduction rate
��ͼ1��֪��̼�Ȼ�ԭ����ʱ��ѡȡ2~5 h�����Ż�ԭ�¶ȵ����ߣ�����þ��ԭ�ʾ����ӣ�����ԭ�¶Ƚ�Ϊ1 523 K����ԭ����ʱ��Ϊ2 hʱ������þ��ԭ�ʽ�Ϊ72%��̼�Ȼ�ԭ��Ӧ���в���֡�����ԭ�¶ȴﵽ1 723 Kʱ����ͬ��ԭ����ʱ�������£�����þ��ԭ�ʾ��������ӣ���ֵ���ﵽ98%��˵����Ӧ���о��ң�������̼�Ȼ�ԭ��Ӧ�Ľ��С����ʵ��ʵ��������ԭ�¶�ѡΪ1 723 K��Ӧ���г�֣����ϻ�ԭ�ʴﵽ98%��
2.2 ̼�Ȼ�ԭ����ʱ���Լ�n(C)/n(MgO)������þ��ԭ�ʵ�Ӱ��
�ֱ�1 523��1 623 �Լ�1 723 K��̼�Ȼ�ԭ�¶������£���ͬ��ԭ����ʱ����n(C)/n(MgO)������þ��ԭ�ʵ�Ӱ�졣�趨̼�Ȼ�ԭ�¶�Ϊ1 523��1 623��1 723 K�Լ�ϵͳѹ��30~100 Pa�����ϳ���ѹ��8 MPa��ѡȡn(C)/n(MgO)Ϊ1.0��1.2��1.4��1.6��1.8��2����ԭ����ʱ��Ϊ2��3��4��5 h����ԭ��Ħ���ȶ�����þ��ԭ���ڲ�ͬ��Ӧʱ���µ�Ӱ�죬�����ͼ2��ʾ��
��ͼ2(a)��֪���ڱ���ʱ����ͬ������£�������̼��(n(C)/n(MgO))�����ӣ�����þ��ԭ�������ӡ�̼�Ȼ�ԭ����ʱ��ĸı䲢��Ӱ�컹ԭ������̼��(n(C)/n(MgO))�����Ӷ����ӡ��Ӷ���ѧ�Ƕȷ�������������Ļ�ԭ��̼��������ԭ�����Ѱ�������þ�Ľ���Ӵ������ܣ������ڹ�-���෴Ӧ�Ľ��У�ʹ����þ��ԭ�����ӡ���ˣ���ԭ���Ĺ���������̼�ȷ���ԭ�Ѱ���ȡ����þ��
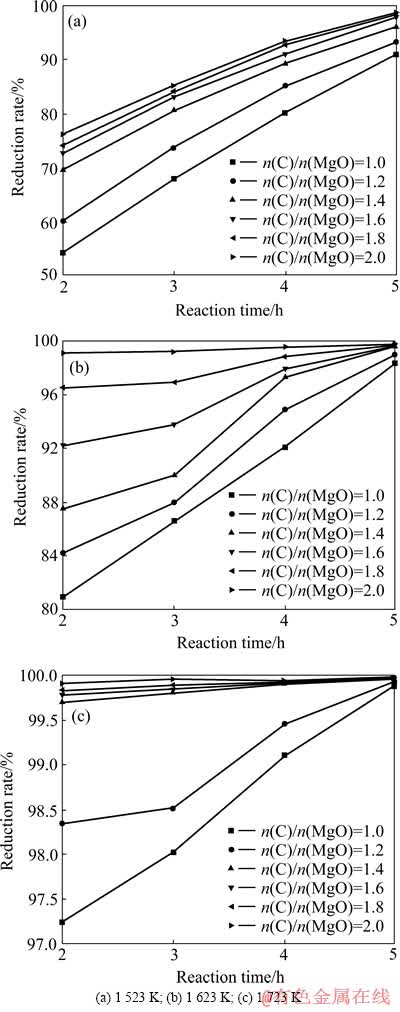
ͼ2 ��ͬ��ԭ�¶Ȳ�ͬ��ú������þĦ����ʱ��ԭ���뷴Ӧʱ��Ĺ�ϵ
Fig. 2 Relationship between reduction rate and reduction time under different temperatures and molar ratio of C to MgO
��ͼ2(b)��֪����1 523 K�����µĻ�ԭ�ʱ仯����һ�£��ڱ���ʱ����ͬ������£�������̼��(n(C)/n(MgO))�����ӣ�����þ��ԭ��Ҳ�����ӡ�ͬ��������ͬ��̼��(n(C)/n(MgO))�����£����Ż�ԭʱ����ӳ�������þ��ԭ�����ӡ�����̼��(n(C)/n(MgO))ֵ����1.6�Ժ�����þ��ԭ�ʾ�����90%����ԭ��Ӧ���г�֡�
��ͼ2(c)��֪������þ��ԭ�ʵ����ӹ�����ǰ�������¶������µ�ʵ�������һ�µģ��������ڻ�ԭ�¶Ƚϸߣ�����������̼��ԭ����þ�ķ�Ӧ�������⣬̼��ԭ����þ����̼���Ƶķ�ӦҲͬ�����г�֣��������ɵ�̼����Ҳ���뵽����þ�Ļ�ԭ�����У�ʹ������þ��ԭ��Ӧ���еó�֡����ס���ͼ�л����Կ���������̼��(n(C)/n(MgO))ֵ����1����ԭʱ���Ϊ2 hʱ������þ��ԭ�ʳ���97%������̼��(n(C)/ n(MgO))ֵ����1.4ʱ������þ��ԭ�ʾ�����99%������������þ������ȫ����ԭ����ԭ��Ӧ���г��ס�
2.3 ��ԭ�����������X�����������
������5% CaF2��n(C)/n(MgO)=2�����ϣ��ڲ�ͬ��ԭ�¶ȡ���ͬ����ʱ��������£���Ӧ��������ʣ�ԭ������X������������������ͼ3��ʾ��
��ͼ3(a)���Կ������Ѱ�̼�Ȼ�ԭ��Ӧ������������ʣ������ҪΪ�ƵĻ����������ǿ�弰��������������ǿ���Ӧ�����Ѱ��к��е�CaO����������CaO�ڷ�Ӧ���������ɵĹ����λ������Լ�ˮ�����ɵ�Ca(OH)2������֮�⣬���л�ԭ������δ��Ӧ�Ļ�ԭ��C���Ѱ��е�MgO�����ɵĹ���þ�Լ����ӵĴ���CaF2���ԱȲ�ͬ����ʱ�������µ�XRD�������Կ��������ű���ʱ����ӳ�����ԭ��Ӧ���г�֣�����ʱ�䳬��4 h��ԭ����MgO������þ��������������ֲ���ʧ��
��ͼ3(b)���Կ������Ѱ�̼�Ȼ�ԭ��Ӧ������������ʣ������ҪҲ�ǸƵĻ����������ǿ�弰��������������ǿ���Ӧ�����Ѱ��к��е�CaO����������CaO�ڷ�Ӧ���������ɵĹ����λ������Լ�ˮ�����ɵ�Ca(OH)2������֮�⣬���л�ԭ������δ��Ӧ�Ļ�ԭ��C�Լ����ӵĴ���CaF2�����ǰ�������֪�����ڻ�ԭ�¶ȵ�����������̼�Ȼ�ԭ��Ӧ�Ľ��У�MgO����ֻ�ԭ���ʻ�ԭ���м�ⲻ��MgO������þ���ԱȲ�ͬ����ʱ�������µ�XRD�������Կ��������ű���ʱ����ӳ���������C�Ļ�ԭ������ʱ�䳬��4 h��������ʣ�����м�ⲻ��C����ԭ��Ӧ��֡�
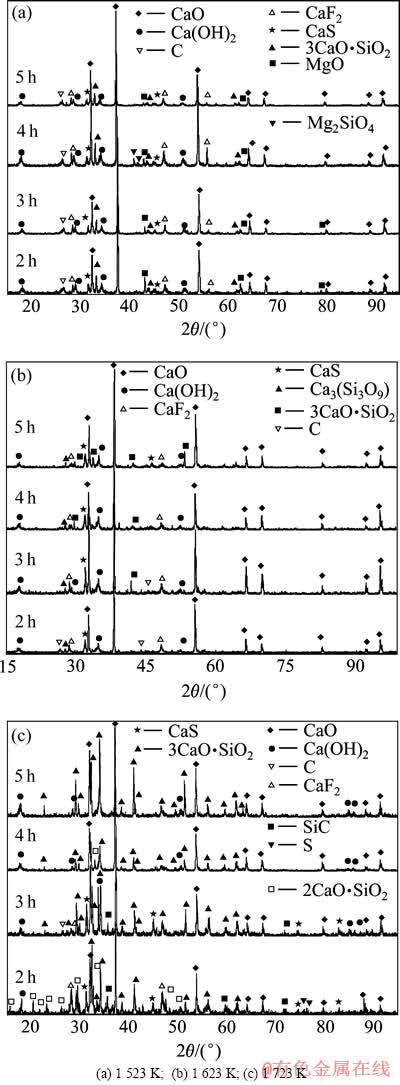
ͼ3 ��ͬ��ԭ�¶ȡ���Ӧʱ���»�ԭ����XRD��
Fig. 3 XRD patterns of reduction residual under condition of different reduction temperatures and reaction times
��ͼ3(c)���Կ������Ѱ�̼�Ȼ�ԭ��Ӧ������������ʣ����ͬ����Ҫ�ǸƵĻ����������ǿ�弰��������������ǿ���Ӧ�����Ѱ��к��е�CaO����������CaO�ڷ�Ӧ���������ɵĹ����λ������Լ�ˮ�����ɵ�Ca(OH)2������֮�⣬���л�ԭ���������ӵĴ���CaF2������SiC�����������ڸ��������µ�̼�ȷ�ԭ��Ӧ�����У���ԭ��C���Ѱ���SiO2��Ӧ���ɵġ����ǰ�������֪�����ڻ�ԭ�¶ȵ����ߣ�������̼�Ȼ�ԭ��Ӧ�Ľ��У�MgO��ֱ���ԭ���ʻ�ԭ���м�ⲻ��MgO��C�Լ�����þ������塣
ͼ4��ʾΪ��Ӧ��õ������������Ƭ����ͼ4��֪�����Ͼ���̼�Ȼ�ԭ��Ӧ�����ɵĽ���þ�������������ᾧ�������õ��˽ϴ�Ŀ�״����þ������������ò���Կ�����������ṹ���ܣ����ͽϺá�
ͼ5��ʾΪ�������XRD�ס���ͼ5���Կ��������������ռ�������������ҪΪ����Mg��������ǿ�弸�����ǽ���Mg������壬˵��MgO����̼�Ȼ�ԭ�����ɽ���þ�������������õ���Ч�ռ�����ԭЧ�����á�ͨ������忴������������MgO���ڣ��������ڽ���Mg��CO�����������淴Ӧ���������ɵ�[14]�����⣬�������м�Mg(OH)2�����������淴Ӧ���ɵ�MgO���������¶Ƚ�����ȴ��������ˮ�������ɵġ�

ͼ4 ��Ӧ��õ�����������Ƭ
Fig. 4 Photograph of condensation product after reaction
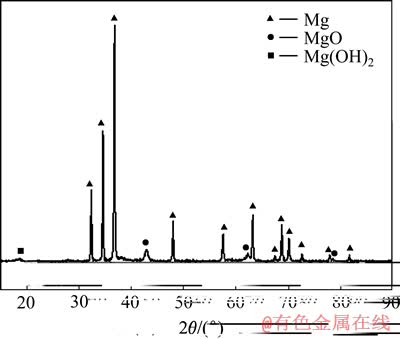
ͼ5 �������XRD��
Fig. 5 XRD pattern of condensation products
ͼ6��ʾΪ�Ѱ����̼�Ȼ�ԭ�¶�1 623 K����ԭʱ��3 h�����µõ��������SEM��ͼ6�п��Կ�����Mg�ʿ�״�ᾧ����ò�Ϻã��ṹ���ܡ���EDS�������������к�Mg 97.78%��O 2.22%(��������)������Mg���Ƚϸߣ��������������������ã��������в�δ����K��Na�����ʣ�����Mg�������������ʵõ�����Ч�ķ��롣

ͼ6 ���������SEM��
Fig. 6 SEM image of condensation products
3 ����
1) ͨ�����Ѱ����̼�Ȼ�ԭ���յ��о���������ϵͳѹ��30~100 Pa�����£���ԭ�¶ȵ������������Ѱ���MgO�Ļ�ԭ���¶ȴﵽ1 723 Kʱ���Ѱ���MgO����ȫ����ԭ������ʱ����ӳ��Լ���ԭ��̼����̼�ȵ����Ӿ�������̼�Ȼ�ԭ��Ӧ�Ľ��С����XRD�������Ѱ�������þ�Ļ�ԭ�ʣ������жϻ�ԭ�¶ȸ���1 623 K������ʱ��ﵽ4 h���ϡ���̼��Ϊ1.6ʱ��̼�Ȼ�ԭ��Ӧ���г��ף�MgO��ԭ�ʳ���99%��
2) �������ò���Կ����������ռ�����������Ľṹ���ܣ����ͽϺá�ͨ�����������X�������估ɨ��羵������֪���������̵õ��Ľ���ΪMg���Ҵ��Ƚϸߡ������ڽ���þ��CO�������淴Ӧ���ɵ�MgO����ͨ����һ��������������Ч���롣
REFERENCES
[1] MORDIKE B L, EBEN T. Magnesium properties-application- potential[J]. Materials Science Engineering A, 2001, 302: 37-45.
[2] �� ��. ����þ���̼�Ȼ�ԭ����þ����������ʵ���о�[D]. ����: ����������ѧ, 2012.
TIAN Yang. Basic theory and experimental research on magnesia carbothermal reduction in vacuum[D]. Kunming: Kunming University of Science and Technology, 2012.
[3] ����ƽ, ������, ������, ��Ծ��, ��С��, ������. CaC2��ԭMgO����ѧ������ʵ���о�[J]. ��տ�ѧ�뼼��ѧ��, 2009, 29(6): 637-640.
PENG Jian-ping, FENG Nai-xiang, CHEN Shi-dong, DI Yue-zhong, WU Xiao-lei, HU Wen-xin. Experimental and thermodynamical studies of MgO reduction with calcium carbide[J]. Chinese Journal of Vacuum Science and Technology, 2009, 29(6): 637-640.
[4] MINIC D, MANASIJEVIC D, DOKIC J, ZIVKOYIC D, SILICOTHERMIC Z Z. Silicothermic reduction process in magnesium production[J]. Journal of Thermal Analysis and Calorimetry, 2008, 93(2): 411-415.
[5] �ܳʻ�, ������, �� ��, лˮ��. �ҹ����ȷ���þ��״����չ����[J]. �����, 2005(11): 49-51.
XIONG Cheng-hui, ZHOU Tian-rui, XU He, XIE Shui-sheng. The status quo and developmental tendency of smelting magnesium by means of heating silicon in china[J]. Light Metals, 2005(11): 49-51.
[6] ������, ��. ����̼��ԭ������þ�����������¹����о�[J]. ������ɫ����, 2007(1): 53-55.
LI Xiao-bo, YIN Jian-hua. Studies on new craft of manufacturing magnesium and alumina by carbon reduction method[J]. World Nonferrous Metals, 2007(1): 53-55.
[7] �����, �ι�ǿ, ���, ��˼Զ, ���ں�. ��������ѧ��������ʯ�ж�������Թ��ȷ���þ��Ӱ��[J]. �й���ɫ����ѧ��, 2011, 21(12): 3129-3136.
DOU Shao-xu, YOU Guo-qiang, LI Ai-ting, LONG Si-yuan, ZHANG Zong-he. Thermodynamics analysis effect of silicon dioxide in dolomite on magnesium production by silicothermic process[J]. The Chinese Journal of Nonferrous Metals, 2011, 21(12): 3129-3136.
[8] BROOKS G, NAGLE M, TASSIOS S, TRANG S. The physical chemistry of the carbothermic route to magnesium in magnesium technology[C]// TMS Annual Meeting. San Diego: The Minerals, Metals and Materials Society, 2006: 25-31.
[9] PRENTICE L, NAGLE M. Mechanism and kinetics of reduction of magnesium oxide with carbon in magnesium technology[C]// TMS Annual Meeting. San Francisco: The Minerals, Metals, and Materials Society, 2009: 35-39.
[10] PRENTICE L. Psuedo-steady-state control of high temperature gas-solid reaction in Chemeca2011[C]// TMS Annual Meeting. Sydney, Australia: Engineers Australia, 2011: 1-9.
[11] ��־��. �����ú��ԭ����þ���о�[D]. ����: ����������ѧ, 2004.
LI Zhi-hua. Study on MgO reduction by coal in vacuum[D]. Kunming: Kunming University of Science and Technology, 2004.
[12] �� ʤ. ����þ���̼�Ȼ�ԭ�о�[D]. ����: ����������ѧ, 1999.
ZHONG Sheng. Study on magnesia carbothermal reduction in vacuum[D]. Kunming: Kunming University of Science and Technology, 1999.
[13] ������. ���̼�ȷ�ұ������þ��ʵ���о�[D]. ����: ����������ѧ, 2008.
LIU Hong-xiang. Study on the method of carbothermal reduction making magnesium in vacuum[D]. Kunming: Kunming University of Science and Technology, 2008.
[14] BROOKS G, TRANG S, WITT P, KHAN M N H, NAGLE M. The carbothermic route to magnesium[J]. JOM, 2006, 58(5): 51-55.
(�༭ ����)
������Ŀ������ʡ�Ƽ��ƻ�������Ŀ(S2012FZ0110)
�ո����ڣ�2012-10-10�������ڣ�2013-07-01
ͨ�����ߣ��������ڼ�������ʦ���绰��13608858239��E-mail: lcd_2002@sohu.com
ժ Ҫ��������������þ��ԭ�ʡ�XRD��SEM���ֶ��뷽���о�����������Ѱ�̼�Ȼ�ԭ�¶ȡ�������ȡ�̼�Ȼ�ԭ����ʱ��ȶ�̼�Ȼ�ԭ�Ѱ���ȡ����þ���յ�Ӱ�졣�����������30~100 Paʱ��̼�Ȼ�ԭ�¶ȸ���1 623 K������þ�Ļ�ԭ���������ӣ�������̼�Ȼ�ԭ��Ӧ�Ľ��С����Ž�ú��ԭ��������þĦ���ȵ������Լ�̼�Ȼ�ԭʱ����ӳ���̼�Ȼ�ԭ��Ӧ��Ӧ���ʼӴ�ԭ����ߣ���̼�Ȼ�ԭ�¶�Ϊ1 623 K����ԭʱ��Ϊ4 h����̼��Ϊ1.6ʱ������þ��ԭ�ʳ���99%����ˣ�ѡ���ʵ��Ľ�ú��ԭ��������þĦ����ֵ�Լ�̼�Ȼ�ԭʱ�䣬���¶ȸ���1 623 K�����£���������̼�Ȼ�ԭ����þ���̵�˳������������þ��ԭ�ʵ���ߡ�
[2] �� ��. ����þ���̼�Ȼ�ԭ����þ����������ʵ���о�[D]. ����: ����������ѧ, 2012.
[5] �ܳʻ�, ������, �� ��, лˮ��. �ҹ����ȷ���þ��״����չ����[J]. �����, 2005(11): 49-51.
[6] ������, ��. ����̼��ԭ������þ�����������¹����о�[J]. ������ɫ����, 2007(1): 53-55.
[11] ��־��. �����ú��ԭ����þ���о�[D]. ����: ����������ѧ, 2004.
[12] �� ʤ. ����þ���̼�Ȼ�ԭ�о�[D]. ����: ����������ѧ, 1999.
[13] ������. ���̼�ȷ�ұ������þ��ʵ���о�[D]. ����: ����������ѧ, 2008.


