���±�ţ�1004-0609(2010)S1-s1030-04
�����λ�����Һ��Ti-24Nb-4Zr-8Sn�Ͻ�ĵ绯ѧ��ʴ��Ϊ
�� ܿ1��������1��������1���� ��1��������2
(1. �й���ѧԺ �����о��� �������Ͽ�ѧ����(����)ʵ���ң����� 110016��
2. �ش�ѧѧԺ ��ѧѧԺ���� WC1H 0AJ)
ժ Ҫ��
���ÿ�·��λ����������λ�������߲����ȷ����о�ҽ�æ��ѺϽ�Ti-24Nb-4Zr-8Sn��ģ��������Һ�еĵ绯ѧ��ʴ��Ϊ������úϽ���ģ��������Һ�еĸ�ʴ��λ(��corr)����ʴ��λ(��pit)����ʴ����(Icorr)���ۻ�����(Ipass)��һϵ�е绯ѧ���������봿�Ѻ�Ti-6Al-4V�Ͻ���бȽϡ�����������봿�Ѻ�Ti-6Al-4V�Ͻ���ȣ�ģ��������Һ��Ti-24Nb-4Zr-8Sn�Ͻ��ܹ�Ѹ���γɱ���������Ĥ���伫�����߾��и�Ϊ�����Ķۻ���λ���䣬�ۻ�Ĥ״̬��Ϊ�ȶ�����ʴ��λ(��corr)�Ϳ�ʴ��λ(��pit)���ϴ�ʴ����(Icorr)��С�����ۻ�����(Ipass)��ӹ������еı���ȱ�ݳ�Ϊ��ʴ�Ļ���λ�á�
�ؼ��ʣ�
Ti-24Nb-4Zr-8Sn�Ͻ��������λ�����Һ����ʴ��Ϊ����·��λ������������
��ͼ����ţ�TG 146.2+3���� ���ױ�־�룺A
Electrochemical corrosion behavior of Ti-24Nb-4Zr-8Sn in phosphate buffer saline solutions
BAI Yun1, LI Shu-jun1, HAO Yu-lin1, YANG Rui1, GUO Zheng-xiao2
(1. Shenyang National Laboratory for Materials Science, Institute of Metal Research, Chinese Academy of Sciences,
Shenyang 110016, China;
2. Department of Chemistry, University College London, London WC1H 0AJ U.K.)
Abstract: The electrochemical corrosion behavior of Ti-24Nb-4Zr-8Sn alloy in phosphate buffer saline (PBS) solutions was investigated by studying open-circuit potential and potentiodynamic polarization curve. The corrosion potential (��corr), pitting potential (��pit), corrosion rate (Icorr) and passive current density (Ipass) were also evaluated and compared with those of purity titanium and Ti-6Al-4V alloy. The results show that the oxide film forms on Ti-24Nb-4Zr-8Sn quickly once it is put into PBS. The passivation region of this alloy in PBS is more extensive than that of pure titanium and Ti-6Al-4V alloy and its passivation-film is most stable. It shows higher ��corr and ��pit and lower Icorr values compared to another two materials, but its Ipass is the highest. Pre-existed surface defects on Ti-24Nb-4Zr-8Sn might be the preferred locations for corrosion.
Key words: Ti-24Nb-4Zr-8Sn alloy; phosphate buffer saline solutions; corrosion behavior; open-circuit potential; polarization curve
�Ѽ���Ͻ����ھ��нϵ͵��ܶȡ����õ���ʴ���ܡ��߱�ǿ�ȡ��ӽ����˹ǵĵ���ģ���Լ����õ����������Զ�����Ϊҽ��ֲ����Ϸ�����ʾ��Խ��Խ�����Խ��[1-2]��Ŀǰ��������(CP Ti)�⣬�ٴ�Ӧ����Ϊ�㷺���ѺϽ�ΪTi6Al4V(TC4)[3-4]�����úϽ��к����ж�Ԫ��V[5]�����䵯��ģ��Զ�����˹ǵģ�������ɽ���ֲ������ɶ���Ti-24Nb-4Zr-8Sn(Ti2448)�Ͻ��ǹ����½����Ƶ�һ��ҽ�æ��ѺϽ����������˹���֯����ĵ���ģ����ǿ�ȸߣ������ж�Ԫ�أ��dz��ʺ�����ҽѧֲ�����[6-7]��
�������鼰�ٴ�Ӧ���ж�������ֲ�������Χ����֯���ֺڻ�����ԭ�����Ѽ��Ͻ�Ԫ�ظ�ʴ�ܽ⣬����Χ��֯�в���Ũ����ʹϸ�����ԡ�һ���浼�¸�ʴ����������壬�������ص�����Σ��������֯������ϸ������ȣ���һ�������ֲ���������ѡ����ڶ��ѵ�ʧЧ��Ϊ��������һ�����临�ӡ����������������ֲ����ѺϽ��������Ҫ��������Һ��ø��ϸ�������ɻ����л�����ӵȽӴ���������Щ�Ӵ��������������������ĸı����ʱ�����仯��ѪҺ��������pH��С�����������ӡ�����ȱ���Ļ����Լ����ֵ�����ø�����öԲ��ϵ���ʴ��Ӱ�춼�ܴ���ˣ��о�ֲ�������������Һ�ĸ�ʴ��Ϊ������Ҫ��
�������߲���ģ��������Һ(PBS)��Ϊ��ʴ���ʣ�������ģ�����ﻷ������Ti2448�Ͻ�ĵ绯ѧ��ʴ��Ϊ�����о�������CP Ti��TC4�Ͻ���бȽϡ�
1 ʵ��
�Դ���Ϊ99.6%�ĺ���Ti��99.25%��Nbм��99.4%�ĺ���Zr��TiSn�м�Ͻ�Ϊԭ�ϣ���������Ժĵ绡¯3�������Ʊ�Ti2448�Ͻ���������������850 ���������ȶͳɰ廵��Ȼ�廵��750 ���ȴ���1 h�����䡣���ȴ�����IJ����и�ɳߴ�Ϊ10 mm��10 mm��5 mm�Ŀ�״��Ʒ�����������ӵ�Ti2448�Ͻ���Ʒ�ϣ������������ಿ�־��û�����֬�ܷ⣬����������Ϊ1 cm2����ȷ�����߲����븯ʴҺ�Ӵ�����Ʒ��Ԥĥ������SiCɰֽ��ĥ������ĥ��2000#��Ȼ����������������ֱ��ñ�ͪ����ˮ�Ҵ���ȥ����ˮ������ϴ����紵�ɺ������������á�CP Ti��TC4�Ͻ���Ʒͬ���Ƴɳߴ�Ϊ10 mm��10 mm��5 mm�Ŀ�״�����������������ĥ���⡢��ϴ���á�
PBS�����ΪNaCl 8.0 g��KCl 0.2 g��Na2HPO4��
12H2O 2.9 g��KH2PO4 0.2 g������ˮ1 L����HCl��NaOH��Һ��pH����Ϊ7.4���������Ȼ����������ʵ���¶�Ϊ37 �档
����2273�ͺ��λ��(EG&G PAR)�ⶨ�����绯ѧ��ʴ���ܣ�����Ϊ���缫ϵͳ������Ϊ�����缫��������Ƭ�������缫(������ڹ����缫)������KCl�ʹ��缫(SCE)Ϊ�αȵ缫������������������ȶ�1 h��ÿ�β����������µĹ����缫��
��������������п�ʼ��·��λ��������� 60 ks���������߲�����0.667 mV/s��ɨ�����ʴ�-1.0 V (vs OCP)��3.0 V (vs SCE)������SEM(Hitachis��3400N��)�۲츯ʴ��ı�����ò��
2 ���������
Ti2448�Ͻ�CP Ti��TC4��3�ֲ�����PBS�еĿ�·��λ��ʱ��ı仯������ͼ1��ʾ����ͼ1���Կ�����Ti2448�Ͻ���뵽PBS��Һ�к��λѸ�����ߣ�������н��ͣ���ʱ��ﵽ5 000 sʱ�������ȶ���-160 mV��CP Tiͬ������һ����λ��ʱ��������ӵĹ��̣�֮��ܿ�(1 100 s)�ȶ���-170 mV����TC4�Ͻ�Ŀ�·��λ�Ⱦ���һ��С�Ľ����̺�Ҳ�������ߣ���ʱ��ﵽ5 900 sʱ������ȶ���-210 mV����ˣ�Ti2448�Ŀ�·��λ�Ը���CP Ti��TC4�ġ�
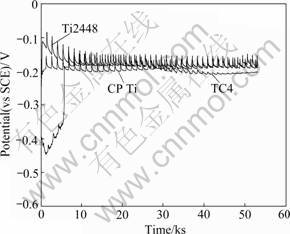
ͼ1 3�ֲ�����37 �������PBS��Һ�п�·��λ��ʱ��ı仯����
Fig.1 Open-circuit electrode potential as function of time for three materials in aerated PBS at 37 ��
����Ȼ���������У���·��λ��������������������(������Ӧ)�������ߵĽ����λ[8]������ʱ������ӣ��ۻ�ĤԽ��Խ����֮��������ǿ����ʱ�������������ߵĽ���λ��Ҳ���Ž���ۻ���������ƣ����ۻ�Ĥ�ı������ôﵽ����λ��ʱ���Ը�ʴ��λ�ʹﵽ�ȶ�ֵ���ɴ˿����ж�Ti2448��CP Ti��PBS��Һ������Ĥ�������ٶ��൱����Ҫ��TC4�Ͻ�Ŀ죬��������Ĥ���ɵij���ʱ��Ҫ�������Դﵽ���״̬���ȶ��Ը�ʴ��λҲ�Ը���TC4�Ͻ�ġ�
ͼ2������3�ֲ�����37 ����Ȼ������PBS��Һ�еĶ���λ�������ߣ���ͼ2�п��Կ�����3�ֲ�����PBS��Һ�ж����ֳ����ԵĻ���ۻ���Ϊ��Ti2448�Ͻ�ĵ����ܶ����ŵ�λ��-430 mV�仯��-118 mV��Ѹ�����ӣ���ʱ�ﵽ3.930 ��A/cm2��������һ��ֵһֱά�ֲ��䣬ֱ����λ�ﵽ1.072 V��Ҳ���ǵ�ʴ��λ��pit��Ԥʾ�Ͻ���뵽�ۻ�״̬�������1.072��1.559 V�ڣ������ܶ��ٴ����ŵ�λ����������ӣ�����λ�ﵽ1.559 V�Ժ�Ti2448�Ͻ���뵽�ڶ��ζۻ����̣���ʱ�Ķۻ�����Ϊ5.96 ��A/cm2���������ֶۻ�״̬һֱ������ɨ�������3.0 V��ͬʱ�����Կ��������������ܶ����λ��������ӵ�������ֱ�߶ε�б��������ͬ����CP Ti��TC4�Ͻ���������Һ�еĸ�ʴ��Ϊ���������߽��뵽һ�ζۻ�����ĵ�λ��Ҫ��Ti2448�ĸ���һЩ���ֱ���-61 mV��-86 mV�����ǵĦ�pit�ֱ�Ϊ523 mV��506 mV�����Ǵ���һ�ζۻ�����ĵ����ܶ�ҲҪ��Ti2448��СһЩ���ֱ���2.179 ��A/cm2��1.898 ��A/cm2��
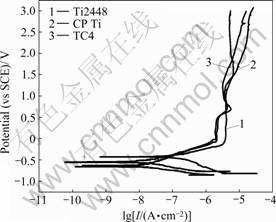
ͼ2 3�ֲ�����37 �������PBS��Һ�еĶ���λ��������
Fig.2 Polarization curves for three materials in aerated PBS at 37 ��
��1����Ϊ�ɼ�����������ĵ绯ѧ��ʴ��������ʴ��λ(��corr)�ɸߵ��͵�˳����Ti2448��CP Ti��TC4����ʴ����(Icorr)�ɴ�С��˳����TC4��CP Ti��Ti2448��
�Ը�ʴ��λ�Ǹ�ʴ��ϵ������Ӽ��������µ��ȶ���λ����һ������ӳ���ϵ�����ѧ���Ժ͵缫�ı�
��1 3�ֺϽ���37 ����Ȼ������PBS��Һ�е绯ѧ��ʴ����
Table 1 Corrosion parameters of three materials in aerated PBS at 37 ��

��״̬[9]����������ѧԭ������corrԽ�ͣ���ʴ����Խ��corrԽ�ߣ���ʴ����ԽС�����ԣ�����һ�Ƕȶ��ԣ�Ti2448��CP Ti��TC4�Ͻ���PBS��Һ�еĸ�ʴ������TC4���Ti2448��С������ʴ����������������ѧ���룬ֻ��˵����ʴ���������׳̶ȣ����������ڽ����еķ�Ӧ����Ҫ��ʵ�ʷ�����Ӧ��Icorr�Ĵ�С��Ҳ���Ƕ���ѧ�����ϵ��ٶȣ�Icorr����˵����ʴ��Ӧ�ٶȿ죬�̶�����Դ�Icorr�ĽǶ��жϣ���3�ֲ����У�Ti2448�ĸ�ʴ�ٶ���С��Ӧ�������ڼ������ܹ��������ʴ���ܵ�Ԫ��Nb��Zr��
����һ����ʴ��ϵ�Ķۻ���Ϊ�����Դ������Ƕȿ��ǣ�1) �Ƿ�������ۻ�״̬���Ƿ����״ӻ״̬ת��Ϊ�ۻ�״̬�����ж���һ��ΪҪ������������һ���Ƕۻ������ܶ�(Ipass)�Ĵ�С����һ���ǽ���ۻ�״̬��λ�ĸߵͣ�2)�ۻ�״̬�Ƿ��ȶ���Ҫ��ά�ֶۻ�״̬�ĵ�λ���伴������ʴ�ĵ�λ(��pit)�������ۻ������λ�IJ�ֵ�Ƿ����һ��ֵԽ�ۻ�״̬���ȶ���Խ�ߣ��ۻ�ĤԽ��������ƻ�[10]����PBS��Һ�У�Ti2448��CP Ti��TC4�Ͻ�ӻ״̬���뵽һ�ζۻ�״̬�ĵ�λֵ�ֱ�Ϊ-118��-61��-86 mV��Ti2448�ĵ�λֵ��ӽ��ڦ�corr�������������ֲ��ϸ����״ӻ״̬���뵽�ۻ�״̬�������ڶۻ�״̬��3�ֲ��ϵĵ����ܶ�Ipass�ֱ�Ϊ3.930��2.179��1.898 ��A/cm2��Ti2448��IpassҪ�Ը��ں����ߵġ�MAAN��[11]�о�������Ipass�Ĵ�С����ϱ���ۻ�Ĥ�Ŀ�϶���йأ���һ��ֵԽ���ʾ���ϵıȱ����Խ����ô��������������Ҳ��Խ�ߣ���ˣ�Ti2448��Ipass��Ȼ�Ըߣ������ʺ�Ӧ����������ֲ����ϡ�3�ֲ��Ϧ�pit�����ۻ�����ĵ�λ��ֵ�Ĵ�С�ֱ�Ϊ1.296��0.589��0.592 V�����ԣ�Ti2448�Ķۻ���λ����ҪԶ�����������ֲ��ϵģ�������ò��ϵĶۻ�״̬��Ϊ�ȶ����ٴδӶۻ�״̬ת��Ϊ�״̬������ѡ�
ͼ3��ʾΪTi2448��37 ����Ȼ������PBS��Һ�ж���λ������ĸ�ʴ������ò����ͼ3���Թ۲쵽����ʴ��ı����и����ʴ�����������Ҹ�ʴ���������ڼӹ����������µı���ȱ���ϣ�HUANG��[12]��ʵ��Ҳ�������ӹ��������γɵı���ȱ��ȷʵ���Ϊ��ʴ���ȷ����Ļ��Ե㡣���ԣ���ʵ�ʵ�ֲ��Ӧ�ù����У��Բ��ϵı���Ҫ���쳣�ϸ�

ͼ3 Ti2448��37 ����Ȼ������PBS��Һ�ж���λ������ĸ�ʴ������ò
Fig.3 Corrosion morphology of Ti2448 after potentiodynamic polarization in aerated PBS at 37 ��
3 ����
1) ��PBS��Һ�У�Ti2448�Ͻ�Ŀ�·��λ����ʱ��Ѹ�����ߣ�����ȶ���-160 mV������������Ѹ�����ɱ���������Ĥ��
2) ��CP Ti��TC4��ȣ���PBS��Һ�У�Ti2448���и�Ϊ�����Ķۻ���λ���䣬�ۻ�Ĥ״̬��Ϊ�ȶ�����ʴ��λ(��corr)�Ϳ�ʴ��λ(��pit)���ϴ�ʴ����(Icorr)��С�����ۻ�����(Ipass)���
3) ��ʴ��Ti2448�ı����п�ʴ�������ӹ������еı���ȱ���Ǹ�ʴ���ȳ��ֵĻ���λ�á�
REFERENCES
[1] OHKUBO C, OHKUBO C, SHIMURA I, AOKI T, HANATANI S, HOSOI T, HATTORI M, ODA Y, OKA T.Wear resistance of experimental Ti-Cu alloy [J]. Biomaterials, 2003, 24(20): 3377-3381.
[2] VANNOORT R. The implant material of today [J]. Journal of Materials Science, 1987, 22(11): 3801-3811.
[3] LONG M, RACK H J. Titanium alloys in total joint replacement��A materials science perspective [J]. Biomaterals, 1998, 19(18): 1621-1639.
[4] ������, �� ��, ���Ľ�, ������, ţ����, Ԭ˼��, ���Ƿ�, �ʸ�ǿ, ���ٻ�. ����Ӳ��֯����������ѺϽ���ϵĿ�����Ӧ��[J].���ܲ���, 2006, 37(6): 664-670.
YU Zhen-tao, ZHOU Lian, HE Xin-jie, LUO Li-juan, NIU Jin-long, YUAN Si-bo, ZHANG YA-feng, HUANG Fu-qiang, LIU Shao-hui. Development and application on Ti alloy material used in human hard tissue [J]. Journal of Functional Materials, 2006, 37(6): 664-670.
[5] ����ƽ, ��˼��, ������. �������ѺϽ��о���״[J].ϡ�н��������빤��, 2004, 33(12): 1243-1250.
ZHANG Xin-ping, YU Si-rong, HE Zhen-ming. The present status of study of Ti alloy for dentistry [J]. Rare Metal Materials and Engineering, 2004, 33(12): 1243-1250.
[6] HAO Yu-lin, LI Shu-jun, SUN Su-ying, ZHENG Cai-yun, HU Qing-miao,YANG Rui. Super-elastic titanium alloy with unstable plastic deformation [J]. Applied Physics Letters, 2005, 87: 91-93.
[7] HAO Yu-lin, LI Shu-jun, SUN Su-ying, ZHENG Cai-yun, YANG Rui. Elastic deformation behaviour of Ti-24Nb-4Zr-7.9Sn for biomedical applications [J]. Acta Biomaterialia, 2007, 3(12): 277-286.
[8] LAVOS-VALERETO I C, COSTA I, WOLYNEC S. The electro-chemical behaviour of Ti-6Al-7Nb alloy with and without plasma sprayed hydroxyapatite coationg in Hank��s solution [J]. Journal of Biomedical Materials Research, 2002, 63(5): 664-670.
[9] �� ��. ����ҽ���ѺϽ�TZNT��е������ʴ���ܼ������������ܵ��о�[D]. ����: ������ѧ����ѧԺ, 2002: 56-58.
LI Jun. The research on mechanical properties, corrosion resistance and biocompatibility of a new type TZNT alloy [D]. Shenyang: Northeastern University, School of Materials, 2002: 56-58.
[10] ������, �� ��. ҽ���ѺϽ�ķ�չ���о���״[J]. ���Ͽ�ѧ�빤��, 2002, 10(1): 100-111.
NING Cong-qin, ZHOU Yu. Development and research status of biomedical titanium alloys [J]. Materials Science and Technology, 2002, 10(1): 100-111.
[11] MAAN A-K, KENNETH G, FENELON ANNA M, FARRELL T, BRESLIN CARMEL B. Electrochemical studies on the stability and corrosion resistance of titanium-based implant materials [J]. Biomaterials, 2001, 22(12): 1531-1539.
[12] HUANG H H, CHIU Y H, LEE T H, WU S C, YANG H W, SU K H, HSU C C. Ion release from NiTi orthodontic wires in artificial saliva with various acidities [J]. Biomaterials, 2003, 24(20): 3585-3592.
������Ŀ��������Ȼ��ѧ����������Ŀ(50631030��50901080)������ʡ��Ȼ��ѧ����������Ŀ(20092075)
ͨ�����ߣ������գ��о�Ա����ʿ���绰��024-83978841��E-mail��ylhao@imr.ac.cn


