��ѧ�Ʋ����Ʊ����ӽ���Ĥȼ�ϵ��Ĥ�缫
�й���ѧԺ�Ϻ�ұ���о���!�Ϻ�200050,������ɫ�����о���Ժ!����100088,����������ѧ!����100081
ժ Ҫ��
�û�ѧ�Ʋ����Ʊ����ӽ���Ĥȼ�ϵ��Ĥ�缫 , �����Ĥ�缫���۽ṹģ�ͼ�Ĥ�缫�Ļ�ѧ�Ʋ�������ͨ������Ʋ����ն�Ĥ�缫���ܵ�Ӱ�� , ȷ���˻�ѧ�Ʋ����Ʊ�Ĥ�缫����ѹ������� :��Nafion 117Ĥ�������ȶ���һ�㲬 , ѹ��̼�ڻ�̼�ز� , Ȼ���õ�Ũ�ȵ����Ȳ����Ũ�ȵ�����Һ��ѧ�Ʋ���
�ؼ��ʣ�
��ͼ����ţ� TM911.48
�ո����ڣ�1999-05-25
Preparation of Membrane Electrode Assembly of Proton Exchange Membrane Fuel Cell by Chemical Platinum Deposition
Abstract��
The MEAs of PEMFC were made with the method of chemical platinum deposition.The microstructure of MEA and the principle of chemical platinum deposition were described, the best method to manufacture the MEA of PEMFC was determined by studying the effect of deposition conditions on the property of MEA, that is, platinum was deposited chemically onto the surface of the membrane of Nafion117 and C or Pt/C was compacted onto it, then platinum was deposited chemically to the membrane with the solution of N 2H 4 and the solution of H 2PtCl 6 which are of equal equivalent concentration.
Keyword��
Proton exchange membrane fuel cell (PEMFC) ; Membrane electrode assembly (MEA) ; Chemical platinum deposition;
Received�� 1999-05-25
������, �������������������������, ����β�� CO2 �ȵ��ŷŲ����Ӿ�������ЧӦ, ���µ����¶�����, ����ֱ����в����������ĺͽ���;����, ���緶Χ�ڵ�ʯ����Դ�����Ͻߡ���Լ��Դ�����������ĺ���Խ��Խǿ�ҡ����, ����������ڿ�������������Ⱦ����Ч�ܵĵ綯����������, ���ӽ���Ĥȼ�ϵ�� (PEMFC) �ǵ綯��������Դ�����ѡ��, ��Ĥ�缫 (MEA) ���� PEMFC �����ಿ��, �����ܵ�����ֱ�ӹ�ϵ��ȼ�ϵ�ص��������ܡ�Ŀǰͨ�õ����ӽ���Ĥȼ�ϵ��Ĥ�缫���Ʊ�����
1 ʵ��
���ӽ���Ĥȼ�ϵ��Ĥ�缫���Ʊ�������Ҫ������������: (1) �����۵� Nafion 117 Ĥ�� H2O2 �� H2SO4 ���д����Գ�ȥ���е�����; (2) �� Nafion Һ��ճ�����̼�ز� (Pt/C) ��̼�����ڴ������� Nafion117 Ĥ�����ಢ����ѹ������ѹ; (3) ���Ȳ�����Һ������Һ�����ӽ���Ĥ���л�ѧ�Ʋ�������ʵ�������, Ϊ�˿���Ʋ����ն�Ĥ�缫���ܵ�Ӱ��, ������������Ա�ʵ��, �������� (2) �� (3) ���е�˳��������ͬ�����, �������������:
��һ��ʵ��:����Һ��Ũ��Ϊ�Ȳ�����Һ��10��
1# �缫 Nafion117 Ĥ����ֱ�ӻ�ѧ�Ʋ�
2# �缫 Nafion117 Ĥ����ѧ�Ʋ����κ�ѹ��̼���ٻ�ѧ�Ʋ�
3# �缫:Nafion117 Ĥ����ѹ��̼�ں�ѧ�Ʋ�
�ڶ���ʵ��:����Һ��Ũ�����Ȳ�����Һ���
4#�缫:Nafion117 Ĥ����ѹ��̼�ں�ѧ�Ʋ�
5#�缫:Nafion117 Ĥ����ѧ�Ʋ����κ�ѹ��̼���ٻ�ѧ�Ʋ�
6#�缫:Nafion117 Ĥ����ѹ��̼�ز� Pt/C ��ѧ�Ʋ�
���Ʊ��õ�Ĥ�缫�������̨��, һ��ͨH2, һ��ͨ O2 , �� H2��O2 ѹ����Ϊ 1.013��105 Pa ʱ������صĿ�·��ѹ Emax��0.6V ʱ�Ĺ������� I0.6V�Ͷ�·���� Imax, ������������Ʋ����� n �ı仯��ϵ���ߡ�
2 ���������
2.1 Ĥ�缫���۽ṹģ�ͼ��仯ѧ�Ʋ�����:
������ Nafion Һȡ�� PTFE ��Ϊճ����Ʊ����ӽ���Ĥȼ�ϵ��Ĥ�缫����Ϊ Nafion Һ�ľ���ת���¶�Ϊ 125��, ���� 125��Ϊ��̬, ���� 125��Ϊճ��״��Һ̬�����, �ڱ������õ���ѹ�¶� (��130��) ��Χ�� Nafion Ĥ������в����ۻ�̬�� Nafion ���뵽̼�ز� (Pt/C) ��̼�ڵķ�϶��, ������ѹ����ȡ����, ���뵽̼�ز� (Pt/C) ��̼�ڵķ�϶�е� Nafion ��ת��Ϊ�����ṹ�Ĺ�̬ Nafion, �������� Nafion ��ǿ��ճ���������� Pt/C �ι̵ؽ���� Nafion Ĥ������ʹ���㲻������, �������ڴ����е�ճ�ϼ����� Nafion �����ṩ��, ���ʹ�ô����е� Nafion �����ӽ���Ĥ�е� Nafion �γ����������Ӵ���ͨ����
���ӽ���Ĥ������ṹ���临��, ���ڶ��������ӽ���Ĥ�ṹ��������, ���Ӵ�����ģ�� (��ͼ1��ʾ) �Ǵ�ҹ��ϵ�һ��ģ��, �����Ӵؼ������ṹ��Ĥ�����Ӻ�ˮ����Ǩ�ƹ����е�Ψһͨ��
�����������, ���������Ĥ�缫����ľֲ�ģ��, ��ͼ2��ʾ��
ͼ1 ���Ӵ�����ģ��
�ڷŵ�Ĺ�����, ����������ͨ��ëϸ�� B ��������� (D��) �ı���, �ڲ���������ʧȥ�������� H+ �� H2O ������� H3O+, H3O+ ͨ�����Ӵ����� A �е�-SO-3 �IJ�㴫��, ��������������Nafion Ĥ, ���������Ĵ���������������, H3O+ �����Ӵ������е� -SO-3 �Ĵ��ݵ���̼����� D �㼴�������ı���, ��ëϸ���е� O2 ������� H2O ��ëϸ���ų���
��ѧ�Ʋ������ǽ����ӽ���Ĥ��������, ���߷ֱ�����Ȳ�����Һ������Һ, ʵ���� N2H5+ ����ͨ��Ĥ������ṹ�������������̼����̼���ز���λ����ëϸ���е� PtCl62- ��Ӧ���ɲ�������ؽ�, ���º��Ȳ�����Һ�����ӽ���Ĥ��ѧ�Ʋ��ķ�Ӧ�������� (�м�����ߴ������ӽ���Ĥ, ���߷ֱ�Ϊ����Һ���Ȳ�����Һ) :
����, �� H2H4 ˮ��ƽ��, �Ȳ��� H2PtCl6 ����ƽ��:
����, N2H5+�� H3O+ ��Ϊ������, ������ H3O+�����С, ��������ͨ�����ӽ���Ĥ�� OH-��Ӧ����ˮ:
ͼ2 Ĥ�缫����ľֲ�ģ��
A��Nafion ���Ӵ�����;B��ëϸ��;C��̼�ڿ���;D��̼���ز���λ��

���, ���� H3O+ ����ͨ�����ӽ���Ĥ, �µ�ˮ��ƽ������, Ĥ�������� H3O+ Ũ���ݶ���С, N2H5+ Ũ���ݶ�������, ��һ���̶Ⱥ�, N2H5+ ������ H3O+ ͨ�����ӽ���Ĥ�� PtCl
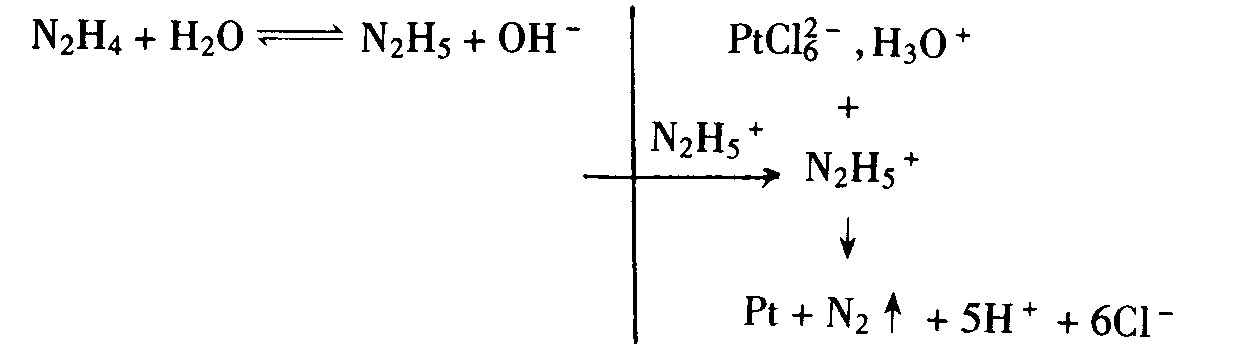
���ͼ2���Զ���˵���÷�Ӧ�ľ������:
�տ�ʼ, �Ȳ�����Һ�е� H3O+ ͨ��ëϸ�� B ���� -SO3- ���, �� H3O+ Ũ���ݶȵ�������, ��-SO3- ���ݵ�Ĥ����һ�ࡣ���, N2H5+ Ҳͬ�������ݹ���, ���� D ��ʱ��̼�� (��̼�����صIJ�) ������Ϊ��������, ��ëϸ���е� PtCl62- ��Ӧ���ɲ�ԭ��, ������̼�� (�����еIJ�) ���档Ȼ��, �����ɵIJ�ԭ����Ϊ��һ����Ӧ�Ļ�������, ��������, ������λ�ѧ�ƺ�ΪĤ�缫��
2.2 ��ѧ�Ʋ���缫������
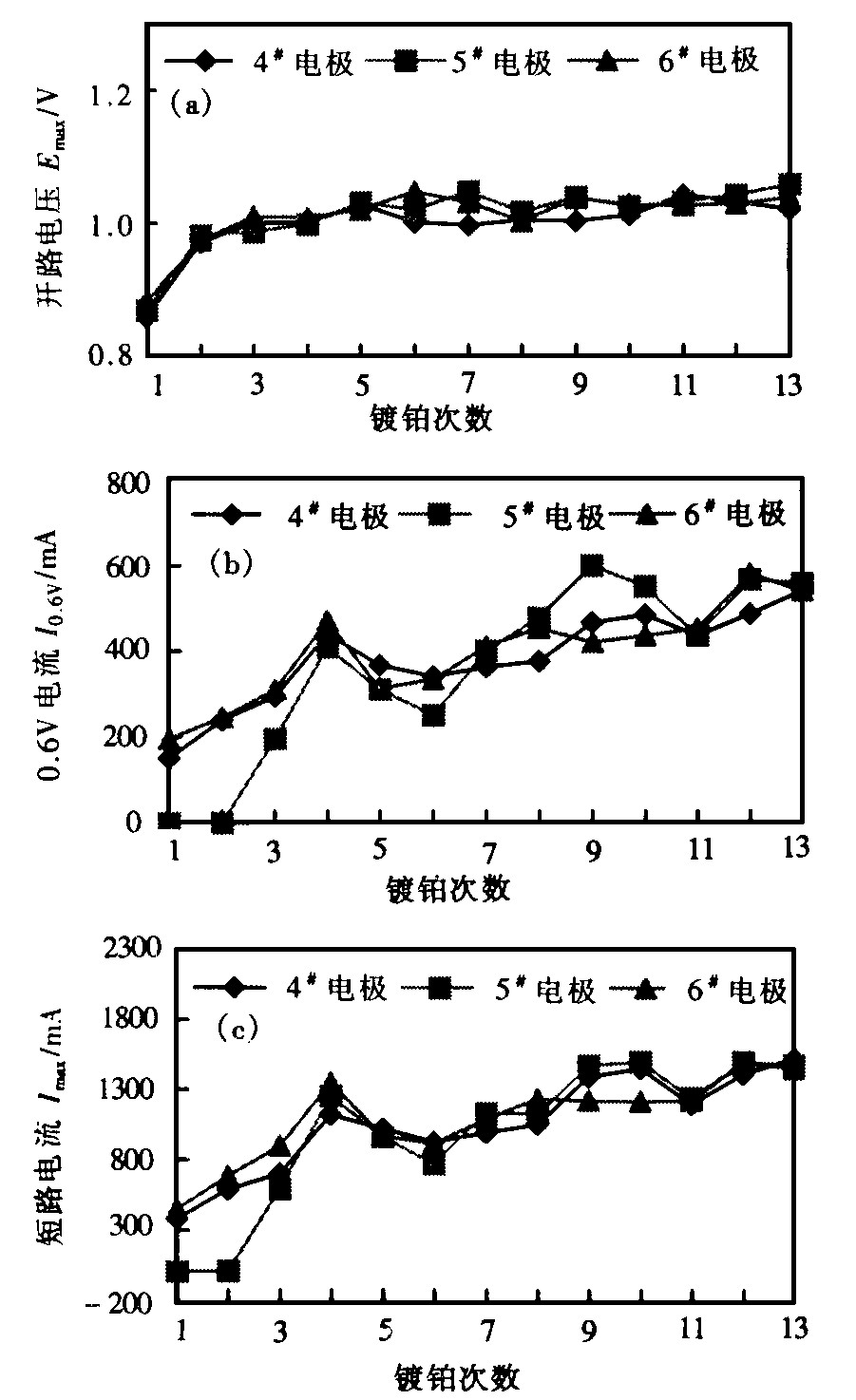
�Ա�ʵ���и��缫�� Emax��I0.6V��Imax ��Ʋ����� n �ı仯��ϵ��ͼ3��4��ʾ��
��ͼ3���Կ���, 1# �缫�Ŀ�·��ѹ Emax��0.6V �������� I0.6V�Ͷ�·���� Imax��Զ���� 2#��3# �缫, �������������ͼ2���Խ���:�ڶƲ��Ĺ�����, ���� 1# �缫, ���� N2H5+��Ĥ������ṹǨ�ƹ�����û������������, ֱ��Ĥ�ı�����뱾����Һ�е��Ȳ��ᷴӦ, �����IJ���Ϊ�Ժ�Ӧ�Ļ������ġ�����, ���ŶƲ�����������, Ĥ�ı����γ�һ�����ƽ������ۼ���һ��IJ�����Ȼ������������, ���ȱ���С, ���ұ������Ե�ط�Ӧ����û������, �������谭����Ĵ���, ��˵����dz�С���ɴ˿���, ��Ĥ����ֱ�ӶƲ�������ȡ��
ͼ3 ��һ��ʵ����缫������
(a) Emax��Ʋ������ı仯; (b) I0.6V��Ʋ������ı仯; (c) Imax��Ʋ������ı仯
�Ա�ʵ����, 3#��4#��2#��5# �缫�������ջ�����ͬ, ֻ�ǻ�ԭ���µ�Ũ�Ȳ�ͬ����ͼ3��ͼ4���Կ���:�õ�Ũ�ȵ��¶Ƴ��ĵ缫, ��·��ѹ�ܿ�������1V, ���ø�Ũ���¶Ƴ��ĵ缫��·��ѹȴ��������;��Ũ�ȵ��¶Ƴ��ĵ缫�� 0.6 V ������������·������Զ�����ø�Ũ�ȵ��¶Ƴ��ĵ缫��������Ϊ:���ø�Ũ�ȵ�����ҺʱĤ���� N2H5+ Ũ���ݶȽϴ�, ��� N2H5+ ����Һ��Ǩ�Ƶ��ٶȺܿ�, ���� D��ʱ��ëϸ���е� PtCl
ͼ4 �ڶ���ʵ����缫������
(a) Emax��Ʋ������ı仯; (b) I0.6V��Ʋ������ı仯; (c) Imax��Ʋ������ı仯
��ͼ3 (b) �� (c) ���Կ���, 2#�缫�� I0.6V ����3#�缫�����ֵ, 2#�缫�� Imax ��3#�缫������Ϊ����Ҫ����Ϊ 2# �缫�ײ�IJ����˻������ĵ�����, ʹ��Ч�����в��������ٶȱ� 3#�缫�졣
��ͼ4���Կ���:����2��3�λ�ѧ�Ʋ���, 4#��5#��6#�缫���ܲ���Ǻ����ԡ�������Ϊ����Ҫ����Ϊ�ڵ�Ũ�ȵ����л�ѧ�Ʋ�ʱ��Ĥ�ĵײ����ڱ���, ����Ũ�Ƚϵ�ʱ����Һ�� N2H5+ ���ݻ���, ��Ϊ������ѧ�Ʒ�Ӧ���̵��ٶȿ��Ʋ��衣���, ���۵ײ�Ĵ�����������̼��̼�ز����Dz�, ��Ч���IJ��ֻ�����ڻ�ѧ�Ƶ�����ڽ� (ǰ����) , ���������λ�ѧ�Ʋ��������������ȫ���Dz�, ��ʱ��Ч��������ԡ�
�ۺ�����ʵ�������Եó�:�õ�Ũ�ȵ�����Һ�����ӽ���Ĥ���л�ѧ�Ʋ����Ʊ�Ĥ�缫�Ŀ��з���������, �ڿ�·��ѹ Emax����·���� Imax������Ե������, 5#�缫�� 0.6V ���� I0.6V�ﵽ���Զ���������缫, ���Ա�����Ϊ����������Ϊ��ѧ�Ʋ����Ʊ����ӽ���Ĥȼ�ϵ��Ĥ�缫����ѹ���������
3 ����
�Դ�ͳ�����ӽ���Ĥȼ�ϵ��Ĥ�缫���Ʊ����ս����˸Ľ�, �û�ѧ�Ʋ����Ƴ�������������Ĥ�缫;�����Ĥ�缫���۽ṹģ�ͺ�Ĥ�缫��ѧ�Ʋ��Ļ���;ͨ������Ʋ����ն�Ĥ�缫���ܵ�Ӱ��, ȷ���˻�ѧ�Ʋ����Ʊ�Ĥ�缫����ѹ�������:�� Nafion117 Ĥ�������ȶ���һ�㲬��ѹ��̼�ڻ�̼�ز�, Ȼ���õ�Ũ�ȵ����Ȳ�������ʵ���Ũ�ȵ�����Һ��ѧ�Ʋ���
�����
[1] ��SasiKumarGetal.J .PowerSources , 1995 , 40 (3) :2 85