���±�ţ�1004-0609(2014)11-2900-06
�������ȥ��ұ�������е��ؽ���
ʩ �£���ѧǫ������������ܲ�ǣ������ɣ��� ƽ
(����������ѧ ������ѧ�빤��ѧԺ������ 650500)
ժ Ҫ��
�Թ�ʽ����¯����������ͨ�������ؽ��������ģ��ұ�����ؽ���������������麟�����������Ǧ���ӡ�����ұ�������������������Һ��Ũ�ȡ�pH��SO2�������������ӡ���ȥ��Ч����Ӱ�졣�����������立����վ�����Ǧ���ӡ������������Ũ�ȷֱ�Ϊ0.2��0.2��0.8 mol/L����ѷ�ӦpH��Ϊ10������ѷ�Ӧ�����£�Ǧ���ӡ����ľ���Ч�ʿɷֱ�ﵽ95.5%��93.2%��99.9%����������Ǧ���ӡ���Ũ�Ⱦ��ﵽ��������Ⱦ���ۺ��ŷű���(GB16297��1996)�����⣬SO2��������վ����ؽ������������á�
�ؼ��ʣ�
��ͼ����ţ�X51���� ���ױ�־�룺A
Removal of heavy metals from smelting flue gas by ammonium sulfide
SHI Yong, WANG Xue-qian, GUO Xiao-long, MA Yi-xing, WANG Lang-lang, NING Ping
(Faculty of Environmental Science and Engineering,
Kunming University of Science and Technology, Kunming 650500, China)
Abstract: Tubular resistance furnace was used as a reactor to simulate smelter flue gas of heavy metals by heating heavy metal oxides. And the flue gas containing Pb, Cd and Hg was treated with ammonium sulfide solution. The experiment was conducted to investigate the effects of (NH4)2S concentration, pH value of solution and the existence of SO2 on removal efficiency. The results show that the optimal concentration of Pb, Cd and Hg absorbed by ammonium sulfide solutions are 0.2, 0.2 and 0.8 mol/L, respectively. And the optimal pH value is 10. Under the optimum conditions, the removal efficiency of Pb, Cd and Hg reach 95.5%, 93.2% and 99.9%, respectively. The emission concentration of Pb, Cd and Hg reach the requirements of Air Pollutant Emission Standard (GB16297-1996). In addition, SO2 can reduce the removal efficiency of heavy metals of smelter flue gas.
Key words: ammonium sulfide; heavy metal; removal efficiency
�ؽ�����Ⱦ��Ҫ������ͭ��Ǧ���ܡ�п���������ɫ����ұ�������У�����Ǧпұ����Ⱦ��Ϊ���ء�Ǧпұ�������������ؽ�����Ⱦ����Ҫ����Ǧ���ӡ��顢���ȣ���Ⱦ��Χ����ˮ������������[1-2]��
������Ǧ��Ⱦ��Ҫ����̬��Ⱦ����Ǧ�̺�Ǧ����ʽ���ڣ���Դ�ڲɿ���������Ǧ���͵�ȼ�ա���Ǧ��Ʒ�������ȹ���[3-4]������������Ǧ�Ļӷ��̶ȴ� ���Ի�����������������Ǧ�Ļӷ���ʧ�Լ�����Ļ�����Ⱦ��Ǧ����������̬��䣬��������Pb3O4��PbO2�Լ�PbO�����¶���Pb3O4���ڣ����¶���PbO���ڡ�����Ⱦ������Ǧп��ұ����ú̿��ȼ�պ���������[5]���ӵĶ����ܳ־õش����ڻ������������ڡ��������ӵ���̬�������ӡ������ӡ����Ӻ������ӵȣ���Ҫ�����ڹ���������С�����һ�־��г־��ԡ������ۻ��Ժ������������õ��ж���Ⱦ������ཡ������̬�������кܴ�ĸ���Ӱ�졣�����й��Ĵ�����ʽ��Ҫ�����֣���̬��(Hg2+��Hg0)��̬������������¶ȸ���800 ��ʱ�����Ļ������ֽ����̬������̬���Ļӷ��Խϸߡ�ˮ���Խϵͣ����ѿ���[6]��
Ŀǰ����������顢���ؽ������о��Ӷ࣬Ǧ������Խ��١������������ؽ�����Ҫ����������[7-10]����������[11-12]����ѧ������[13]������Ǧ���ӵļ�̬����ȶ�������ϸС����̬���ڣ������������������ȷ����������á�����[14-16]���ڻ�ѧ������֮һ���ڹ���Ӧ�ý�Ϊ�㷺����Ҫ����ȥ����ˮ������ؽ���������������ȥ���������ؽ������о���Ӧ�ú��١����������ص��о���立����վ���ұ��������Ǧ���ӡ���3���ؽ���������Ҫ��Ӱ�����أ��÷����ǻ��������Һ��S2-��������Ǧ���ӡ�����Ӧ���ɳ������ﵽ����Ŀ�ģ�Ҳ������Ǧ�ӹ��Ļ������ã�ʵ��ѭ�����ã�Ϊ�����������ؽ����Ĺ���Ӧ���ṩ�����о����������ݡ�
1 ʵ��
1.1 ʵ�顢�����豸���Լ�
ʵ�������豸��Ҫ�й�ʽ����¯������ܣ������ã����������ƣ�PHS-3C��ȼƣ�Z-2010ƫ������ԭ�ӷֹ��ȼƣ�F-732��ԭ�����ղ�ǡ�
ʵ������ҩƷ��Ҫ�����((NH4)2S)����ɫ����Ǧ(Pb3O4)��������(CdO)���Ȼ���(HgCl2)����Ϊ�������������Ϻ���ҩ�����Ź�˾��
1.2 ʵ��װ��
��立��������ؽ���ұ��������ʵ��װ����ͼ
1��ʾ�����Ϊ��������ʽ����¯Ϊ����ģ�ⷢ������ʢ�������Һ������ƿΪ����װ�á�ʵ����ģ���������Ϊ��һ�ؽ���������ʵ�������ģ�⺬Ǧ���ӡ����������õĻ�����ֱ�Ϊ��ɫ����Ǧ(Pb3O4)��������(CdO)���Ȼ���(HgCl2)����Ӧ��β������ҺΪHNO3��H2O2���Һ(V(HNO):V(H2O2)=1:1)��HNO3��H2O2���Һ(V(HNO3):V(H2O2)=1:1)������KMnO4��Һ��ʵ������У��ؽ���������(Pb3O4��CdO��HgCl2)�ڷ�Ӧ���б����¼��ȳɻӷ�̬�����������γ�ģ����������ͼ1��ʾ��������1����2���رշ�3����4ʱ����β������װ��1(����������������EPA�ⶨ������ȷ��ģ���������ؽ�����Ũ��)�ռ�ģ���������ؽ�����ʱ��Ϊ15 min���õ�δ�������Һ����ʱģ���������ؽ�����Ũ��C0���رշ�1����2��������3����4����β������װ��2�ռ��������Һ���պ�ģ���������ؽ�����ʱ��Ϊ15 min���õ��������Һ������ģ���������ؽ�����Ũ��Cn�����������������ؽ����ĺ�����
1.3 ʵ�鷽��
ұ������ģ��ʵ�顣ͨ�����ƹ�ʽ����¯�����¶ȡ������������õ��̶�Ũ�ȵ��ؽ�����������������Ԥʵ�飬ģ��Ǧ���ӡ�������������¶ȷֱ�Ϊ900��1000��450 �棬�����ֱ�Ϊ200��200��150 mL/min��ģ��������Ǧ���ӡ�����Ũ�ȿɴﵽ10~15��2~7��10~30 mg/m3����ұ����ʵ��״�������
��立����վ�����Ǧ���ӡ�����ұ����������Ҫ�����������������ʹǦ���ӡ�����PbS��CdS��HgS����ʽ�����������Ӷ��ﵽ����������Ŀ�ģ���ѧ��Ӧ��ʽ(1)~(4)��ʾ��
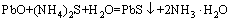 (1)
(1)
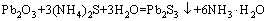 (2)
(2)
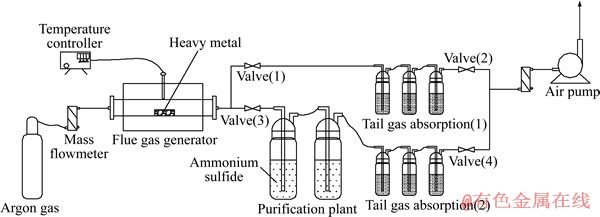
ͼ1 ʵ��װ��ͼ
Fig. 1 Schematic diagram of experimental apparatus
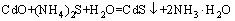 (3)
(3)
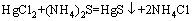 (4)
(4)
����0~0.8 mol/L��ͬŨ�������Һ����ȡ50mL�������վ���ģ��������Pb��Cd��Hg��3���ؽ���������Ũ�ȶ��侻��Ч�ʵ�Ӱ�죬����ȷ��(NH4)2S��Һ�����Ũ�ȡ�
���ʵ����ȷ�������Ũ�ȵ������Һ��ͨ��1% NaOH��1%������Һ������pH���Ƴɲ�ͬpH�������Һ���ٸ�ȡ50 mL�������վ���Pb��Cd��Hg������pH���侻��Ч�ʵ�Ӱ�졣
������Ũ�ȵ������Һ���������������ͨ�������Һ������ʱ������ӣ������Һ��pH����½����ڴ˹����У���ȡ50 mL��ͬpH�������Һ���վ���Pb��Cd��Hg���������������侻��Ч�ʵ�Ӱ�졣
�������ؽ�����Ũ��(mg/m3)����ʽ��ʽ(5)��ʾ��
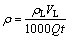 (5)
(5)
ʽ�У���LΪβ������Һ���ؽ���Ũ�ȣ�mg/L��VLΪβ������Һ�����mL��QΪ����������mL/min��tΪ�����ռ�ʱ�䣬min��
����Ч�ʼ��㹫ʽ��ʽ(6)��ʾ��
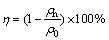 (6)
(6)
ʽ�У���nΪ��������պ��������ؽ�����Ũ�ȣ���0Ϊδ���������ʱ�������ؽ�����Ũ�ȣ�mg/L��
β������Һ��Ǧ��Ũ�ȸ��ݻ���ԭ�����շֹ��ȷ�(HJ538-2009)�ⶨ��β������Һ���ӵ�Ũ�Ȼ���ԭ�����շֹ��ȷ�(HJ/T 64.1-2001)�ⶨ��β������Һ�й���Ũ����ԭ�����շֹ��ȷ�(HJ542-2009)�ⶨ��
2 ���������
2.1 ������XRD����
ͼ2��ʾΪ�ؽ���������XRD�ס���ͼ2(a)��֪�����պ���ģ�������������ij�������Ҫ��CdS��CdSO3Ϊ����CdO�������١�����˵��������պ��ӵ��ؽ���������Ҫ�Ի�ѧ����Ϊ������ͼ2(b)��֪�����պ�Ǧģ�������������ij�����Ҫ��Pb3O4Ϊ����PbSO4��֮��PbS�������١��ɴ˿�֪��������պ�Ǧ���ؽ���������Ҫ����������Ϊ�����ٲ���Ǧ����立�Ӧ���ɺ�Ǧ�ij�����ͼ2(c)����������պ�������������ij������XRD��������ͼ2(c)��֪��������HgSΪ��Ҫ���࣬����������պ���������Ҫ�ǻ�ѧ�������á�
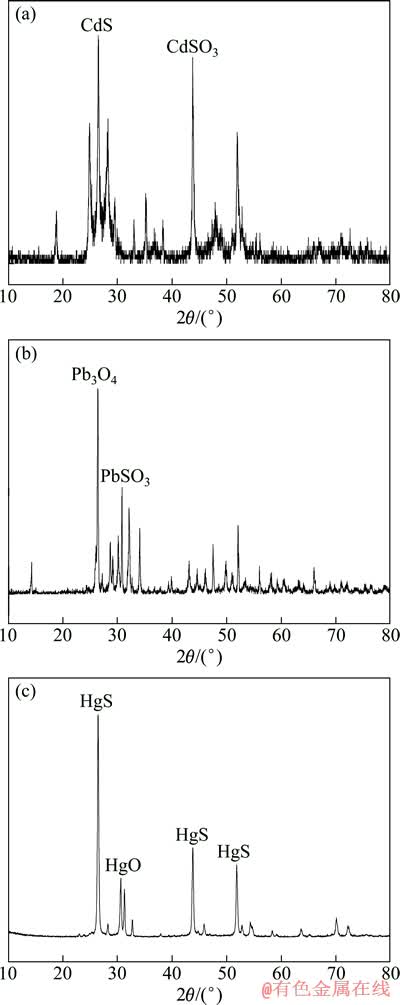
ͼ2 �ؽ���������XRD��
Fig. 2 XRD patterns of heavy metals precipitation containing Cd (a), Pb (b) and Hg (c)
2.2 ���Ũ�ȶ�������Ǧ���Ӻ�����Ч����Ӱ��
�����Һ��Ũ����Ӱ����立��ľ���Ч�������гɱ�����Ҫ�����������Һ��Ũ�ȹ��߲��������ˮ��S2-Ũ�ȹ��ߣ����һ����Ӵ����ɱ��������Һ��Ũ�ȹ���Ҳ��ʹ�������ؽ�������Ч�ʽ��ͣ�����ŷ��������ؽ������ꡣʵ�鿼�������Ũ�ȶ�������Pb��Cd��Hg����Ч����Ӱ�죬������ͼ3��
��ͼ3�ɿ�����Ǧ���ӡ�������Ч�ʾ����������ҺŨ�ȵ����߶����ߡ����Ũ�ȴ�0��0.2 mol/L��Ǧ���Ӿ���Ч�����߷dz����ԣ�Ǧ�ľ���Ч�ʴ�86.4%��ߵ�95.5%���ӵľ���Ч�ʴ�85.2%��ߵ�93.2%��ͬʱ�����ľ���Ч�ʴ�82.3%��ߵ�98.1%�����Ũ��Ϊ0.2 mol/Lʱ������������Ǧ���ӵ�Ũ�ȷֱ�Ϊ0.65��0.45 mg/m3�����Ѵﵽ������Ⱦ���ۺ��ŷű�(GB16297-1996)��������Ũ��Ϊ0.1 mg/m3��δ�ܴ�ꡣ��Ũ�ȴ���0.2 mol/Lʱ��Ǧ���Ӻ��ľ���Ч�ʾ��ɴﵽ95%���ϣ���������ƾ���ƽ��������������Ũ����0.8 mol/Lʱ�����ľ���Ч�ʴﵽ99.9%�����������й���Ũ�ȣ�0.01 mg/L���ﵽ������Ⱦ����ۺ��ŷű�����ͬһŨ���£�3���ؽ����ľ���Ч���ɴ�С��˳������ΪHg��Pb��Cd��˵����笠���Hg��Ӧ���ɳ�������3�ֽ�����Ksp��С�����˳������ΪHgS��PbS��CdS����茶���������Ǧ���Ӻ���Ч���Ϻã���Ͼ���Ч�ʺ;���Ч�濼�ǣ��������Һ������Ǧ���Ӻ����������Ũ�ȷֱ�Ϊ0.2��0.2��0.8 mol/L��
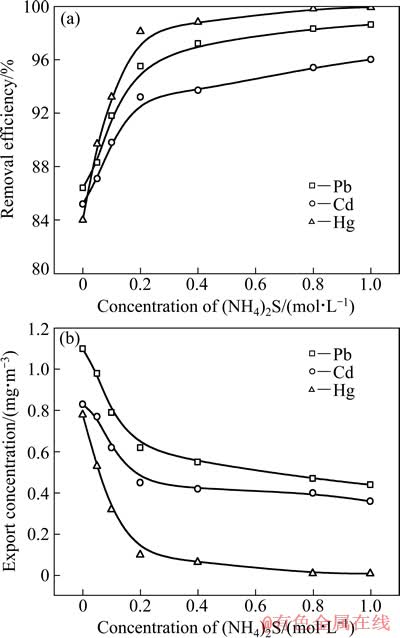
ͼ3 ���Ũ�ȶ�������Pb��Cd��Hgȥ����Ӱ��
Fig. 3 Influence of (NH4)2S concentration on removal of Pb , Cd and Hg from flue gas
2.3 ��ӦpH��������Ǧ���ӡ�������Ч����Ӱ��
������������ؽ�����Ӧʱ����ҺpHҲ��Ӱ����立����������ؽ���ȥ���ʵ���Ҫ���ء�S2-��ˮ�еĴ�����̬����Һ��H+����γ�HS-��H2S����ѧ��Ӧ��ʽ(7)~(8)��ʾ[17]��
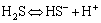 ��
��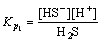 ��
��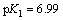 (7)
(7)
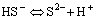 ��
��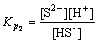 ��
��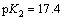 (8)
(8)
H+��S2-�Ľ�Ͻ�����S2-��ʹ��Ч�ʡ�ʵ�鿼����pH��������Pb��Cd��Hg����Ч����Ӱ�죬ʵ������ͼ4����ͼ4��֪����pHΪ2~10�������£��ؽ�������Ч����pH��������ʽ(2)~(6)�����½����ƣ���ʽ(6)~(10)�г������������ơ�Pb�IJ�������Ϊ89.5%~95.5%��CdΪ83.1%~93.2%��HgΪ96.4%~ 99.9%�����У���pHΪ6~7ʱ������Ч����͡������Ժ�ǿʱ����̬�ؽ������ֽ������̬������̬Ǧ���������ӷ�Ӧ���ɵ���Ǧ�����ӳ�����Ѹ�ٱ��ֽ⣬�����ؽ�����������̬Ǧ�ӱ���������ˮ�У����ڼ��Ժ�ǿʱ����̬Ǧ�ӹ�һ�����������ӷ�Ӧ�����ؽ��������������������һ��������ʵ�ֹ������룬ֱ��ͣ����ˮ�С�pH=10ʱ��Pb��Cd��Hg�ľ���Ч�ʾ���92%���ϣ��ҳ���������Ǧ���ӡ�����Ũ�ȷֱ�Ϊ0.65��0.45�ͣ�0.01 mg/m3�������ϴ�����Ⱦ���ۺ��ŷű�(GB16297-1996)�����ǵ�����̬���ؽ��������һ�������������������ʺ�Ǧ�������ľ�������ˣ��������Һ������Ǧ���ӡ������������pH��Ϊ10��
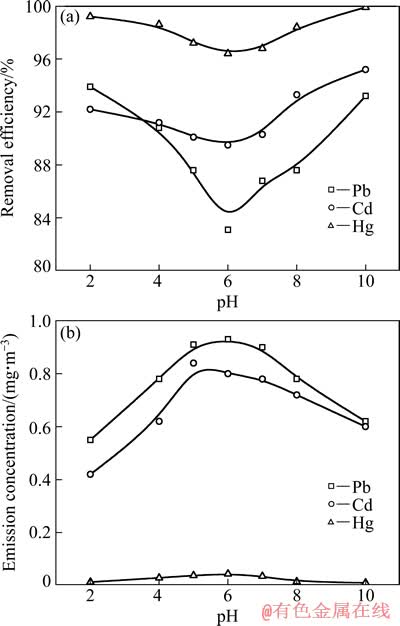
ͼ4 pH��������Pb��Cd��Hgȥ����Ӱ��
Fig. 4 Influence of pH on removal of Pb , Cd and Hg from flue gas
2.4 SO2��������Ǧ�ӹ�����Ч����Ӱ��
Ǧпұ����ԭ����ԭ��;���ԭ��ʯ��������������ɷ�Ϊ�����������Ȼ����Ǧп��ʯ��������࣬���������ߴ�27%~32%[18]��ұ�������л����������SO2����ˣ�SO2Ҳ��Ӱ�����������ؽ�������Ҫ���ء�
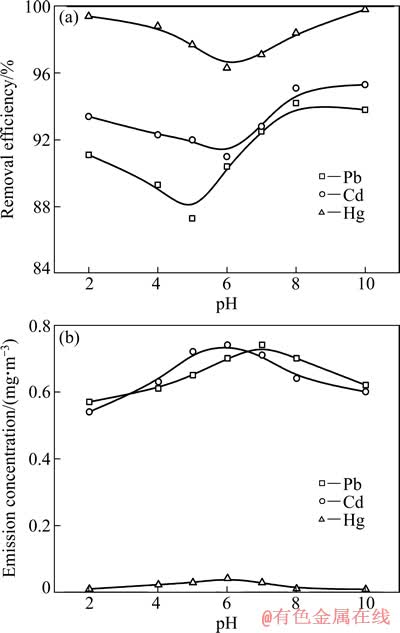
ͼ5 SO2��������Pb��Cd��Hgȥ����Ӱ��
Fig. 5 Influence of SO2 on removal of Pb , Cd and Hg from flue gas
ʵ�鿼����SO2��Pb��Cd��Hg����Ч����Ӱ�죬ʵ�������ͨ�벻ͬʱ���SO2������SO2����立�Ӧ����Һ��S2-���ٶ�S2O32-����������������(��ʽ(9))����������淋�pH�ͻ����½����Ϳ����Ƶò�ͬPH�������Һ�������ͼ5����ͼ5��֪����pHΪ2~10�����£��ؽ���ȥ������pH���ߣ��Ƚ��������ߡ���ʽ(9)��(10)��֪����һ�����У��������SO2��Ӧ����������Һ�е�S2-���Ӷ�������S2-���ؽ�����Ӧ������SO2����ͨ�룬��Һ�ɼ��Խ���������ԣ���̬�ؽ������ֽ������̬����������Һ�С���pHΪ5~6ʱ��Hgȥ���ʴ�99.9%���͵�96.4%��Pb����Ч�ʴ�95.2%���͵�93.2%��Cd����Ч�ʴ�93.7%���͵�91.7%����ˣ�SO2�������ؽ�������Ч����һ�����������á�
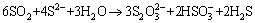 (9)
(9)
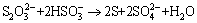 (10)
(10)
3 ����
1) ��Ͼ���Ч�ʺ;���Ч�濼�ǣ��������Һ����Ǧ���ӡ������������Ũ�ȷֱ�Ϊ0.2��0.2��0.8 mol/L����ͬһ��Ӧ�����£�3���ؽ����ľ���Ч���ɴ�С��˳������ΪHg��Pb��Cd��
2) ������վ����ؽ���Ч����pH�����߳����½����ƣ��ڳ������������ơ�pH=6ʱ��3���ؽ���ȥ���ʾ�������ͣ����������£�Pb��Cd��Hg����������������ķ�ʽʵ�ַ��롣��ˣ���立����վ����ؽ��������pHΪ10��
3) ��������ѷ�Ӧ�����£�Ǧ���ӡ����ij���Ũ�ȷֱ�Ϊ0.65��0.45����0.01 mg/m3�����Ѵﵽ��������Ⱦ���ۺ��ŷű���(GB16297-1996)��
4) ��������վ���ұ���������ؽ����Ĺ����У�SO2�Ĵ��ڻ����������Һ�������ӣ��Ӷ������ؽ�����ȥ��Ч�ʡ�
REFERENCES
[1] ���ǽ�. Ǧұ����ҵ�ؽ�����Ⱦ��״�����ζԲ�[J]. ��ɫ��������, 2011, 1(4): 23-27.
LIN Xing-jie. Present situation and control methods of heavy metals pollution from lead smelting industry[J]. Nonferrous Metallurgical Engineering, 2011, 1(4): 23-27.
[2] ����Ӣ. ��ɫұ������ѧ[M]. ��ɳ: ���Ϲ�ҵ��ѧ������, 1992: 34-39.
LIN Shi-ying. Environmental engineering for nonferrous metallurgy[M]. Changsha: Central South Industry University Press, 1992: 34-39.
[3] ���ұ�. ������Ⱦ���ƹ���[M]. ����: ��ѧ������, 2002: 54-55.
WU Zhong-biao. Engineering for air pollution control [M]. Beijing: Science Press, 2002: 54-55.
[4] �� Ƽ. ������Ǧ�̼�Ǧ������Ⱦ���о���״[J]. �Ƽ����µ���, 2009, 3(8): 109-110.
HUANG Ping. Current situation of pollution and research on lead smoke and lead dust in the atmosphere[J]. Science and Technology Innovation Herald, 2009, 3(8): 109-110.
[5] �� ��. �ɶ�����������������Ǧ���ӵĻ�����ѧ��Ϊ�о�[D]. �ɶ�: �ɶ�������ѧ, 2006: 2-5.
ZHOU Lin. Environmental chemical behavior research of lead and cadmium in atmospheric dust from Chengdu economic zone[D]. Chengdu: Chengdu University of Technology, 2006: 2-5.
[6] �� ��, ����Ƽ, �˴���, ���ľ�, ë ��. ȼú�����й�ȥ�����о���չ[J]. ������չ, 2011, 30(7): 1607-1613.
CUI Xia, MA Li-ping, DENG Chun-ling, XU Wen-juan, MAO Yu. Research progress of removing mercury from coal-fired flue gas[J]. Chemical Industry and Engineering Progress, 2011, 30(7): 1607-1613.
[7] MERCEDES D S, ROSA M T. High-temperature removal of cadmium from a gasification flue gas using solid sorbents[J]. Fuel, 2005, 84: 717-721.
[8] THOMAS K, ISABEL M L. Feasibility of mercury removal from simulated flue gas by activated chars made from poultry manures[J]. Journal of Environmental Management, 2010, 91: 2466-2470.
[9] JOST O L, WENDT, SUNG J L. High-temperature sorbents for Hg, Cd, Pb and other trace metals: Mechanisms and applications[J]. Fuel, 2010, 89: 894-903.
[10] YANG X F, SHEN Z G. Silica nanoparticles capture atmospheric lead: Implications in the treatment of environmental heavy metal pollution[J]. Chemosphere, 2013, 90: 653-656.
[11] �� �A, �Խ���, ������, �� ��. ����̿�������ѳ����ʹ����о�[J]. ȼ�ϻ�ѧѧ��, 2011, 39(5): 373-377.
ZHANG He, ZHAO Jian-tao, FANG Yi-tian, WANG Yang. Stabilized oxidation and adsorption of elemental mercury by activated carbon[J]. Journal of Fuel Chemistry and Technology, 2011, 39(5): 373-377.
[12] FANG P, CEN C P, WANG X M. Simultaneous removal of SO2, NO and Hg0 by wet scrubbing using urea KMnO4 solution[J]. Fuel Processing Technology, 2013, 106: 645-653.
[13] ����. ϡ�н���ұ��ѧ[M]. ����: ұ��ҵ������, 1990: 55-56.
LI Hong gui. Rare metals metallurgy[M]. Beijing: Metallurgical Industry Press, 1990: 55-56.
[14] BJORGE D, JOEL H. Removal of heavy metals occurring in the washing water of flue gas purification[J]. Chemical Engineering Journal, 2009, 150: 196-203.
[15] ̷��ǿ, ���Ľ�, �����, ֣��־, �� Խ, ������, ����ΰ. ��ѧ������ǿ�����湤��Ӧ��ȥ��ˮ�е���[J]. ��������ѧ��, 2013, 7(3): 848-852.
TAN Hao-qiang, HE Wen-jie, HAN Hong-da, ZHENG Cheng-zhi, MA Yue, CHEN Yu-zhuo, PU Jian-wei. Cadmium removal in water emergency treatment of conventional process enhanced by chemical precipitation[J]. Chinese Journal of Environmental Engineering, 2013, 7(3): 848-852.
[16] л �, ����ΰ, �ܲŷ�, �� ��, ���. ��������������������Ϊ[J]. ���ϴ�ѧѧ��: ��Ȼ��ѧ��, 2012, 43(2): 435-439.
XIE Hao, ZHAO Zhong wei, CAO Cai fang, LIANG Yong, LI Jiang-tao. Behavior of arsenic in process of removing molybdenum by sulfide method[J]. Journal of Central South University: Science and Technology, 2012, 43(2): 435-439.
[17] PEKKA S, WILLIS F. Precipitation of lead sulfide for surface chemical studies[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2000, 172: 17-31.
[18] κ ��, �����. п����ұ��ѧ[M]. ����: ұ��ҵ������, 2013: 6-7.
WEI Chang, LI Cun-xiong. Zinc extractive metallurgy[M]. Beijing: Metallurgical Industry Press, 2013: 6-7.
(�༭ ����)
������Ŀ�����Ҹ����о���չ�ƻ�������Ŀ(2012AA062504)��������Ȼ��ѧ����������Ŀ(U1137603��51268021��51368026)
�ո����ڣ�2014-03-04�������ڣ�2014-07-30
ͨ�����ߣ���ѧǫ�����ڣ���ʿ���绰��13888183303��E-mail��wxqian3000@aliyun.com
ժ Ҫ���Թ�ʽ����¯����������ͨ�������ؽ��������ģ��ұ�����ؽ���������������麟�����������Ǧ���ӡ�����ұ�������������������Һ��Ũ�ȡ�pH��SO2�������������ӡ���ȥ��Ч����Ӱ�졣�����������立����վ�����Ǧ���ӡ������������Ũ�ȷֱ�Ϊ0.2��0.2��0.8 mol/L����ѷ�ӦpH��Ϊ10������ѷ�Ӧ�����£�Ǧ���ӡ����ľ���Ч�ʿɷֱ�ﵽ95.5%��93.2%��99.9%����������Ǧ���ӡ���Ũ�Ⱦ��ﵽ��������Ⱦ���ۺ��ŷű���(GB16297��1996)�����⣬SO2��������վ����ؽ������������á�
[1] ���ǽ�. Ǧұ����ҵ�ؽ�����Ⱦ��״�����ζԲ�[J]. ��ɫ��������, 2011, 1(4): 23-27.
[2] ����Ӣ. ��ɫұ������ѧ[M]. ��ɳ: ���Ϲ�ҵ��ѧ������, 1992: 34-39.
[3] ���ұ�. ������Ⱦ���ƹ���[M]. ����: ��ѧ������, 2002: 54-55.
WU Zhong-biao. Engineering for air pollution control [M]. Beijing: Science Press, 2002: 54-55.
[4] �� Ƽ. ������Ǧ�̼�Ǧ������Ⱦ���о���״[J]. �Ƽ����µ���, 2009, 3(8): 109-110.
[5] �� ��. �ɶ�����������������Ǧ���ӵĻ�����ѧ��Ϊ�о�[D]. �ɶ�: �ɶ�������ѧ, 2006: 2-5.
[6] �� ��, ����Ƽ, �˴���, ���ľ�, ë ��. ȼú�����й�ȥ�����о���չ[J]. ������չ, 2011, 30(7): 1607-1613.
[11] �� �A, �Խ���, ������, �� ��. ����̿�������ѳ����ʹ����о�[J]. ȼ�ϻ�ѧѧ��, 2011, 39(5): 373-377.
[13] ����. ϡ�н���ұ��ѧ[M]. ����: ұ��ҵ������, 1990: 55-56.
LI Hong gui. Rare metals metallurgy[M]. Beijing: Metallurgical Industry Press, 1990: 55-56.
[18] κ ��, �����. п����ұ��ѧ[M]. ����: ұ��ҵ������, 2013: 6-7.


