���±�ţ�1004-0609(2008)07-1336-06
������Ĥ���Ʊ�������
�� ����³�۸գ��³����� ǫ�����غͣ����춫
(�Ϻ���ѧ ���Ͽ�ѧ�빤��ѧԺ���Ϻ� 200072)
ժ Ҫ��
���ù�����Ĥ(SOM)��ֱ�ӵ�ԭNb2O5�Ʊ�����Nb����CaCl2������ϵ�У�����ѹ����Ϊ3.2 V���Ծ���1 200 ��Ԥ��4 h���͵�Nb2O5Ϊ����������ﯹ���̼���͵�Һ̬ͭ�Ͻ�Ϊ�������о����ʱ��ֱ�Ϊ0.5��1��2��4 h�Լ���ͬ�¶��µ����������ɺͲ�ͬ����¶ȶ����������ṹ��Ӱ�졣������������ŵ��Ľ��У�Nb2O5����ת��ΪNb��һϵ�еͼ�����������ű���ԭ�ɽ���Nb��������ʵ���¶ȵ����ߣ�����ٶ���Ӧ�ӿ죬����������ߴ�������FFC����ȣ�SOM�����и��ߵĵ��Ч�ʣ�1 150 ���µĵ��Ч�ʿɴ�81.7%��
�ؼ��ʣ�
������Ĥ��Nb2O5��Nb���绯ѧ����ԭ��
��ͼ����ţ�TG 146.4��TF 111.52���� ���ױ�ʶ�룺A
Metal niobium by solid oxygen-ion membrane
HE Li, LU Xiong-gang, CHEN Chao-yi, LI Qian, LI Chong-he, ZHONG Qing-dong
(School of Materials Science and Engineering, Shanghai University, Shanghai 200072, China)
Abstract: Niobium was produced directly from Nb2O5 using solid oxygen-ion membrane (SOM). In molten flux CaCl2 system, electrolysis voltage is 3.2 V, Nb2O5 pellets preformed and sintered at 1 200 �� for 4 h and liquid metal saturated with carbon loaded in zirconia tube act as the cathode and anode, respectively. The electrochemical character of electrolytic process and the micro-structural features of the cathode pellets were studied at different temperatures for 0.5, 1, 2 and 4 h, respectively. The results show that Nb2O5 is transformed to a series of low value oxides firstly, and then proceed to the metal Nb with electrolysis. The electrode reaction rate and the grain of reduced metal increases with temperature increasing. SOM process has higher electrolysis efficiency comparing with FFC process. The electrolysis efficiency can be as high as 81.7%.
Key words: solid membrane; Nb2O5; Nb; electrochemistry; reduction
����Nb�����۵�ߡ�ǿ�ȸߡ����ȡ����������Ժá�����ʴ��ǿ�����ӷ������͵��������ܡ�Nb ��;�㷺����ұ��ҵ�����պ��칤ҵ�����ӹ�ҵ��ҽ����е�����������ԭ���ܹ�ҵ�еõ��㷺Ӧ��[1?2]����ҵ��������������Ҫ����̼�Ȼ����Ȼ�ԭNb2O5���գ������������øߴ���۶�����ƻ�ԭK2NbF7����[3?4]����Щ�����ձ���ڹ��ո��ӡ��ɱ��ߡ��ܺĴ����Ⱦ���ص����⣬ʹ�䷢չ��Ӧ���ܵ����ơ���ˣ��о�����Ҳ�����ڸý����¹��յĿ� ��[5?6]��2000�꣬������һ����ӱ����������ֱ���Ʊ�������FFC���Ź��գ��������ѧ�����ô˷������Ѿ��Ʊ����˽����ѡ��㡢������[7?10]�����÷���Ҳ����һЩ���⣺�������е���ѹ������ϸ�Ŀ����Ա������ν��ʱ���⣻���ʱ�и���Ӧ��������ή�͵��ĵ���Ч�ʣ����ӵ���ʱ�䣻ʯī���������������⽫ʹ������Ӧ���̴��ڲ��ȶ���״̬��
������Ĥ(SOM)����Ϊһ����ӱ�Ķ�����ұ������ʵ�����ѳɹ����ڽ����㡢�Ѻ�þ [11?13]���Ʊ����������߶�SOM��ֱ�ӵ�ԭNb2O5�Ʊ������������ʵ���о��������˵�ԭ���̺Ͳ�ͬ����¶ȶ����������Ӱ�죬����FFC������������Ӧ�� �Աȡ�
1 ʵ��
SOM���ɽ���������ֱ���Ʊ�������ԭ��������[6, 11]������ϸ����, ��Ϊͨ���绯ѧ�ķ������������е���ֱ���ѳ���ʵ�ֽ���������Ļ�ԭ������ԭ����������ɸ��ݲ�ͬ�����Ʊ�Ϊ���ϵͳ���������������У������������е����뻯�������Σ��������ӻ�õ����γɽ�����ͼ۽������ӣ�O2?ͨ�����δ�����������������ʧȥ���ӡ�
��FFC�����ϵͳ������������������ͬһ������ϵ��ͬ��SOM��ʹ���˾���������ѡ���ԵĹ�����Ĥ���������������뿪������ֻ���������ܲ���������Ӧ������FFC��ͬ����������ϵ�£�SOM�����ڸ��ߵĵ���ѹ�½��й������Ӷ��ɻ�ø���ĵ�ⷴӦ�ٶȣ���߹���Ч��ͬʱ���⸱��Ӧ�ķ�����
��Һ��ʯ��Ϊճ�������Nb2O5ϸ��(��ѧ����������С��98%)ѹƬ����1 200 �����ս�4 h���Ƴ�Բ��Ƭ����(ֱ��Ϊ20 mm����Ϊ3 mm������ԼΪ3 g)������Ϊ����ﯹ���̼���͵�ͭ�Ͻ����ε����ΪCaCl2(��ѧ����������С��99%)������װ����ͼ1��ʾ��������ĤΪ��ʵ�������Ƶ������Ʋ����ȶ�������ﯹܣ�����Ϊd 15 mm��120 mm��
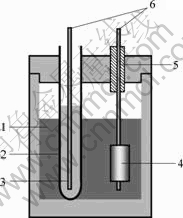
ͼ1 ���ʵ��װ��ͼ
Fig.1 Schematic diagram of reactor electrolytic cell arrangements: 1��Molten electrolyte; 2��Solid oxygen-ion membrane; 3�� Copper alloy liquid; 4��Nb2O5; 5��Alumina separator; 6��Molybdenum rod
ʵ���ڸߴ�����ı����½��У�ϵͳ���µ��趨��Ŀ�����ȶ��������缫��ʩ�Ӻ㶨��ѹ��ʼ��⣬ÿ��5 min��¼ϵͳ����ֵ�����о�����ѹΪ3.2 V�����ʱ��Ϊ4 h��ʵ����е��¶ȷֱ�Ϊ950��1 050��1 150 �档��������������������ϴ(ϡ����)������ˮˮϴ�����ﴦ������м�⡣
ʵ�����FP93�����¿��ǽ��и���¯���£�YB1720A�Ϳɵ�ʽֱ����ѹ��Դʩ�ӵ�ѹ����¼��3086��X��Y��¼�ǡ���������?��ȡ������������ȡ������550 ��Ŀ���������10 hǰ����������ֵΪ��ԭ�����������������������������������ձ���ѧD/max22500PC ��X���������Ƿ�����������Ƭ����ṹ����JSM?6700F��ɨ����������۲�����Ƭ�����ṹ����ò��
2 ��������
2.1 ��ͬ���ʱ��������������
Ϊ�о�SOM������Nb2O5��������Ĺ��̣��ڵ���¶ȼ���ѹ�ֱ�Ϊ1 150 ���3.2 V�������£���Ե��ʱ��0.5��1��2��4 h��ʵ�������½�����ϵ��ʵ�顣��ʵ��õ��������Ʒ۽���XRD�����������ͼ2��ʾ��
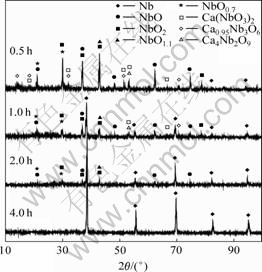
ͼ2 ��ͬ��ԭʱ����Ʒ��XRD��
Fig.2 XRD patterns of sample reduced for different times
�о�֤����Nb2O5����ת��ΪNb��һϵ�еͼ��������������ԭ�ɽ���Nb���ڵ�ԭ�ij�ʼ�Σ���������������������������ɣ���Ӧ��ʼ���������ٶȽϿ죻��ԭ2h��������XRD���г��������ĵͼ��������⣬�Ѿ�û����������������壻��ԭ4 h��XRD�����ʾֻ�н���Nb������壬��ⷴӦ��ȫ��
����FFC����Nb2O5�Ʊ������꣬��ʼ���������ϻ��д�����O2(g)���ɣ��Ӷ���ʹ��Ӧ(1)�ķ�����ʹ��������(CaO)�ĺ������ӣ�
![]()
���ɵ�(CaO)����Nb2O5��Nb�ĵͼ����������Ӧ����CaNb2O6��Ca3Nb2O8��Ca0.95Nb3O6���м�����ˣ�O2(g)���������ɽ��������������IJ������о�[10]���֣��������������������̽�Ϊ���ѣ���Ȼ���о�[14]��Ϊ����������ͨ�����ӵ��ʱ�����ջ�ԭΪ��������������Ĵ����ĵ��ܣ��Ӷ�ʹ���������̵ĵ���Ч�ʽ��͡�
ʹ��SOM�����Nb2O5�Ʊ�����Nbʱ���������������ӻ��������ӣ���ͨ��������Ĥ��������ͭ�Ͻ�Һ�е�ʯī������Ӧ���������������α�������Ĥ���룬����/������Ĥ��������O2(g)���ɣ��⽫ʹ��Ӧ(1)���ᷢ�����Ӷ���ֹ������������������е����ɡ�����[14]������FFC����ԭNb2O5������ԼΪ1 g���������6~8 h�缫��Ӧ��Ҫ��Nb-O������������������о�����SOM������3.04 g��Nb2O5������1150��ĵ���¶��£�Nb���������Լ�Nb-O�������������4 h���Ѿ���ɣ������SOM�������Լӿ��ԭ���ٶȣ�����������Ч�ʡ�
2.2 ����¶ȶ���Ʒ��ò��������Ӱ��
������[10]���֣���850 ���µ��24 h�缫�����Ĵ�С���ս������������ȱ仯����������Щ���ɡ���CHEN��[15]�о����֣���ԭΪ���ȷ�Ӧ�������������ս���ۼ�����
���о��ֱ��ڵ���ѹΪ3.2 V��ʵ���¶ȷֱ�Ϊ 950��1 050��1 150 ���¶��µ��4 h���֣���ͬ�ĵ���¶ȶԵ�������Ƭ��������ò�����Ե�Ӱ�죬ʵ����������SOM���Ʊ���������������[16]��
ͼ3��ʾΪNb2O5ԭʼ�缫�Ͳ�ͬ����¶��º�����SEM��ͼ3(a)��ʾΪNb2O5��ĩѹ�Ƴ��͡��ս�����ò����ͼ3�ɿ�����������¶�Ϊ950 ��ʱ��������ս��������������ߴ�������С�����������ܣ���϶����ܣ���ɢ����Ƭ�ϳ��˰�ɫ���⣬����һЩ��ɫ�ϰ�������(��ͼ3(b))��������¶�Ϊ 1 050 ��ʱ��������Ϊ���ο����������ϵ��ǰ�������ṹ��Ϊ���ܣ�������Ӵ���ϴ����˽ϴ�Ŀ�϶��������Ϊ��������ת��Ϊ�������������������(��ͼ3(c))��������¶�Ϊ1 150 ��ʱ��������ۼ������Ϊ���ԣ�С�������ۻ��������������ƣ����ڴ�����������ڽϳ�ʱ����ս��ѿ�ʼ���ֳ��������ò�������������˸����Ŀ�϶(��ͼ3(d))��
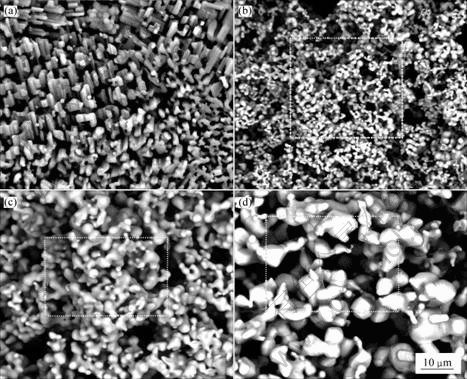
ͼ3 Nb2O5ԭʼ�缫�Ͳ�ͬ�¶��µ��4 h�缫��SEM��
Fig.3 SEM images of cross sections of Nb2O5 pellets before(a) and after electrolysis at 950(b), 1 050(c) and 1 150 ��(d) for 4 h
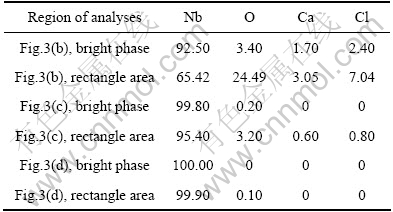
��������������������ʾ��������¶�Ϊ950 ��ʱ����ɫ����������ϸߣ�ԼΪ3.40%�������������������������ﵽ24.49%������Nb��O��Ħ����ԼΪ2.7?1��Ca��Cl��Ħ����ԼΪ1?2�������������Ӧ����ȫ�������������������δ��ڣ����ǵ�Ca��Cl��Ħ���ȣ�����Ƭ���Ѿ�û����ƻ�����Ĵ���(��ͼ3(b))�����ŵ���¶����ߣ���������������һ�����ͣ�������¶�Ϊ1 050 ��ʱ����ɫ������������0.20%������������������������Ϊ3.20%������Ƭ�л���������ĵͼ��������Nb-O���������(��ͼ3(c))��������¶�Ϊ1 150 ��ʱ����ɫ��Ϊ100%�Ľ����꣬ͼ�г�������������������������0.10%(��ͼ3(d))��������������1���С�
��1 ��ͬ����¶�ʱ�������������������
Table 1 EDX results of cathode at different electrolysis temperatures (mole fraction, %)
ͼ4��ʾΪ��ͬ����¶��²����XRD�ס���ͼ4�ɼ�����950 ����4 h�����м���NbO������壬��������NbO2��NbO1.1��NbO0.7������壬��˵����ⷴӦ�����ף����������������ϣ���1 050 ��������г��˽���Nb�������֮�⣬��������NbO������壻��1 150 ���������ֻ�н���Nb������壬δ���������ʷ塣��XRD�о����пɷ��֣���ⷴӦ���ڣ�������û�з�����ƻ����������壬���ǰ��ķ��������о���ΪSOM���ܺܺõؿ�����ƻ��������ɣ����ٵ����̸���Ӧ�ķ���������ʱ��Ӧ�����ף����������ڽϵ��¶�ʱ���γɿ���ϸС���ṹ���ܵĽ������O2?�ھ����ڵ���ɢϵ����С����֮�����ڵ��µ�ճ�Ƚϴ������������ڲ������ѡ�ͬʱ�����£���Ĥ�������Ӵ�����Ҳ�ܵ�һ������Լ������������ؽ����������ڲ���������������̼�������ˣ�����������Ӧ��ϳ�ʱ�䣬�������ܱ���ȫ��ԭ�����¶�Ϊ1 150 ��ʱ����ⷴӦ����4 h����ɣ���ʵ��Ч����Ϊ���룬�ʵ���¶ȶԻ�ԭ��Ӧ�Ľ����нϴ��Ӱ�졣
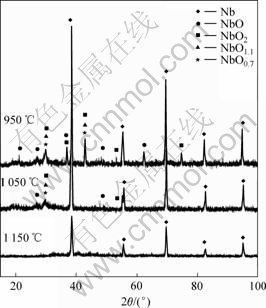
ͼ4 ��ͬ����¶��µ��4 h���������XRD��
Fig.4 XRD patterns of products electrolyzed at different temperatures for 4 h
2.3 ��ⷴӦ�ĵ绯ѧ��������
ͼ5��ʾΪ����ѹΪ3.2 V������¶ȷֱ�Ϊ950��1 050��1 150 ��ʱ��������ʱ��仯�����ߡ�ͼ��ʵ�����ݱ��ֳ����µı仯���ɣ���·������ʵ���¶ȵ����߶�������ʼ�ε����ϴ���ֵ˥���Ͽ죻����Լ1 h����˥�����������������̵����IJ�����С��
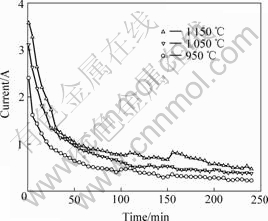
ͼ5 ��ԭ���̵ĵ����仯
Fig.5 Changes of current during electrolysis process
��FFC���������Ʊ�������[10, 14]��ȣ�SOM������ýϴ�ĵ�����������Ҫ�����ڹ�����Ĥ�Ĵ���ʹ�ò���������Ӧ��ֻ��O2?���о������ڽϸߵĵ���ѹ�½��ж�û�и���Ӧ��Ӱ�졣ͬʱ�����������ⲿ���Ʒ�ʽ�������缫˿������Ƭ�ĽӴ�����ϴ�ӦԴ�϶࣬�����������ٶȽϿ죬����·�еĵ���������O2?�Ķ��ݶ���������˱������ĵ����ϴ��о�����к��ڣ���������������ļ�̬���ͣ������۷ֽ��ѹ�����ں㶨�ĵ���λ
�£����ŵ��Ľ��У���ĸ������ﱻ��ԭΪϵ�еͼ������O2?�ĵ����ٶȽ��������ͬʱ����������ı��棬O2?���������ڲ���ɢ�����ε��ٶȱ�������˵�����С��˥��������
���ݷ����ڶ��ɣ���950 ����4 h�����ĵĵ���Ϊ2.8 A?h�������ϵ���ѳ�������ӦΪ52.2 mmol��ͨ�����о�������õ�����������������?��ȡ������������ʵ���ϴ�Nb2O5Ƭ�е���ѳ�������Ϊ41.1 mmol���ʿ�֪ʵ�������µĵ���Ч��Ϊ78.8%, ͬ����������õ�1 150 ���¶��µĵ���Ч��Ϊ81.7%��
3 ����
1) ����SOM����1 150 ���CaCl2������ϵ�У�������ѹΪ3.2 V�����ʱ��Ϊ4 hʱ����ֱ����Nb2O5�Ʊ��������ꡣ
2) ����¶ȶԻ�ԭ���ٶȺͻ�ԭ���������ò����Ҫ��Ӱ�죬���¶�Ϊ1 150 �棬���ʱ��Ϊ4 hʱ�������ܱ���ֻ�ԭ����������Ҳ���ŵ���¶ȵ����Ӷ����
3) ������Ĥ��ʹ�ÿ��Լ��ٸ���Ӧ�ķ�����������ĵ���Ч�ʣ��ӿ컹ԭNb2O5���ٶȣ�1 150 ���µĵ���Ч�ʿɴ�81.7%��
[1] �μ���. ���깤ҵ�Ľ�����չ��[J]. ϡ�н���, 2003, 27(1): 23?27.
HE Ji-lin. Progress and prospect of tantalum & niobium industry[J]. Chinese Journal of Rare Metals, 2003, 27(1): 23?27.
[2] ������, �¾�¼. ���Ӧ����״��չ��[J]. ������ɫ����, 1998, 11: 16?19.
QU Nai-qin, CHEN Jiu-lu. Actuality and prospect of application of niobium[J]. National Nonferrous Metal, 1998, 11: 16?19.
[3] KAMAT G R, GUPTA C K. Open aluminothermic reduction of columbium (Nb) pentoxide and purification of the reduced metal[J]. Matel Trans, 1971, 2: 2817?2823.
[4] �μ���, ���ڹ�, ����ͤ. �й�����ʪ��ұ��[J]. ϡ�н��������빤��, 1998, 27(1): 9?14.
HE Ji-lin, ZHANG Zong-guo, XU Zhong-ting. Hydro- metallurgical extraction of Ta & Nb in China[J]. Rare Metal Materials and Engineering, 1998, 27(1): 9?14.
[5] FRAY D J, FARTHING T W, CHEN Z. Removal of oxygen from metal oxides and solid solution by electrolysis in a fused salt. UK International Patent PCT/GB99/01781[P]. 1998?06?05.
[6] ³�۸�, �ܹ���, ��ΰ��, ������, ����. �������������Ƽ�����ұ������е�Ӧ�ü�ǰ��[J]. �����о�ѧ��, 2003, 15(5): 69?73.
LU Xiong-gang, ZHOU Guo-zhi, DING Wei-zhong, JANG Guo-chang, XU Kuang-di. Application and prospect of control technologies for electrified particles in metallurgical process[J]. Journal of Iron and Steel Research, 2003, 15(5): 69?73.
[7] GORDO E, CHEN G Z, FRAY D J. Toward optimization of electrolytic reduction of solid chromium oxide to chromium powder in molten chloride salts[J]. Electrochimica Acta, 2004, 49(13): 2195?2208.
[8] CHEN G Z, FRAY D J, FARTHING T W. Direct electrochemical reduction of titanium dioxide to titanium in molten calcium chloride[J]. Nature, 2000, 407(21): 361?363.
[9] ��С��, �� ��. CaCl2-NaCl���ε��������Ʊ�����Ta[J]. ����ѧ��, 2006, 42(3): 285?289.
HU Xiao-feng, XU Qian. Preparation of tantalum by electro-deoxidation in a CaCl2-NaCl melt[J]. Acta Metallurgica Sinica, 2006, 42(3): 285?289.
[10] YAN X Y, FRAY D J. Production of niobium powder by direct electrochemical reduction of solid Nb2O5 in a eutectic CaCl2-NaCl melt[J]. Metallurgical and Materials Transactions B, 2002, 33(5): 685?693.
[11] �̺�ΰ, ³�۸�, �� ǫ, ������, ��ΰ��, �ܹ���. ������Ĥ���Ʊ�������[J]. ����ѧ��, 2006, 42(5): 500?504.
CHENG Hong-wei, LU Xiong-gang, LI Qian, LIU Jian-min, DING Wei-zhong, ZHOU Guo-zhi. Preparation of metal tantalum by solid oxygen-ion membrance[J]. Acta Metallurgical Sinica, 2006, 42(5): 500?504.
[12] ������, ³�۸�, �� ǫ, �³���, �̺�ΰ, �ܹ���. SOM����ԭTiO2��ȡ�����ѵ��о�[C]//κ����Ժʿ�����ٳ������ļ�. ����: ��ѧ������, 2006: 292?298.
LIU Jian-min, LU Xiong-gang, LI Qian, CHEN Chao-yi, CHENG Hong-wei, ZHOU Guo-zhi. Solid oxide membrane process for titanium production directly from titanium oxide[C]//Collection of Essays in Commemoration of the 100th Birth of WEI Shou-kun Academicians. Beijing: Science Press, 2006: 292?298.
[13] KRISHNAN A, LU X, PAL U. Solid oxide membrane process for magnesium production directly from magnesium oxide[J]. Materials and Metallurgical Transactions B, 2005, 36(4): 463?473.
[14] ������, �� ��, �� ��, ����, ������. ����������Nb2O5ֱ���Ʊ�������[J]. �й���ɫ����ѧ��, 2005, 15(4): 541?545.
DENG Li-qin, XU Qian, LI Bing, ZHAI Yu-chun, HUANG Zhen-qi. Preparation of niobium by direct electrochemical reduction of solid Nb2O5[J]. The Chinese Journal of Nonferrous Metals, 2005, 15(4): 541?545.
[15] CHEN G Z, GORDO E, FRAY D J. Direct electrolytic preparation of chromium powder[J]. Metallurgical and Materials Transactions B, 2004, 35(2): 223?233.
[16] �³���, ³�۸�, �� ǫ, �̺�ΰ, ������, �ܹ���. Ta2O5ֱ���Ʊ���������о�[J]. ϡ�н���, 2007, 31(3): 306?310.
CHEN Chao-yi, LU Xiong-gang, LI Qian, CHENG Hong-wei, LIU Jian-min, ZHOU Guo-zhi. Tantalum production directly from Ta2O5[J]. Chinese Journal of Rare Metal, 2007, 31(3): 306?310.
������Ŀ�����Ҹ����о���չ�ƻ�������Ŀ(2006AA06Z124)��������Ȼ��ѧ����������Ŀ(50774052)���Ϻ�������ѧ�ƴ�ͷ�˼ƻ�������Ŀ(06XD14032)
�ո����ڣ�2007-11-05�������ڣ�2008-04-28
ͨѶ���ߣ�³�۸գ����ڣ���ʿ���绰��021-56335768��E-mail: luxg@shu.edu.cn
ժ Ҫ�����ù�����Ĥ(SOM)��ֱ�ӵ�ԭNb2O5�Ʊ�����Nb����CaCl2������ϵ�У�����ѹ����Ϊ3.2 V���Ծ���1 200 ��Ԥ��4 h���͵�Nb2O5Ϊ����������ﯹ���̼���͵�Һ̬ͭ�Ͻ�Ϊ�������о����ʱ��ֱ�Ϊ0.5��1��2��4 h�Լ���ͬ�¶��µ����������ɺͲ�ͬ����¶ȶ����������ṹ��Ӱ�졣������������ŵ��Ľ��У�Nb2O5����ת��ΪNb��һϵ�еͼ�����������ű���ԭ�ɽ���Nb��������ʵ���¶ȵ����ߣ�����ٶ���Ӧ�ӿ죬����������ߴ�������FFC����ȣ�SOM�����и��ߵĵ��Ч�ʣ�1 150 ���µĵ��Ч�ʿɴ�81.7%��


