��ѡ�߹�������п���е�������о�
����ΰ1, 2����˫1, 2���°���1, 2��������1, 2����ϣ��1, 2������1, 2���ֺ�Ȫ3
(1. ���ϴ�ѧ ұ���ѧ�빤��ѧԺ������ ��ɳ��410083��
2. ���ϴ�ѧ ϡ�н���ұ��������Ʊ�����ʡ�ص�ʵ���ң����� ��ɳ��410083��
3. ������ɫ������˾������ ������730900)
ժ Ҫ���������п���ۺ����ù��յ���״�Ͳ��㣬����������������İݶ�����ֲ������п���ʪ���������̶��γɡ�п�ݶ��������������п���е���������¹��ա�ʵ������������NaOH������Ϊ����������3.5�����¶�Ϊ140 �棬����ʱ��2 h��Һ�̱�Ϊ10?1(mL/g)ʱ��п�Ľ����ʴﵽ95.1%����Ľ�����Ϊ45.5%������п���ڸ��¡���ʱ���ǿ��е��������������ܲ���Na2ZnSiO4�ǵ���п�����ʽ��͵���Ҫԭ��
�ؼ��ʣ�
��ͼ����ţ�TF813 ���ױ�־�룺A ���±�ţ�1672-7207(2010)04-1246-05
Alkali leaching of refractory high silica zinc oxide ore by mechanical activation
ZHAO Zhong-wei1, 2, LONG Shuang1, 2, CHEN Ai-liang1, 2, HUO Guang-sheng1, 2,
JIA Xi-jun1, 2, LI Hong-gui1, 2, YAN Hai-quan3
(1. School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China;
2. Key Laboratory of Hunan Province for Metallurgy and Material Processing of Rare Metals, Changsha 410083, China;
3. Baiyin Nonferrous Ltd., Baiyin 730900, China)
Abstract: The present state and shortages comprehensive utilization of zinc oxide ores were described in this paper, and the Bayer process used to treat bauxite was transplanted to treat zinc oxide ores. So, this process can be regarded as ��zinc Bayer process��. And a new method for alkaline leaching of refractory hemimorphite by mechanical activation was put forward. Optimized leaching parameters are obtained through experiments, as follows: the sodium hydroxide dosage = 3.5 times as much as the theoretical quantity, the leaching time = 2 h, temperature = 140 �� and ratio of leaching liquid to leaching solid (L/S) =10?1. Under these conditions, the leaching rate of zinc and silicon can reach 95.1% and 45.5%. Overlong leaching time and intense mechanical activation will deteriorate the zinc leachability and thus accelerate the Na2ZnSiO4 formation.
Key words: Bayer process; leaching; mechanical activation; leaching rate
����п���ڹ��ⱻ��Ϊ������п��[1]������п����Ҫ����������п��(Zn2SiO4)����п��(ZnCO3)���켫��[Zn4(Si2O7)2(OH)2��H2O]��[2-3]��Ŀǰ������п��ʯ�Ĵ�����ʽ��2�֣�(1) ����п��ʯ��ѡ�������ұ������ý���п������������п��������ص�(��ѡ���߹����) ������ѡұ�������Ѷȣ�(2) ����п��ʯֱ����ұ������ֱ��ұп���ַ�Ϊ��ʪ��2�ࡣ��������п�������û��������Ǹù��ջ��ڶ࣬���̳����豸�Ӵ��ܺĸߣ����һ����������ˣ�һ�㶼����ʪ��(�����ᷨ�ͼ����)����[4]�������ں��д����������������п����˵�������������ᷨ�������������ɵĹ��Ὣ��������[5]��������ֹ����п��Һ���ཬ�ķ��롣Ŀǰұ�������Ѿ��������ø��������������۹��ᣬ�����ʹ��������������������ӣ����һ������䱸���ӵľ����� ��[6]��Ϊ�˽���������⣬������Խ��Խ����о��߿�ʼ��������п��ļ�����о���
����п��ļ������Ҫ�����������ƻ�ˮ�����Խ�����������ZnCO3�����ߵ�����п��������[7]�о��˰���������ZnCO3����������п��ʹп�백ˮ����п�������ӽ�����Һ��Ȼ���ٽ�����Һ��ȥ�����п����Frenay[8]�����������п���ڲ�ͬ���Խ����е��ܽ�ʵ�飬����Ϊ�ڽϸߵ��¶�����������������������������п�������п����п��Ч���� �á�Ȼ��������ұ�����߶Ը߹�������п��[Zn4(Si2O7)2(OH)2��H2O]���о����١�Ϊ�˳�����ø߹�������п�����Դ�Լ���������������[9]�����о���������ĥ���Ը߹�������п����л�е��� ��[10]����ͼǿ���߹�������п��ļ�ֽ���̡�
1 ʵ��
1.1 ʵ��ԭ�ϼ��豸
���о����õ�ʵ��ԭ��Ϊ������ƺ������п����XRD����ͼ����ҪԪ�صĻ�ѧ�ɷ�(��������)�ֱ���ͼ1�ͱ�1��ʾ��
��ͼ1��֪������п������Ҫ�����켫��[Zn4Si2O7(OH)2?H2O]��ʯӢ[SiO2]��������[Fe2O3]��������[FeO(OH)]�����ʡ�
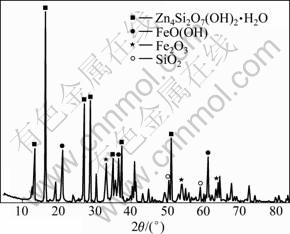
ͼ1 ����п���XRD����
Fig.1 Results of XRD analysis of zinc oxide ores
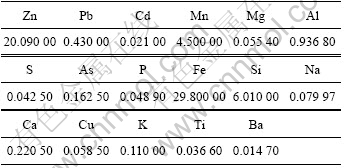
��1 ����п��ѧ�ɷ�
Table 1 Chemical composition of zinc oxide ores %
��е��豸Ϊ����װ���Ϸ��õ���������ƳɵĹ�Ͳĥ����Ͳ�ߴ�Ϊ580 mm��120 mm�������豸��3������¯��ɣ��¶���KSY-18�¶ȿ�����ͨ��E��(����-��ͭ)��װ�ȵ�ż���ƣ�������ɲ�ͬ��С��һ��������ɵĸ�����ɣ������豸ΪL-600��̨ʽ�����Զ�ƽ�����Ļ���
1.2 ʵ�鷽��
����ʯϸĥ����ȡ25 g ����п���ĩ��һ�������Ũ�ȵ�NaOH��Һͬʱ������װ�л���ʵĹ�Ͳ�С�Ȼ������¶ȿ�������Ԥ��ֵ�����¶�������Ԥ��ֵʱ��ʼ��ʱ���ﵽԤ��ʱ���ֹͣ���ȣ���ʱʹ�����Ļ����з��룬��Һ����ϵζ�����������Zn������(Zn)���ù�������ȷ���������Si����Ũ�Ȧ�(Si)��Ȼ����ʽ(1)�ֱ��������п����Zn��Si�Ľ����ʡ�
![]() (1)
(1)
���У�RΪZn��Si�Ľ����ʣ�%����Ϊ����Һ��Zn��Si������Ũ�ȣ�g/L��VΪ����Һ�������L��wΪ����п����Zn��Si������������%��
2 ʵ����������
2.1 �¶ȶ�п�������Ӱ��
��Һ�̱�Ϊ10?1��NaOHŨ��Ϊ5 mol/L������ʱ��Ϊ2 h�������£������¶ȶ�п������ʵ�Ӱ�죬�����ͼ2��ʾ��
��ͼ2��֪��п�������ͬ�Ľ������ԡ����¶ȵ���140 ��ʱ��п��Ľ��������¶����������ӣ����������ڼ�����Һ�У�����п����п�跢�����·�Ӧ[11-13]��
ZnO+2NaOH+H2O��Na2Zn(OH)4 (2)
Zn4(OH)2Si2O7��H2O+12NaOH��Na2Zn(OH)4+Na2SiO3 (3)
SiO2+2NaOH��Na2SiO3+H2O (4)

ͼ2 �¶ȶ�п������ʵ�Ӱ��
Fig.2 Effect of temperature on leaching rate of zinc and silicon
���ң��ڻ�е������ͨ���߹�������п����ѧ�о����֣���Ӧ���E=45.7 kJ/mol�����ܻ�ѧ��Ӧ���ƶ���ѧ���䣬�����¶ȵ�����������Ӧ�����Ӿ��ң�п��Ľ�������֮���ӡ����ǵ��¶ȳ���140 �棬п��Ľ�������ͬʱ�����С��ͨ������п����165���½�������XRD����ͼ(ͼ3)��֪������ǿ��е����ã���Ӧ�õ�һ�ֽ�״Na2ZnSiO4����ò����¶�Խ�߶�������Խ����[14-15]���⽫�������к�п�費�����ӣ��Ӷ�����п��Ľ����ʽ��͡�Ϊ�����̶Ƚ�������п���е�п�������ܼ���п�ڽ��������е���ʧ��ʵ��ѡȡ��ѽ����¶�Ϊ140 �档
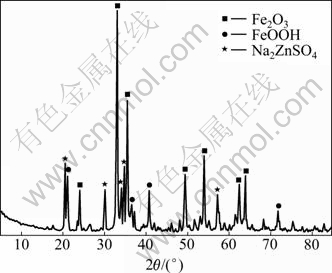
ͼ3 ��������XRD����ͼ
Fig.3 Results of XRD analysis of leaching slag
2.2 ����ʱ���п�������Ӱ��
��Һ�̱�Ϊ10?1��NaOHŨ��Ϊ5 mol/L�������¶�140 ��������£��������ʱ���п������ʵ�Ӱ�죬�����ͼ4 ��ʾ��
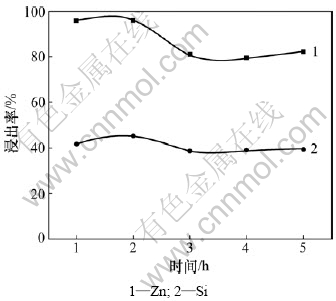
ͼ4 ʱ���п������ʵ�Ӱ��
Fig.4 Effect of time on leaching rate of zinc and silicon
��ͼ4��֪����Ӧʱ���п��������м�����ͬ��Ӱ�죬����Ӧʱ��С��2 hʱ�����ŷ�Ӧʱ����ӳ���п��Ľ����ʻ������䣻������Ӧʱ�䳬��2 hʱ��п��Ľ����ʲ��Ͻ��ͣ�������ڲ��䣬������Ϊ��ǿ��е��������£���Ӧʱ���Na2ZnSiO4���������ƶ����ã��������к�п�費�����࣬п��Ľ������Ͻ��ͣ��������ƽ�⡣��ѡ��ѽ���ʱ��2 h��
2.3 ��Ũ�ȶ�п���������Ӱ��
��������ѧƽ����㣬��Ũ��Խ��п���ܽ��Խ��[12]���Խ���Խ��������ϼ���ܽ���ۺϿ��ǣ�����ѡȡNaOH����Ϊ��������(12.8 g)��1��2��3��4��5�����¶�Ϊ140 �棬Һ�̱�Ϊ10?1������ʱ��Ϊ2 h����������ͼ5��ʾ��
��ͼ5��֪��п��Ľ����������ҺNaOH���������Ӷ����ӣ�����NaOH�����ﵽ����������3.5���Ժ�п�Ľ��������ӱ�û�������NaOH�����ﵽ����������4���Ժ��Ľ��������ӱ�û�����������Ϊ�ڽ���������Zn�������ォ��NaOH�ֱ���(2)��(3)ʽ��Ӧ�����ɿ����Ե�Na2Zn(OH)4(aq.)(��Na2ZnO2)����,��һ����Χ������NaOH ��Ũ�ȶԷ�Ӧ(2)��(3)�ķ����������ƶ����ã������ڹ����ܻ�ѧ��Ӧ������ƣ����¶�һ����ǰ���£�����NaOH Ũ�ȵ����ӣ��������ƶ�������֮��С����������㡣�ʵ�NaOH������������������3.5��ʱ��Zn�Ľ����ʻ������ڲ��䡣��ȷ����ѽ�������NaOH������Ϊ����������3.5����

ͼ5 NaOH������п������ʵ�Ӱ��
Fig.5 Effect of sodium hydroxide concentration on leaching rate of zinc and silicon
2.4 Һ�̱ȶ�п�������Ӱ��
�ڼ���Ϊ2?1���¶�Ϊ140 �棬����ʱ��2 h�������£�����Һ�̱ȶ�п������ʵ�Ӱ�죬�����ͼ6��ʾ��
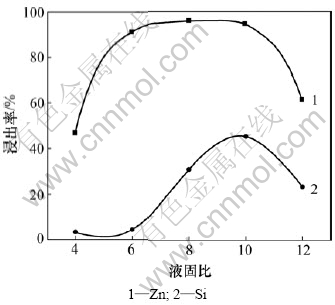
ͼ6 Һ�̱ȶ�п��������ʵ�Ӱ��
Fig.6 Effect of ratio of leaching liquid to leaching solid on leaching rate of zinc and silicon
��ͼ6��֪��Һ�̱ȶ�п������ʵ�Ӱ��ϴ�Һ�̱�С��10?1ʱ��п��Ľ�������Һ�̱ȵ����Ӷ����ӣ�ֻ�ǵ�Һ�̱ȴﵽ6?1�Ժ�п�Ľ��������ӱ�ñ�У����������Ҫ����ΪҺ�̱���һ���̶������ӽ����������Ӽ����ɢ�������Ǻ�п����������Һ��Ҳ��һ�����ܽ�ȣ�Һ�̱�С������п�Ľ����̶ȡ�����Һ�̱ȴ���10?1�Ժ�п��Ľ�������Һ�̱ȵ����ӷ�����С��������ΪҺ�̱�̫���ʹ������ĥ�ĻЧ�����Ҽ��Ũ�ȱ��̫��Ҳ������п��Ľ����ʽ��͡��ۺϿ���ȷ����ѽ���Һ�̱�Ϊ10?1��
3 ����
(1) ���¶ȳ���140 ��ʱ����п����ǿ��е������½��������ܲ���Na2ZnSiO4������п��������ʧ�Ӷ������ʽ��͡�
(2) ����п���ڳ��Ľ���ʱ�䡢ǿ��е������½��������ܲ���Na2ZnSiO4������п�Ľ����ʽ��͡�
(3) ��NaOH������Ϊ����������3.5�����¶�Ϊ140 �棬����ʱ��2 h��Һ��Ϊ10?1ʱ������п���е������п�Ľ����ʴﵽ95.1%����Ľ�����Ϊ45.5%��
�ο����ף�
[1] ���Ǵ�, ����ƽ, �, ��. ��Ʒλ����п��İ�-��ν����о�[J]. ����ۺ�����, 2008(2): 3-5.
LIU Ya-chuan, LIU Shu-ping, LI Bo, et al. Research on ammonia-ammonium chloride leaching of a low-grode zinc oxide ore[J]. Multipurpose Utilization of Mineral Resources, 2008(2): 3-5.
[2] ������, ŷ����, ������, ��. ��Ʒλ����п��ʯ�ļ����[J]. ʪ��ұ��, 2005, 24(1): 23-25.
LIU San-jun, OU Le-ming, FENG Qi-ming, et al. Alkaline leaching of Zn from zinc oxide ore[J]. Hydrometallurgy of China, 2005, 24(1): 23-25.
[3] Ҧҫ��, ����, ��ƽ. ��ѡ����п���Ķ���ѧ�о�[J]. ��ɫ����, 2004, 53(3): 49-51.
YAO Yao-chun, ZHU Yun, WANG Ping. Kingetic study on ammonia leaching of refractory minerals of zinc oxide[J]. Nonferrous Metals, 2004, 53(3): 49-51.
[4] ��Խ, ������, ��ά��. ��Ʒλ����п��������������о�[J]. ��ұ����, 2002, 22(3): 63-65.
LAN Zhuo-yue, HU Yue-hua, LI Wei-zhong. Sulfuric acid leaching of low-grade zinc oxide ore��A study[J]. Mining and Metallurgical Engineering, 2002, 22(3): 63-65.
[5] ���, ������, ������. �����߹�п��ɰ�й轺�۳��Ĺ���[J]. �й���ɫ����ѧ��, 2003, 13(6): 1114-1117.
LI Feng, JIN Zuo-mei, WANG Li-sheng. Silica gel aggregation under acidic leaching of high-silica containing zinc calcine[J]. The Chinese Journal of Nonferrous Metals, 2003, 13(6): 1114-1117.
[6] ������, ������, �ƺ��. �߹�����п������ѹ�����о���չ[J]. ������ɫ����, 2005(2): 14-16.
CHEN Yong-hai, TAN wen-qing, HUANG Hong-jun. Development of silica-removal study on leaching high-grade silico zinc oxide ore with sulfuric acid[J]. Hunan Nonferrous Metals, 2005(2): 14-16.
[7] ������, ŷ����, ������. ����п��ļ�����о�[J]. �������������, 2004(4): 39-43.
LIU San-jun, OU Le-ming, FENG Qi-ming. Alkaline leaching of a zinc oxide ore[J]. Conservation And Utilization of Mineral Resources, 2004(4): 39-43.
[8] Frenay J. Leaching of oxided zinc ores in various media[J]. Hydrometallurgy, 1985(15): 243-253.
[9] ����, ���Ʒ�, ��С��, ��. �ݶ����ܳ����̽��ͳ�����[J]. �й���ɫ����ѧ��, 2006, 16(3): 555-559.
LIU Gui-hua, LIU Yun-feng, LI Xiao-bin, et al. Reducing loss of soda in red mud in process of Bayer digestion[J]. The Chinese Journal of Nonferrous Metals, 2006, 16(3): 555-559.
[10] ����, ����, ��ïʢ. ����ĥ�մ��������¹����о�[J]. �й���ҵ, 1997, 21(4): 16-18.
GU Heng, LI Hong-gui, LIU Mao-sheng. Study on the new technology for treatment of the molybdenum residue of ammonia-leaching with sodium carbonat in a heat ball-millreactor[J]. China Molybdenum Industry, 1997, 21(4): 16-18.
[11] ������, ��һ��. �߹�����п����������Ĺ��ռ������о�[J]. ��ɫ����: ұ������, 2003(5): 9-11..
LIN Zuo-yan, HUA Yi-xin. Technology and mechanism study on leaching high silicon zinc oxide ore with sulfuric acid[J]. Nonferrous Metals: Smelting, 2003(5): 9-11.
[12] �ų���, ������, ��ϣ, ��. ��пΣ�շ���ļ�����о�[J]. ��ɫұ��������о�, 2007, 28(23): 88-90, 102.
ZHANG Cheng-long, QIU Yuan-yuan, HUANG Xi, et al. Research on alkaine leaching of hazardous waste bearing Zn[J]. Nonferrous Metals Engineering and Research, 2007, 28(23): 88-90, 102.
[13] ��С��, ������, ����, ��. NaOH-NaAl(OH)4-H2O��ϵ���ϵ���ļ���ģ��[J]. ���ϴ�ѧѧ��: ��Ȼ��ѧ��, 2006, 37(3): 493-497.
LI Xiao-bin, REN Wan-neng, LIU Gui-hua, et al. Activity coefficient calculation model for NaAl(OH)4-NaOH-H2O system[J]. Journal of Central South University: Science and Technology, 2006, 37(3): 493-497.
[14] Malavasi G, Lusvardi G, Pedone A, et al. Crystallization kinetics of bioactive glasses in the ZnO-Na2O-CaO-SiO2 system[J]. J Phys Chem, 2007, 111: 8401-8408.
[15] ������, ������, ����. Na2ZnSiO4�����ϳɼ����ӵ������ʵ��о�[J]. ���ɹ������ѧѧ��: ��Ȼ��ѧ��, 2004, 19(5): 511-513.
FU Ge-yan, BAO Yu-min, FU Ke. Microwave synthesize of Na2ZnSiO4 and study of its electric conductivity[J]. Journal of Inner Mongolia University for Nationalities, 2004, 19(5): 511-513.
�ո����ڣ�2009-08-22�������ڣ�2009-11-30
������Ŀ����973�������ص�����о���չ�ƻ�֧����Ŀ(2007CB613603)���������������������˲�֧�ּƻ���(NCET-05-0692)
ͨ�����ߣ�����ΰ(1966-)���У��ӱ������ˣ����ڣ���ʿ����ʦ��������ɫ����ұ����ȡ��ұ����ϵ��Ʊ��о����绰��0731-88830476��E-mail: zhaozw@mail.csu.edu.cn
(�༭ �γ���)
[6] ������, ������, �ƺ��. �߹�����п������ѹ�����о���չ[J]. ������ɫ����, 2005(2): 14-16.
[8] Frenay J. Leaching of oxided zinc ores in various media[J]. Hydrometallurgy, 1985(15): 243-253.
[10] ����, ����, ��ïʢ. ����ĥ�մ��������¹����о�[J]. �й���ҵ, 1997, 21(4): 16-18.
[11] ������, ��һ��. �߹�����п����������Ĺ��ռ������о�[J]. ��ɫ����: ұ������, 2003(5): 9-11..


