ʪ����п���γ��ܹ����з������ӿ����о�
������1, 2��������1�����¸�1�������1��������1��������1
(1. ���ϴ�ѧ ��Ϣ��ѧ�빤��ѧԺ������ ��ɳ��410083��
2. �������ĿƼ�ѧԺ ���繤��ϵ������ ¦�ף�417000)
ժ Ҫ��
�̷�������Ӱ�����ضࡢ��Ӧ������������ķ���������ѵ����⣬����������ӵ���ѧģ������ڱ�����ģ��ר�ҹ���ķ�������ģ�����ϵķ������ӿ��Ʒ��������ǵ�Ӱ�����γ��ܹ����з������ӵ�������������������������п�ۼ�����3����Ҫ���أ��о������������γ��ܷ�Ӧ��ѧ��Ӧ���������Ϻ���ķ���������ѧģ�ͣ�����������Һ��Ũ�ȡ�����Ũ�Ⱥ͵���BT����Ĵ�ʱ�Ͷ�Ӱ������ȷ���ӣ����һ�ֱ�����ģ��ר�ҹ�������������ѧģ�͵ļ���ֵ��������֤���˸÷�������Ч�ԣ�Ϊʵ�����ξ��������̵��ȶ����д�����������
�ؼ���: ʪ����п�������ѧģ�ͣ�������ģ��ר�ҹ���
��ͼ����ţ�TP273 ���ױ�־�룺A ���±�ţ�1672-7207(2013)12-4881-06
Spent acid adding control in cobalt removal using arsenic in zinc hydrometallurgy
WU Tiebin1, 2, YANG Chunhua1, LI Yonggang1, ZHU Hongqiu1, GUI Weihua1, WANG Yalin1
(1. School of Information Science and Engineering, Central South University, Changsha 410083, China;
2. Department of Electrical and Mechanical Engineering,Hunan Institute of Humanities Science and Technology, Loudi 417000, China)
Abstract: To solve the spent acid control problem caused by complexity of the reaction mechanism and the large numbers influence factors of the cobalt removal process using arsenic salt, spent acid adding control method integrated by mathematical model and modified model based on variable universe fuzzy expert rule was proposed. Considering the main factors (arsenic adding, the thickener underflow and the amount of zinc dust) that influence the spent acid adding, a mathematical model based on material balance principle and chemical mechanism of the cobalt removal process was established. At the same time, based on the large time-delay of the concentration of arsenic solution, the concentration of spent acid and the BT (back titration) of underflow influence the accurate adding of spent acid, variable universe fuzzy expert rule was used to amend the spent acid adding calculated by mathematical model. The simulation results show the effectiveness of the control method, which provides convenient conditions for the stability operation of cobalt removal process using arsenic salt.
Key words: zinc hydrometallurgy; spent acid; mathematical model; variable universe fuzzy expert rule
���������dz�ѹ����ʪ����п�����йؼ�����֮һ��������Ũ�ȹ���������ʱп����(�����հ塱)[1-2]�����ξ������ܾ���п�۵��ĵ͡��������ĵͺ�����Ⱦ��������ӵ��ŵ㣬�õ��˹㷺Ӧ��[3-5]����Һ��pH��Ӱ�쾻�����ܵ�һ����Ҫ����[6]����pH̫�ߣ������״������ɼ�ʽ������[7-8]���谭���ܷ�Ӧ�Ľ��в����ѹ�˻�ѹ�����������˲�����[9-10]����pH���ʽ�����εĺ�����û��һһ��Ӧ��ϵ��������Ũ�ܻ�����(���и�Ũ�ȵļ�ʽ������)���صij�ѹ����ʪ����п���γ��ܹ��̣�����pH������Һ�����ȴ��ڽϴ�ľ����ԣ������γ��ܹ��̲��÷��ζ�ֵ(back titration��BT)������Һ�����ȣ�ͨ���������ӵ���ķ�����(��ơ����ᡱ)���Ʒ�Ӧ������Һ��BT�������γ��ܹ����У�BTӰ�����ص�ʱ��������ػ�����ػ�ѧ��Ӧ�ĸ��Ӷ�����Ҫ��������Ĵ��ͺ���ɿ���BT�ķ������Ӽ�Ϊ���ѡ��������Ӳ�������ɳ���������Ũ�ȳ����ѹ�˻�ѹ�����������˲������������ξ������ܹ��̵��ȶ����д����˼������ѣ���ˣ��������ӷ�������γ��ܹ����ȶ����Ż����о��м�����Ҫ�����塣�������߿���Ӱ�����γ��ܹ��̷������ӵ�������������������������п�ۼ�����3����Ҫ���أ��о������������ξ������ܻ�ѧ��Ӧ���������Ϻ���ķ���������ѧģ�͡�������������Һ��Ũ�ȡ�����Ũ�Ⱥ͵���BT����Ĵ�ʱ��Ӱ���˷���������ѧģ�ͼ����ȷ�ԣ�Ϊ�ˣ����һ���ʺ����γ��ܹ�������Ƶ�������ĵı�����ģ��ר�ҹ���������������������ͨ��ʵ���������ݷ�����֤���÷������ӿ��Ʒ�������Ч�ԡ�
1 ���ξ������ܹ��շ���
����ijпұ����ҵ�����Ĺ������ȵij�ѹ����ʪ����п�����ľ��������Ϊ3���֣�����ͭ(��Һ�б���һ��Ũ�ȵ�ͭ����)�����γ��ܺͳ��ӡ�
���γ��ܹ���������ͼ1��ʾ�����γ��������¶ȡ���Һ�кϽ���(ͨ������Ũ�ܻ��������ڣ��Ͻ��ܴٽ����ܷ�Ӧ����)��BT��Cu2+Ũ�ȵȺ���������£�����Һ�м������������κ�п�ۣ��Ӷ�ʹ��Һ�е�Co2+��CoAs�Ͻ���ʽ����Һ�г������������ʹ����п��Һ�е������ӽ����ʺϵ��ij̶ȡ�
Ӱ�����γ��ܵ������У�BT������Ҫ������֮һ��
BT��ⷽ����ȡ��Ʒ��Һ25 mL����25 mL����ˮһ��ӵ�(�ݻ�125 mL)��ƿ�У�������2~4�μ��ȣ�Ȼ����0.1 mol/L������Һ�ζ���ֱ����ɫ���(pH��3.1ʱ���ȱ��)���ιܵ������ΪBT(���磬�պõζ���������Һ1 mL����BTΪ1)��
����Ϊ��������0.004 mol/L��BT=0�൱�ڼ��ȵĵζ��յ㡣
��BT̫��(1�ų��ܷ�Ӧ������ҺBTÿ2 h�˹����1��)����ζ����Һ�м�ʽ�����κ����ϸߣ������ή�ͳ��ܷ�Ӧ�����ʣ����һ����ѹ�˻�ѹ�����������˲���������BT̫�ͣ�����Һ������������п�۷�Ӧ����������������п�۵��˷ѣ��������������û������Ǿ�����ԭ��ϵ���ή�ͳ��ܷ�Ӧ�����ʡ���ˣ��������ӷ��������Һ��BT�����ξ������ܵ��ȶ����Ż�����������Ҫ��
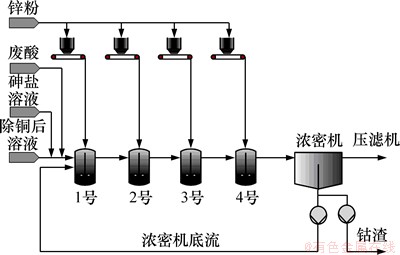
ͼ1 ���ξ������ܹ�������
Fig. 1 Cobalt removal process using arsenic salt
2 �������ӿ���
���о����ó�Ӱ��1�ŷ�Ӧ����ҺBT������Ҫ�������¡�
(1) ���ӵ�������Һ��������ҺΪǿ������Һ(�������������ĩ�ܽ��ڸ�Ũ��NaOH��Һ)�������β���ķ�Ӧ���������ӻ�������ҺBT������
(2) ���ص�Ũ�ܻ�������Ũ�ܻ������к��д�����ʽ������(��BT�ܸ�)����Ҫ���ӷ��ή����BT��
(3) ���ӵ�п�ۡ�����п���û����ܲ��ɱ���س���п�ۺ���Һ��H+��Ӧ����ɷ�Ӧ���оֲ���ҺBTѸ��������
��3����Ҫ�����ֱַ��ܶ������(��������������Χ�ϴ�)Ӱ�죬�Ҹ��ӵ����ξ������ܻ�ѧ��Ӧ��ʹ�÷���������������һЩ�ؼ�ϵ������ȷ�������¿���BT�ķ�������������ȷ����ͨ�������γ��ܹ��̵��о�������Ӱ��������ӵ�3����Ҫ���أ������˻������ξ������ܻ�ѧ��Ӧ���������Ϻ���ķ���������ѧģ�͡����ڵ���BT������Ũ�Ⱥ�������Һ�����Ũ�ȼ�NaOHŨ�ȵȹ��ղ�������Ĵ��ͺ�(ÿ8 h����1��)Ӱ���˷����ȷ���ӣ��ʷ���������ѧģ�͵ļ���ֵ�����ƫ���Ҫ�Է���������ѧģ�ͼ���ķ�������������������ģ���������������仯��Ϊ������п��ƣ���Ȼ���������������Ҫ��ר��ϵͳ(expert systems��ES)��Ϊ����֪ʶ��ϵͳ�������ܹ���Ч�ʡ�ȷ��Ѹ�ٵؽ��ʵ�����⣬�õ��˹㷺Ӧ�á�����ר�������ȡ��ר��֪ʶ����δ������ྭ����֪ʶ�й㷺���ڲ�ȷ���Ժ�ģ���ԣ���BT�������������һ����Ը����Ӧ�ô�ͳ��ר��ϵͳ����ںܴ�����⣬��ˣ�����ģ�������������䲻ȷ�������⣬�����ģ��ר��ϵͳ���������γ��ܹ��̽ϸ��ӣ�������ǰ���������ҵ����Ŀ���Ӱ�죬��ͭ��Һ�����͵����������������������й����лᷢ���仯����Ȼ����ͨ��ģ��ר�ҹ�������Ӧ�����ֱ仯��Ϊ���ϵͳ������Ӧ�ԣ��������һ�ֱ�����ģ��ר�ҹ���Է�������������������������ѧģ���������ģ��ר�ҹ�������ģ�����ϵķ������ӿ��Ʒ�������ͼ2��ʾ��
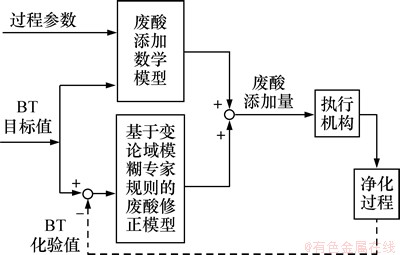
ͼ2 1�ŷ�Ӧ���������ӿ��ƿ�ͼ
Fig. 2 Control block of spent acid adding of the first reactor
2.1 ����������ѧģ��
2.1.1 �����������������
�����ξ������ܹ����У��������ȶ����ͻ�����ã������������Ǹ��ݵ�λʱ���ڽ��뷴Ӧ����ͭ���ܺ������ӵ����ʵ���(����Ũ��ÿ2 h�˹�����1��)��ʽ(1)�����������ӣ�
 (1)
(1)
���У�nCu��nCo��nNi�ֱ�Ϊ��λʱ�������ͭ����Һ���뷴Ӧ����ͭ���ܺ��������ܵ����ʵ�����nAsΪ��λʱ��������Ҫ��������ʵ�������Ϊ����ϵ����0.2�ܦΡ�0.9��
���ε������������1�ŷ�Ӧ����ڵij�ͭ����Һ������������ͭ���ܺ������ӵ�Ũ�� (����Խ��λʱ�������뷴Ӧ��������Խ��)��ء����ڹ���пұ����ҵ������ԭ�ϸ��ӣ��ɷֲ��ȶ����ټ�����Ϊԭ�����豸���أ�ʹ��ʵ�������и�������Ũ�Ⱥͳ�ͭ����Һ���������Ƚϴ������������������dz���
��������������ܽ�������п��Һ�����������������ĩ��Ч�����Բ�������Һ̬������Һ��Ч��[6]�����Ƚ������������ĩ�ܽ��ڸ�Ũ��NaOH��Һ��(����NaAsO2��AsO2-��������Һ����H+����γ�����HAsO2)��������ҺΪǿ������Һ�����������ữ�������ɷ�Ӧ���оֲ���Һ����ˮ�����ɼ�ʽ�����Σ����һ�ʹ������ˮ�Ķ�������ת���ɲ�����ˮ�Ĺ轺���谭�û����ܷ�Ӧ�Ľ��У������ѹ�˻�ѹ����������ѹ�˻��˲���������ˣ���Ҫ�������ӷ��ᡣ��������Һ�ữ�ķ�����������FAcid_As1Ϊ
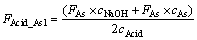 (2)
(2)
ʽ�У�FAsΪ������Һ������(m3/h)��cNaOHΪ������Һ��NaOH��Ũ��(1.8��cNaOH��2.6 mol/L)��cAsΪ������Һ��NaAsO2��Ũ��(2.7��cAs��3.5 mol/L)��cAcidΪ������Һ��H2SO4��Ũ��(1.6��cAcid��2.0 mol/L)��
���β����˾������ܷ�Ӧ����Ӧ�������������ӣ���ɼ�ʽ�����ε�����(����BT����)��
���γ��ܽΣ���Ҫ��ѧ��Ӧ����[6, 9]��
 (3)
(3)
 (4)
(4)
 (5)
(5)
 (6)
(6)
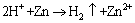 (7)
(7)
 (8)
(8)
 (9)
(9)
 (10)
(10)
��Ӧ(3)~(6)����Ҫ��Ӧ������Ӧ(7)��(9)��(10)�ķ�����������ԭ��λ(oxidation reduction potential��ORP)[11-12]��Ӱ�죬ֻ�е�ORP�ϸ�ʱ�Żᷢ����ORP��������һ�ֻ�ϵ�λ������Һ���ڶ�̬ƽ��ʱ�ĵ�λ(Ee)����ˣ������ñ���Ee��ʾORP(���ϵ�λ)��
��������������黯������(AsH3)��1-���������ɺϽ���ʣ������������ķ�Ӧ����Ҫ���ӵķ��������FAcid_As2Ϊ
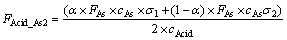 (11)
(11)
ʽ�У���1ΪÿĦ��HAsO2�����黯�����������ĵ��������ʵ�������2ΪÿĦ��HAsO2���ɺϽ���������ĵ����������ʵ�������(����[5%��40%])�������ξ������ܻ�ѧ��Ӧ��ص�ϵ�������ھ������ܻ�ѧ��Ӧ�������ӣ�����ͨ�����淽��ȷ����ϵ�����������ó���HAsO2���ɺϽ�����������黯��ı��缫��λ��һ������Һ��ƽ���λEeԽ��(��ԭ��Խǿ)��Խ���������黯�⣻����Һ�¶�Խ�ߣ�ҲԽ�������黯�����塣
����ʵ�����ݣ��ó�����ƽ���λEe(-600~-520 mV)����Һ�¶�t(65~85 ��)�����ϵʽ��
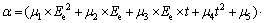
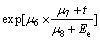 (12)
(12)
ʽ�У���1=3.232 5��10-6����2=1.700 0��10-2����3=-3.020 7��10-6����4=-2.012 1��10-7����5=3.390 0��10-2����6=5.990 0��10-2����7=-50.098 0����8=730.251 1��
��������Ҫ���ӵķ����������FAcid_AsΪFAcid_As1��FAcid_As2֮�͡�
2.1.2 ��������������
ͨ������Ũ�ܻ��������Ʒ�Ӧ������Һ�ĺϽ������������л����д����ļ�ʽ������(��BT�ܸ�)����Ȼ�������ļ�ʽ�����λ��谭���ܷ�Ӧ�Ľ��У�����ͨ�����ӷ��Ὣ����BT����Ŀ��BT�����͵���BT��Ҫ�ķ�����������FAcid_UnderflowΪ
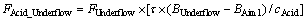 (13)
(13)
ʽ�У�FAcid_UnderflowΪ���������������������FUnderflowΪ��������(m3/h)����Ϊ����1 L��Һ1 BT����������ʵ�����BUnderflowΪ����BT��BAim1Ϊ1�ŷ�Ӧ��Ŀ��BT��
2.1.3 п�����ĵ�������
�����γ��ܹ����У����ӵ�п������һ�����������ӷ�Ӧ������������ɾֲ�pHѸ�����ߣ������ɴ�����ʽ������ (���ֲ���ҺBTѸ������)����Ӧ���ӷ������ƾֲ�BTѸ�����ߡ�п���������ӷ�Ӧ��Ҫ�ķ�����������mZn_feedΪ
 (14)
(14)
���У�mZn_feedΪ��λʱ�������ӵ�п������(kg)��MZnΪпԪ�ص�Ħ��������mZn_useΪ��λʱ������Һ�е�ͭ���Ӻ�HAsO2���ĵ�п������(���������ĵ�п����Ժ�С)����Ϊ�����ij���λʹ�������ӱ�ͭ���Ӻ�HAsO2���Ի�ԭ�ö࣬���Խ�����Ϊͭ������HAsO2��ȫ��ԭ�������ӲŻỹԭ����ͭ���Ӻ�HAsO2��Ӧ��ʣ���п�����Ц�(�¡�[45%��90%])�����������ӷ�Ӧ����������ƽ���λEԽ�����¶�Խ�ߣ�Խ�����������������⣬��Һ�еĺϽ�(Cu3As��CoAs)���������������������ã���Һ�кϽ�����Ũ��(��alloy)Խ�ߣ�Խ����������(���ǣ����Ͻ�����Ũ�ȴﵽһ��ֵʱ���������ò�������)����ˣ��������������׳̶��뷴Ӧ������Һ��ƽ���λ(Ee)����Һ�еĺϽ�����Ũ�Ȧ�alloy (35~80 g/L)���¶�t��أ��������¹�ϵʽ��
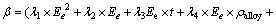
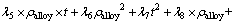
 (15)
(15)
ʽ�У���1=6.503 8��10-6����2=5.500 0��10-3����3=6.965 4��10-6����4=-2.973 2��10-5����5=1.065 4��10-7����6=1.688 2��10-5����7=-2.399 4��10-4����8=-5.547 0�� 10-4����9=2.410 0��10-2����10=1.716 0��10-1����11=1.490 0�� 10-2����12=-19.111 8����13=750.081 5����14=-48.533 5��
�������ξ������ܻ�ѧ��Ӧ���������Ϻ���ֱ�õ�������������������������п�ۼ���������Ҫ�ķ������������ۺ�3�����ؽ�������������ѧģ�ͣ��ܵķ�����������Ϊ
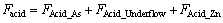 (16)
(16)
�������γ��ܹ��̼�Ϊ���ӣ�����������ѧģ��ֻ��������Ҫ�����أ�����BT������д�ʱ���ص㣬��ˣ�����ķ������������ܴ���һЩƫ���Ҫ�������������
2.2 ���ڱ�����ģ��ר�ҹ���ķ�������
����Ũ�ȡ�����BT��������Һ�����Ũ�ȼ�NaOHŨ�ȵȹ��ղ�������ÿ8 h�Ż���1��(����Ӧ������Һ��BTÿ2 h����1��)���仯��Ĵ�����ʱ��Ӱ���˷�����ѧģ�͵ļ���ȷ�ԣ���ˣ�����Է�����ѧģ�͵ļ���ֵ��������������BT�ͷ���������һ��ģ�������ͳ��ר��ϵͳ����������ģ�����������ģ��ר��ϵͳ����֪ʶ��ȡ��֪ʶ��ʾ�в�����ģ��������ר��ϵͳ���ܽϺõؽ���������⡣
������������������Ҫ����BT�Ļ���ֵ��ǰһʱ�̵ķ��������������������赱ǰBT����ֵ��Ŀ��BT�IJ�Ϊ��BT����BT������Ϊ(-0.7��0.7)��ǰһʱ�̵ķ��Ჹ����Ϊ��Acid1����ǰʱ�̷��Ჹ����Ϊ��Acid2�����������γ��ܹ���ǰ������ҵ����Ŀ��ȵ�Ӱ�죬��ͭ����Һ������Ũ�ܻ�����������ʱ�仯�ϴ�(0.5 h���ϲŻ��нϴ�仯)��������ͬ�����£��ܵ�����Խ����IJ�����ҲӦ����Ӧ��Խ����Ȼ��һ���ģ��ר��ϵͳ������Ӧ���������Ľϴ�仯��Ϊ��֤����������������Ӧ�ԣ��������һ�ֱ������ģ��ר�ҹ�������������������������ͭ����Һ�����������仯ʱ����������������������Ӧ�仯�ģ���Acid1������Ϊ(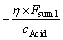 ��
��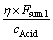 )����Acid2������Ϊ(
)����Acid2������Ϊ(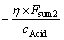 ��
�� )(���У�Fsum1��Fsum2�ֱ��ʾǰһʱ�̺͵�ǰʱ�̵ij�ͭ����Һ������Ũ�ܻ�������������֮�ͣ��������������������ԶԶС�ڳ�ͭ����Һ������Ũ�ܻ�����������������������ʱ���Բ��ƣ���Ϊ����1 L��Һ0.7BT����Ҫ�ķ�������ʵ���)��
)(���У�Fsum1��Fsum2�ֱ��ʾǰһʱ�̺͵�ǰʱ�̵ij�ͭ����Һ������Ũ�ܻ�������������֮�ͣ��������������������ԶԶС�ڳ�ͭ����Һ������Ũ�ܻ�����������������������ʱ���Բ��ƣ���Ϊ����1 L��Һ0.7BT����Ҫ�ķ�������ʵ���)��
���ȣ�����BT����Acid1�͡�Acid2 3�������ֱ�ģ���������IJ��������㡢��״���Һ������ϸ��ӵ�������������С������������������������U��[0��1]�������һӳ��Ϊ ����
���� ��U��[0��1]��ȷ��U��һ��ģ���Ӽ�
��U��[0��1]��ȷ��U��һ��ģ���Ӽ� ��
�� ��ʾԪ��x(x��R)����ģ���Ӽ�
��ʾԪ��x(x��R)����ģ���Ӽ� �ij̶Ȼ�ȼ���
�ij̶Ȼ�ȼ��� ��1��ģ������ģ���Ӽ�
��1��ģ������ģ���Ӽ� �����������Ⱥ�������Ϊ[13-14]��
�����������Ⱥ�������Ϊ[13-14]��
 (17)
(17)
ģ���� ��Ϊ7�����Ա�������ģ���Ӽ��ֱ�Ϊ{NB��NM��NS��ZO��PS��PM��PB}���Ӽ���Ԫ��NB��NM��NS��ZO��PS��PM��PB�ֱ���������С���С���㡢��С�����к�����Ȼ����ģ��֪ʶ����ȷ��ģ���������������г�3�����͵ı�����ģ��ר�ҹ���������ʽ��
��Ϊ7�����Ա�������ģ���Ӽ��ֱ�Ϊ{NB��NM��NS��ZO��PS��PM��PB}���Ӽ���Ԫ��NB��NM��NS��ZO��PS��PM��PB�ֱ���������С���С���㡢��С�����к�����Ȼ����ģ��֪ʶ����ȷ��ģ���������������г�3�����͵ı�����ģ��ר�ҹ���������ʽ��
(1) if ��BT��PB and ��Acid1=NB��then ��Acid2=ZO��������BTΪPB(ʵ�ʻ���ֵԶ����Ŀ��ֵ����ʾ�������ӹ��٣����BT̫��)����Acid1ΪNB(����������Ϊ�������ڷ���������ѧģ�ͼ���ֵ�ϼ����˷�����)ʱ����Ȼ��ǰһʱ�̡�Acid1ΪNB�����Բ�������(��ɷ������ӹ���) ����ǰ����������Ӧ��ΪZO�����������ݡ�BT�������������������ΪPB���ᵼ�·������ӹ��࣬����Ȼ�Dz������ġ�
(2) if ��BT=ZO and ��Acid1=NM��then ��Acid2=NM��������BTΪZO(ʵ�ʻ���ֵ����Ŀ��ֵ����ʾ��������������)����Acid1ΪNMʱ(������������Ϊ�����ڷ���������ѧģ�ͼ���ֵ�ϼ����˷�����)����Ȼ��ǰһʱ����������Acid1ΪNM�Ǻ����ģ���ǰ������������Acid2Ӧ��ΪNM�����������ݡ�BT�������������������ΪZO���ᵼ�·������ӹ��ࡣ
(3) if ��BT=NB and ��Acid1=PB��then ��Acid2 =ZO��������BTΪNB(ʵ�ʻ���ֵԶ����Ŀ��ֵ����ʾ�������ӹ��࣬���BT̫С)����Acid1ΪPBʱ(����������Ϊ�����ڷ���������ѧģ�ͼ���ֵ�������˽϶������)����Ȼ��ǰһʱ�̡�Acid1ΪPB�����Բ�������(��ɷ������ӹ���) ����ǰ����������Ӧ��ΪZO�����������ݡ�BT�������������������ΪNB���ᵼ�·������ӹ��١�
���ݡ�BT�͡�Acid1��������Acid2����ģ�������ɵõ�ǰʱ�̵ķ�������������ǰ�µķ���������Ϊ������ѧģ�ͼ���ֵ�����������֮�͡�
3 �������
Ϊ���鱾������ķ������ӿ��Ʒ��������ξ������ܹ�����Ӧ�õĿ����ԣ�ѡȡ2012-03ijпұ����ҵ���ξ������ܹ���1�ŷ�Ӧ��������������60��(ÿ2 hһ��)���з�����֤���Ȳ���ģ��LSSVMģ��[15]����BT���������������������ͷ�������������ع��ղ���֮��Ĺ�ϵģ��(��������ģ��������ƽ�����������ֵΪ5.6%, ������������ֵΪ16.2%������������Ҫ��)��Ȼ������ģ��LSSVM�Բ��÷������ӿ��Ʒ������BT��������������������ͼ3��ʾ(���У�ʵ��BTΪʵ����������ֵ��ADCM-BTΪ���ñ�������ķ������ӿ��Ʒ���(acid dosage control method)�õ���BT(����ģ��LSSVM�������õ���ֵ)��Ŀ��BTΪ1.3��
��ͼ3�ɼ���ʵ��BT��11�δ��ڵ���1.7�����ߵļ�ʽ�����ι������2��ѹ�˻�ѹ�����Ѻ�1��ѹ�˻��˲����������⣬����BT��1.7��BT��0.9ʱ(��20��������)����϶࣬Ӱ���˳������ʣ�������5��������Ũ�Ȳ��������(��8��)��Զ��������BTʱ�IJ���������ɴ˿�֪���������Ӳ������ᵼ��ѹ�˻�ѹ�����������˲����������һ����������Ӳ����ĸ��ʡ���ͼ3����֪�����ñ�������ķ������ӿ��Ʒ�����BT�IJ�����Χ��1.2��С��0.7����Ŀ��BT��ƫ��ľ���ֵ���ڵ���0.3�������34���½���8�����ɼ�����������ķ������ӿ��Ʒ�����С��BT�Ĵ���Ȳ��������������ڷ������Ӳ�������ɵ�BT����ƫ��ƫ�͵�������ʸ÷������ӿ��Ʒ����ܼ���ѹ�˻�ѹ�����ѵ��������߳��������Ӵ���ʡ�
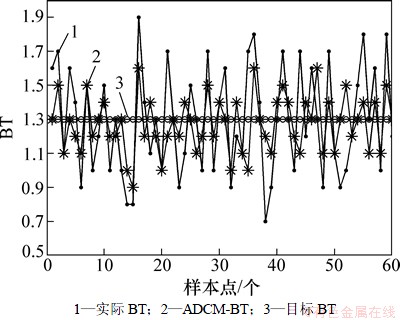
ͼ3 ������ͼ
Fig. 3 Simulation results
4 ����
(1) �����γ��ܹ����У�BTӰ����ܷ�Ӧ���ʺ�ѹ�˻�ѹ�ˣ����ֺ��ʵ�BT�������γ����Ż����е���Ҫ�����������ڷ���Ӱ�����γ��ܵ���Ҫ���صĻ����ϣ������˻��ڳ��ܻ�ѧ��Ӧ����������ƽ��ķ���������ѧģ�͡�
(2) ���ڳ�ͭ����Һ��BT�IJ����ͷ���Ũ�ȡ�����Ũ�Ⱥ͵���BT�ȹ��ղ�������Ĵ��ͺ�����IJ�ȷ���Զ�Ӱ���˷����ȷ���ӣ������һ���ʺ���������Ƶ���ı�����ģ��ר�ҹ���������������������ǿ�˷�������ģ�͵�����Ӧ������������������������ķ�����Ʒ���������С��BT�IJ�����Χ����������BT����߳��������Ӻϸ��ʣ�������ѹ�˻���ѹ��״����Ϊ���ξ������ܵ��Ż����д����˱�Ҫ������
�ο����ף�
[1] B ckman O,
ckman O,  stvold T. Products formed during cobalt cementation on zinc in zinc sulfate electrolytes[J]. Hydrometallurgy, 2000, 54(2): 65-78.
stvold T. Products formed during cobalt cementation on zinc in zinc sulfate electrolytes[J]. Hydrometallurgy, 2000, 54(2): 65-78.
[2] Boyanov B, Konareva V, Kolev N. Purification of zinc sulfate solutions from cobalt and nickel through activated cementation[J]. Hydrometallurgy, 2004, 73(2): 163-168.
[3] Tozawa K, Nishimura T, Akahori M, et al. Comparison between purification processes for zinc leach solutions with arsenic and antimony trioxides[J]. Hydrometallurgy, 1992, 30(1/2/3): 445-461.
[4] Nelson A, Wang W, Demopoulos G P, et al. The removal of cobalt from zinc electrolyte by cementation: A critical review[J]. Mineral Processing and Extractive Metallurgy Review, 2011, 20(4): 325-326.
[5] Vakil S. Technological innovation in the zinc electrolyte purification process of a hydrometallurgical zinc plant through reduction in zinc dust consumption[J]. Hydrometallurgy, 1996, 40(1/2): 247-262.
[6] Satoshi Y, Masakazu O, Sakichi G, et al. Purification of zinc leaching solution: Mechanism of removal of cobalt by zinc dust with arsenious oxide and copper ion[J]. Metallurgical Review of MMIJ, 1997, 14(1): 37-52.
[7] ������. ����п��Һ��п���û����ܵĻ����о�[D]. ����: ����������ѧ������ұ��ѧԺ, 2006: 1-22.
ZENG Guisheng. The mechanism of cobalt removal from zinc sulfate solution[D]. Kunming: Kunming University of Science and Technology. Faculty of Materials and Metallurgical Engineering, 2006: 1-22.
[8] Polcaro A M, Simona P, Stella D. Kinetics of cobalt cementation on zinc powder[J]. Industrial and Engineering Chemistry Research,1995,34(9): 3090-3095.
[9] Jari N. Statistical analysis of cobalt removal from zinc electrolyte using the arsenic-activated process[J]. Hydrometallurgy, 2004, 73(1/2): 123�C132.
[10] DAI Jun, WANG Dequan, JIANG Lan, et al. Removal of cobalt from zinc sulphate solution using rude antimony trioxide as additive[J]. The Transactions of Nonferrous Metals Society of China, 2002, 12(6): 172-175.
[11] Bohn H. Redox potentials[J]. Soil Science, 1970, 112(1): 39-43.
[12] Hiroyoshi N, Kitagawa H, Tsunekawa M. Effect of solution composition on the optimum redox potential for chalcopyrite leaching in sulfuric acid solutions[J]. Hydrometallurgy, 2008, 91(1/2): 144-149.
[13] ����, �ܹ���, ���¼�. ���ӽ���Ĥȼ�ϵ���¶�ģ����ģ������[J]. ����������Ӧ��, 2011, 28(10): 1371-1375.
HU Peng, CAO Guangyi, ZHU Xinjian. Temperature model and fuzzy control for the proton-exchange-membrane fuel cell[J]. Control Theory and Applications, 2011, 28(10): 1371-1375.
[14] LI Shengtun, HO Heifong. Predicting financial activity with evolutionary fuzzy case-based reasoning[J]. Expert systems with Applications, 2009, 36: 411-422.
[15] �����, ������, ������. ����ģ�������ģ��֧����������ʪ����п�������ܹ��̽�ģ[J]. ����ͨѶ, 2010, 20(10): 1068-1071.
ZHU Hongqiu, YANG Chunhua, GUI Weihua. Modeling of cobalt removal purification process in zinc hydrometallurgy based on FCM-SVM[J]. Chinese High Technology Letters, 2010, 20(10): 1068-1071.
(�༭ �²ӻ�)
�ո����ڣ�2012-12-12�������ڣ�2013-02-18
������Ŀ��������Ȼ��ѧ����������Ŀ(61174133��61273159��61273185)�����ҡ�ʮ���塱�Ƽ�֧�żƻ���Ŀ(2012BAF03B05)������ʡ�Ƽ��ƻ���Ŀ(2012CK4018)
ͨ�����ߣ����¸�(1974-)���У����ϳ�ɳ�ˣ���ʿ�������ڣ����¸��ӹ�ҵ���̽�ģ���Ż��о����绰��0731-88876864��E-mail��liyonggang@csu.edu.cn
ժҪ��������γ��ܹ��̷�������Ӱ�����ضࡢ��Ӧ������������ķ���������ѵ����⣬����������ӵ���ѧģ������ڱ�����ģ��ר�ҹ���ķ�������ģ�����ϵķ������ӿ��Ʒ��������ǵ�Ӱ�����γ��ܹ����з������ӵ�������������������������п�ۼ�����3����Ҫ���أ��о������������γ��ܷ�Ӧ��ѧ��Ӧ���������Ϻ���ķ���������ѧģ�ͣ�����������Һ��Ũ�ȡ�����Ũ�Ⱥ͵���BT����Ĵ�ʱ�Ͷ�Ӱ������ȷ���ӣ����һ�ֱ�����ģ��ר�ҹ�������������ѧģ�͵ļ���ֵ��������֤���˸÷�������Ч�ԣ�Ϊʵ�����ξ��������̵��ȶ����д�����������


