п��ѹ��������ѡ������븻���о�
������1, 2, 3�������1, 2, 3��������1, 2, 3�������1, 2, 3��������1, 2, 3���°�Ȼ1, 2, 3
(1. ����������ѧ ����ʡ������ɫ������Դ������ù����ص�ʵ����(��������)������ ������650093��
2. ����������ѧ �dz���ұ��ʡ�������������ص�ʵ���ң����� ������650093��
3. ����������ѧ ����ʡ����Ӧ�ü�װ����������ʵ���ң����� ������650093)
ժ Ҫ��
����ѡ������еĹ�����롢�����Լ���ǻ��ս����о���ȷ�������Һ�������̹������ͽ���ĸҺ�ȷֽ������ǵ���ѹ����������������������ڳ��³�ѹ�£�(NH4)2SŨ��Ϊ2.5 mol/L��Һ�̱�6:1��ʱ��10 min�Ľ��������£�������ʴ�98.66%���������еĸ�����Ϊ93.8%���������й�����Ϊԭ���6�����ϣ�����ĸҺ���ȷֽ��¶�94 �桢�ֽ�ʱ��90 min�������£���ǻ�������98%���ң���Ǵ��ȷ���GB/T 2449��2006��ҵ���һ��Ʒ��������Լ���ѭ�����ã�������Ϊ91.76%��
�ؼ��ʣ�
п��ѹ����������ѡ���������������ǻ����������
��ͼ����ţ�TF111��TQ125.1+1 ���ױ�־�룺A ���±�ţ�1672-7207(2013)03-0901-06
Separation and enrichment of mercury and sulfur from flotation sulfur concentrate derived from zinc pressure leaching residue
WANG Ziyang1, 2, 3, ZHANG Zebiao1, 2, 3, LIU Nengsheng1, 2, 3, PENG Jinhui1, 2, 3, WANG Wankun1, 2, 3, CHEN Anran1, 2, 3
(1. State Key Laboratory of Complex Nonferrous Metal Resources Cleaning Utilization in
Yunnan Province (Breeding Base), Kunming University of Science and Technology, Kunming 650093, China;
2. Key Laboratory of Unconventional Metallurgy, Ministry of Education,
Kunming University of Science and Technology, Kunming 650093, China;
3. Yunnan Engineering Laboratory of Microwave Energy Application and Equipment Technology,
Kunming University of Science and Technology, Kunming 650093, China)
Abstract: The separation and enrichment of mercury and sulfur recovery from flotation sulfur concentrate derived from zinc pressure leaching residue were studied. The optimum procedure parameters were determinated for separation of mercury and elemental sulfur in flotation sulfur concentrate leaching with ammonium sulfide and the recovery of elemental sulfur in polysulfide solution by thermal decomposition. The results show that 98.66% of elemental sulfur is leached, and 93.8% mercury is enriched in residue at liquid/solid ratio of 6:1 with 2.5 mol/L ammonium sulfide concentration in 10 min at room temperature, and the content of mercury is enriched 6 times or more in leaching residue. About 98% sulfur is recovered in polysulfide solution thermal decomposing at 94 �� in 90 min��with a purity of sulfur in accordance with the GB/T 2449��2006 industrial first-rate product standard. Ammonium sulfide can be recycled back into process and the efficiency of ammonium sulfide recovery is 91.76%.
Key words: zinc pressure leaching residue; flotation sulfur concentrate; separation of mercury and elemental sulfur; sulfur recovery; ammonium sulfide
��ʯȼ��ȼ�պ���ɫ����ұ��������������Ҫ����Ϊ���ŷ�Դ[1]��������пұ������Ϊ����Ϊ���ŷ�����Ҫ����Դ֮һ[2]��1999���й���ɫұ���������ŷ���ռ��Ϊ���ŷ�������45%������Լ28%���Խ���пұ��[3]��������Ҳ����ƶ���ǿ�ƵĹ��ŷ����ߺ���Ч�Ŀ��ƴ�ʩ������һЩпұ�����ӷ������л��չ���Ϊ����Ʒ[4]����������һЩ�о��߿�չ��п���̴������ŷ����Ӽ������Χ����Ӱ����о�[5-7]���⽫Ϊ�ҹ���ҵ����п�����й���Ⱦ���ƺ������ṩ�ɿ��Ŀ�ѧ���ݡ��ڴ�ͳʪ����п�����У���п�����ڱ���ʱ����SO2�����������й��Թ���������ʽ��SO2������������ϵͳ��ұ�������������ȥ������Ӧ�÷����е⻯�ط����Ȼ���[8-9]����ҵ�ϴ���������ˮ�ķ����������Ƽ���[10]����ѧ������[11]��������[12]�ȡ���ȫʪ����п�����У���п�����е���Ԫ���ڼ�ѹ����ʱ��Ҫ�Ա��ڴ洢������Ĺ�̬Ԫ������ڽ������У�����Ҫ������ʽ������������������Ĵ����ѻ�������Ⱦ�������������Դ�˷ѡ�ʪ��ұ�����л���Ԫ����ķ����ܶ�[13-14]����Ҫ������ ��[15]�ͻ�ѧ��[16-18]����立�����Ԫ������й������̼���ǻ����ʸߺͻ��յ���Ǵ��ȸߵ��ص�[19]��������������������������ܽ�Ĺ����ӷ�Ӧ�����ܶȻ���С����(���ܶȻ���Ϊ4��10-53)��Ϊ�ˣ��������߲�����立���п��ѹ����������ѡ�������Ԫ����Ļ����Լ����ķ�����������о����ڻ������ʱ��ʹ�������и���������Լ�ѭ��ʹ�ã�ʹ�Լ����ĺ������ɱ���ͣ����й����Ĺ�ҵӦ��ǰ����
1 �����о�
1.1 ����ԭ��
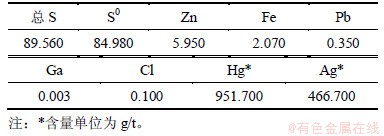
����ԭ��Ϊп��ѹ����������ѡ�����Ԫ������(��������)Ϊ84.980%��ռ��������94.89%��������Ϊ951.700 g/t��������Ҫ������ʽΪ����������������ܵ����ṯ���Ȼ�������ѡ�����Ҫ��ѧ�ɷ�(��������)���1��ʾ���������õ����Ϊ��������
1.2 ����ԭ��
��һ�������£�Ԫ�����뺬��S2-��(NH4)2S��Һ�������ɶ���臨��ܽ�ת����Һ�У���ӦʽΪ��
(x-1)S0+(NH4)2S=(NH4)2Sx
��������У�pH��9~10�����仯ʱ����Һ��Hg2+��S2-����HgS���������ڽ������У���ӦʽΪ��
��1 ��ѡ��ѧ�������
Table 1 Results of chemical analysis of flotation sulfur concentrate %
Hg2++S2-=HgS��
��ʯ��Ԫ����(NH4)2S�ܽ������Һ���뼴���벻�ܵĽ��������룬֮�õ��Ķ����ĸҺ��һ���¶��¼��ȷֽ⣬����Ԫ����ӦʽΪ��
(NH4)2Sx=H2S��+2NH3��+(x-1)S0
�ֽ�������������H2S��NH3������ͨ���������ٽ��䵼��ˮ��Һ�����տ��Ƶ������Һ���ٷ���ѭ�����ã��ֽ�������Ԫ��������������ײ�����Ӧ��������Һ��ȴ�����˳���ǣ���ɺ���Dz�Ʒ��
���ǣ���һ�������£�(NH4)2S��Һ�й�����S2-���ܺ�HgS������Ӧ����������ˮ�Ĺ���������Ӷ����������еĸ�����[12]����ˣ���Ѱ�Һ��ʵĹ���������ʹ��ѡ������Ľ���������Ľ�������С���Ӷ�ʹ�����������С�
1.3 ��������
(NH4)2S��������ѡ����������ͼ1��ʾ��
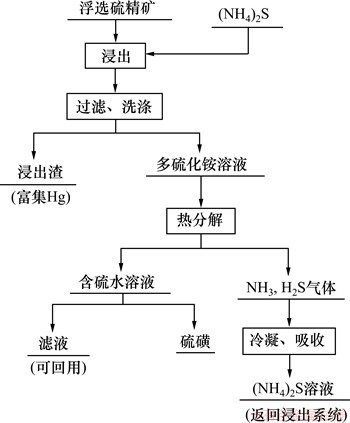
ͼ1 (NH4)2S��������ѡ��������
Fig.1 Flowsheet of flotation sulfur concentrate treated by (NH4)2S method
2 ������������
2.1 �����Һ�Ľ�������
2.1.1 (NH4)2SŨ�ȶ�������ʺ������ʵ�Ӱ��
ȡ��ѡ��50 g��Һ�̱�Ϊ6:1, �����½���40 min������(NH4)2SŨ�ȶ�������ʺ������ʵ�Ӱ�졣��������ͼ2��ʾ��
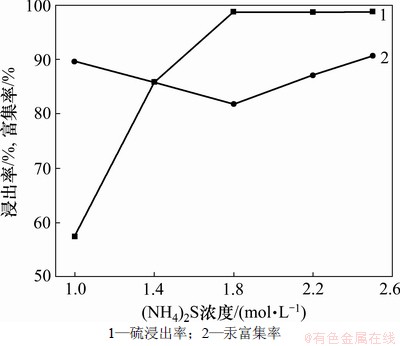
ͼ2 (NH4)2SŨ�ȶ�������ʺ������ʵ�Ӱ��
Fig.2 Effect of (NH4)2S concentration on sulfur leaching and mercury enrichment
��ͼ2���Կ���������(NH4)2SŨ�ȴ�1.0 mol/L���ӵ�1.8 mol/Lʱ��Ԫ��������ʼ�����������ҺŨ�ȴﵽ1.8 mol/L��Ԫ���������ά����98%���ϡ��Թ�Ԫ����˵������(NH4)2SŨ�ȵ����������еĸ������ȼ�С������Ԫ��������ʽϵ�ʱ���Թ��γɰ���������������ʵ���ߣ�Hg2+���ͷŵ���Һ�У���������(NH4)2SŨ�ȣ������S2-��Hg2+�γ�HgS�������������еĸ�����������ߡ�
2.1.2 Һ�̱ȶ�������ʺ������ʵ�Ӱ��
ȡ��ѡ��50 g���ڳ����£��ֱ���Ũ��Ϊ2.2��2.5 mol/L�����Һ����10 min������Һ�̱ȶ�������ʺ������ʵ�Ӱ�졣��������ͼ3��ʾ��
��ͼ3���Կ�������Һ�̱�Ϊ4:1~8:1�ķ�Χ�ڣ�(NH4)2SŨ�ȷֱ�Ϊ2.2��2.5 mol/Lʱ��Ԫ��������ʱ仯�����ԣ�ά����98%���ҡ���һ��(NH4)2SŨ���£�����Һ�̱ȵ����������еĸ�������������С������Һ�̱ȶԹ������ʵ�Ӱ��ȶ�������ʵ�Ӱ������ԡ���������Һ��������������HgS��������������S2-����HgS������Ӧ�����ɿ��������������[HgS2]2-���������ĸ����ʡ��ۺϿ�����Ľ����ʺ��ĸ����ʣ���������ѡȡ��(NH4)2SŨ��2.5 mol/L��Һ�̱�6:1�����½��С�
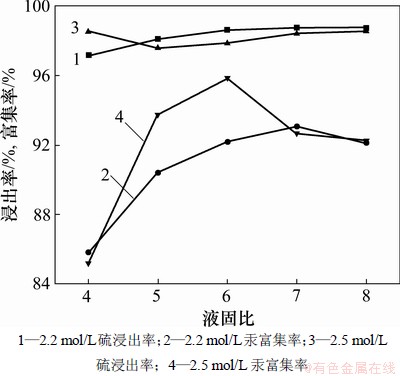
ͼ3 ��ͬŨ����Һ�̱ȶ�������ʺ������ʵ�Ӱ��
Fig.3 Effect of liquid/solid ratio on sulfur leaching and mercury enrichment
2.1.3 ����ʱ���������ʺ������ʵ�Ӱ��
ȡ��ѡ��50 g���ڳ����£�Һ�̱�Ϊ6:1����Ũ��Ϊ2.5 mol/L�������Һ�������������ʱ���������ʺ������ʵ�Ӱ�졣��������ͼ4��ʾ��
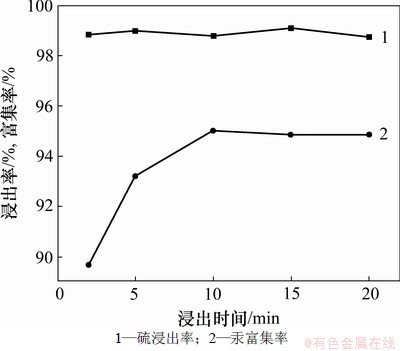
ͼ4 ����ʱ���������ʺ������ʵ�Ӱ��
Fig.4 Effect of leaching time on sulfur leaching and mercury enrichment
��ͼ4���Կ�������ѡ����������������Һ����ʱ������Ч�ʺܸߣ�����ʱ��Ϊ2 minʱ������ʾʹﵽ98.5%���ϣ����Ž���ʱ����ӳ����������������Ա仯�����������ڽ���ʱ��2~10 min֮�������ӣ�10 minʱ�ﵽ���ֵ��
2.1.4 �����¶ȶ�������ʺ������ʵ�Ӱ��
ȡ��ѡ��50 g��Һ�̱�Ϊ6:1����Ũ��Ϊ2.5 mol/L�������Һ����10 min����������¶ȶ�������ʺ������ʵ�Ӱ�졣��������ͼ5��ʾ��
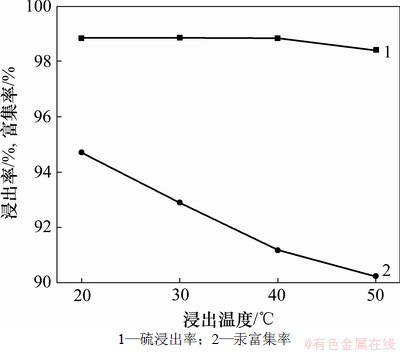
ͼ5 �����¶ȶ�������ʺ������ʵ�Ӱ��
Fig.5 Effect of leaching temperature on sulfur leaching and mercury enrichment
��ͼ5���Կ����������Һ��������У��¶ȶ��������Ӱ���С����20~25����ܻ�úܸߵ�������ʡ�Ȼ�����Ž����¶ȵ����ߣ����ĸ��������Խ��͡������¶ȹ����������Լ��Ļӷ��ͷֽ����ģ�������Һ��S2-Ũ�ȣ�������HgS�����γɣ����������еĸ����ʡ�
2.2 �����ĸҺ���ȷֽ�����
���Խ����������õ��ĺ��������ӵĶ���什���ĸҺ������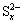 ���ȶ��Խϲ�����Ի���ȵ������¿ɱ��ֽ������Ԫ����������������ȷֽⷽ��������ǡ�
���ȶ��Խϲ�����Ի���ȵ������¿ɱ��ֽ������Ԫ����������������ȷֽⷽ��������ǡ�
2.2.1 �ȷֽ�ʱ����������ʵ�Ӱ��
���ȷֽ��¶�90 �������£���ͬ�ȷֽ�ʱ����������ʵ�Ӱ�죬�����ͼ6��ʾ��
��ͼ6���Կ����������ȷֽ�ʱ����ӳ�������ĸҺ���������������ӡ��ֽ�ʱ��30 min�����������������ӣ��˺�����ʱ����ӳ������������������Ʊ仺��90 minʱ�������ʴﵽ97%���ϡ����鷢�֣�ĸҺ�ֽ�110 min��IJ�Һ��ɫ�Դ�����ɫ�������ֽⲻ���ס��������ֻ�ӳ��ȷֽ�ʱ��û��̫�����壬Ӧ�ʵ�����ȷֽ��¶ȼӿ��������ķֽ���ݳ���
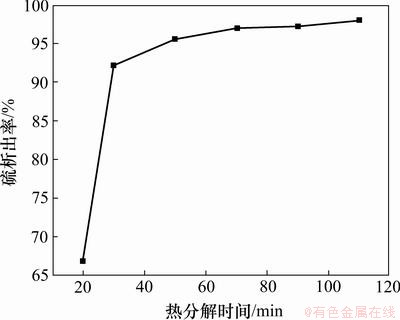
ͼ6 �ȷֽ�ʱ����������ʵ�Ӱ��
Fig.6 Effect of time of thermal decomposition on recovery of elemental sulfur
2.2.2 �ȷֽ��¶ȶ��������ʵ�Ӱ��
�ȷֽ�ʱ��90 min���ȷֽ��¶���75~94 ��(�ѷ���)��Χ�ڶ��������ʵ�Ӱ�죬�����ͼ7��ʾ��
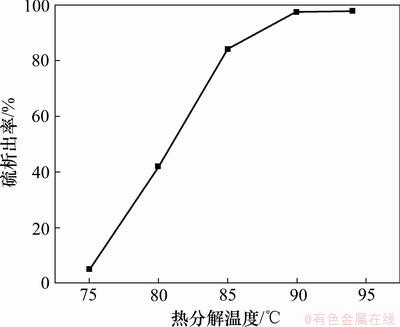
ͼ7 �ȷֽ��¶ȶ��������ʵ�Ӱ��
Fig.7 Effect of temperature of thermal decomposition on recovery of elemental sulfur
��ͼ7���Կ������ȷֽ��¶ȶ��������ʵ�Ӱ��ܴ�90 ��֮ǰ�������������¶ȵ������������������������¶ȵ�94 �棬����������Ȼ����ƽ�������ֽ�������Һ��ɫΪ��ɫ�������ֽ�ܳ��ף����������������Һ�Ĵ��������á�
2.3 �����Һ��ѭ������
�ۺ�����Ӱ�����أ�ȷ����ѽ�������Ϊ�������¡�(NH4)2SŨ��2.5 mol/L��Һ�̱�6:1������ʱ��10 min���ȷֽ�����Ϊ���ȷֽ�ʱ��90 min���¶�94 �档ÿ��ȡ��ѡ��100 g���������Һѭ������10�Σ�������յ������Һ�ٷ�����һ��ʹ�á�����������2��
��2 ���ѭ������������
Table 2 Results of recycling of ammonium sulfide
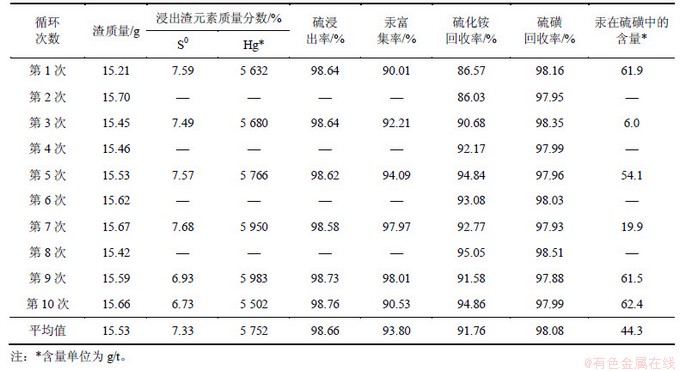
�ɱ�2��֪�������Һ������ѡ�����Ч�����ԣ�100 g��ʯ������������ƽ��Ϊ15.53 g������Ԫ������(��������)��7%���ң�ƽ���������Ϊ98.66%�������Һ���ѭ������ʱ������ǵĻ��ջ���û��Ӱ�죬��ǵĻ�������98%���ҡ�����������������Ǵ���Ϊ99.54%������GB/T 2449��2006��ҵ���һ��Ʒ����
�������е�ƽ������Ϊ5 752 g/t����ԭ��ʯ�еĹ�������ȸ�����6�����ϣ�ƽ��������Ϊ93.8%���˺������ɳ�ΪƷλ�ϸߵĹ������һ�����չ�����������еĺ����Ƚϵͣ����Ϊ62.4 g/t���������Һ�й�����⣬������Ũ��Ϊ0.021 mg/L�����ڹ��ҹ�ҵ��ˮ�й����ŷű�(0.05 mg/L)��
��淋�ƽ��������Ϊ91.76%����1�κ͵�2������ʱ��炙����ʽϵͣ�����Ϊϴ�ӽ�������ˮ�����٣����в����н϶�Ľ���ĸҺ����˼�����Һ�����еIJ��������еĻӷ����Լ�����������嶼���Խ�һ�������淋Ļ����ʡ�
3 ����
(1) ʹ�������Һ��������п��ѹ��������ѡ��Ĺ������̼����ڿ��ơ��������Ч���ã�ƽ���������Ϊ98.66%����ǻ�������98%���ң��������е�ƽ��������Ϊ93.8%����ԭ��ʯ�еĹ�������ȸ�����6�����ϡ�
(2) ���յ���Dz�Ʒ���ȸߣ��ﵽ99.5%���ϣ�����GB/T 2449��2006��ҵ���һ��Ʒ����
(3) �����Һ��ѭ�����ã��Լ���Ľ�С��ƽ��������Ϊ91.76%����������ɱ����������չ��̻�������ȫ��·ѭ���������Ի�����������µ���Ⱦ�����й����Ĺ�ҵӦ��ǰ����
�ο����ף�
[1] Pacyna E G, Pacyna J M, Sundseth K, et al. Global emission of mercury to the atmosphere from anthropogenic sources in 2005 and projections to 2020[J]. Atmospheric Environment, 2010, 44: 2487-2499.
[2] Nriagu J O, Pacyna J M. Quantitative assessment of worldwide contamination of air, water and soil by trace metals[J]. Nature, 1988, 333: 134-139.
[3] Streets D G, HAO Jiming, WU Ye, et al. Anthropogenic mercury emissions in China[J]. Atmospheric Environment, 2005, 39: 7789-7806.
[4] Mukherjee A B, Melanen U M, Ekqvist M, et al. Assessment of atmospheric mercury emissions in Finland[J]. Science of the Total Environment, 2000, 259: 73-83.
[5] FENG Xinbin, QIU Guangle. Mercury pollution in Guizhou, Southwestern China-An overview[J]. Science of the Total Environment, 2008, 400: 227-237.
[6] LI Guanghui, FENG Xinbin, LI Zhonggen, et al. Mercury emission to atmosphere from primary Zn production in China[J]. Science of the Total Environment, 2010, 408: 4607-4612.
[7] WANG Shuxiao, SONG Jingxiang, LI Guanghui, et al. Estimating mercury emissions from a zinc smelter in relation to China��s mercury control policies[J]. Environmental Pollution, 2010, 158: 3347-3353.
[8] ���ѻ�. ұ����������ij�������[J]. ���Ṥҵ, 1986(2): 12-16.
MENG Zhaohua. Technologies of mercury removal from roasting exhaust gas in making acid[J]. Sulphuric Acid Industry, 1986(2): 12-16.
[9] ����». ����Ǧпұ������������[J]. ���Ṥҵ, 1997(5): 28-30.
DONG Silu. Technologies of mercury removal at Northwest lead and zinc smelter[J]. Sulphuric Acid Industry, 1997(5): 28-30.
[10] ����ΰ, ����Ԫ, ������, ��. пұ���������������Ƽ������¼���[J]. �й���ɫ����ѧ��, 2008, 18(1): s416-s421.
WANG Qingwei, CHAI Liyuan, WANG Yunyan, et al. Novel technology for treatment of acidic wastewater containing Hg by biologics in zinc smelter[J]. The Chinese Journal of Nonferrous Metals, 2008, 18(1): s416-s421.
[11] Hutchison A, Atwood D Q, Santilliann-Jiminez E. The removal of mercury from water by open chain ligands containing multiple sulfurs[J]. Journal of Hazardous Materials, 2008, 156: 458-465.
[12] ������, ����, ��, ��. ��ˮ�й�����ȥ���������о���չ[J]. ��������, 2007, 27(2): 135-138.
HUANG Meirong, WANG Lin, YI Hui, et al. Progresses in research on removing mercury ion from wastewater[J]. Environmental Protection of Chemical Industry, 2007, 27(2): 135-138.
[13] ���ڼ�. ʪ��ұ������Ԫ����Ļ��շ���[J]. ʪ��ұ��, 1997(3): 50-54.
ZHOU Qinjian. Method of reclaim elemental sulfur from hydrometallurgical slag[J]. Hydrometallurgy of China, 1997(3): 50-54.
[14] Halfyard J E, Hawboldt K. Separation of elemental sulfur from hydrometallurgical residue: A review[J]. Hydrometallurgy, 2011, 109: 80-89.
[15] Fujita T, Shibayama A, Miyazaki T, et al. Sulfur recovery from the leached residue produced in the direct leaching of zinc concentrates[C]//Mishra B, Yamauchi C. Second International Conference on Processing Materials for Properties. USA: Minerals, Met & Mat Soc, 2000: 689-692.
[16] ����÷, κ᷽�, ����, ��. ͭ���Ƚ������м�Ԫ�����븻������[J]. ���ϴ�ѧѧ��, 2005, 36(1): 38-43.
SUN Peimei, WEI Daijin, LI Honggui, et al. Separation and enrichment of valuable elements from copper residue leached by chlorine[J]. Journal of Central South University, 2005, 36(1): 38-43.
[17] ���, �����, ����, ��. ��ͭ���е������ú�ͽ�ȡ���չ���[J]. ��ѧ����, 2009, 37(8): 75-78.
LI Jingfei, WANG Baolu, XU Min, et al. Process technology on recovery of sulphur from copper-bearing gold concentrate by using kerosene method[J]. Chemical Engineering(China), 2009, 37(8): 75-78.
[18] PENG Peng, XIE Huiqin, LU Lizhu. Leaching of a sphalerite concentrate with H2SO4-HNO3 solutions in the presence of C2Cl4[J]. Hydrometallurgy, 2005, 80: 265-271.
[19] ������, �����, ����ǰ, ��. �Ӻ���������л���Ԫ������о�[J]. ���Ͽ�ұѧԺѧ��, 1992, 23(3): 287-291.
DENG Rizhang, ZHAO Tiancong, ZHONG Zhuqian, et al. Investigation on recovery of elemental sulphur from leach residue containing sulphur[J]. Journal of Central South Institute of Mining and Metallurgy, 1992, 23(3): 287-291.
(�༭ �Կ�)
�ո����ڣ�2012-05-25�������ڣ�2012-08-10
������Ŀ������������ѧ�������Ի���������Ŀ(2011196)
ͨ�����ߣ������(1954-)���У����������ˣ�������ʦ�����½�����ȡ����������ﴦ�����о����绰��15987126280��E-mail: zebiaozhang@yahoo.com.cn
ժҪ����п��ѹ����������ѡ������еĹ�����롢�����Լ���ǻ��ս����о���ȷ�������Һ�������̹������ͽ���ĸҺ�ȷֽ������ǵ���ѹ����������������������ڳ��³�ѹ�£�(NH4)2SŨ��Ϊ2.5 mol/L��Һ�̱�6:1��ʱ��10 min�Ľ��������£�������ʴ�98.66%���������еĸ�����Ϊ93.8%���������й�����Ϊԭ���6�����ϣ�����ĸҺ���ȷֽ��¶�94 �桢�ֽ�ʱ��90 min�������£���ǻ�������98%���ң���Ǵ��ȷ���GB/T 2449��2006��ҵ���һ��Ʒ��������Լ���ѭ�����ã�������Ϊ91.76%��
[8] ���ѻ�. ұ����������ij�������[J]. ���Ṥҵ, 1986(2): 12-16.
[9] ����». ����Ǧпұ������������[J]. ���Ṥҵ, 1997(5): 28-30.
[12] ������, ����, ��, ��. ��ˮ�й�����ȥ���������о���չ[J]. ��������, 2007, 27(2): 135-138.
[13] ���ڼ�. ʪ��ұ������Ԫ����Ļ��շ���[J]. ʪ��ұ��, 1997(3): 50-54.
[16] ����÷, κ᷽�, ����, ��. ͭ���Ƚ������м�Ԫ�����븻������[J]. ���ϴ�ѧѧ��, 2005, 36(1): 38-43.
[17] ���, �����, ����, ��. ��ͭ���е������ú�ͽ�ȡ���չ���[J]. ��ѧ����, 2009, 37(8): 75-78.
[19] ������, �����, ����ǰ, ��. �Ӻ���������л���Ԫ������о�[J]. ���Ͽ�ұѧԺѧ��, 1992, 23(3): 287-291.


