�ߴ��ص�⾫�����о�
����ұ�����Źɷ�����˾ ��������410007
ժ Ҫ��
�ڸߴ��ص���ᴿ�Ĺ�ҵʵ����, �о��˵����ܶȡ�NaOHŨ�ȡ��缫��ʽ�����ڷ���������ضԵ����̵�Ӱ��, ȷ�������˵Ĺ�����������������1#��ֻ��һ�ε��, ��Ʒ��ȫ�ܹ��ﵽ99.999%�ߴ��ص�Ҫ��, ��70%���ϵIJ�Ʒ�ﵽ99.9999%�ص�������, ����Ч�ʴ�98%���ϡ�
�ؼ��ʣ�
��ͼ����ţ� TF843.1
�ո����ڣ�2007-03-26
High-Purity Gallium Electrolysis Refining Process
Abstract��
The influence factors on high-purity gallium electrolysis refining such as current density, NaOH concentration, platinum electrode, cyclical reverse electrolysis and so on were studied.The optimum technical parameters were determined based on plant practice.The 1# gallium after one-cycle electrolyzing, almost all of the product met meanwhile, the criterion of 99.999% high-purity gallium, over 70 percent rearched 99.9999%.The current efficiency exceeded 98%.
Keyword��
high pure gallium;current density;cyclical reverse electrolysis;
Received�� 2007-03-26
�ߴ�����һ����Ҫ�İ뵼���������, ������ϵ�л������黯�ء� ���ء� ��������ڸ��ټ��ɵ�·�� LED�� ����Ԫ���������ڹ㷺Ӧ��, �ߴ��ص��г�����Ѹ�����ӡ� Ŀǰ����ߴ��ص�������Ϊ200 t��a-1, ���ձ����������ͳ���120 t��a-1, ��ȫ��������ÿ���Գ���20%�ķ������ӡ� �ߴ���Ҳ���ҹ��ص㷢չ�ĸ��²��ϡ�
�ֽ�99.999%~99.9999%�ߴ��ص�������Ҫ���ûӷ�-��⾫����ϵĹ���
1 �ߴ��ص��ԭ��
�ߴ��ص������1#����Ϊ����, ��Ϊ����, NaOHˮ��ҺΪ���Һ�� ��������������������, ԭ���е�������Ҫ����Cu, Fe, Pb, Sn, Al, Zn, Ca����������λ�IJ���
������Ӧ: Ga+4OH--3e=GaO2-+2H2O
������Ӧ: GaO2-+2H2O+3e=Ga+4OH-
2 ����ʵ��
��99.99%���ػӷ�������ȥ�л��������ϴ����, ϴ����װ�������������, ����ɫ�״�NaOH���Ƴ�һ��Ũ�ȵ�NaOH��Һ, ͨ����Һ��
������Һ���øߵ����ܶ�, �ɳ�ȥ��Һ�еĴֵ�Pb, Zn, Sn, Fe����, ͬʱ����40 g��L-1���ϵ�Ga����Ũ�ȡ�
��Һ���յ��, ȡ����������������, �����������������ϸߴ�����, ���ӵ�·, ����������ʱ���, �������ڷ����������� ��ɵ���������ں�, ���������Ʒ, ϴ�Ӻ��, ��װ��������������ԭ�ϡ�
����������, ��ˮҪ������ʡ�15 m����cm, �����õ����ӻԹ������� (ICP-MS) ��
3 ���������
3.1 �����ܶȶ�����������Ӱ��
�����ܶȶ�����������Pb, Zn, Sn������Ӱ�����1��ʾ�� �����ܶ�С��100 A��m-2ʱ, ����H2��������, ����Ч�ʵ�; �������ܶȳ���400 A��m-2ʱ, Pb, Zn, Fe, Sn�����ʺ�������99.9999%�ߴ��ر�; �����ܶ�����500 A��m-2����, Pb, Fe���ʼ�������2��10-4%���ϡ� ��Ϊ�����ܶȹ���ʱ, ���������GaO2-Ũ�ȸ��׳��־ֲ������ͽᾧ�����ǵ缫, ʹ�����ۻ���ɲ�ѹ����, ���������� �����е�������500 A��m-2ʱ, ��ѹ��2~3 V��������10 V����, ���� �����ܿ챻��ɫ�ᾧ�����ס�� ����������Ҫ���Ʒ�����ﵽ99.9999%�ر�, �����ܶ�Ӧ������200~300 A��m-2; ��Ҫ���Ʒֻ�����99.999%�ر�, �����ܶȿ�����300~450 A��m-2��
3.2 NaOHŨ�ȶ����������� �۵�ѹ��Ӱ��
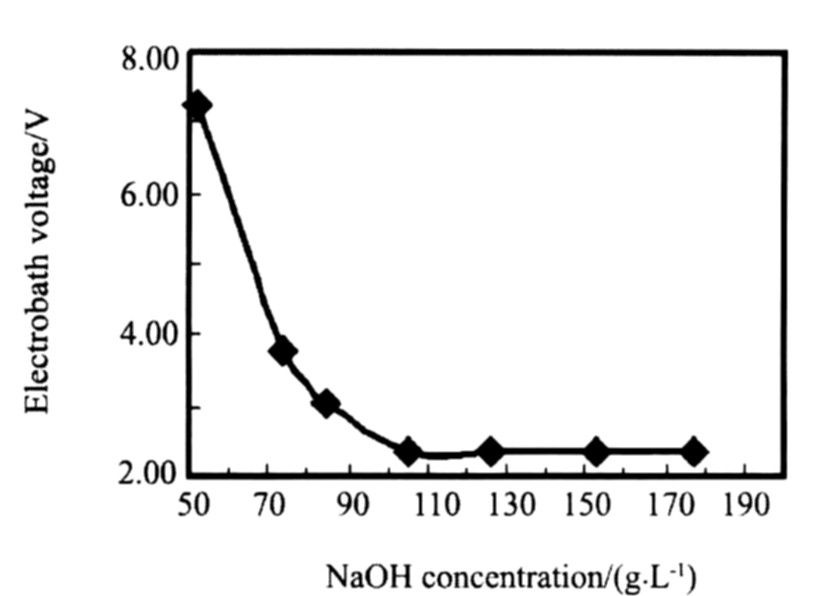
NaOHŨ�ȶ�����������Ӱ�����2, �Բ۵�ѹ��Ӱ����ͼ1��ʾ�� ��ͼ1�� ��2֪��, ��NaOHŨ��80~180 g��L-1��Χ��, ��ѹ��3.26 V����2.3 V, ������Pb, Fe, Zn, Sn������Ӱ�첻�� NaOHŨ��С��80 g��L-1ʱ, ��ѹ�����ܿ�, ������Ʒ�е�����Pb, Fe, Zn, Sn��������99.999%�صı��� ��Ϊ��ҺNaOHŨ�ȱ����ڽϸߵ�Ũ��, �ܷ�ֹ��Һ��GaO2-Ũ�ȹ���, ����ᾧ�����缫, ͬʱ��������Һ�ĵ絼��
3.3 �缫��ʽ�Ե���Ч�ʵ�Ӱ��
�ߴ��ص��
��1 �����ܶȶ����ʵ�Ӱ��
Table 1Impurity of product at different current densities in electrolyte
| Current density/ (A��m-2) |
Condition | Impurity | ||||
| Tempreture/ �� |
NaOH/ (g��L-1) |
Pb | Fe | Zn | Sn | |
| 10-4% | ||||||
| 87 | 43 | 128 | 1.7 | 0.81 | 0.16 | 0.112 |
| 257 | 41 | 141 | 0.009 | 0.008 | 0.007 | 0.005 |
| 324 | 42 | 135 | 0.012 | 0.004 | 0.004 | 0.002 |
| 380 | 45 | 149 | 0.023 | 0.014 | 0.012 | 0.008 |
| 450 | 43 | 143 | 0.35 | 0.41 | 0.06 | 0.011 |
| 520 | 55 | 135 | 2.05 | 2.7 | 0.53 | 0.92 |
ͼ1 NaOHŨ�ȶԲ�ѹ��Ӱ��
Fig.1 Electrobath voltage versus NaOH concentration
�����ж����ô������缫�� ����H2�Բ���������, ����λ��, �ڲ�����������λ��GaO2-/Ga��, ����Ga����������ʱ��Ȼ������������, ���������NaOH, H2O������, �ƻ���̬ƽ��, �������Ч���½�, �����ڵ�����ʱֻ����H2��������Ga����, ��ɲм��ʸߡ� Ϊ���������, ����ʵ���в���������Ͻ����缫����Һ�Ӵ������ܷ�, ���ಿ�����ذ���, ʹ���Һ���벬�缫ֱ�ӽӴ��� ���ֵ缫��װ��ʽ�Ľ�����3��ʾ�� �ӱ�3�ɿ���, �����ܷⲬ�缫���趨�ڴ����缫, ����Ч������1%~2%, ֱ���������20%~30%�� ��Ϊ�ܷ����ʱʵ�ʵ缫����ص缫, ����H���ر���ij���λ�����ڲ��������������λ��1.1 V����
3.4 ���ڷ�����Ե���Ч�ʵ�Ӱ��
�ߴ��ص�������, Ga��������ɢ�Ƿ�Ӧ����Ҫ�Ŀ��Ʋ���, ���ô������ �ߵ����ܶȡ� ����۵���������ʱ, ����GaO2-��ɢ�ٶ���, ���淽ʽ����׳��ֶۻ�, ���������������С� ����ʵ���з���, ���ó�����, ����������120 A, �����ܶȴﵽ350 A��m-2ʱ, �������������Ĵ���GaO2-��������������ɢ, Ѹ�ٶۻ�, ����ʱ������������������ر�ɻҰ�ɫ�ᾧ��, ��ѹ��4.3 V����37 V�� �������ڷ�����, ��·����ʱ�����е�GaO2-��ΪGa, ��������GaO2-Ũ�ȸ߶������ᾧ�ۻ�, ��
��2 NaOHŨ�ȶ�����������Ӱ��
Table 2Impurity of product at different NaOH concentrations in electrolyte
| NaOH/ (g��L-1) |
Condition | Impurity | ||||
| Tempreture/ �� |
Current density/ (A��m-2) |
Pb | Fe | Zn | Sn | |
| 10-4% | ||||||
| 45 | 41 | 158 | 2.43 | 0.64 | 0.21 | 0.91 |
| 72 | 45 | 189 | 1.64 | 0.15 | 0.112 | 0.54 |
| 94 | 46 | 197 | 0.087 | 0.074 | 0.084 | 0.016 |
| 125 | 45 | 285 | 0.014 | 0.092 | 0.018 | 0.024 |
| 135 | 43 | 257 | 0.007 | 0.053 | 0.067 | 0.007 |
| 167 | 42 | 247 | 0.029 | 0.015 | 0.012 | 0.013 |
ʹ�����ر������������GaO2-, ����������ʱGa�������� ͬʱ���ڷ�����һ����������, �ܼ���GaO2-����Һ�е���ɢ�� ������ʵ���������ڷ������, ��������140 A, Ҳ���ٳ��ֶۻ��� ֻҪ���ƺ�����ͷ���ʱ���, ������Ե���Ч�ʵ�Ӱ���С, �ܵ���Ч�ʿ��Դﵽ98%����, ���������Ч��, ��ʡ�˳ɱ�, ʵ�����ȶ��Ĵ��ģ������
Ӱ��������ػ����¶ȡ� ���ʱ�䡢 Ga����Ũ�ȵȡ� ����ʵ�����¶ȿ�����35~65 ��, Ga����Ũ��һ�㾻����Һ��ﵽ40 g��L-1, �������������Ga����Ũ�Ȳ�����200 g��L-1�� һ�ε���õ��ϸ�ĸߴ��ز�Ʒ, ���ﵽ����IJ�Ʒ��
��3 �缫��ʽ�Ե���Ӱ��
Table 3 Effect of electrode on electrolyte
| Current/ A |
Type of electrode |
Change of electrode surface and separates out conditione | Current efficiency/% |
Straight receiving rate/% |
| 60 | Naked | Platinum electrode surface chang black and is packaged by grey crystal, has hydrogen to separate out, cathode space surface covers entirely oxide film | 97.45 | 44.2 |
| 3120 | Naked | Platinum wire becomes dark even blows fuse, by white crystallization package. Hydrogen separates out intensely. Anode region surface changesthe black deactivation | 93.16 | 13.21 |
| 60 | Airproofed | Platinum wire acme luminous, separates out without gas, anode region surface does not have oxide compound | 98.27 | 61.35 |
| 120 | Airproofed | Platinum wire acme does not have platinum black, separates outwithout gas, separates out normally | 98.64 | 69.87 |
��4 ����Ʒ���ʳɷ�*
Table 4 Impurity component of electrolysis product
| Batch number |
Impurity/10-4% | ||||||||||
| Si | Al | Cu | Fe | Mg | Ni | Pb | Sn | Zn | Mn | Cr | |
| 1# | 0.074 | 0.017 | 0.002 | 0.048 | 0.03 | 0.012 | 0.091 | 0.34 | 0.23 | 0.017 | <0.05 |
| 2# | 0.12 | 0.005 | 0.002 | 0.017 | 0.007 | 0.006 | 0.018 | <0.1 | 0.013 | <0.05 | 0.009 |
| 3# | 0.087 | 0.005 | 0.004 | 0.008 | 0.009 | 0.009 | 0.007 | 0.008 | 0.007 | 0.007 | 0.011 |
| 4# | 1 | 0.1 | 1.5 | 0.8 | 0.6 | 0.1 | 1.8 | 0.8 | 0.4 | - | - |
| 5# | 0.2 | - | 0.05 | 0.1 | 0.1 | 0.05 | 0.06 | 0.1 | 0.1 | 0.05 | 0.05 |
4# as 99.999% Ga Criterion, 5# as 99.9999%Ga criterion
4 �� ��
1. ��ҵ����ʵ������, �����ܶ�Ϊ200~300 A��m-2, Ga��Ũ�ȿ�����20~200 g��L-1, NaOHŨ��Ϊ100~160 g��L-1, ����35~65 ��, �ʵ������ڷ�����������, һ�ε���õ��IJ�Ʒ���ܷ���99.999%�ߴ��ر�, ����70%���ϴﵽ99.9999%�ߴ��صı���
2. �������в��缫�ܷ������, �������ʱ�س�Ϊʵ�ʹ���������, �����ĸ߳���λ��ֹ����������������, �����˴�ͳ���������������� ���������ɲ�����Ҫ���ڴ���������, ����Ч�����1%~2%, ���ֱ���������20%~30%��
3. �����в������ڷ�����, �ܼ���GaO2-����ɢ, ��Ч��������GaO2-�ֲ��ᾧ����Ķۻ�, ������������ܶ�, ʹ�����豸�ɴ��ͻ��� �Զ���, ��������ʡ�
�����
[1] ����, �����, ����, ����.�ߴ��������Ʊ������о���չ[J].ϡ�н���, 2003, 27 (4) :495.
[2] ����.�Ʊ��ߴ��ع��յĸĽ�[J].�Ĵ���ɫ����, 2000, 3:8.
[3] ��֥��, ��.ϡ�н����ֲ�[M].����:ұ��ҵ������, 1992.62.
[4] ���������.������ѧ[M].��ɳ:���Ϲ�ҵ��ѧ������, 1992.184.