���±�ţ�1004-0609(2009)02-0346-07
7A04���Ͻ��ں�����������г��ڸ�ʴ�ĵ绯ѧ����
����������Ӣ�ԣ������գ��� ����Ф ��
(�����Ƽ���ѧ ��ʴ��������ģ����� 100083)
ժ Ҫ��
ͨ��������ʴ����ģ���о�7A04���Ͻ��ں�����������еĸ�ʴ���ڹ��ɣ����õ绯ѧ�����迹���Ժ�ɨ��Kelvin̽�뼼�����о�7A04���Ͻ��ڳ��ڸ�ʴ�����еĵ绯ѧ��Ϊ�����������Cl?�����Ͻ�ʴ�������ļ������ã�����������ڱ�����ֵ�ʴ�ӣ�������ʱ����������ʴ����Ӳ���չ���绯ѧ��Ӧ�迹�½���ɨ�迪����̽����Խ���������港ʴ�IJ��Ͻ��У��������������������������Ϸ����仯�����־ֲ���ʴ�������������λҲ��ʱ�������ߣ���������������������ԣ���ʴ��Ӧ���ڲ��ϼ��ٹ��̡�
�ؼ��ʣ�
7A04���Ͻ���������ʴ���绯ѧ�����迹��ɨ��Kelvin̽����
��ͼ����ţ�TG 172.3 ���ױ�ʶ�룺 A
Electrochemical performance of initial corrosion of
7A04 aluminium alloy in marine atmosphere
DONG Chao-fang, AN Ying-hui, LI Xiao-gang, SHENG Hai, XIAO Kui
(Corrosion and Protection Center, University of Science and Technology Beijing, Beijing 100083, China)
Abstract: The initial corrosion of 7A04 aluminium alloy in marine atmosphere was studied. Salt fog test was used to simulate the marine atmospheric environment. Electrochemical impedance spectroscopy (EIS) and scanning Kelvin probe (SKP) were employed to investigate the electrochemical behavior of 7A04 aluminium alloy in marine atmosphere. The results show that the Cl? can accelerate the atmospheric corrosion of 7A04 aluminium alloy during the beginning exposure period. Pittings appear in the initial stage of salt fog test and link each other to expand with prolonging test time. The electrochemical impedance magnitude declines during the corrosion test. The SKP results indicate that the anodic and cathodic areas change constantly with distinct character of localized corrosion. When the corrosion process continues, the surface potential of 7A04 aluminium alloy increases, while anodic and cathodic area distinguish evidently from each other. Atmospheric corrosion of 7A04 aluminium alloy is promoted during the initial stage in marine air.
Key words: 7A04 aluminium alloy; atmospheric corrosion; EIS; SKP
7A04���Ͻ���Al-Zn-Mg-Cuϵ�У�����ǿ�ȸߡ��ܶȵ͵��ŵ㣬��Ϊ�ɻ�����Ҫ�����������Ѿ��㷺Ӧ���ں�����������ʴ�Խϲ�����ں��������ӵ�ʪ�Ⱥ�����������У��������㸯ʴ�����丯ʴ�Ⱦֲ���ʴ������ʱ����ɹ���ʧЧ�Ӷ�Ӱ�쵽�ɻ������ķ�����������������о��߶����Ͻ�Ĵ�����ʴ�Ѿ���չ�˹㷺���о�����������˲�ͬ�����ڼ������鷽����ģ�⻧��Ĵ�����ʴ[1?3]����ʪ�����顢�������顢�����������ϸ�ʴ���顢���ڽ��ϸ�ʴ�����Լ�������ѭ�����ϸ�ʴ����ȡ�
�绯ѧ�����Ǹ�ʴ��ѧ�о��е���Ҫ�ֶΡ����Ͻ������ʴ�ĵ绯ѧ�о�����Ŀǰ���ý϶���У����������͵绯ѧ�迹���Է������绯ѧ��������������ʴ����صȡ�����ɨ��Kelvin̽����Լ������Բ��Ӵ���������ⶨ�丯ʴ��λ����ֲ����Խ���״̬С�仯��Ϊ���У������ڸ�ʴ�����ij�ʼ�μ���ʴ������λ�ú�״����Ϊȫ���˽�����ڴ����еĸ�ʴ״̬�ṩ�ḻ����Ϣ�����ڲ��ϵĴ�����ʴ��Ϊ�о������й㷺��Ӧ��ǰ����STRATMANN ��[4]�����������������Ƶ�Kelvin̽��װ�òⶨ��Fe��Cu��Zn�Ƚ����ڼ������ҺĤ���µĸ�ʴ��λ���������ߡ�TAHARA��[5]��Kelvin̽�뼼���о���Fe/Zn�ڱ�ҺĤ�µĵ�ż��ʴ��JUZELIUNAS��[6]����Kelvin̽�뼼���о���Al-Mg�Ͻ��ڲ�ͬ��Һ�г��ڵĸ�ʴ��Ϊ��DE WIT��[7?8]��FRATILA-APACHITEI��[9]����ɨ��Kelvin̽��������(SKPFM)�����Ͻ�ڶ���ijɷ֡��ṹ����״�ʹ�С�����ʴ��Ӱ��������о�������ѧ��Ҳ��չ����ص��о����������ѵ�[10]���� ��[11]�ֱ�ʹ��Kelvin̽���о��˲�ͬ�ֽ����ڱ�ҺĤ�µĸ�ʴ�绯ѧ��Ϊ����־����[12]����Kelvin̽�뼼���о����������Ͻ�Ĵ�����ʴ��
�����������ñ�����������ģ�⺣�������ʴ������ɨ��Kelvin̽�뼼�����и�ʴǰ��ľֲ��绯ѧ���ԣ�����ϴ�ͳ�ĵ绯ѧ�迹���Ժ�ɨ��羵�۲���ֶΣ���7A04���Ͻ���ģ�⺣����������еij��ڸ�ʴ��Ϊ�����о���
1 ʵ��
1.1 ʵ�����
ʵ�����Ϊ7A04���Ͻ�(T6)���仯ѧ�ɷּ���1��ʵ���ò��Ͼ���ȥ�������㡣
��1 7A04���Ͻ�ѧ�ɷ�
Table 1 Chemical compositions of 7A04 aluminium alloy (mass fraction, %)

ɨ��羵�۲��õ������ߴ�Ϊ30 mm��20 mm��2.5 mm����200�š�400�š�600�š�800����1000��ˮĥɰֽ���δ�ĥ����ȥ����ˮ��ϴ���ƾ���ϴ��紵�ɺ���á��绯ѧ�����ò��ϳߴ�Ϊ10 mm��10 mm��2.5 mm�������û�����֬������ˮĥɰֽ��ĥ��1500�ţ����ý��ʯ����⡣�������ɨ��羵������������ò���й۲죬ͬʱ�Ը�ʴ�����������������
1.2 ��������
�������鰴��ASTM B117��97�����У���������Ϊ��5%��0.5%����NaCl��Һ����������pH��ΧΪ6.5~7.2�������¶ȿ�����35 ���1 �棬�����豸Ϊ����Q-Panel��˾��Q-Fog CCT1100��ѭ����ʴ�����䡣Ϊ���о�7A04���Ͻ������������еij��ڸ�ʴ��Ϊ������ȡ��ʱ���趨Ϊ4��12��24��48 h��Ȼ����е绯ѧ���Ժ�����ò�۲졣
1.3 �绯ѧ�迹����
�绯ѧ�迹����ϵͳ��PAR M273A���λ�Ǻ�M5210����Ŵ�����ɣ��������缫��ϵ���Ա��ʹ��缫(SCE)Ϊ�αȵ缫��ʯī�缫Ϊ�����缫������ǰ������3.5%NaCl��Һ�н���5~10 min������λ�ȶ���ʼ������ ���Լ����ź�Ϊ��ֵ10 mV�����Ҳ���Ƶ�ʷ�ΧΪ10 mHz~100 kHz�����Ժ�Ӧ��ZSimpWin�����Ե绯ѧ�迹������Ϸ�����
1.4 ɨ��Kelvin̽�����
ɨ��Kelvin̽�����ʹ��PAR M370�绯ѧɨ�蹤��վ�������������¿����н��У�������ɨ��ģʽ��ɨ�貽��100 ��m��ɨ�����4 000 ��m��3 000 ��m��̽�������30 ��m��̽��������������С��100 ��m������ǰ���ñ��ʹ��缫(SCE)��ɨ��Kelvin̽�����ϵͳ����У����
2 ���������
2.1 ��ʴ��ò��ʴ����
ͼ1��ʾΪ7A04���Ͻ�����������4��12��24��48 h��ĸ�ʴ��ò����ͼ�п��Կ������ڸ�ʴ������Ҫ����Ϊ���͵ĵ㸯ʴ���������Ÿ�ʴʱ����ӳ�����ʴ�����ٽ��ĵ�ʴ������Ӳ�����չ����ʴ�ӱ����ɵĸ�ʴ���������ǡ�

ͼ1 7A04���Ͻ��������鲻ͬʱ���ĸ�ʴ��ò
Fig.1 Surface morphologies of 7A04 aluminium alloy after salt fog test for different times: (a) 4 h; (b) 12 h; (c) 24 h; (d) 48 h
����������48 h��ĸ�ʴ�������EDS������(ͼ2�ͼ���2)����ʴ����������ҪԪ��ΪAl��O������������Mg��Zn��Cl��
���Ͻ��ڴ��������з�����ʴ���丯ʴ������Ҫ�ǵ绯ѧ��ʴ����缫��ӦΪ

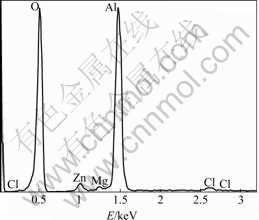
ͼ2 7A04���Ͻ�ʴ�����EDS����
Fig.2 EDS results of corrosion products of 7A04 aluminium alloy
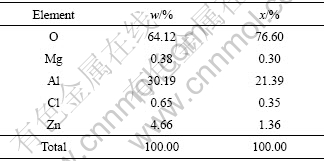
��2 7A04���Ͻ�ʴ����EDS������
Table 2 Elements analysis of corrosion products of 7A04 aluminium alloy by EDS
������Ⱦ��ֱ���Ϊ�Ǽ��ٽ���������ʴ����Ҫ���أ��ر���Cl?�������Ͻ�ĸ�ʴ������Ӱ��������Cl?���������Ͻ����Ļ���λ��������Ĥ����������ʲ����ȴ�������������������������������������Ĥ�Ļ�ѧ��Ӧ������Ĥ�ļ��������Ѻ���¶����ֱ���ܽ�[13]��Cl?ͨ����������������һϵ�з�Ӧ�����ղ���Ϊ������ˮ��AlCl3����Ӧ����Ϊ[14]
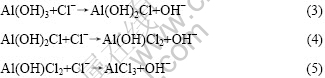
Ϊ������Ͻ��ǿ��ͨ��ͨ��һ���ķ�ʽ(��ʱЧ�ȴ���)�ںϽ�������ڶ���(ʱЧ������)��7A04���Ͻ�����Al-Zn-Mg-Cuϵ���Ͻ�����Ҫ���еĵڶ���ΪAl7Cu2Fe��(Al, Cu)6 (Fe, Cu)��MgZn2[15?16]������Al7Cu2Fe ��(Al, Cu)6 (Fe, Cu)���������ĵ�λҪ�����ھֲ���ʴ����Ϊ������������Χ����ĸ�ʴ��MgZn2�����������ĵ�λ��������Ϊ���������ȷ�����ʴ�ܽ⡣���Ͻ�ĵ�ʴ����ӵڶ������������ʼ��ͨ���ڶ������֮��������Ͻ�����γɵ�ż�ԣ����������ܽ⣬Cl?�Ĵ��ڻ�������Ͻ��������Ĥ�����ѴӶ����ٸ�ʴ��
2.2 �绯ѧ�迹����
ͼ3��ʾΪ7A04���Ͻ���ͬʱ��������ʴ��ĵ绯ѧ�迹�ף���Nyquistͼ�пɼ�����ʴ4~12 h�ڼ䣬��绯ѧ�迹����һ����?��Ƶ�ݿ�����һ����?��Ƶ�п�����ɡ��港ʴʱ���ӳ���24~48 h����?��Ƶ�п��ɷ���������ʧ���ݿ����뾶Ҳ���ϼ�С����48 h���ֲ�̫���Ե������ݿ�����
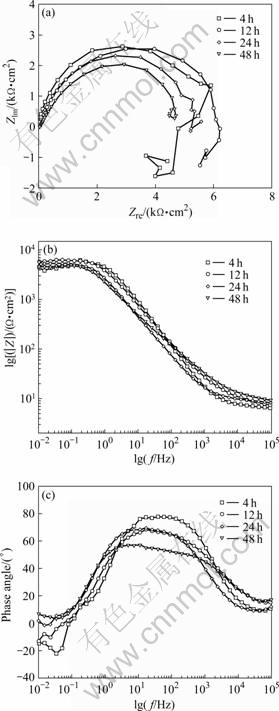
ͼ3 7A04���Ͻ�������ʴ��ĵ绯ѧ�迹��
Fig.3 Electrochemical impedance spectrum (EIS) of 7A04 aluminium alloy after salt fog: (a) Nyquist diagram; (b), (c) Bode diagrams
�Ͻ�绯ѧ�迹���ϳ�����?��Ƶ�п�����ԭ�����������ۡ�KEDAM��[17]��Ϊ�����ںϽ����ԭʼ����Ĥ�����Լ������¡��ܳ��ϵ�[18]��Ϊ�жۻ�Ĥ���ǵĽ�����������ڶۻ�Ĥ��ʴ�յ��ڲ����п���һ���ۻ�Ĥ���ף���ʴ���뷢չ�ڣ��п��ɷּ���ʧ���������ֹ۵�ʵ���϶�����˵����7A04���Ͻ��������������ںϽ��������Ĥ�ĸ�ʴ�������ºϽ�绯ѧ�迹���ϳ�����?��Ƶ�п�����ͬʱ��������ʱ����ӳ������ڱ�������Ĥ�����Լ�������Ӧ���轵�ͣ�����Ϊ��?��Ƶ�ݿ����뾶��С������������Ĥ���ϼ��������¸п��ɷֲ��ϼ�����������Ĥ�ܽ��¶���Ͻ����ʱ���Ͻ���忪ʼ��ʴ���п��ɷ���ʧ��
��Bodeͼ�ɼ������Ÿ�ʴʱ����ӳ����迹ģֵ�����½�����ǵı仯��Ϊ���ԣ���ʴ4 h���ڸ�?��Ƶ�����Ե���Ƿ塣���Ÿ�ʴʱ���ӳ�����Ƿ�ֵ�����½�������Ƿ����Ƶ�����ƶ���������ʴ48 h���ֳ���̫���Ե�����ʱ�䳣���������е�Ƶ��Ƿ�ij��ֶ�Ӧ���Ͻ���巢����ʴ�绯ѧ��Ӧ��
�������Ͻ���������ʴ�еĸ�ʴ��������ϲܳ��ϵĵ绯ѧ��ʴԭ��[19]������˵�Ч��·ģ����ͼ4��ʾ������RsΪ��Һ���裬CPE1��R1�ֱ�Ϊ������ݺ͵���(��������Ĥ��ʴ����)��LΪ��У�CPE2��Rct�ֱ�Ϊ��Ӧ����˫�����ݺ͵��ת�Ƶ��衣
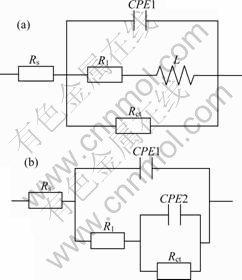
ͼ4 7A04���Ͻ���������ʴ����EIS���Եĵ�Ч��·ģ��
Fig.4 Equivalent circuits of 7A04 aluminium alloy after salt fog test using for EIS analysis: (a) 4?12 h; (b) 24?48 h
�Ե�Ч��·�еĵ���Ԫ���ó���λ��Ԫ��CPE���滻���ܵõ����õ���Ͻ��������CPE=Y0?1(j��)?n����n=0ʱ��Y0�൱��1/R����CPEΪ�����ԣ��迹ΪR����n=1ʱ��Y0�൱��C����CPEΪ�����ԣ��迹Ϊ1/(j��C)����n=?1ʱ��Y0�൱��1/L����CPEΪ����ԣ��迹Ϊj��L����n=0.5ʱ����ΪWarburg�迹��
������ʴ4~12 h��ĵ绯ѧ�迹�ײ��õ�Ч��·ģ��(��ͼ4(a))����ϣ�������ʴ24~48 h��ĵ绯ѧ�迹�ײ��õ�Ч��·ģ��(��ͼ4(b))����ϣ���Ͻ������3��
1/Rctֵ�ı仯���Է�ӳ����ʴ�����ƺ����ʡ���ͼ5�п��Կ�����1/Rctֵ������ʱ����ӳ������ӣ������������ڸ�ʴ���ʳ��������ƣ��Ǽ��ٸ�ʴ���̡�
2.3 ɨ��Kelvin̽����Խ�������
ͼ6��ʾΪ������ʴ��ͬʱ���7A04���Ͻ�����SKP��λ�ֲ�ͼ����ͼ�п��Կ�����������״̬�ı仯�����
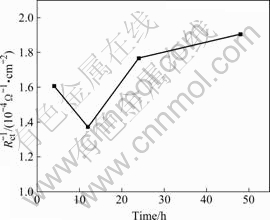
ͼ5 7A04���Ͻ�������ʴ��1/Rct��ʱ��ı仯����
Fig.5 Reciprocal curves of Rct changing with test time for salt fog
δ��ʴ�����Ͻ�����λ�ֲ���Ϊ���ȣ���λ��Χ��?827~?722 mV֮�䣬���������������ĵ�λ����105 mV���ڣ�����ά����ͼ6(a)�ϱ�����Ժ�ƽ̹���ڵ�λ�ֲ�ͶӰͼ��Ҳ���Կ���������Ե������Էֲ�����ʴ����4 h��Ͻ�����λ��������Χ��?876~?464 mV֮�䣬���������������ĵ�λ������412 mV���ڣ�˵������4 h�����Ͻ�����Ѿ���ʼ��ʴ�����Ҹ�ʴ�ٶȺܿ죬��4 h�ĵ�λͶӰͼ�п��Կ������Ե�������������������ʴ���е�12 h�����λ�ֲ���Χ��4 h��ı仯�������ʴ24~48 hʱ���Ͻ�����λ��Χ�������������������������ĵ�λ��仯������
���Ÿ�ʴʱ����ӳ����ڵ�λ�ֲ�ͼ�ϳ��������Ե�������������������������Cl?�����ڽ������棬�ƻ��˺Ͻ���������Ĥ��Al7Cu2Fe��(Al, Cu)6 (Fe, Cu) ��MgZn2�ȵڶ�����������Ͻ���屩¶�ڸ�ʴ�����У��Ͻ���溬Al7Cu2Fe��(Al, Cu)6 (Fe, Cu)���������Ϊ������������Χ����Ϊ����������MgZn2����������Ϊ������������Χ����Ϊ���������γ�����ֲ���أ������ڵڶ���������˵�ʴ��
�Ƚ�ͼ6(b)~(e)���Է��֣��港ʴ���Ͻ��У��������������������������Ϸ����仯�����־ֲ���ʴ�����������⣬�����λҲ��ʱ�������ߣ���������������������ԣ�˵����ʴ��Ӧ���ڲ��ϼ��ٹ��̣�������ò�۲�͵绯ѧ�迹����������Ǻϡ�
��3 ������ͬʱ��ĵ绯ѧ��ϲ���
Table 3 Fitting results of EIS equivalent circuits of 7A04 aluminium alloy after salt fog test
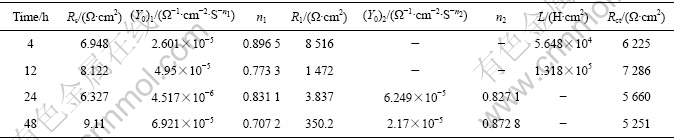
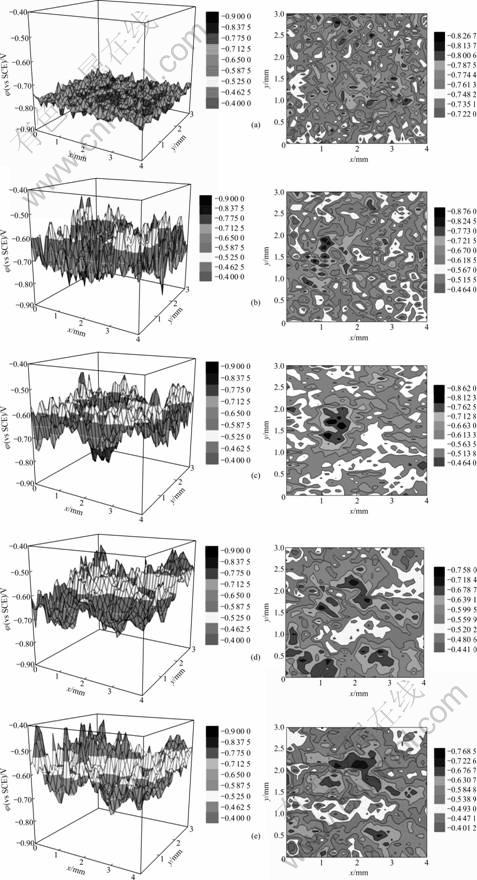
ͼ6 �������������7A04���Ͻ����SKP��λ�ֲ�ͼ
Fig.6 SKP diagrams of 7A04 aluminium alloy after salt fog test: (a) 0 h; (b) 4 h; (c) 12 h; (d) 24 h; (e) 48 h
3 ����
1) ��ģ�⺣������У�Cl?��7A04���Ͻ�ʴ�������ļ������ã�����������ںϽ������ֵ�ʴ�ӡ�������ʱ����������ʴ������������չ��
2) 7A04���Ͻ�ʴ�����е绯ѧ��Ӧ�迹���½�����ʴ�ٶȲ������ӡ�
3) ���Ͻ�����SKP��λ�ֲ�����������港ʴ���Ͻ��н������������������������Ϸ����仯�����־ֲ���ʴ�������������λҲ��ʱ�������ߣ�����������������������ԣ���ʴ��Ӧ���ڲ��ϼ��ٹ��̡�
[1] �� ��, ���价, �����, IJ����. ������ʴ��ģ��������鷽���о�[J]. ��ʴ��ѧ���������, 1995, 7(3): 214?215.
JIN Lei, TANG Qi-huan, PONG Chang-hao, MU Xian-liang. Accelerated testing for simulating acedic pollution and marine environment induced atmospheric-corrosion[J]. Corrosion Science and Protection Technology, 1995, 7(3): 214?215.
[2] ��־��, ����, �����. �������ϴ�����ʴ���������о��ķ�չ����[J]. ���Ϲ���, 1995(12): 41?42.
SUN Zhi-hua, LI Jin-gui, LI Mu-zheng. Future of accelerated atmospheric corrosion testing of metal materials[J]. Journal of Materials Engineering, 1995(12): 41?42.
[3] �� ��, �̻�ΰ. ��ǿ���Ͻ���ٸ�ʴ�������о�[J]. ����ѧ��, 2000, 21(S): 39?42.
ZHANG Qi, CHENG Ji-wei. Study of the accelerated corrosion tests of high-strength aluminum alloys[J]. Acta Aeronautica et Astronautica Sinica, 2000, 21(S): 39?42.
[4] STRATMANN M, STRECKEL H. On the atmospheric corrosion of metals which are covered with thin electrolyte layers ����. Verification of the experimental technique[J]. Corrosion Science, 1990, 30(6/7): 681?734.
[5] TAHARA A, KODAMA T. Potential distribution measurement in galvanic corrosion of Zn/Fe couple by means of Kelvin probe[J]. Corrosion Science, 2000, 42(4): 655?673.
[6] JUZELIUNAS E, SUDAVICIUS A, JUTTNER K, FURBETH W. Study of initial stages of Al-Mg alloy corrosion in water, chloride and Cu(II) environment by a scanning Kelvin probe and XPS[J]. Electrochemistry Communications, 2003(5): 154?158.
[7] de WIT J H W. Local potential measurements with the SKPFM on aluminium alloys[J]. Electrochimica Acta, 2004, 49: 2841?2850.
[8] ANDREATTA F, TERRYN H, de WIT J H W. Corrosion behaviour of different tempers of AA7075 aluminium alloy[J]. Electrochimica Acta, 2004, 49: 2851?2862.
[9] FRATILA-APACHITEI L E, APACHITEI I, DUSZCZYK J. Characterization of cast AlSi(Cu) alloys by scanning Kelvin probe force microscopy[J]. Electrochimica Acta, 2006, 51: 5892?5896.
[10] �� ��, ˮ����. ʹ��Kelvin ̽ͷ�αȵ缫�����о�Һ���ȶ�����ԭ�ٶȵ�Ӱ��[J]. �й���ʴ�����ѧ��, 1995, 15(3): 180?188.
WANG Jia, TSURU T. An investigation on oxygen reduction under thin electrolyte layer using Kelvin probe reference electrode[J]. Journal of Chinese Society for Corrosion and Protection, 1995, 15(3): 180?188.
[11] �� ��, �� ޱ. ����Kelvin ̽����н�����Һ���µ绯ѧ����[J]. ��ʴ��ѧ���������, 1995, 7(3): 192?195.
ZOU Feng, HAN Wei. Electrochemical study of metals under thin electrolyte layer with Kelvin probe method[J]. Corrosion Science and Protection Technology, 1995, 7(3): 192?195.
[12] ��־��, ������, ������, ������, ½ ��, �մ���, �� ��. ��Kelvin̽ͷ�����о����Ͻ�Ĵ�����ʴ[J]. ��ʴ��ѧ���������, 2006, 18(2): 87?91.
SUN Zhi-hua, LIU Ming-hui, ZOU Li-ming, ZHANG Xiao-yun, LU Feng, TAO Chun-hu, WANG Jia. Study on atmospheric corrosion of aluminum alloy by Kelvin probe technique[J]. Corrosion Science and Protection Technology, 2006, 18(2): 87?91.
[13] ELOLA A S, OTERO T F, PORRO A. Evolution of the pitting of aluminum exposed to the atmosphere[J]. Corrosion, 1992, 48(10): 854?863.
[14] GRAEDEL T E. Corrosion mechanisms for aluminum exposed to the heat atmosphere[J]. Journal of the Electrochemical Society, 1989, 136(4): 204?212.
[15] ANDREATTA F, TERRYN H, de WIT J H W. Corrosion behaviour of different tempers of AA7075 aluminium alloy[J]. Electrochimica Acta, 2004, 49: 2851?2862.
[16] ���, ֣����, ���Ĵ�. �ڶ��������Ͻ�ֲ���ʴ�е����û���[J]. ���ϵ���, 2005, 19(2): 81?83.
LI Jin-feng, ZHENG Zi-qiao, REN Wen-da. Function mechanism of Secondary phase on localised corrosion of Al alloys[J]. Materials Review, 2005, 19(2): 81?83.
[17] KEDDAM M, KUNTZ C, TAKENOUTI H, SCHUSTER D, ZUILI D. Exfoliation corrosion of aluminum alloys examined by electrode impedance[J]. Electrochimica Acta, 1997, 42(1): 87?97.
[18] �ܳ���, �� ��, �ֺ���. �����ӶԶ�̬�����缫�迹Ƶ��Ӱ��[J]. �й���ʴ�����ѧ��, 1989, 9(4): 261?270.
CAO Chu-nan, WANG Jia, LI hai-chao. Effect of Cl? ion on the impedance of passive-film-covered electrodes[J]. Journal of Chinese Society for Corrosion and Protection, 1989, 9(4): 261?270.
[19] �ܳ���. ��ʴ�绯ѧԭ��[M]. �ڶ���. ����: ��ѧ��ҵ������, 2004: 276?305.
CAO Chu-nan. Principle of corrosion electrochemical[M]. 2nd ed. Beijing: Chemical Industry Press, 2004: 276?305.
������Ŀ�����һ�������ƽ̨����������Ŀ(2005DKA10400)��������Ȼ��ѧ����������Ŀ(50499331-8)
�ո����ڣ�2008-06-29�������ڣ�2008-09-29
ͨѶ���ߣ��������������ڣ���ʿ���绰��010-62333931-518��E-mail: dongchf@sina.com
ժ Ҫ��ͨ��������ʴ����ģ���о�7A04���Ͻ��ں�����������еĸ�ʴ���ڹ��ɣ����õ绯ѧ�����迹���Ժ�ɨ��Kelvin̽�뼼�����о�7A04���Ͻ��ڳ��ڸ�ʴ�����еĵ绯ѧ��Ϊ�����������Cl?�����Ͻ�ʴ�������ļ������ã�����������ڱ�����ֵ�ʴ�ӣ�������ʱ����������ʴ����Ӳ���չ���绯ѧ��Ӧ�迹�½���ɨ�迪����̽����Խ���������港ʴ�IJ��Ͻ��У��������������������������Ϸ����仯�����־ֲ���ʴ�������������λҲ��ʱ�������ߣ���������������������ԣ���ʴ��Ӧ���ڲ��ϼ��ٹ��̡�


