DOI: 10.11817/j.issn.1672-7207.2015.03.005
����CaO-SiO2-Al2O3����ҺFe-Si-C����ƽ���Ԥ��
����骣����������ն�ƽ
(����������ѧ ұ������Դ����ѧԺ������ ������650093)
ժ Ҫ��
�����ģ��(MIVM)������CaO-SiO2-Al2O3����ҺFe-Si-C��ϵ֮�����ƽ�����Ԥ�⡣�о������������Һ��Si��ȼ���ƽ��Ũ�ȡ�������SiO2��ȵ�Ԥ��ֵ����ʵ�����ݽϷ��ϣ�������1 693 K�� 1 773 K��Fe-Si-C������Si��ȵ�MIVMԤ��ƽ��������Ϊ9%����Wagner��ʽ��ƽ��������Ϊ56%������MIVM����α��Ԫ��Ԥ����1 873 K����Һ��Siƽ��Ũ�ȵ�ƽ��������Ϊ17%��������Wagner��ʽ��SiO2��ʵ�����������ƽ��������Ϊ41%�������MIVM��Ԥ��Ч�����н�ǿ���ȶ��ԺͿɿ��ԣ���ģ�ͽ�ͨ������Ӷ�Ԫϵ��Ȼ���ֱ��������ϡ���ϵ�������ܹ�Ԥ����ԪҺ̬�Ͻ�����������������ѧ���ʡ�
�ؼ��ʣ�
��-����ƽ������¯ұ����������������ģ����Ԥ����
��ͼ����ţ�TF01 ���ױ�־�룺A ���±�ţ�1672-7207(2015)03-0794-10
Prediction of phase equilibrium between CaO-SiO2-Al2O3 molten slag and Fe-Si-C iron melt
LIU Zhennan, LI Yayu, TAO Dongping
(Faculty of Metallurgical and Energy Engineering, Kunming University of Science and Technology,
Kunming 650093, China)
Abstract: Phase equilibrium between the CaO-SiO2-Al2O3 molten slag and the Fe-Si-C iron melt was predicted based on the molecular interaction volume model (MIVM).The results indicate that the predicted activities and equilibrium contents of Si in the iron melt and the predicted activities of SiO2 in the slag are in good agreement with experimental results. The average relative error of activity of Si in the Fe-Si-C melt predicted by MIVM is 9% at 1 693 K and 1 773 K, while the average relative error of activity of Si calculated by Wagner formula is 56%.The average relative error of the equilibrium contents of Si in the iron melt predicted by both MIVM and its pseudo-multicomponent approach is 17% at 1 873 K, while the average relative error of equilibrium contents of Si calculated by using both the Wagner formalism and the experimental activities of SiO2 is 41%, which shows that the prediction effect of the proposed method is of better stability and reliability. A significant advantage of the model lies in its ability to predict thermodynamic properties of ternary liquid alloys and molten slags by only using the experimental results of component activities or infinite activity coefficients in their sub-binary systems.
Key words: phase equilibrium of slag-metal; blast furnace smelting; molecular interaction volume model; prediction
Si�Ǹ�¯ұ�������еĻ���Ԫ�أ�ͨ������ѧ�����о�������������Һ���е�ƽ�������ɣ������˽�Si�ڸ�¯ұ�������µ�����ѧ��Ϊ�Ƿdz���Ҫ�ġ����������ѧģ�Ͷ�ұ������е���-����ƽ���о�����Ҫ���ã�������ѧ�߶���������о���Wagner��ʽ[1]�ڸ���ұ���б��㷺Ӧ�ã����ù�ʽ������ò�����Ҫͨ����Ԫϵ��ƽ��ʵ�����ȷ����ʵ���ѶȽϴ����ѹ�����448��һ������ò����У���21%�����ݿɿ��Բ���ȷ��[2]��Wagner��ʽ������һ���¶�����Һ��Si��Mn���м�Ԫ�ص�ƽ��Ũ�ȼ��㣬��������������Ԫ�Ļ����Ȼ��Ҫ��ʵ��ⶨ���[3]���ż�[4]����������Ũ��ģ���ڹ㷺��ұ���������Һ���нϺ�Ӧ�ã������ڲ�����Ԫϵ(��Ag-In-Snϵ)���漰�ĸ����������ɷ�Ӧ��ƽ�ⳣ������ģ����Ҫ�ɸ���Ԫϵ��Ԫ��ȵ�ʵ�����ݻع鼰�Ż��õ���������������ģ��(MIVM)[5-6]ͨ����϶�Ԫϵ������ݻ���ֱ��������ϡ���ϵ��������Ԥ���ԪҺ̬�Ͻ�����������������ѧ���ʡ����ij���Ӧ�ø�ģ�ͼ���α��Ԫ��[7]�����������̼Һ̬�Ͻ���ϵMIVM��������Ϸ�����Ԥ��һ���¶���̼������Һ��Si��ƽ��Ũ�ȣ�����Wagner��ʽ���бȽϡ�
1 ģ��
1.1 ������������ģ��
����ͳ������ѧ��������ƽ�����ۣ��Ƶ���Һ�弰������������ֺ����ı���ʽ�����Һ��������Ӿֲ���λ����������ʽ���Ӷ�����Һ����������ѧ�ķ�����������ģ��(molecular interaction volume model��MIVM)[5-6]�����ڶ�Ԫ��ϵ����Ħ����������˹������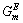 �ɱ�ʾΪ
�ɱ�ʾΪ

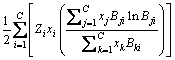 (1)
(1)
���У�xi��Vmi��Zi�ֱ�Ϊ��Ԫi��Ħ��������Ħ������͵�һ��λ�����λ����CΪ��Ԫ������Bij��BjiΪ��Ԫ�����i-j�ķ��Ӷ�λ������ò�����
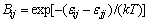 ��
��
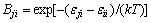 (2)
(2)
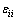 ��
��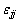 ��
��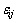 �ֱ�Ϊi-i��j-j��i-j���Ӷ�λ�ܣ���
�ֱ�Ϊi-i��j-j��i-j���Ӷ�λ�ܣ���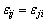 ��kΪBoltzmann������TΪ����ѧ�¶ȡ����ö���Ԫ������ϵ��ijһ��Ԫ��ƫ���ʵ�����������ϵ�����ʵ���֮��Ĺ�ϵʽ���ɵ�����Ԫi�Դ�����Ϊ��̬�Ļ��ϵ��
��kΪBoltzmann������TΪ����ѧ�¶ȡ����ö���Ԫ������ϵ��ijһ��Ԫ��ƫ���ʵ�����������ϵ�����ʵ���֮��Ĺ�ϵʽ���ɵ�����Ԫi�Դ�����Ϊ��̬�Ļ��ϵ�� ����Ȼ��������ʽΪ
����Ȼ��������ʽΪ


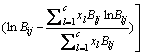 (3)
(3)
��ʽ(3)���Կ�����MIVM��������ģ�ͣ������ڶ���Ԫ���壬ֻ��֪�����Ӷ�Ԫϵ�Ļ��ʵ��ֵ������ϡ���ϵ�������ȷ����Ԫ����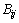 ��
��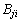 ������Ԥ��ö�Ԫϵ������ѧ���ʡ�
������Ԥ��ö�Ԫϵ������ѧ���ʡ�
1.2 Wagner��ʽ
������Һ�и���Ԫ�Ļ��ʱ����ֻ����һ������ã���Wagner��ʽ[3]Ϊ
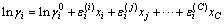 (4)
(4)
���У�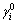 Ϊ��Ԫi����Һ�е�����ϡ���ϵ����
Ϊ��Ԫi����Һ�е�����ϡ���ϵ����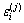 ΪFe-i-j��Ԫϵ����Ԫj��i��һ������ò�����
ΪFe-i-j��Ԫϵ����Ԫj��i��һ������ò����� Ϊ��Ԫi��Ħ������������֪��Ӧ������ò���������ϡ���ϵ��������ʽ(4)��
Ϊ��Ԫi��Ħ������������֪��Ӧ������ò���������ϡ���ϵ��������ʽ(4)�� �����������Ԫi�Դ�����Ϊ��̬�Ļ�ȡ�
�����������Ԫi�Դ�����Ϊ��̬�Ļ�ȡ�
1.3 ������������ģ�͵�α��Ԫ��
�ڶ�Ԫ�����������У����ǵ���Ԫ֮����ڵĻ�ѧ����ã���������������-�ѧ��Ӧ����ô�������оͻ��������ʲ�����ʹ��������ϵ����Ԫ�����ӣ��Ӷ����ɸ���Ԫ����ϵ��α��Ԫ��ϵ��Ȼ��ͨ��MIVMԤ�����α��Ԫ��ϵ�и���Ԫ������ѧ���ʣ�������ķ����ͳ�Ϊ������������ģ�͵�α��Ԫ��(pseudo-multicomponent approach)��
�������������У���Ϊ���ӡ������ǹ���ģ����ӷ�Ӧ�����ӷ�Ӧ�ǵ�Ч�ġ������������Ļ�ѧ���ã�����ѡ����ӷ�Ӧ�����о�����Ϊ
A+B=AB (5)
���У�A��B�������������AB����A��B���γɵĻ����Ϊ�˷�����д���������±�1��2��12�ֱ��ʾ����A��B��AB�����跴Ӧ��ʼʱ����A��B��AB�����ʵ����ֱ�Ϊn1��n2��0������Ӧ�ﵽƽ��ʱ����A��B��AB�����ʵ����ֱ��Ϊn1-n12��n2-n12��n12�����ԣ�A-B��Ԫ����������ͱ����A-B-ABα��Ԫ��ϵ���������ϵ�и���Ԫ����ʵĦ��������Ϊ
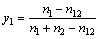 ��
��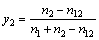 ��
��
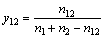 (6)
(6)
�跴Ӧ(5)�ķ�Ӧƽ�ⳣ��ΪK12������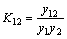 ��������ʽ(6)���������ɽ��������AB�����ʵ���n12��
��������ʽ(6)���������ɽ��������AB�����ʵ���n12��
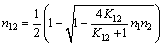 (7)
(7)
����1 mol��Ԫ���壬��x1=n1 ��x2=n2���������ǣ���x1��x2����ʽ(6)��(7)���������y1��y2��y12��
ͬ��������A-B-C��Ԫ���������壬��ƽ����γ�A-B-C-AB-ACα��Ԫϵ�������Ԫ����ʵĦ������Ϊ
 ��
��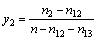 ��
��
 ��
��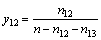 ��
��
 (8)
(8)
���У�n=n1+n2+n3�������Ԫ����Ϊ1 mol������x1=n1��x2=n2��x3=n3���������ǣ�Ӧ��MIVM�Ϳ�Ԥ�����α��Ԫ��ϵ������ѧ���ʡ�
2 �������
2.1 Fe-Si-C��ϵMIVM�����Ļ�ȡ
Һ̬����Fe��Si��C����λ��Zi��������ʽ����[8]��
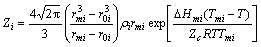 (9)
(9)
���У�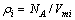 ��Ϊ��Ԫi�ķ������ܶȣ�NAΪ����٤��������VmiΪҺ̬����i��Ħ�������Tmi�͡�Hmi�ֱ�Ϊ��Ԫi���۵���ۻ��ʣ�Zc=12��Ϊ�ܶ���λ����TΪҺ̬����������ѧ�¶ȣ�RΪ����ѧ���峣����r0i��rmi�ֱ�ΪҺ̬����i���۵㴦����ֲ������п�ʼ�͵�1��ľ������[8]��
��Ϊ��Ԫi�ķ������ܶȣ�NAΪ����٤��������VmiΪҺ̬����i��Ħ�������Tmi�͡�Hmi�ֱ�Ϊ��Ԫi���۵���ۻ��ʣ�Zc=12��Ϊ�ܶ���λ����TΪҺ̬����������ѧ�¶ȣ�RΪ����ѧ���峣����r0i��rmi�ֱ�ΪҺ̬����i���۵㴦����ֲ������п�ʼ�͵�1��ľ������[8]��
 ;
;  (10)
(10)
dcoviΪԭ�ӵĹ���ֱ����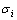 Ϊ��Ԫi��ԭ��ֱ��������ȱ��Һ̬̼������ѧ���ݣ����ļ���̼Һ���Ħ���������λ�������¶��أ����Ƶ���̼�۵㴦��ֵ�������ʵ���ز���[8-11]����1����λ���ļ���������2��
Ϊ��Ԫi��ԭ��ֱ��������ȱ��Һ̬̼������ѧ���ݣ����ļ���̼Һ���Ħ���������λ�������¶��أ����Ƶ���̼�۵㴦��ֵ�������ʵ���ز���[8-11]����1����λ���ļ���������2��
����Fe-Si�Ӷ�Ԫϵ�IJ���Bij��Bji���Էֱ�ͨ����Ԫi��j����Ӧ����ϡ���ϵ��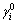 ��
��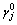 ����
��á��� ʱ��
ʱ��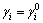 ����
����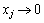 ʱ��
ʱ��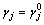 �������Ƿֱ����ʽ(3)��
�������Ƿֱ����ʽ(3)��
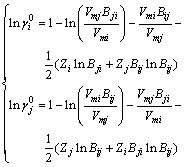 (11)
(11)
ʽ(11)Ϊ����B ji��Bij�Ķ�Ԫ�����Է����飬��ͨ��ͼ�ⷨ��ţ�ٵ�������⡣��1 873 Kʱ�����Fe-Si��Ԫϵ������ϡϵ�����ϵ��[12]Ϊ 0.016 20��
0.016 20��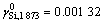 ��
��
��ԪϵFe-C��C-Si�IJ���Bij��B ji��ͨ��ʽ(3)��i-j�Ӷ�Ԫϵ��ʵ����[12-13]���ȷ����Ϊ�˵õ��õ����Ч������Ҫ��̼�Ա�����ҺΪ��̬������Ũ�ȷ�Χ��ʵ����ת�����Դ�����Ϊ��̬��ȫŨ�ȷ�Χ�Ļ�ȣ��ٽ��в������ڡ�������Һ�������ڶ����ɣ���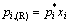 �����ԣ���һ���¶��£�������Һ�ı�������ѹ
�����ԣ���һ���¶��£�������Һ�ı�������ѹ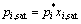 ����
����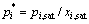 ���Դ�����Ϊ��̬��ȫŨ�ȷ�Χ�Ļ�ȿɱ�ʾΪ
���Դ�����Ϊ��̬��ȫŨ�ȷ�Χ�Ļ�ȿɱ�ʾΪ
 (12)
(12)
�Ա�����ҺΪ��̬������Ũ�ȷ�Χ�ڻ��Ϊ
 (13)
(13)
ͨ��ʽ(12)��(13)���Ե�����2�ֲ�ͬ��̬��ȵ�ת����ϵ[14]Ϊ
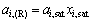 (14)
(14)
���У�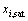 Ϊһ���¶�����Ԫi�ı�������������������Ӧ�Ķ�Ԫ��ͼ[12-13]��á�ͨ��ʽ(14)�ɽ�̼��ʵ����
Ϊһ���¶�����Ԫi�ı�������������������Ӧ�Ķ�Ԫ��ͼ[12-13]��á�ͨ��ʽ(14)�ɽ�̼��ʵ����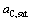 ת��Ϊ��Fe��Si������ͬ��̬�Ļ��
ת��Ϊ��Fe��Si������ͬ��̬�Ļ��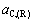 ���Դ���ϲ���B��
���Դ���ϲ���B��
����ʽ(2)���������е�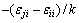 ��
��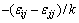 �����¶��أ����ʽ�ɱ�ʾBij��Bji���¶�T�ĵ�ֵ������ϵ������֪ijһ�¶��µ�Bij��Bji����ɼ���������¶��µ�Bij��Bji��������ݺͼ���������2����������ͼ1~3��ʾ�����У�
�����¶��أ����ʽ�ɱ�ʾBij��Bji���¶�T�ĵ�ֵ������ϵ������֪ijһ�¶��µ�Bij��Bji����ɼ���������¶��µ�Bij��Bji��������ݺͼ���������2����������ͼ1~3��ʾ�����У�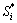 ��Si�ֱ�Ϊ��Ԫi��ȵļ���ֵ���ʵ��ֵ�ı�ƫ���ƽ�����������ʽ���£�
��Si�ֱ�Ϊ��Ԫi��ȵļ���ֵ���ʵ��ֵ�ı�ƫ���ƽ�����������ʽ���£�
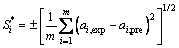 ��
��
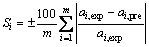 (15)
(15)
����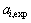 ��
�� �ֱ�Ϊ��Ԫi��ʵ���Ⱥͼ����ȣ�mΪʵ��ֵ�ĸ��������У�
�ֱ�Ϊ��Ԫi��ʵ���Ⱥͼ����ȣ�mΪʵ��ֵ�ĸ��������У� Ϊi��Ԥ����(������)��
Ϊi��Ԥ����(������)��
��1 ����Ԫ����ز���[8-11]
Table 1 Related parameters of pure components[8-11]

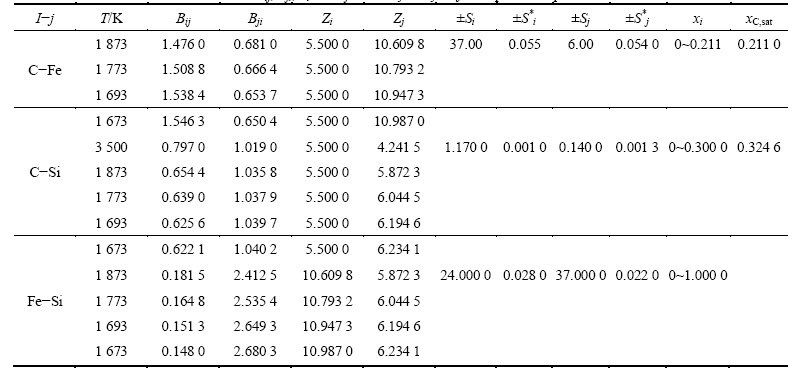
��2 �����¶���i-j��Ԫϵ��Bij��Bji��Zi��Zj
Table 2 Bij, Bji, Zi and Zj of binary alloys i-j at required temperatures

ͼ1 1 873 K��C-Fe������C��Fe��MIVM��������ʵ��ⶨֵ[12]�ıȽ�
Fig. 1 Comparison of calculated activity by MIVM and experimental results[12] of components C and Fe in C-Fe melt at 1 873 K
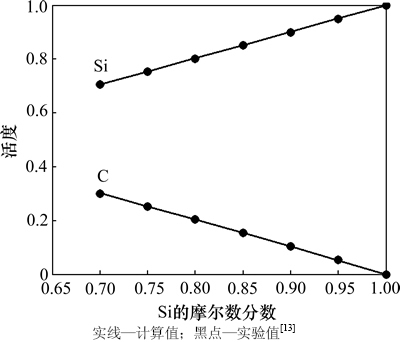
ͼ2 3 500 K��C-Si������C��Si��MIVM��������ʵ��ⶨֵ[13]�Ƚ�
Fig. 2 Comparison of calculated activity by MIVM and experimental results[13] of components C and Si in C-Si melt at 3 500 K

ͼ3 1 873 K��Fe-Si������Fe��Si��MIVM��������ʵ��ⶨֵ[12]�ıȽ�
Fig. 3 Comparison of calculated activity by MIVM and experimental results[12] of components Fe and Si in Fe-Si melt at 1 873 K
2.2 Fe-Si-C��ϵWagner�����Ļ�ȡ
������[3,15]�п��Բ鵽1 873 Kʱ��Һ�и���Ԫ������ϡ���ϵ��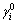 ��һ������ò���
��һ������ò���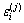 ������������Һ������ѧ��ϵʽ����
������������Һ������ѧ��ϵʽ����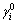 ��
��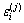 ���¶ȹ�ϵʽ���£�
���¶ȹ�ϵʽ���£�
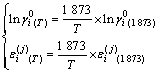 (16)
(16)
����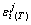 ��
��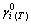 �ֱ�Ϊ�����¶�T�µ�����ò���������ϡ���ϵ����
�ֱ�Ϊ�����¶�T�µ�����ò���������ϡ���ϵ���� ��
�� �ֱ�Ϊ 1 873 Kʱ������ò���������ϡ���ϵ������ز����ͼ���������3�������Ǵ���ʽ(4)�Ϳɼ���������̬�µĻ��ϵ����
�ֱ�Ϊ 1 873 Kʱ������ò���������ϡ���ϵ������ز����ͼ���������3�������Ǵ���ʽ(4)�Ϳɼ���������̬�µĻ��ϵ����
��3 �����¶��µ�����ò�����Si������ϡ���ϵ��[3, 15]
Table 3 Values of interaction parameters and infinite activity coefficients of Si at required temperatures[3, 15]

2.3 CaO-Al2O3-SiO2��ϵMIVM�����Ļ�ȡ
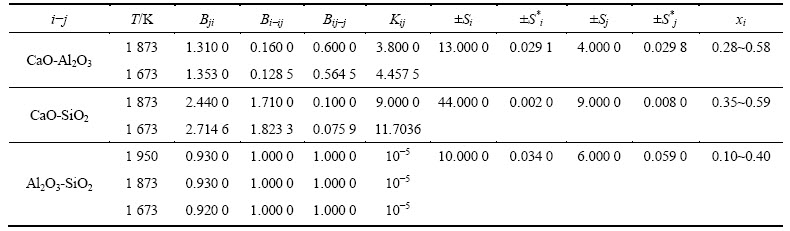
����CaO��Al2O3��SiO2�������е���λ��������������Ӧ�����ӵ���λ�����ֱ�Ϊ6��4��4[16]�������������е�Ħ��������Ƶ���������Ħ��������ֱ�Ϊ16.9��25.5��27.3 cm3/mol[16]�����γɻ��������λ����Ħ��������Ƶ�������Ӧ���ƽ��ֵ������Bij=Bji����ֱ���������Ԫ֮�������ð�������Һ����������CaO-Al2O3-SiO2��Ԫ��ϵ�����±�1��2��3�ֱ��ʾ����CaO��Al2O3��SiO2���±�4��5��6�ֱ����������CaO��Al2O3��CaO��SiO2��Al2O3��SiO2�����ڷ�Ӧ(5)���γɵ�α��Ԫ����CaO-Al2O3-CaO��Al2O3�IJ���B12��B14��B24��K12��CaO-SiO2-CaO��SiO2�IJ���B13��B15��B35��K13��Al2O3-SiO2-Al2O3��SiO2�IJ���B23��B26��B36��K23, ��ͨ������(3)�ɶ�Ӧ�Ӷ�ԪϵCaO-Al2O3��CaO-SiO2��Al2O3-SiO2��ʵ����[7]��ϵõ��������ֱ�����������Ԫ��Ķ����ܲ�����Ϊ1������B25= B52=1���ڲ�����Ϲ����У�����Ӧ�ں��Ի�ѧ�����Ӱ���������(Kij=10-5)�����ڶ����ܲ���Bij�����ﵽ��ѷ���Ч������ͨ������ƽ�ⳣ��Kij����һ���Ż�������ڲ�ͬ�¶��µIJ���Bij����ʽ(2)�����á���ͬ�¶��µ�ƽ�ⳣ��Kij������ʽ���㣺
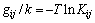 (17)
(17)
���У�kΪ��������������gijΪi-j�Ļ�������ܡ�����gij/k ���¶��أ���ʽ(17)��ΪKij���¶�T�ĵ�ֵ��ϵʽ���Ӷ����������㲻ͬ�¶��µ�ƽ�ⳣ����������Ͻ������ؼ���ֵ����4����������ͼ4~6��ʾ����Kij�����������Կ���Al2O3��SiO2��Ļ�ѧ����ú�С�����Ժ��Բ��ơ����ԣ�����Ԫ��ϵ��ת��ΪCaO-Al2O3-SiO2-CaO��Al2O3-CaO��SiO2α��Ԫ��ϵ������ʽ(8)���������ֵ���ʵĦ����������ͨ��ʽ(3)����Ԫչ��ʽ����Ԥ�����ϵ�������ѧ���ʡ�

ͼ4 1 873 K��CaO-SiO2������CaO��SiO2��MIVM��������ʵ��ⶨֵ[7]�ıȽ�
Fig. 4 Comparison of calculated activity by MIVM and experimental results[7] of components CaO and SiO2 in CaO-SiO2 melt at 1 873 K
��4 �����¶���i-j��Ԫϵ��Bij, Bi-ij, Bij-j��Kij
Table 4 Values of Bij , Bi-ij, Bij-j and Kij of binary alloys i-j at required temperatures
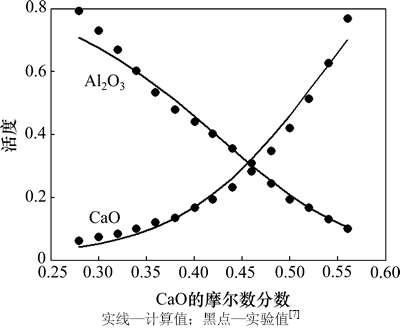
ͼ5 1 873 K��CaO-Al2O3������CaO��Al2O3��MIVM��������ʵ��ⶨֵ[7]�ıȽ�
Fig. 5 Comparison of calculated activity by MIVM and experimental results[7] of components CaO and Al2O3 in CaO-Al2O3 melt at 1 873 K

ͼ6 1 950 K��Al2O3-SiO2������Al2O3��SiO2��MIVM��������ʵ��ⶨֵ[7]�ıȽ�
Fig. 6 Comparison of calculated activity by MIVM and experimental results[7] of components Al2O3 and SiO2 in Al2O3-SiO2 melt at 1 950 K
2.4 ��Һ��Siƽ��Ũ�ȵļ���
����MIVM����α��Ԫ���Ը���-����ϵ������ƽ��Ԥ�⡣��¯����ʱ��SiO2����Һ�е�̼����ԭ����Ӧ����ʽ���£�
(SiO2)+2[C]=[Si]+2CO (18)
��������������������Ӷ�Ԫϵ�Ļ�ȱ�̬�������涨ʽ(18)�и���Ӧ��Ļ�ȱ�̬��SiO2�Ļ��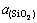 �Դ�SiO2����Ϊ��̬��C�Ļ�����䱥����ҺΪ��̬���������Դ�ʯīΪ��̬��Si�Ļ���Դ�SiҺ��Ϊ��̬����Ӧʽ(18)�ı�Ħ������˹������
�Դ�SiO2����Ϊ��̬��C�Ļ�����䱥����ҺΪ��̬���������Դ�ʯīΪ��̬��Si�Ļ���Դ�SiҺ��Ϊ��̬����Ӧʽ(18)�ı�Ħ������˹������ �������з�Ӧ���������ã�
�������з�Ӧ���������ã�

����
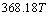 (J/mol)����֪��¯����Һ�е�̼�ﵽ����״̬��������
(J/mol)����֪��¯����Һ�е�̼�ﵽ����״̬�������� ����¯¯����CO�ķ�ѹ
����¯¯����CO�ķ�ѹ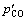 Ϊ101~152 kPa[17]������ѡ��
Ϊ101~152 kPa[17]������ѡ��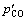 =120 kPa���м��㣻����ȷ�����¶Ⱥ�¯����ɣ���ͨ��MIVMα��Ԫ�����¯����SiO2�Ļ��
=120 kPa���м��㣻����ȷ�����¶Ⱥ�¯����ɣ���ͨ��MIVMα��Ԫ�����¯����SiO2�Ļ��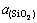 ����¯��ˮ��̼�ı�����������
����¯��ˮ��̼�ı�����������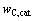 ���¶Ⱥ�Si�����������仯��ϵΪ
���¶Ⱥ�Si�����������仯��ϵΪ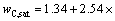
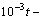
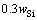 [3](����
[3](���У�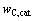 Ϊ̼����ˮ�еı�������������
Ϊ̼����ˮ�еı�������������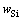 Ϊ��ˮ��Si������������tΪ�¶�)������ʽ�и�������������ת��ΪĦ�����������ٴ���ʽ(3)�ɵõ�Si�Ļ��ϵ��
Ϊ��ˮ��Si������������tΪ�¶�)������ʽ�и�������������ת��ΪĦ�����������ٴ���ʽ(3)�ɵõ�Si�Ļ��ϵ��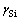 ����Si��Ħ��������
����Si��Ħ�������� �ĵ�ֵ��������ͨ���������·���
�ĵ�ֵ��������ͨ���������·���

�Ϳɽ���¶�T����̶���ɵ�¯��ƽ�����Һ�е�xSi��
�����ý��������[3]�з������ý����Ƚϡ�����[3]�з���Ӧ��Wagner��ʽ������Һ��������Ԫ�Ļ�Ƚ�������Ӧ��ʵ��Ȼ��������ȡ���Դ˽��� ��-����ƽ����㡣����ͬ������(1 873 K��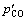 = 120 kPa)����������������ķ��̼�����Һ��Si��ƽ��Ũ��[3]��
= 120 kPa)����������������ķ��̼�����Һ��Si��ƽ��Ũ��[3]��
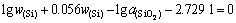 (19)
(19)
���У�wSiΪ��Һ��Si��ƽ������������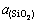 Ϊ��Ӧ������ϵ��SiO2�Ļ�ȣ���ֵ��Ӧ���ڲ巨��ʵ��ĵȻ������[3, 19]��ȡ��
Ϊ��Ӧ������ϵ��SiO2�Ļ�ȣ���ֵ��Ӧ���ڲ巨��ʵ��ĵȻ������[3, 19]��ȡ��
3 ��������
3.1 Fe-Si-C��ϵ
Fe-Si-C������Si�Ļ�ȼ���������5�ͱ�6��������Ũ�Ƚϵ͵���Һ�У���1 873 K�����ⶨ��һ������ò�������Wagner��ʽ������Ԫ��ȣ���������һ���IJο���ֵ�����ԣ��ڸ��¶��¿���Wagner��ʽ�ļ���ֵ������MIVM��Ԥ�������ӱ�5���Կ�����MIVM��Si��ȵ�Ԥ������Wagner��ʽ�ļ������Ϸ��ϣ�ƽ��������Ϊ4%�������ͨ��ʽ(14)ת��̼�Ļ�ȱ�̬����MIVM������ϵķ����Ǻ����ҿ��еġ��ӱ�6���Կ�������1 693 K��1 773 K�£�Fe-Si-C������Si��ȵ�MIVMԤ������ʵ����[18]���Ǻϣ�ƽ��������Ϊ9%����Wagner��ʽ��ƽ��������Ϊ56%��������ڸ��¶���MIVM��Ԥ��������Wagner��ʽ�ļ�������
3.2 CaO-Al2O3-SiO2��ϵ
CaO-Al2O3-SiO2������SiO2�Ļ��Ԥ������ ��7 ��ͼ7[19]���ӱ�7��ͼ7���Կ�������1 873 K��SiO2����Ũ�ȷ�Χ�ڣ�SiO2��ȵ�Ԥ��ֵ��ʵ��ֵ�Ϸ��ϣ�ƽ�������������ʵ����Χ30%����[20]�������ڽϵ͵�SiO2Ũ�ȷ�Χ�ڣ�Ԥ��ֵ��ʵ��ֵƫ��ϴ���Щƫ����һ���̶�����ʵ������ͼ���������Լ���ģ�ͺͷ���������ȱ����ɵģ�����Ԫ��Ļ�ѧ��Ӧֻ�����˷���(5)��������������Ԥ������н�����һЩ���裬�Լ���Ԫ������Ҫƾ���۾�����ڻ�õȣ����������ģ����Ҳû�п��ǵ���ܶȶԷ������ܵ�Ӱ�졣������ˣ���������Լ�����[7]�е��о����ͬ����ʾ��MIVMα��Ԫ���ܹ���������Ч��Ԥ����Ԫ������������Ԫ��ȵ�������Ϊ��ƽ��Ԥ��춨�˻�����
��5 1 873 KʱFe-Si-C������Si��MIVMԤ������Wagner��ʽ����ֵ�ıȽ�
Table 5 Comparison of predicted activities of MIVM with calculated activities by Wagner formula of Si in Fe-Si-C melt at 1 873 K
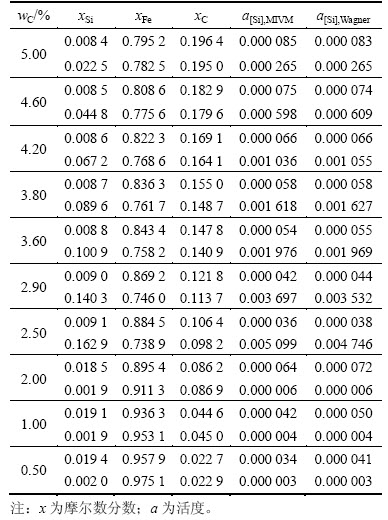
��6 1 693 K��1 773 KʱFe-Si-C������Si�Ļ�ȼ���ֵ��ʵ��ⶨֵ[18]�ıȽ�
Table 6 Comparison of calculated activities with experimental results[18] of Si in Fe-Si-C melt at 1 693 K and 1 773 K
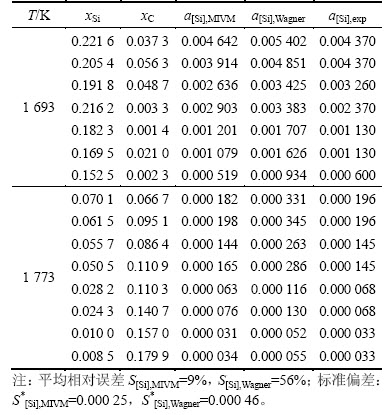
��7 1 873 KʱCaO-Al2O3-SiO2������SiO2��MIVMԤ������ʵ��ֵ[19]�ıȽ�
Table 7 Comparison of predicted activities by MIVM with experimental results[19] of SiO2 in CaO-Al2O3-SiO2 melt at 1 873 K
3.3 ��Һ��Si��ƽ��Ũ��
Siƽ��Ũ�ȵ�MIVMԤ��ֵ��ʵ��ֵ�Լ�����[3]�з������ü���ֵ��Ƚϡ�������8��ͼ8��ʾ���ӱ�8���Կ�����MIVMԤ��ֵ��ʵ��ֵ[3]��ƽ��������Ϊ17%����ͼ8����ֱ�۵ؿ������ڴ�������ɷ�Χ�ڣ�Ԥ��ֵ��ʵ��ֵ�Ϸ��ϡ���Ӧ������[3]�еķ������ü�������ʵ������ƽ��������Ϊ41%�������Ӧ��MIVM����Ԫ������-����ƽ���Ԥ��Ч��Ҫ���ڳ��õ�Wagner��ʽ��ϴ�ͼ����ȡ������ʵ���ȷ�����Ԥ��Ч����
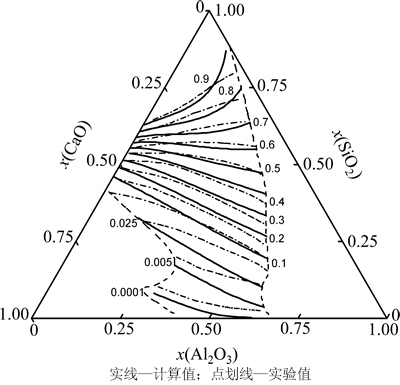
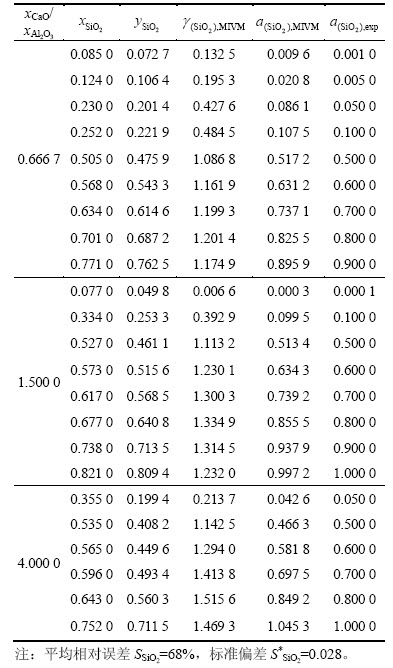
ͼ7 1 873 K��CaO-Al2O3-SiO2������SiO2��MIVMԤ������ʵ����[19]�ıȽ�
Fig. 7 Comparison of predicted activity of MIVM with experimental results[19] of component SiO2 in CaO-Al2O3-SiO2 melt at 1 873 K
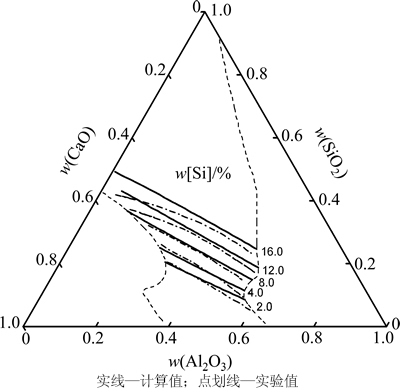
ͼ8 1 873 K����CaO-Al2O3-SiO2����ƽ�����Һ��Siƽ��Ũ�ȵ�MIVMԤ��ֵ��ʵ��ֵ[3]�ıȽ�
Fig. 8 Comparison of predicted values of MIVM with experimental data[3] of Si contents at equilibrium between molten slag CaO-SiO2-Al2O3 and iron melt at 1 873 K
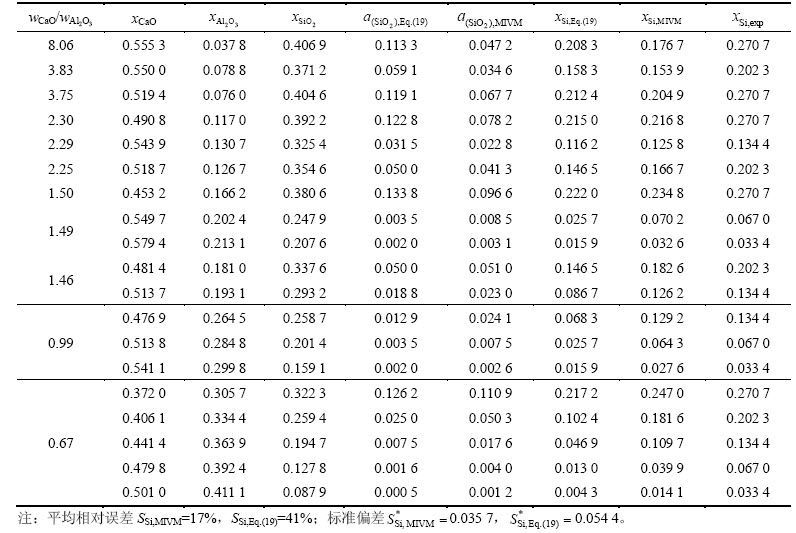
��8 1 873 K����CaO-Al2O3-SiO2������ƽ�����Һ��Siƽ��Ũ�ȵ�MIVMԤ��ֵ��(19)ʽ����ֵ��ʵ��ֵ[3]�ıȽ�
Table 8 Comparison of predicted values of MIVM and calculated values of Eq.(19) with experimental data[3] of Si contents at equilibrium between molten slag CaO-SiO2-Al2O3 and iron melt at 1 873 K
ģ��Ԥ��õ���Si����-�����ƽ�����������¶�T�Ͷ�Ԫ���w(CaO)/w(SiO2)��Ӱ����ͼ9��ͼ10��ʾ����ͼ9���Կ�����Ԥ��õ�Si��ƽ�����ϵ�����¶ȵ����߶�������������ȵ����Ӷ����͡�ʽ(20)�У�w[Si]Ϊ��ˮ����Si��ƽ������������w(SiO2)Ϊ¯������SiO2��ƽ��������������ʵ������У���Ӧ(18)Ϊǿ���ȷ�Ӧ��ƽ�ⳣ��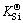 ���¶����߶����ӺܴӶ�ʹ��LSi��������CaO��SiO2�и�ƫ��Ӱ�죬������������ȵ����ӣ�SiO2�Ļ��ϵ��
���¶����߶����ӺܴӶ�ʹ��LSi��������CaO��SiO2�и�ƫ��Ӱ�죬������������ȵ����ӣ�SiO2�Ļ��ϵ�� ���ͣ��Ӷ�������Si��ƽ����䳣������ͼ10���Կ���������Al2O3Ũ�����ӣ��ڵͼ������Si��ƽ��Ũ�Ƚ��ͣ��Ӷ�������LSi���ڸ������ʹ��Si��ƽ��Ũ�����ߣ��Ӷ�������LSi������ʵ�������Al2O3����������������������Լ��ԣ���SiO2�и�ƫ��Ӱ�죬�ή��
���ͣ��Ӷ�������Si��ƽ����䳣������ͼ10���Կ���������Al2O3Ũ�����ӣ��ڵͼ������Si��ƽ��Ũ�Ƚ��ͣ��Ӷ�������LSi���ڸ������ʹ��Si��ƽ��Ũ�����ߣ��Ӷ�������LSi������ʵ�������Al2O3����������������������Լ��ԣ���SiO2�и�ƫ��Ӱ�죬�ή�� ���Ӷ�����LSi���ڼ������������ԣ���SiO2����ƫ��Ӱ�죬������
���Ӷ�����LSi���ڼ������������ԣ���SiO2����ƫ��Ӱ�죬������ ���Ӷ�����LSi������������MIVM��Ԥ�������ʵ�ʹ�������ϣ������ģ�Ͷ�ұ����ϵ�е� ��-����ƽ����н�ǿ��Ԥ��������
���Ӷ�����LSi������������MIVM��Ԥ�������ʵ�ʹ�������ϣ������ģ�Ͷ�ұ����ϵ�е� ��-����ƽ����н�ǿ��Ԥ��������
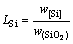 (20)
(20)
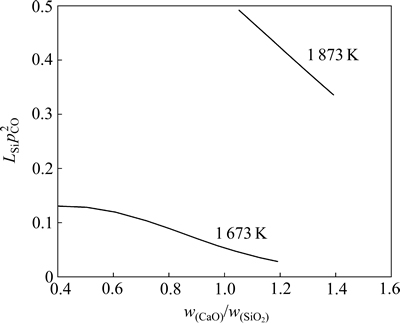
ͼ9 wAl2O3=10%ʱ�¶ȺͶ�Ԫ��ȶ�LSi��Ӱ��(MIVMԤ������)
Fig. 9 Effects of temperature and basicity of CaO-Al2O3-SiO2 on LSi (predicted curves by MIVM), when wAl2O3=10%
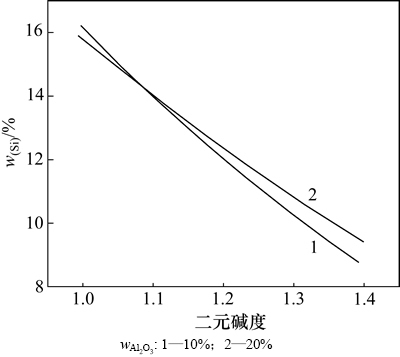
ͼ10 1 873 KʱAl2O3����������Siƽ��Ũ�ȵ�Ӱ��(MIVMԤ������)
Fig. 10 Effects of contents of Al2O3 on equilibrium contents of Si at 1 873 K (predicted curves by MIVM)
4 ����
1) ������Ĵ�����̼��ϵMIVM������ϵķ����Ǻ������еģ�MIVM��Ԥ��������Wagner��ʽ��Ԥ������
2) ������SiO2��ȵ�Ԥ��ֵ����Ӧ��ʵ��ֵ�Ϸ��ϣ�MIVM����α��Ԫ���Ը���Ԫ��ϵ��Ⱦ��нϺõ�Ԥ��Ч����
3) MIVM�Ը���-��ϵ��ƽ���Ԥ��Ч�����нϺõ��ȶ��ԺͿɿ��ԡ�
�ο����ף�
[1] Wagner C. Thermodynamics of alloys[M]. MA: Addison-Wesley, 1952: 51-53.
[2] The Japanese Society for the Promotion of Science, 19th Committee on Steelmaking. Steelmaking data sourcebook[M]. Switzerland: Gordon & Breach Science Publishers, 1988: 273-296.
[3] ��ϣ��. ����ұ��ԭ��[M]. 3��. ����: ұ��ҵ������, 2002: 46, 321.
HUANG Xihu. The principle of ferrous metallurgy[M]. 3rd ed. Beijing: Metallurgical Industry Press, 2002: 46, 321.
[4] �ż�. ұ���������Һ������ѧ����[M]. ����: ұ��ҵ������, 2007: 30-80.
ZHANG Jian. Thermodynamic calculation of metallurgical melt and solution[M]. Beijing: Metallurgical Industry Press, 2007: 30-80.
[5] TAO Dongping. A new model of thermodynamics of liquid mixtures and its application to liquid alloys[J]. Thermochim Acta, 2000, 363: 105-113.
[6] TAO Dongping. A comparison of the molecular interaction volume model with the subregular solution model in multicomponent liquid alloys[J]. Metall Mater Trans A, 2004, 35: 419-424.
[7] TAO Dongping. A pseudo-multicomponent approach to important ternary silicate melts[J]. Metall Mater Trans B, 2012, 43: 1247-1262.
[8] TAO Dongping. Prediction of the coordination numbers of liquid metals[J]. Metall Mater Trans A, 2005, 36(12): 3495-3497.
[9] Iida T, Guthrie R I L. The physical properties of liquid metals[M]. Oxford: Clarendon Press, 1988: 1-30.
[10] ��ʤ��, ����ƽ, л��. ��ѧԪ�����ڱ�[M]. 2��. ����: ��ѧ������, 2006: 175-909.
GAO Shengli, CHEN Sanping, XIE Gang. A periodic table of the chemical elements[M]. 2nd ed. 2nd ed.Beijing: Science Press, 2006.
[11] Ҷ����, ������. ʵ����������ѧ�����ֲ�[M]. 2��. ����: ұ��ҵ������, 2002: 175-909.
YE Dalun, HU Jianhua. Handbook of thermodynamic data for the practical inorganic substances[M]. 2nd ed. 2nd ed.Beijing: Metallurgical Industry Press, 2002.
[12] Hultgren R, Desai P D, Hawkins D T. Selected values of the thermodynamic properties of binary alloys[M]. OH: ASM, Metals Park, 1973: 477-883.
[13] Predel B, Landolt-Bornstein. Group IV physical chemistry, Volume 19: Thermodynamic properties of inorganic materials[M]. New York: Springer-Verlag, 2002.
[14] TAO Dongping. Prediction of activities of three components in ternary molten slag CaO-FeO-SiO2 by the molecular interaction volume model[J]. Metall Mater Trans B, 2006, 37: 1091-1097.
[15] �ն�ƽ. Һ̬�Ͻ������¯��������[M]. ����: ���ϿƼ�������, 1997: 318-321.
TAO Dongping. The properties of liquid alloys and molten slags[M]. Kunming: Yunnan Science and Technology Press, 1997: 318-321.
[16] Volf M B. Chemical approach to glass[M]. Amsterdam: Elsevier Science Publishers, 1984: 52-138.
[17] ������. ����ұ��ѧ��������[M]. 2��. ����: ұ��ҵ������, 2008: 96-103.
WANG Xiaoliu. Ferrous metallurgy, Ironmaking[M]. 2nd ed. 2nd ed. Beijing: Metallurgical Industry Press, 2008: 96-103.
[18] Jyrki M. Reassessed thermodynamic solution phase data for ternary Fe-Si-C system[J]. Calphad, 1998, 22(2): 231-256.
[19] VDEh. Slag atlas[M]. 2nd ed. Germany: Verlag Stahleisen GmbH Press, 1995: 226-238.
[20] Turkdogan E T. Physicochemical properties of molten slags and glasses[M]. London: The Metals Society, 1983: 95-105.
(�༭ �²ӻ�)
�ո����ڣ�2014-04-10�������ڣ�2014-06-22
������Ŀ(Foundation item)��������Ȼ��ѧ����������Ŀ(51090381��50764006) (Projects(51090381,50764006) supported by the National Natural Science Foundation of China)
ͨ�����ߣ��ն�ƽ����ʿ�����ڣ�����ұ��������ƽ��ķ�������ѧ�о���E-mail: dongpingt@aliyun.com
ժҪ��Ӧ�÷�����������ģ��(MIVM)������CaO-SiO2-Al2O3����ҺFe-Si-C��ϵ֮�����ƽ�����Ԥ�⡣�о������������Һ��Si��ȼ���ƽ��Ũ�ȡ�������SiO2��ȵ�Ԥ��ֵ����ʵ�����ݽϷ��ϣ�������1 693 K�� 1 773 K��Fe-Si-C������Si��ȵ�MIVMԤ��ƽ��������Ϊ9%����Wagner��ʽ��ƽ��������Ϊ56%������MIVM����α��Ԫ��Ԥ����1 873 K����Һ��Siƽ��Ũ�ȵ�ƽ��������Ϊ17%��������Wagner��ʽ��SiO2��ʵ�����������ƽ��������Ϊ41%�������MIVM��Ԥ��Ч�����н�ǿ���ȶ��ԺͿɿ��ԣ���ģ�ͽ�ͨ������Ӷ�Ԫϵ��Ȼ���ֱ��������ϡ���ϵ�������ܹ�Ԥ����ԪҺ̬�Ͻ�����������������ѧ���ʡ�
[1] Wagner C. Thermodynamics of alloys[M]. MA: Addison-Wesley, 1952: 51-53.
[3] ��ϣ��. ����ұ��ԭ��[M]. 3��. ����: ұ��ҵ������, 2002: 46, 321.
[4] �ż�. ұ���������Һ������ѧ����[M]. ����: ұ��ҵ������, 2007: 30-80.
[10] ��ʤ��, ����ƽ, л��. ��ѧԪ�����ڱ�[M]. 2��. ����: ��ѧ������, 2006: 175-909.
[11] Ҷ����, ������. ʵ����������ѧ�����ֲ�[M]. 2��. ����: ұ��ҵ������, 2002: 175-909.
[15] �ն�ƽ. Һ̬�Ͻ������¯��������[M]. ����: ���ϿƼ�������, 1997: 318-321.
[16] Volf M B. Chemical approach to glass[M]. Amsterdam: Elsevier Science Publishers, 1984: 52-138.
[17] ������. ����ұ��ѧ��������[M]. 2��. ����: ұ��ҵ������, 2008: 96-103.
[19] VDEh. Slag atlas[M]. 2nd ed. Germany: Verlag Stahleisen GmbH Press, 1995: 226-238.


