L-��ʯ��������ȡ������������ӳ��
��ϼ��1, 2, �ƿ���2, ������2, ��ѧ��2, �ڽ��2
(1. ��ɳ��ѧ ��ѧ�뻷����ѧϵ, ���� ��ɳ, 410003;
2. ���ϴ�ѧ ��ѧ����ѧԺ, ���� ��ɳ, 410083)
ժ Ҫ��
�����������ӳ�������ѡ����L-��ʯ�������� �о����������ӳ��������ѡ����L-��ʯ��������ˮ��1, 2-��������������ϵ�е���ȡ������Ϊ�� ����pHֵ�� L-��ʯ������Ũ�Ⱥ�������Ũ�ȶԷ���ϵ��(K)�ͷ�������(��)��Ӱ�졣 �о��������: L-��ʯ���������������I(+)-��ӳ���L-��ʯ��������� (-)-��ӳ���γɸ��ȶ��ķǶ�ӳ�帴��� ����ϵ������pHֵ�����Ӷ�����, ������������pHֵ���߶��½�; ����ϵ������L-��ʯ������Ũ�ȵ����������, ������������Ũ��������ȶ�����, ����Ũ�����ӷ��������½�; ������Ũ�ȶԷ���ϵ���ͷ�������Ҳ�нϴ�Ӱ�졣
�ؼ���: ���Բ��; �������; L-��ʯ������
��ͼ�����:O657.71 ���ױ�ʶ��:A ���±��: 1672-7207(2005)06-0983-05
Separation of propranolol enantiomers by extraction with L-n-octyl tartrate
PENG Xia-hui1, 2, HUANG Ke-long2 , JIAO Fei-peng2, ZHAO Xue-hui2, YU Jin-gang2
(1. Department of Chemical and Environment Science, Changsha University, Changsha 410003, China;
2. School of Chemistry and Chemical Engineering, Central South University, Changsha 410083, China)
Abstract: Distribution behavior of propranolol enantiomers was examined in aqueous-1, 2-diochloroethane of a two-phase system containing the synthesis of chiral selector L-n-octyl tartrate. The influences of pH value, concentrations of L-n-octyl tartrate and phosphate salt on partition coefficients(K) and separation factors(��) were investigated. The experimental results show that L-n-octyl tartrate can form more stable diasteromeric complexes with propranolol��(+)-enantiomer than with �� (-)-enantiomer. With the increase of pH value, partition coefficient (K) increases, but separation factor (��) decreases. With the increase of concentration of chiral selector K increases, and �� increases in lower concentrations and decreases in higher concentrations. And concentrations of phosphate salt also have a big influence on K and ��.
Key words: chiral separation; propranolol; L-n-octyl tartrate
����������ٴ��㷺Ӧ�õ���Ҫ��-�������ͼ�ҩ��, �������Ƹ�Ѫѹ�� ����ʧ�����Ľ�ʹ, ��Ч����[1-4]�� һֱ�������������ʽ��ҩ, ����ʵ��������, S(-) ��������Ԧ���������ͳ̶ȱ�R(+) ���������Լ��100��[5-7], R(+) ������������Ԧ�������������ú�С, �����б�������, ����Ϊһ����Ч�ı���ҩ�� ���, ������������ʽ��ҩ���������������������ϵͳ������Ч�ܲ���, �������״��������á� ������������������Ϊ���Դ�������, ����Ϊ2�ֲ�ͬ��ҩ��ֱ���ҩ, ������ҹ��������ҩƷ��������Ч������ ��λ�õ�һ��������ҩ���Ϊ��ǰ����ҩ���о������ſ���[8-12]�� ���������������������Ʊ��Է����о�, Ŀǰ������δ��������
Ϊ��, �����о���L-��ʯ�������ĺϳ�, ������L-��ʯ��������Ϊ����ѡ����Һ-Һ��ȡ�������, ʹ���Ķ�ӳ�����, ������pHֵ�� ����ѡ����L-��ʯ������Ũ�Ⱥ�����Ũ�ȵ����ضԷ���ϵ��(K)�ͷ�������(��)��Ӱ�졣
1 ʵ�鲿��
1.1 �������Լ�
��Ҫ������: ZD-2�͵��ٶ�������(��̳�н��ܷ�������������), Waters��ЧҺ��ɫ����, 484UV�������
��Ҫ�Լ���: L-��ʯ��(�Ϻ����ֻ���������),[��]20D=+12.2��, ����Ϊ99%, �������(�������Լ�����˾����); N-�����ʻ�-S-����-L-���װ������(MBPCE)(�������Լ�����˾����); ����(�Ϻ���ѧ�Լ�վ�����Լ�������)��
1.2 ɫ��������
ɫ��������[13]: ɫ����ΪNova Pak CN HP 8 mm��100 mm cartridge; ����Ϊ����; ������ΪV(��������)��V(�Ҵ�)=97��3, ����c(MBPCE)=3.5 mmol/L; ����Ϊ0.5 mL/min; ��Ⲩ��Ϊ254 nm��
1.3 L-��ʯ�������ĺϳ�
��ȡ0.15 mol L -��ʯ�ᡢ 0.375 mol������0.01 mol�Լױ��������װ��300 mL�ױ���Բ����ƿ��, ��ԡ����, ���ַ�Ӧ�¶�110 ��, ��������, ��Ӧ5 h����, �ֳ������������ˮԼ5 mL��, ֹͣ��Ӧ�� ����Ӧ�������ȴ������, ��ӦҺ�ֱ���100 mL�ı���NaHCO3��Һϴ��2��, 100 mL��ȥ����ˮϴ1��, ��ˮMgSO4�����ҹ, ����, ��Һ�ü�ѹ�����ȥ�ܼ��ױ�����������, ��ȴ�õ���ɫ����L-��ʯ������[14]��
1.4 ��ȡʵ��
��10 mL����L-��ʯ��������1, 2-����������Һ��10 mL�������������������Na2HPO4/H3PO4������Һ����60 mL�ķ�Һ©����, ������2.5 h�� �����, ���ྲֹ�ֲ��ȡˮ����и�ЧҺ��ɫ����, �л��౻����Ũ�Ȳ��ò�������, ����ʱδ������ȡǰ�����������仯�� ����ӳ�����ϵ��(![]() ��
��![]() ) ��ͨ��
) ��ͨ��![]() ��á� ����,
��á� ����, ![]() ��
��![]() �ֱ�Ϊˮ����I(+)�͢�(-)��ӳ�����ʼŨ��,
�ֱ�Ϊˮ����I(+)�͢�(-)��ӳ�����ʼŨ��,![]() ��
��![]() �ֱ�Ϊ��ȡƽ��ʱ, ˮ����I(+)�͢�(-)��ӳ���Ũ��; ��������(��)������ѡ����, ��ͨ��
�ֱ�Ϊ��ȡƽ��ʱ, ˮ����I(+)�͢�(-)��ӳ���Ũ��; ��������(��)������ѡ����, ��ͨ��![]() ��á�
��á�
2 ���������
2.1 L-��ʯ�������Ľṹ
L-��ʯ�����ĺ������ͼ��ͼ1��ʾ��

ͼ 1 L-��ʯ�������ĺ������ͼ
Fig. 1 Infrared spectrum for L-n-octyl tartrate
��ͼ1��֪: ��Լ3500 cm-1����һ�������շ�, ����OH��������, ˵�����ǻ�����, û������������ ��1000~1200 cm-1�������ǻ���C��O���������շ�, 1740 cm-1��Ϊ����C-O�����������շ�, ��2800~3000 cm-1�����ֵ���C��H���������շ塣
2.2 pHֵ��K�ͦ���Ӱ��
���о����������ӳ�����ȡ������Ϊʱ, ��ȷ�ⶨ2��ӳ���������еĺ����� ͼ2��ʾΪ���������ӳ����Ʒ��ɫ����ͼ�� ��ͼ�ɼ�, �����������ӳ�弸���ﵽ���߷��롣 ���ȳ����ΪR�칹��, ������ΪS�칹�塣
Ϊ����pHֵ��K �ͦ���Ӱ��, �о������������ӳ���ڲ�ͬpHֵʱ, ����L-��ʯ����������ѡ�����ˮ���л��ܼ�(1, 2-����������Һ)����ϵͳ�еķ�����Ϊ�� ��ҺpHֵ�ͷ���ϵ��(K)�Լ���������(��)�Ĺ�ϵ��ͼ3��ͼ4��ʾ��
��ͼ3�ɼ�, ���������ӳ��ķ���ϵ������pHֵ�����Ӷ�����; Ȼ��, ��ͼ4��֪, ������������pHֵ���߶��½�; ��ʵ��pHֵ��Χ��, K�����Ǵ���K��, ��������1�� pHֵ��ͬʱ, ���������ӳ�������Ϊ�IJ������DZ�������ȡ��ϵ�д������Ƕ�ӳ�帴����, ��L-��ʯ�����������������ӳ���γ������Ƕ�ӳ�帴���

ͼ 2 ���������ӳ���ɫ����
Fig. 2 Chromatography separation of propranolol enantiomers
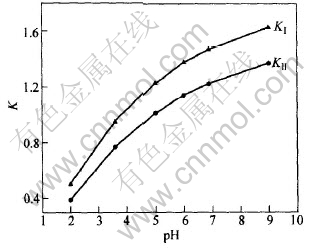
ͼ 3 pHֵ�Է���ϵ��K����K����Ӱ��
Fig. 3 Influence of pH value on partition coefficients

ͼ 4 pHֵ�Է������Ӧ���Ӱ��
Fig. 4 Influence of pH value on separation factor
2.3 L-��ʯ������Ũ�ȶ�K�ͦ���Ӱ��
������ȡ�������漰L-��ʯ�����������������ӳ���������ַ���֮���������������Ƕ�ӳ�帴����ķ�Ӧ, L-��ʯ��������Ũ�Ȳ����Է���ϵ���нϴ��Ӱ��, ���ұؽ�Ӱ��������ӡ� ��1, 2-��������Ϊ�л����ܼ�, ��pH=7.0ʱ, ����L-��ʯ������Ũ�ȶ�K�ͦ���Ӱ��, �����ͼ5��ͼ6��ʾ��

ͼ 5 L-��ʯ������Ũ�ȶԷ���ϵ��![]() ��
��![]() Ӱ��
Ӱ��
Fig. 5 Influence of concentration of L-n-octyl tartrate on partition coefficients

ͼ 6 L-��ʯ������Ũ�ȶԷ������Ӧ���Ӱ��
Fig. 6 Influence of concentration of L-n-octyl tartrate on separation factor
��ͼ5��6���Է���, ��ӳ�����ϵ������L-��ʯ������Ũ�ȵ���������� �������Ӧ�����Ũ��������ȶ�����, Լ1.1 mol/Lʱ, �������, Ȼ����Ũ������, �����������½�; ��ʵ��Ũ�ȷ�Χ��, K�����Ǵ���K��, ��������1, ˵��L-��ʯ�����������������(+)-��ӳ�����ȡ�������ڶ����������(-)-��ӳ�����ȡ������
2.4 ������Ũ�ȶ�K�ͦ���Ӱ��
ʵ�鷢��, ������Ũ�ȶ����������ˮ�е��ܽ���нϴ��Ӱ��, ��0.3 mol/L��Na2HPO4/H3PO4������Һ(pH 7.0)�е��ܽ��ԼΪ�ڴ�ˮ��Һ���ܽ�ȵ�3���� ���, ���о��������������ȡʱ, �б�Ҫ��������Ũ�ȶ�K�ͦ���Ӱ����п��졣 ��1, 2-��������Ϊ�ܼ�, L-��ʯ������Ϊ����ѡ����, Ũ��Ϊ0.31 mol/L, ��pH=7.0ʱ, ����������Ũ�ȶ�K �ͦ���Ӱ�졣 ��ͼ7�ɼ�, ��ӳ�����ϵ������������Ũ�ȵ����Ӷ��ȶ�����; ����ͼ8���Է���, ����������������Ũ�ȵ����Ӷ��½���
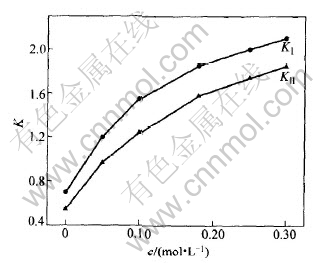
ͼ 7 ������Ũ�ȶԷ���ϵ��K����K����Ӱ��
Fig. 7 Influence of concentration of phosphate salt on partition coefficients

ͼ 8 ������Ũ�ȶԷ������Ӧ� ��Ӱ��
Fig. 8 Influence of concentration of phosphate salt on separation factor
3 �� ��
a. �ϳ�������ѡ����L-��ʯ��������
b. L-��ʯ���������������I(+)-��ӳ���L-��ʯ��������� (-)-��ӳ���γɸ��ȶ��ķǶ�ӳ�帴���
c. ����ϵ������pHֵ�����Ӷ�����, ������������pHֵ���߶��½�;
d. ����ϵ������L-��ʯ������Ũ�ȵ����������, ������������Ũ��������ȶ�����, ����Ũ�����ӷ��������½�;
e. ����ϵ������������Ũ�ȵ����Ӷ��ȶ�����, ����������������Ũ�ȵ����Ӷ��½���
�����:
[1]Diaz B C, Blanco C C. Simple determination of propranolol in pharmaceutical preparations by heavy atom induced room temperature phosphorescence[J]. J Pharm Biomed Anal, 2002, 30: 987-992.
[2]�Ծ�, ���Ǿ�.(S)-�������������ѡ���Ժϳ�[J]. �㽭��ҵ��ѧѧ��, 1997, 25(3): 252-255.
ZHAO Jun, WANG Ya-jun. The selective synthesis of (S)- propranolol[J]. Journal of Zhejiang University of Technology, 1997, 25(3): 252-255.
[3]El-Saharty Y S. Simultaneous high-performance liquid chromatography assay of furosemide and propranolol HCl and its application in a pharmacokinetic study[J]. J Pharm Biomed Anal, 2003, 33: 699-709.
[4]����, ������, ���Ժ�. �������������Թ̶��������֦�-�������ͼ���ӳ��[J]. ��������ѧ��, 1999, 18(3): 75-77.
ZHANG Yan-hui, ZOU Xiao-rong, YUN Zi-hou. Enantiomer separation of ��-blocking drugs by high-performance liquid chromatography with amide derivativeas chiral stationary phase[J]. Journal of Instrumental Analysis, 1999, 18(3): 75-77.
[5]Steven T, Wu Y P. Stereoselective high-performance liquid chromatography determination of propranolol and 4-hydroxy propranolol in human plasma after pre-column derivatization[J]. Journal of Chromatography B, 1997, 692: 133-140.
[6]���ļ�. ��ЧҺ��ɫ������ɫ���������-���ͼ���ӳ��[J]. ���ҩѧ, 2001, 13(6): 71-72.
ZUO Wen-jian. The separation of ��-blocking agents by high-performance liquid chromatography with chiral Chromatogram columniation[J]. Tianjin Medicine, 2001, 13(6): 71-72.
[7]��¶ɽ, Ҧͮ�, �����, ��. ���Թ̶��෨����������������֦�-������ϼ���ҩ�P��ṹ������[J]. �㽭��ѧѧ��(ҽѧ��), 2002, 31(6): 414 -418.
YU Lu-shan, YAO Tong-wei, WANG Xiang-jun, et al. Enantiomeric separation of ��-blocking agents and analogs[J]. Journal of Zhejiang University (Medical Sciences), 2002, 31(6): 414 -418.
[8]�ƿ���, �ܴ�ɽ. ��ˮ��L-��ʯ��������ѡ������ȡ��������ͪ��ӳ��[J]. ������ѧ, 2004, 32(1): 63-66.
TANG Ke-wen, ZHOU Chun-shan. Separation of chlorothalidone enantiomers by chiral extraction with L-tartaric esters[J]. Chinese Journal of Analytical Chemistry, 2004, 32(1): 63-66.
[9]Roussel C, Favrou A. Cationic ��-cyclodextrin: a new versatile chiral additive for separation drug enantiomers by high-performance liquid chromatography[J]. Journal of Chromatography A, 1995, 704: 67-74.
[10]Williams R C, Edwards J F, Joshi A S, et al. Chiral analysis of drug substance in clinical plasma extracts using achiral HPLC with circular dichroism detection[J]. J Pharm Biomed Anal, 2001, 25: 501-509.
[11]Peterson A G, Ahuja E S, Foley J P. Enantiomeric separations of basic pharmaceutical drugs by micellar electrokinetic Chromatography using a chiral surfactant, N-dodecoxycarbonylvaline[J]. Journal of Chromatography B, 1996, 683: 15-28.
[12]��ر�, ������, ������, ��. ��L-�Ȱ�����Ϊ����ѡ���ëϸ�ܵ�Ӿ��ּ���ҩ�������ӳ��[J]. ������ѧ, 2000, 28(10): 1287-1290.
LI Guan-bin, LIN Xiu-li , ZHU Chen-fu , et al. Enantioseparation of several pharmaceutical racemates with capillary electrophorsis using L-Glutamine as the chiral selector[J]. Chinese Journal of Analytical Chemistry, 2000, 28(10): 1287-1290.
[13]LI Nai-xuan, YAN Xiu-fang, XIAO Ru-ting. Resolution of propranolol enantiomers by high-performance liquid chromatography with chiral ion pair agent[J]. Applied Chemistry Industry, 2003, 32 (2): 48-50.
[14]Eldin E, Lindner K J, Pettersson C, et al. Tartaric acid derivatives as chiral selectors in liquid chromatography[J]. Chromatographia, 1991, 32(9/10): 407-416.
�ո�����:2005-01-02
������Ŀ: ������Ȼ��ѧ����������Ŀ(20376085)
�����: ��ϼ��(1963-), Ů, ����������, ������, ��ʿ�о���, ���¹��ܲ��ϻ�ѧ��ҩ���о�
������ϵ��: ��ϼ��, Ů, ������; �绰: 13077323809(�ֻ�); E-mail: pxiahui@yahoo.com
ժҪ: �ϳ�����ȡ������������ӳ�������ѡ����L-��ʯ�������� �о����������ӳ��������ѡ����L-��ʯ��������ˮ��1, 2-��������������ϵ�е���ȡ������Ϊ�� ����pHֵ�� L-��ʯ������Ũ�Ⱥ�������Ũ�ȶԷ���ϵ��(K)�ͷ�������(��)��Ӱ�졣 �о��������: L-��ʯ���������������I(+)-��ӳ���L-��ʯ��������� (-)-��ӳ���γɸ��ȶ��ķǶ�ӳ�帴��� ����ϵ������pHֵ�����Ӷ�����, ������������pHֵ���߶��½�; ����ϵ������L-��ʯ������Ũ�ȵ����������, ������������Ũ��������ȶ�����, ����Ũ�����ӷ��������½�; ������Ũ�ȶԷ���ϵ���ͷ�������Ҳ�нϴ�Ӱ�졣


