��������Һ�л�ԭ��ȡ�����ڷ�
������1, 2, ������1, ������1, �����3, ������1, �� ��1
(1. ���ϴ�ѧ ұ���ѧ�빤��ѧԺ, ��ɳ 410083;
2. ���Ź�˾, ��� 737100;
3. �����Ƽ���ѧ ұ����̬ѧԺ, ���� 100083)
ժ Ҫ��
����SO2����ԭ���Ӻ��ڵ�������Һ����ȡ�ڷ�, ��ȷ����SO2��������Һ�л�ԭ�ڵ��������: ��Ӧ�¶�80��, NaClŨ��1.2mol/L, SO2����0.1m3/h, ��Ӧʱ��40min, �ڵĻ�ԭ�ʴﵽ99.63%�� ��ԭ���ô��ڷ۾�������������, ������ϴ���Ӵ���, ���� �顢 ���� ͭ���ѳ��ʷֱ�ﵽ99%�� 93%�� 80%�� 87.5%,�õ�����99.669%�Ľ����ڷۡ� XRD��SEM����������ԭ�ڷ۵���̬Ϊ��״���塣
�ؼ���: �ڷ�; ��������; ��ԭ ��ͼ�����: TF111.132
���ױ�ʶ��: A
Preparation of powdered-tellurium by reduction from sulfuric acid solution
MA Yu-tian1, 2, GONG Zhu-qing1, CHEN Wen-mi1,
LI Hong-xu3, YANG Zheng-hui1 , HUANG Jian1
(1. School of Metallurgical Science and Engineering, Central South University,Changsha 410083,China;
2. Jinchuan Group LTD., Jinchang 737100, China;
3. School of Metallurgical and Ecological Engineering,University of Science and Technology Beijing, Beijing 100083, China)
Abstract: The powders of Te were prapared from sulfuric acid solution bearing Te with SO2 as the reducing agent. The experiments show the optimum process parameters are as follows: reaction temperature 80��, NaCl concentration 1.2mol/L, SO2 flow rate 0.1m3/h, reaction time 40min.Under the optimum condition, 99.63% Te is reduced. After the treatment with NaSO3 and hydrochloric acid, 99% Se, 93% As, 80% Sn and 87.5% Cu are removed from the raw powdered-tellurium, and the powders of 99.669% Te are prepared. The results of XRD and SEM indicate that the powdered-tellurium is crystalline with needle form.
Key words: powdered-tellurium; sulfur dioxide; reduction
����ϡɢԪ��, ���ȼ��������н������ǽ�������С�ġ� �ڵ���;ʮ�ֹ㷺, ұ�� �� ʯ�͡� ���ӵ����� ���ϡ� �����մɡ� ҽҩ����ҵ���䴫ͳ��Ӧ������, ���¡� ���졢 ����������µ�Ӧ������ �ڵĻ�������Ҫ���ں���̽������ �й���ϡ� �²����ϡ� �ⴢ����ϵ�[1, 2]; �ڵ������Ļ����������õ��������, ���������״ ˮ�����ȵ�������ȴ��; �ڻ�Ǧ���ڻ������������й������²�����; �ڹ��ӺϽ��Ǻ��ⷢ�����̽��������Ѳ���; �������������ɲ�д�洢���̵���Ҫ���ϡ�
��һ���Ǵ���ȡ�������в����ķ����ͷ�Һ����ȡ����ա� ���ڷ����е��ڶ���ü������ ������ӡ� �к͡� ���Ĵ�ͳ������ȡ[2-4]�� TBP�� �������� ������������ȡ����Ҫ���ڴ����ᡢ �Ȼ����Һ�л�����[5-8], Ҳ�����о�����Һ��������Ĥ��������Һ����ȡ��[9]�� �Ӻ��ڵ�������Һ����ȡ����õķ�������ͭ����ԭ��, �����û��γ�CuTe����, ʹ�ڵõ�����, �ٽ�CuTe�ü����, ������ӡ� �к͵��õ�������[10-12]�� �÷��������̽ϳ�, ����Ҫ���Ĵ�����ͭ���Լ��� ����ѧ�������, ����SO2Ϊ��ԭ��, ����һ���Ӻ��ڵ�������Һ�л�ԭ�Ƶô��ڷ�, ���һ�ԭ���̲��������������Ԫ��, �ڵĻ�ԭ�ܳ��ס� ͨ��ʵ����֤������ѧ�������, ����ԭ���ô��ڷ۾��������Ӻ�, ���Ƶú���99.669%�����ξ���״�����ڷۡ�
1 ����ѧ����
1.1 ˮ��Һ��SO2���ڵ���̬
������SO2ͨ��ˮ��Һ����������H2SO3, H2SO3��һ�����ΪHSO-3��SO2-3, ��Ӧ����ʽ����[13]:
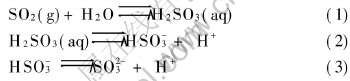
��Һ��SO2��ֵ���Ũ��[SO2]TΪ
![]()
��SO2��ѹp(SO2)=105Pa, ����ѹp��=105Pa��������([H2SO3]=1.20mol/L), ��������ѧ����[13], ��ʽ(1)~(4)�ֱ�������25���75��ʱ��Һ��SO2�����Ũ����pH�Ĺ�ϵ, �����ͼ1��ʾ��
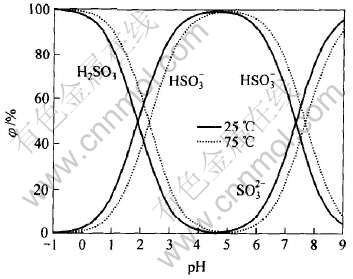
ͼ1 SO2-H2Oϵ���-pHͼ
Fig.1 SO2 in system of SO2-H2O-pH
��ͼ1�п��Կ���, ��pH��0��ǿ������Һ��, SO2�ܽ�����Һ����ȫ��H2SO3��̬����, �����ἰ������Һ����HSO-3��SO2-3��̬Ϊ��, ��Һ�¶���25�����ߵ�75��, H2SO3�ȶ����ڵ�pHֵ��Χ��������
1.2 SO2��ԭ������ѧ����
ʵ��������Һ������Ũ��Ϊ4mol/L, ��Һ����Ҫ�ɷ����1���С� ��Һ��Te��Te4+����, ����NaCl���γ�������TeCl2-6, Se��H2SeO3����, As��HASO2��AsO+����, Sn��Sn2+����, Cu��Cu2+���ڡ�
��1 ��Һ�ɷ�
Table 1 Composition of solution (mol/L)

������Ũ��Ϊ4mol/L���������������Һ��ͨ��SO2, �������ķ�����֪, ֻ����ʽ(1)�ķ�Ӧ, SO2����Һ�л�ԭ�����ķ�Ӧ����:
![]()
�뷴Ӧ�ֱ�Ϊ

��Ȼ, SO2��ԭ��Ӧ�ܹ����е�����ѧ������
![]()
���ߵ��Ʋ�Խ��, ��������ԭ�ij̶�Խ�ߡ� ��ʽ(6)���Կ�����aH2SO3һ��ʱ, ��SO2-4/H2SO3��aSO2-4����Һ��H+Ũ�ȶ��仯, ��˿���ͨ���ı���Һ��Ⱥ�SO2-4Ũ�������ڦ�SO2-4/H2SO3�Ĵ�С, �Ӷ���һ���ķ�Χ�ڿ�ѡ���ԵĻ�ԭ��Һ�еĽ������ӡ� ��Һ�и��������ӿ��ܴ��ڵİ뷴Ӧ����25��ı��缫��λ�� �Լ�����1��Һ�ɷּ����ʵ����Һ�и����ӵĵ缫��λ���ڱ�2�С�
��2 ���缫��λ��ʵ�ʵ缫��λ[1, 14]
Table 2 Standard and actual electrode potential
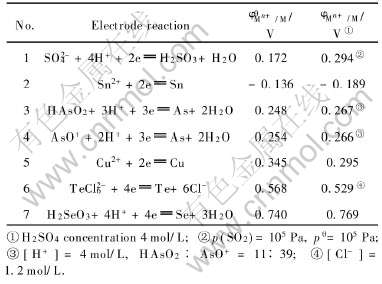
�ӱ�2���еĽ������ӵı��缫��λ���Կ���, ��������Һ�п�����SO2����ԭ���н������Ⱥ�˳����: Se�� Te�� Cu�� As, ��Sn���ܱ�SO2��ԭ�� ����������Һ�����ӵ�ʵ�ʵ缫��λ����, ��SO2ͨ���1���гɷֵ���Һ��, Se�� Te���ܻ�����ԭ, Cu���ܱ����ֻ�ԭ, As�� Sn������ԭ��
2 ʵ��
ʵ������ԭ��Ϊ��1���гɷֵ���Һ, ʵ����3L�ļ������н���, �����Լ�NaCl�� Na2SΪ������, SO2���ȸ���99.99%�� ��ʵ��ѡȡ��Ӧ�¶ȡ� �Ȼ���Ũ�ȡ� ��Ӧʱ�䡢 SO2���������ؽ���ʵ��, ������Щ���ض�Te��ԭ�ʵ�Ӱ��, ���Ի�ԭ����������������Ӵ���, �õ����ȸ���99%�Ľ����ڷۡ� ��������Baird��˾��PS-6����͵����ϵ�����ԭ�ӷ������(ICP)���гɷַ���, �����ձ���ѧD/MAX-RB��X����������(XRD)�����������, �����ձ�����˾SSX-550��ɨ��羵(SEM)�۲��������ò��
3 ���������
3.1 SO2��ԭ
3.1.1 NaClŨ�ȶ�Te��ԭ��Ӱ��
ͼ2��ʾΪNaClŨ�ȶ�Te��ԭ�ʵ�Ӱ�졣 ��ͼ2�п��Կ���, Te�Ļ�ԭ����NaClŨ�����Ӷ�����, ��NaClŨ�ȳ���1.2mol/L��, Te�Ļ�ԭ����NaClŨ�����Ӷ����н��͡� ����������Һ�д���������Cl-ʹ�뷴ӦTeCl2-6+4e=Te+6Cl-�ĵ缫��λ��Mn+/M����, ʹ�û�ԭ��Ӧ���в����ס� ����Һ�в�����NaCl, ��Ӧ60min��Te�Ļ�ԭ�ʲ�����55%; ����������NaCl��Te�Ļ�ԭ��Ѹ�����, NaCl������Һ�к�Cl-��Te4+�γ�������TeCl2-6, ��缫��λ����TeCl2-6/Te=0.55VС�ڦ���Te4+6/Te=0.63V, ����Cl-�ļ��벢���Ǹı�����Һ��Te4+�ĵ缫���ƶ�ʹ��ԭ��Ӧ���Խ���, ����Cl-��Te4+�Ļ�ԭ���ܾ��д�����, ��Cl-�ڷ�Ӧ�е����û����д���һ���о���
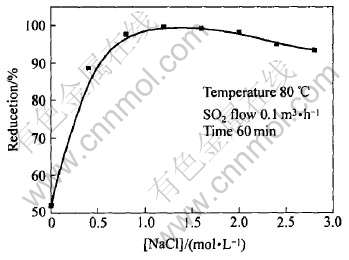
ͼ2 NaClŨ�ȶ�Te��ԭ�ʵ�Ӱ��
Fig.2 Effect of concentration of NaCl on reduction of Te
3.1.2 ��Ӧʱ���Te��ԭ��Ӱ��
ʵ������: NaClŨ��1.2mol/L, �¶�80��, SO2����0.1m3/h�� ��Ӧʱ���Te��ԭ��Ӱ����ͼ3��ʾ�� ͼ����ʾTe�Ļ�ԭ���淴Ӧʱ������Ӷ���������, 40min��ԭ��Ӧ�������, Te�Ļ�ԭ�ʴﵽ99.63%�� ͼ��ͬ����ӳ����Һ�н�������ԭ���Ⱥ�˳����Se�� Te�� Cu�� Se�Ļ�ԭ�ܿ�, �ڷ�Ӧ20minʱSe�ѻ���ȫ������ԭ, ��Cu�Ļ�ԭ��Ӧ��ʼ��Te�Ļ�ԭ��Ҫ��ȫ����ʱ, ����ǰ�������ѧ����һ�¡�
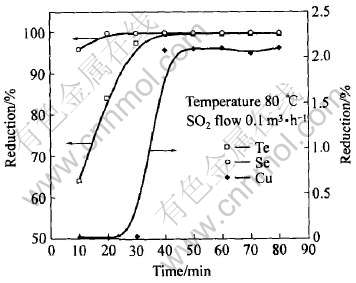
ͼ3 ��Ӧʱ���Te��ԭ�ʵ�Ӱ��
Fig.3 Effect of reaction time on reduction of Te
3.1.3 ��Ӧ�¶ȶ�Te��ԭ��Ӱ��
ʵ������: NaClŨ��1.2mol/L, SO2����0.1m3/h�� �ı䷴Ӧ�¶�, �����¶ȶ�Te��ԭ��Ӱ��, ʵ������ͼ4��ʾ�� ��ͼ�ɼ�, ��Ӧ�¶�Խ��Te����ԭ���ٶȾ�Խ��, ��Ӧ���������Ҫ��ʱ���Խ�̡� �¶�Ϊ80��ʱ, ��ԭ��Ӧ40min����ѻ������, Te��ԭ�ʴﵽ99.63%; �¶�Ϊ60��ʱ��ԭ��Ӧ80min��������; �¶�Ϊ40��ʱ��ԭ��Ӧ80min��Te��ԭ��Ϊ99.20%�� ���, ��ԭ��Ӧ��80�����ϵ��¶Ƚ��бȽϺá�
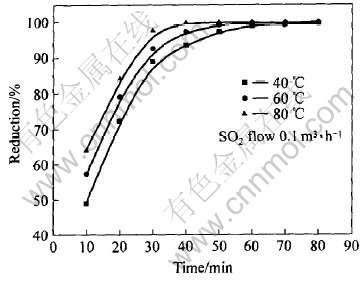
ͼ4 �¶ȶ�Te��ԭ�ʵ�Ӱ��
Fig.4 Effect of reaction temperature on reduction of Te
3.1.4 SO2������Te��ԭ��Ӱ��
�о���SO2������Te��ԭ�ʵ�Ӱ��, ʵ������ͼ5��ʾ�� ��ͼ�ɼ�, SO2����Խ��, ��ԭ��Ӧ�������Ҫ��ʱ���Խ�̡� SO2����Ϊ0.1m3/hʱ, ��ԭ��Ӧ40min���ѻ������; SO2����Ϊ0.06m3/h��0.02m3/hʱ, ��ԭ��Ӧ�ֱ����60min��80min��Ż�����ɡ� SO2������Te��ԭ��Ӱ��ֻ�����ڻ�ԭ�ٶ���, �ڱ�֤���㹻��ͨ��ʱ���ͨ��ѹ����������, ͨ��С������SO2ͬ����ʹTe�ﵽ�ϸߵĻ�ԭ�ʡ�
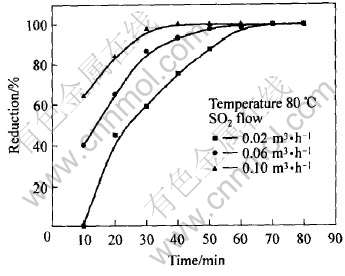
ͼ5 SO2������Te��ԭ�ʵ�Ӱ��
Fig.5 Effect of flow rate of SO2 on reduction of Te
�ۺ�ʵ��õ�SO2��ԭTe�Ϻ�����������: �¶�80��, NaClŨ��1.2mol/L, SO2����0.1m3/h, ��Ӧʱ��40min�� ���ô�������ԭ���ô��ڷۼ���ԭ��Һ�ɷ����3���С�
��3 ���ڷۼ���ԭ��Һ�ɷ�
Table 3 Compositions of raw powdered-tellurium and spent liquor
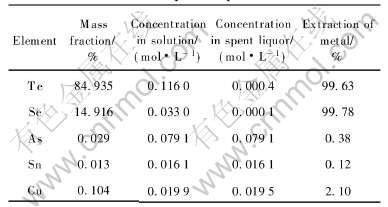
�ӱ�3���Կ���, Te��Se����ȫ������ԭ, Cu�ٲ��ֱ���ԭ�� ��ǰ������ѧ����������As��Snδ����ԭ, ���ڷ��е�As��Snֻ�DZ����������Ĵ��ڷ��������ѡ�
3.2 ���ڷ�������ͭ
���ڷ۵�XRD����ͼ6��ʾ, ��ͼ�ɼ�, ����ǿTe���Ա���һ������Se��, ICP����Ҳ�������ڷ��к���14.916%��Se, ������Dz���Na2SO3�����˳�Seʵ�顣 Na2SO3��Se�ǻ���Se��Na2SO3��Ӧ�γɿ����Ե�Na2SeSO3[15], ��Te������Na2SO3, �Ӷ�ʹSe��Te����:
![]()
��ԭ���ô��ڷ���ˮϴ�ӵ�ϴҺpH�ӽ���7, ��ϴ�Ӻ�Ĵ��ڷ۰�Һ�̱�10��1���뵽Ũ��Ϊ1mol/L��Na2SO3��Һ��, �����¶ȸ���95��, ǿ�ҽ��跴Ӧ60min, ����ϴ�ӵ������ڷۡ������ڷ���ˮϴ�Ӻ�Һ�̱�8��1����Ũ��Ϊ1mol/L��HCl��Һ��, 80��ͨ������Ӧ60min, ���˵���ͭ�ڷۡ� ���ڷۡ� ���������ڷ۳ɷ����4���С�
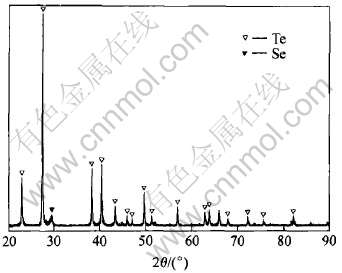
ͼ6 ���ڷ۵�XRD��
Fig.6 XRD pattern of raw powdered-tellurium
��4 �ڷ۳ɷ�
Table 4 Compositions of powdered-tellurium (%)
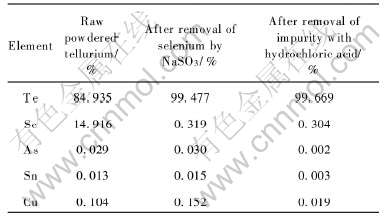
�ӱ�4�ɼ�Na2SO3��Se��Ч���dz���, ��Se�ʴ���99%, HCl��Cu����Ҳ�ѳ���������Se, ��Cu���ڷ۵�XRD����ͼ7��ʾ�� ��ͼ�пɼ�, ��ͼ6����ǿTe���Աߵ�Se������ʧ�� �ӱ���Ҳ�ɿ���, HCl��Cu��ͬʱҲ��ȥ���൱���ֵ�As��Sn, HCl��As�� Sn�� Cu���ѳ��ʷֱ�Ϊ93%�� 80%�� 87.5%�� As��Sn�ڴ��ڷ�����Ҫ��ˮ����̬As2O3��Sn(OH)2����, Cu�Ե��ʴ��ڡ� ��������Һ�зֱ������µķ�Ӧ:
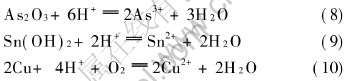
�Ӷ�ʹ�����γ����ӽ�����Һ, �ﵽ�ѳ����ʵ�Ŀ�ġ�
ͼ8��ʾ�ֱ�Ϊ��ͬ�Ŵ������ڷ�SEM��ò�� ��ͼ�ɼ�, ��ԭ�ڷ�Ϊ�������״����, ���ᾶ��ԼΪ10��1�� XRD�ױ����ڷ�Ϊ������״����(��ͼ7), ����������[15]�����ƵķǾ��κ�ɫ���ʡ�
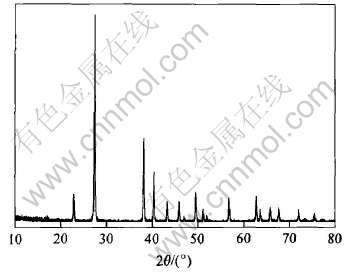
ͼ7 �ڷ۵�XRD��
Fig.7 XRD pattern of powdered-tellurium

ͼ8 �ڷ۵�SEM��ò
Fig.8 SEM photographs of powdered-tellurium
4 ����
1) ��ȷ����SO2����Һ�еĴ�����̬��, ��SO2��ǿ������Һ�л�ԭTe����������ѧ������ ����ѧ�����������SO2�ܽ���Һ�е�Te�� Se������ȫ����ԭ, Cu���ֻ�ԭ, ��As�� Sn������ԭ��
2) ͨ��ʵ����֤������ѧ��������ȷ��, ��ȷ����SO2��ԭ��ȡ�ڷ۵ĺ���������: �¶�80��, NaClŨ��1.2mol/L, SO2����0.1m3/h, ��Ӧʱ��40min��
3) ͨ�����������Ƶõ��ڷ۴��ȴﵽ99.669%��
4) �ڷ۵�XRD������SEM�۲�������, ��ԭ�ڷ�Ϊ������״����, ���ᾶ��Ϊ10��1���ҡ�
REFERENCES
[1]������. ϡɢ�����ֲ�[M]. ��ɳ: ���Ϲ�ҵ��ѧ������, 1993. 372-374.
Zhou Ling-zhi. Handbook of Scattered Metals[M]. Changsha: Press of Central South University of Technology, 1993. 373-374.
[2]Lijima T, Tanabe T, Funakoshi N. Crystallization characteristics of phase-change optical disks[J]. Jpn J Appl Phys, 1989, 28(11): L1985 -L1987.
[3]Rhee K, Lee C K, Ha Y C, et al. Tellurium recovery frome cemented tellurium with minimum waste disposal[J]. Hydrometallurgy, 1999, 53(2): 189-201.
[4]Handle B, Broderick G, Paschen P. A statistical response surface study of the tellurium electrowinning process[J]. Hydrometallurgy, 1997, 46(1-2): 105-120.
[5]Chowdhury M R, Sanyal S K. Diluent effect on extraction of tellurium(��) and selenium(��) by tri-n- butyl phosphate[J]. Hydrometallurgy, 1994, 34(3): 319-330.
[6]Bandyopadhyay M, Datta S, Sanyal S K. A mass transfer model for the hydrometallurgical extraction of Te(��) by tri-n- butyl phosphate[J]. Hydrometallurgy, 1996, 43(1-3): 175-185.
[7]������, ����֥, ��÷. ��������ȡ�ڵ��о�[J]. ������ѧѧ��(��Ȼ��ѧ��), 1999, 26(4): 377-380.
LI Yong-hong, LIU Xing-zhi, TIE Mei. Studies on the extraction of tellurium with tri-n-octyl amine[J]. Journal of Liaoning University (Natural Sciences Edition), 1999, 26(4): 377-380.
[8]Mandal D K, Bhattacharya B, Das D R. Recovery of tellurium from chloride media using tri-iso-octylamine[J]. Separation Purification Technology, 2004, 40(2): 177-182.
[9]Chakraborty R, Datta S. Extraction of Te(��) by liquid surfactant membrane[J]. Hydrometallurgy, 1996, 43(2): 169-174.
[10]Shibasaki T, Abe K, Takeuchi H. Recovery of tellurium from decopperizing leach solution of copper refinery slimes by a fixed bed reactor[J]. Hydrometallurgy, 1992, 29(3): 399-412.
[11]Hoffmann J E. Recovering selenium and tellurium from copper refinery slimes[J]. The Journal of the Minerals Material Society, 1989, 41(7): 33-38.
[12]����֥, ������, ���ٳ�, ��. �ڻ�ͭ�������ڵ�������ѧԭ��[J]. �㶫��ɫ����ѧ��, 2002(12): 55-58.
LIU Xing-zhi, SONG Yu-lin, WU Rong-cheng, et al. Physicochemical principle for recovering tellurium by copper telluride method[J]. Journal of Guangdong Non-ferrous Metals, 2002(12): 55-58.
[13]����ǰ, ÷���. ��ѧλͼ��ʪ��ұ��ͷ�ˮ�����е�Ӧ��[M]. ��ɳ: ���Ϲ�ҵ��ѧ������, 1986.
ZHONG Zhu-qian, MEI Guang-gui. Application of Diagrams of Chemical Potential in Hydrometallurgy and Purification of Waste Water[M]. Changshan: Press of Central South University of Technology, 1986.
[14]Latimer W M. The Oxidation States of the Elememts and Their Potentials in Aqueous Solution[M]. Prerceton Hall, 1952.
[15]�Ϻ��п�ѧ���������. ����������뵼�����(2)[M]. �Ϻ�: �Ϻ��п�ѧ���������, 1965.
The Science and Technology Translation Institute of Shanghai. Super-purity Metal and Semiconductor Materials (2)[M]. Shanghai: The Science and Technology Translation Institute of Shanghai, 1965.
������Ŀ: ������Ȼ��ѧ����������Ŀ(50204001)
�ո�����: 2005-04-26; ������: 2005-07-19
�����: ������(1971-), ��, ������ʦ, ��ʿ�о���
ͨѶ����: ������, ������ʦ; �绰: 13077394490; E-mail: mayutian666@163.com
[1]������. ϡɢ�����ֲ�[M]. ��ɳ: ���Ϲ�ҵ��ѧ������, 1993. 372-374.
[7]������, ����֥, ��÷. ��������ȡ�ڵ��о�[J]. ������ѧѧ��(��Ȼ��ѧ��), 1999, 26(4): 377-380.
[12]����֥, ������, ���ٳ�, ��. �ڻ�ͭ�������ڵ�������ѧԭ��[J]. �㶫��ɫ����ѧ��, 2002(12): 55-58.
[13]����ǰ, ÷���. ��ѧλͼ��ʪ��ұ��ͷ�ˮ�����е�Ӧ��[M]. ��ɳ: ���Ϲ�ҵ��ѧ������, 1986.
[15]�Ϻ��п�ѧ���������. ����������뵼�����(2)[M]. �Ϻ�: �Ϻ��п�ѧ���������, 1965.


