��ͬ�����ߴ��Cu-40Ni�Ͻ������Խ����е���ʴ����
������1, 2, ��ΰ��1, ֣־��1, ţ ��2
(1. ����ʦ����ѧ ʵ������, ���� 110034;
2. �й���ѧԺ�����о��� ������ʴ����������ص�ʵ����, ���� 110016)
ժ Ҫ��
���õ绡����(CA)�ͻ�е�Ͻ�(MA)ͨ����ѹ�սṤ���Ʊ��˾����ߴ���ϴ��Cu-40Ni�Ͻ�, ������PARM273A��M5210�绯ѧ�ۺϲ�����, ���ö���λɨ�跨�ͽ����迹�����Ա��о��������Ͻ������Խ����еĸ�ʴ�绯ѧ�����Լ���ʴ������ �������: ����H+Ũ�ȵ�����, CA Cu-40Ni�Ͻ���Ը�ʴ��λ����, ��MA Cu-40Ni�Ͻ�������, ���ֺϽ�Ķ���λɨ�輫�����߾�δ���ֶۻ�����; ����H+Ũ�ȵ�����, CA Cu-40Ni�Ͻ�ļ�����������, ��ʴ������С, �Ͻ����ʴ��������, ��MA Cu-40Ni�Ͻ�ļ��������С, ��ʴ��������, �Ͻ����ʴ���ܽ��͡� ���ֺϽ�Ľ����迹����˫�ݿ������, ��ʴ�����ܵ绯ѧ��Ӧ���ơ� ����ϸ����, �Ͻ��д��ڴ�������, ���븯ʴ��Ӧ�Ļ���ԭ��������, ��ʹMA Cu-40Ni�Ͻ�ĸ�ʴ�ٶȸ���CA Cu-40Ni�Ͻ�
�ؼ���: ͭ���Ͻ�; �绡����; ��е�Ͻ�; ����; ��ʴ�绯ѧ ��ͼ�����: TG146.1; TG174.44
���ױ�ʶ��: A
Corrosion behavior of Cu-40Ni alloy with different grain sizes in acidic media
CAO Zhong-qiu1, 2, LIU Wei-hua1, ZHENG Zhi-guo1, NIU Yan2
(1. Experimental Center, Shenyang Normal University, Shenyang 110034, China;
2. State Key Laboratory for Corrosion and Protection, Institute of Metal Research,Chinese Academy of Sciences, Shenyang 110016, China)
Abstract: The corrosion mechanism and corrosion-resistances of Cu-40Ni alloy prepared by conventional casting (CA), mechanical alloy (MA) and hot-pressing processes with the great difference in grain size in acidic media were investigated by PARM273A and M5210 electrochemical apparatus through the potentiodynamic polarization method and the electrochemical impedance spectroscopy (EIS) technique. The results show that the corrosion potential of CA Cu-40Ni alloy in acidic medium moves negtively, while MA Cu-40Ni alloy moves positively with the increase of the H+ concentration. There is no passive phenomenon in potentiodynamic polarization curve for the two alloys. With the increase of the H+ concentration, the polarization resistance increases, and the corrosion current decreases, so the corrosion resistance increases for CA Cu-40Ni alloy, while the polarization resistance decreases, and the corrosion current increases, so the corrosion resistance decreases for MA Cu-40Ni alloy. The electrochemical impedance spectroscopy (EIS) composed of double capacitive loops for the two alloys show that the corrosion process is controlled by electrochemical reaction. The corrosion rate of MA Cu-40Ni alloy becomes faster than that of CA Cu-40Ni alloy because the reduction in the grain size of MA Cu-40Ni alloy produces large concentrations of grain boundaries and increases the number of reactive atoms in alloy surface.
Key words: Cu-Ni alloy; conventional casting; mechanically alloying; nanocrystalline; corrosion electrochemistry
���ײ������ھ���һЩDZ�������������ѧ���ܶ�����֮Ϊ��21������Ϊ���ź�����й㷺Ӧ��ǰ����һ�����Ͳ���[1-3]�� Ŀǰ�й����ײ��ϵ��Ʊ��������б���, �糬ϸ��ĩ�̻����� ��ĥ���� ǿ���Ա��η��� �Ǿ��������͵绯ѧ��������, ���л�е�Ͻ�(Mechanical Alloying, ���MA)��һ�ַ�ƽ��̬�µķ�ĩ��̬�Ͻ���[4-9]�� ���ַ������ø�����ĥ����, ʹ��ͬ�ɷֵķ�ĩ����ĥ���б�ĥ������ײʹ��Ϸ�ĩ�������ѡ� ���Ρ� �亸�Ͷ̳���ɢ�Ӷ�ʵ�ֺϽ�, Ȼ������ѹ���ս�ķ����Ʊ���һ����״�����ܵĹ��塣 �ô˷����ѳɹ����Ʊ��˾��й㷺Ӧ��ǰ����Al-Ti, M50, Fe-B��TiO2�������������[10, 11]�� �������ײ��ϵ�����С, ����ԭ������, ��������ǿ, ������Ը�, ��ʹ��dz����ױ���ʴ, ����Ӱ���Ų��ϵ�ʹ�������Ӷ���Լ�����ײ��ϵ�Ӧ�á� Ŀǰ����绯ѧ��ʴ���ܵ��о�ȴ��Խ���, ���, �Ի�е�Ͻ��Ʊ�����������Ͻ��и�ʴ�绯ѧ�����о�, ���������ײ��ϵ�ʵ��Ӧ�ú��ƹ�, �����ɾ�����Ҫ�����塣
Cu-Ni�Ͻ���һ����Լ����д����ԵĶ�Ԫ��ϵ, һ��������Cu-Ni�Ͻ��������ɷַ�Χ��������, ���о��Ͻ�ʴ��Ϊ��������ϵ[12]; ��һ����úϽ����촬�� ������ҵ�ͺ��̵ȷ������Ź㷺��Ӧ�ñ���[13, 14]�� �о�����, Cu-Ni�Ͻ����ʴ������ϵ��Ʊ����ա� ����֯�ṹ����Χ�Ľ��������й�ϵ, ������Ϊֹ, Cu-Ni�Ͻ�ĸ�ʴ�����������Ч�������ʴ�����в���ȫ����� Ϊ��, �������߲��õ绡����(��)�ͻ�е�Ͻ���ͨ����ѹ����(����)�Ʊ��˾����ߴ���ϴ��Cu-40Ni�Ͻ�, �Ա��о������������Խ����еĵ绯ѧ��ʴ����, Ŀ�����ڽ�ʾCu-Ni�Ͻ������Խ����еĵ绯ѧ��ʴ�����Լ�����ϸ����Cu-Ni�Ͻ�绯ѧ��ʴ��Ϊ��Ӱ�졣
1 ʵ��
1.1 ��Ʒ���Ʊ�
��̬Cu-40Ni�Ͻ�(Ħ������, %, ����ͬ, ��CA Cu-40Ni��ʾ)�ɴ���Ϊ99.99%�Ľ���ԭ�������������, �����Ժĵ绡¯������������800������˻�24h����Ӧ�������, �侧���ߴ��СΪ50~100��m�� ����Cu-40Ni�Ͻ�(MA Cu-40Ni)���Ʊ�������ĥ����ѹ���̡� ������С��100��m�Ĵ�ͭ�ʹ�����(��99.99%, ��������)��������Ϻ����Ͼ���ѧ��QR-1SP����ʽ��ĥ������ĥ, �����ĥ����ʾ�Ϊ1Cr18Ni9Ti�����, ����������Ϊ10��1�� Ϊ��ֹ��ĥ��������Ʒ������, �������պ��ٳ������������ ÿ��ĥ1h, ͣ��30min�Ա������, ����ĥ60h�� ��ĥ�õķ�ĩ����d20mm��ʯīģ����, ��ģ������0.06Pa �����¯��, ����750���60MPaѹ���±���10min, Ȼ����¯��ȴ������˻� ����ˮ��������ѹ��Ͻ���ܶȴﵽ����ֵ��98.0%�� ���ձ���ѧD/MAX-rA������(CuK��), ���ð�߷巨(FWHD), Ӧ��Scherrer��ʽ(�۳�K��2����ķ����)������ĥ60h���ĩ��ƽ�������ߴ�ԼΪ10nm�� ��ѹ���ƽ�������ߴ�ԼΪ30nm , �˻��ԼΪ70nm, �Ͻ����Ƴɷ�ΪCu-40Ni, ��ʵ�ʺϽ��ƽ���ɷ�ΪCu-40.2Ni�� �ӺϽ���ȡ���ԼΪ1cm2����Ƭ, �û�����֬��װ, ��ɰֽ��ĥ��800#, ������, ˮ�� ��ˮ�Ҵ�����ͪ��ϴ�����
1.2 �绯ѧ����
�绯ѧ��������0.05mol/L Na2SO4��0.02�� 0.05�� 0.10��0.50mol/L H2SO4��Ϻ����Ƶĸ�ʴ�����н���, ��ѡ�Լ�Ϊ������, ��������ˮ���ơ� ����λ��������������EG&G��˾������PAR273A�绯ѧ����ϵͳ�ⶨ, ���ݾ�������ɼ�������Corrview�������, �����Ӧ�ĸ�ʴ��λ�� ��ʴ�����ȵ绯ѧ����; ����λ����ɨ���ٶ�Ϊ0.5mV/s, ��λɨ�跶ΧΪ-0.25V��0.7V�� �绯ѧ�����������缫ϵͳ, ���ʹ��缫(SCE)�Ͳ��缫�ֱ���Ϊ�αȵ缫�����缫, �Ͻ�Ϊ�����缫, ���ƹ�������Ϊ1cm2��
�绯ѧ�����迹���Բ�������EG&G��˾������PAR273A��M5210����ϵͳ, ����Ƶ�ʷ�ΧΪ105~10-2Hz, Ӧ��Zview2�����Խ����迹���ݽ��з����͵�·��ϡ�
2 ���������
2.1 CA Cu-40Ni�Ͻ�ĵ绯ѧ��ʴ��Ϊ
2.1.1 ��·��λ�붯��λ��������
ͼ1��ʾΪ����PARM273A��õ�CA Cu-40Ni�Ͻ��ڲ�ͬH+Ũ�Ƚ����еĸ�ʴ��λ��ʱ��仯���ߡ� ��ͼ�ɼ�, ����H+Ũ�ȵ�����, �Ը�ʴ��λ�ֱ�Ϊ-4�� -6�� -18��-87mV, �Ը�ʴ��λ����, ��˵���Ͻ��������������ɽ�
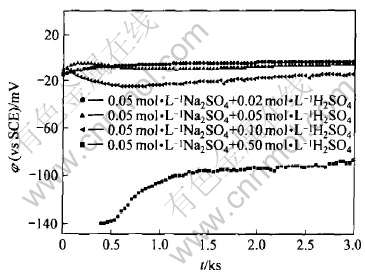
ͼ1 CA Cu-40Ni�Ͻ��ڲ�ͬH+Ũ�Ƚ����еĦ�-t����
Fig.1 ��-t curves of CA Cu-40Ni alloy in different H+ concentration media
�����Ķۻ�Ĥ��
ͼ2��ʾΪCA Cu-40Ni�Ͻ��ڲ�ͬH+Ũ�Ƚ����еĶ���λɨ�輫������, ��Corroview������ϵó��ĵ绯ѧ��������1�� ��ͼ���ɼ�, CA Cu-40Ni�Ͻ������Խ�����δ���ֶۻ�����, �Ͻ��������ܽ�, ������H+Ũ�ȵ�����, ������������, ��ʴ������С�� ��˵����һ����Χ��������Һ�е�H+Ũ�ȿ��Լ����Ͻ�ĸ�ʴ�� ��ͭ���Ͻ�ĸ�ʴ��Ϊ��ͭ����Ҫ����, ��ʴ������Ҫ��ͭ�����������ܽ������������ԭ��Ӧ���ɡ� ���������ܽ����Ϊ
![]()
Cu+ˮ�ⷴӦ����Ϊ
![]()
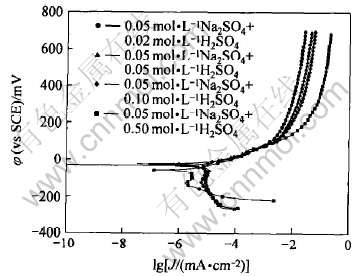
ͼ2 CA Cu-40Ni�Ͻ��ڲ�ͬH+Ũ�Ƚ����еļ�������
Fig.2 Polarization curves of CA Cu-40Ni alloy in different H+ concentration media
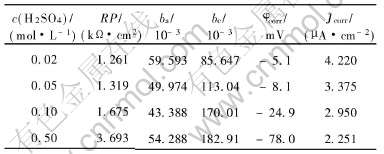
��1 CA Cu-40Ni�Ͻ��ڲ�ͬH+Ũ�Ƚ����еĵ绯ѧ����
Table 1 Electrochemical parameters of CA Cu-40Ni alloy in different H+ concentration media
������ԭ��ӦΪ
![]()
�����Խ�����, ����H+Ũ�ȵ�����, ������Ӧ(2)��(1)�ܵ�����, �Ͻ�ĸ�ʴ�ٶȽ��͡�
2.1.2 �����迹��
ͼ3��ʾΪCA Cu-40Ni�Ͻ��ڲ�ͬH+Ũ�Ƚ����еĽ����迹��(EIS)�� ��ͼ�ɼ�, CA Cu-40Ni�Ͻ��ڲ�ͬH+Ũ����Һ�������Ƶ�����, ����˫�ݿ�����ɡ� �����迹���ڵ�Ƶ��û�г���������Һ�о���Warburg�迹���ʵ���ɢβ, ȡ����֮������һ�뾶���ݿ����� �����ԭ���ڻ�����洦�ۼ��Ŀ����Ը�ʴ������������˻�ѧ��绯ѧ��Ӧ���õ�����, �缫����ĸ�ʴ��������ɢ����ת��Ϊ�绯ѧ���ơ� ��Ƶ�γ����ݿ��������ڵ缫���溬��������Ĥ���ݺ�Ĥ����, ��Ƶ�������ֽ���/��Һ���淴Ӧ����Ϣ, ��Ƶ���ݿ����Ĵ�С�ɷ�ӳ������ʴ���̵ĵ�ɴ��ݵ���[15]�� �ڵ�Ƶ�˳�һ��ѹ���Բ��, �ݿ���Բ��ƫ��ʵ��, ��������ɢЧӦ����� [16]�� ��ʱ�ĵ�Ч��·��ͼ4��ʾ, ��
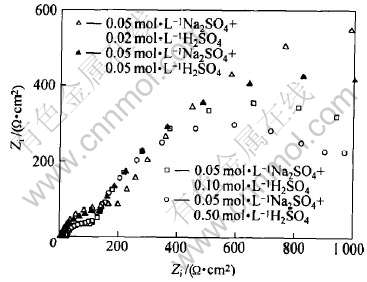
ͼ3 CA Cu-40Ni�Ͻ��ڲ�ͬH+Ũ�Ƚ����еĽ����迹��
Fig.3 EIS of CA Cu-40Ni alloy in different H+ concentration media
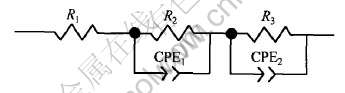
ͼ4 CA Cu-40Ni�Ͻ��ڲ�ͬH+Ũ�Ƚ����еĵ�Ч��·
Fig.4 Equivalent circuit of CA Cu-40Ni alloy in different H+ concentration media
��R1��ʾ��Һ����, R2��ʾĤ����, R3��ʾ��ɴ��ݵ���, CPE1ΪĤ����, CPE2Ϊ�缫����˫������, ����CPEΪ����λ��Ԫ��(constant phase angle element), CPE���迹�ɱ�ʾΪ

��Ͻ�����2���С� �ɱ�2�ɼ�, ��H+Ũ������, Ĥ����R2����, ��ɴ��ݵ���R3��С, ˵��Ĥ����ԺϽ�ĸ�ʴ�ٶ��нϴ�Ӱ��, �Ͻ�ĸ�ʴ�ٶȽ��͡�
2.2 MA Cu-40Ni�Ͻ������Խ����еĵ绯ѧ��ʴ��Ϊ
2.2.1 ��·��λ�붯��λ��������
ͼ5��ʾΪMA Cu-40Ni�Ͻ��ڲ�ͬH+Ũ�Ƚ����еĸ�ʴ��λ��ʱ��仯���ߡ� ��ͼ�ɼ�, �Ͻ���0.02��0.05mol/LH2SO4������, �Ը�ʴ��λ��ʱ���ӳ���С�������ȶ�, ����0.10��0.50mol/LH2SO4������, �Ը�ʴ��λ��ʱ���ӳ�������������ȶ��� ��ʴ��λ���ȶ�ֵ�ֱ�Ϊ-17�� -11�� -8��-2mV�� ����H+Ũ�ȵ�����, �Ը�ʴ��λҲ�����˲�ͬ�̶ȵ����ơ�
ͼ6��ʾΪMA Cu-40Ni�Ͻ��ڲ�ͬH+Ũ�Ƚ����еĵĶ���λɨ�輫������, ��Corroview������ϵó��ĵ绯ѧ�������3���С� �ɼ�, �Ͻ������Խ�����û�г��ֶۻ�, ��H+Ũ������, �������������С, ��ʴ��������, H+Ũ�����ӿɴٽ�������Ӧ�Ľ��С�
2.2.2 �����迹��
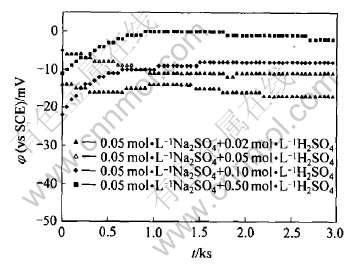
ͼ5 MA Cu-40Ni�Ͻ��ڲ�ͬH+Ũ�Ƚ����еĦ�-t����
Fig.5 ��-t curves of MA Cu-40Ni alloy in different H+ concentration media
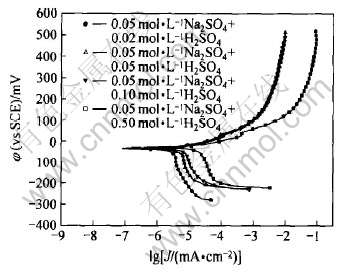
ͼ6 MA Cu-40Ni�Ͻ��ڲ�ͬH+Ũ�Ƚ����еļ�������
Fig.6 Polarization curves of MA Cu-40Ni alloy in different H+ concentration media
ͼ7��ʾΪMA Cu-40Ni�Ͻ��ڲ�ͬH+Ũ�Ƚ����еĽ����迹��(EIS)�� ��ͼ�ɼ�, MA Cu-40Ni�Ͻ��ڲ�ͬ��Ƚ����������Ƶ��迹�������� �佻���迹����˫�ݿ������, ����ʾͭ�������Ĥ���ݺ�Ĥ����ĸ�Ƶ���ݿ��������ֽ���/��Һ���淴Ӧ��Ϣ��Ƶ���ݿ���, ��ʱ�ĵ�Ч��·��ͼ8��ʾ, ��Ч��·Ԫ����ϲ������4���С� ����R1��ʾ��Һ����, R2��ʾĤ����, R3��ʾ��ɴ��ݵ���, C1ΪĤ����, ����λ��Ԫ��CPE2Ϊ�缫����˫�����ݡ� ���Ž�����ȵ�����, R2�� R3��C����С, �Ͻ�ĸ�ʴ�ٶ�����, ���뱾��2.2.1�ڼ������ߵIJ��Խ��һ��, ����������MA Cu-40Ni�Ͻ�����H+Ũ�ȵ�����, �Ͻ����ʴ�������½���
��2 CA Cu-40Ni�Ͻ��ڲ�ͬH+Ũ�Ƚ����еĵ�Ч��·Ԫ������
Table 2 Equivalent circuit parameters of CA Cu-40Ni alloy in different H+ concentration media
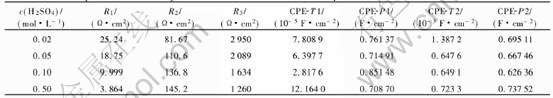
��3 MA Cu-40Ni�Ͻ��ڲ�ͬH+Ũ�Ƚ����еĵ绯ѧ����
Table 3 Electrochemical parameters of CA Cu-40Ni alloy in different H+ concentration media
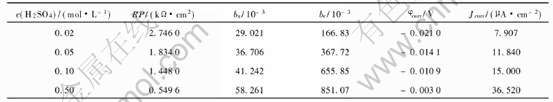
��4 MA Cu-40Ni�Ͻ��ڲ�ͬH+Ũ�Ƚ����еĵ�Ч��·Ԫ������
Table 4 Equivalent circuit parameters of MA Cu-40Ni alloy in different H+ concentration media
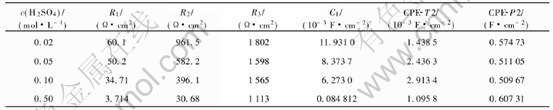
ͼ7 MA Cu-40Ni�Ͻ��ڲ�ͬH+ Ũ�Ƚ����еĽ����迹��
Fig.7 EIS of MA Cu-40Ni alloy in different H+ concentration media
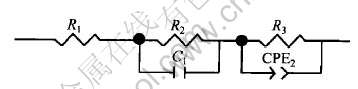
ͼ8 MA Cu-40Ni�Ͻ��ڲ�ͬH+ Ũ�Ƚ����еĵ�Ч��·
Fig.8 Equivalent circuit of MA Cu-40Ni alloy in different H+ concentration media
2.3 ����ϸ����Cu-40Ni�Ͻ������Խ����еĸ�ʴ�绯ѧ��Ϊ��Ӱ��
CA Cu-40Ni�Ͻ��ڲ�ͬ��Ƚ�����, ����H+Ũ�ȵ�����, ������ʴ������С, Ĥ����������, ��ɴ��ݵ����С, ��ʴ�ٶȽ��͡� ��MA Cu-40Ni�Ͻ�, ����H+Ũ�ȵ�����, ��ʴ��������, Ĥ����͵�ɴ��ݵ������С, ��ʴ�ٶ����� �Ա�CA Cu-40Ni�Ͻ��MA Cu-40Ni�Ͻ�����ͬ�����еĸ�ʴ��Ϊ, ���־���ϸ����, ���ںϽ��о����������, ���紦��ԭ�������������ھ�����ԭ��, ��Ӧ���Խ�ǿ, ���븯ʴ��Ӧ�Ļ���ԭ��������, ��ʴ�ٶȼӿ졣
3 ����
1) CA Cu-40Ni�Ͻ������Խ�����, ����H+Ũ�ȵ�����, �Ը�ʴ��λ���ơ� ����λɨ�輫������û�г��ֶۻ�����, ��������������, ��ʴ������С�� �����迹�������Ƶ�����, ������˫�ݿ���, ��ʴ�����ܵ绯ѧ��Ӧ���ơ� ����H+Ũ�ȵ�����, Ĥ����������, ��ɴ��ݵ����С, �Ͻ�ĸ�ʴ�ٶȽ���, ��ʴ�����ӡ�
2) MA Cu-40Ni�Ͻ������Խ�����, ����H+Ũ�ȵ�����, �Ը�ʴ��λ���ơ� ����λɨ�輫��������δ���ֶۻ�, ���������С, ��ʴ�������� �����迹�������Ƶ�����, Ҳ��˫�ݿ������, ��ʴ�����ܵ绯ѧ��Ӧ���ơ� ����H+Ũ�ȵ�����, Ĥ���衢 ��ɴ��ݵ����Ĥ���ݾ���С, ��ʴ�ٶȼӿ�, ��ʴ���½���
3) ����ϸ����, ���ںϽ��о����������, ���紦ԭ���������ھ�����ԭ��, ��Ӧ���Խ�ǿ, ���븯ʴ��Ӧ�Ļ���ԭ��������, ��ʴ�ٶȼӿ�, �Ͻ����ʴ���½���
REFERENCES
[1]������, �Ʋ���, �Ŵ���, ��. �����ٺϽ��ĩ���Ʊ��������սἼ��[J]. Ӳ�ʽ���, 2001, 18(4): 225-231.
FAN Jing-lian, HUANG Bai-yun, ZHANG Chuan-sheng, et al. Technology of sintering and preparation of nanometer tungsten based alloy powder[J]. Cemented Carbide, 2001, 18(4): 225-231.
[2]������, ������. ���װ뵼���о���չ[J]. ��ѧ��չ, 1996, 8(3): 231-239.
LI Xin-yong, LI Shu-ben. Research progress in nano-semiconductor materials[J]. Chemical Progress, 1996, 8(3): 231-239.
[3]Lu K. Nanocrystalline metal crystallized from amorphous solid: nanocrystallization, structure and properties[J]. Mater Sci Eng, 1996, 16: 161-163.
[4]Benjamin J S. Dispersion strengthened superalloys by mechanical alloying [J]. Metall Trans, 1970, 1: 2943-2950.
[5]Benjamin J S, Volin T E. The mechanism of mechanical alloying [J]. Metall Trans, 1974, 5: 1929-1933.
[6]Murphy B R, Courtney T H. Synthesis of Cu-NbC nanocomposites by mechanical alloying[J]. NanoStructured Materials, 1994, 4: 365-370.
[7]Abe S, Saji S, Hori S. Mechanical alloying of Al-20 mass % Ti mixed powders[J]. J Japan Inst Metals, 1990, 54: 895-902.
[8]Zdujic E M, Kobayashi K F, Shingu P H. Mechanical alloying of Al-3 at % Mo powders[J]. Z Metallk, 1990, 81: 380-385.
[9]Xu J, Herr U, Klassen T, et al. Formation of supersaturated solid solution in the immiscible Ni-Ag system by mechanical alloying[J]. J Appl Phys, 1996, 79: 3935-3942.
[10]Shigeoki H A, Okabe T, Minamino Y, et al. Consolidation of mechanical alloyed Al-10.7%Ti powder at low temperature and high pressure of 2GPa[J]. Materials Trans JIM, 1995, 36: 465-468.
[11]Hahn H, Logas J, Avverback R S. Sintering characteristics of nanocrystalline TiO2 [J]. J Mater Res, 1990, 5: 609-613.
[12]Haugsrud R, Kofstad P. On the high-temperature oxidation of Cu-rich Cu-Ni alloys[J]. Oxid Met, 1998, 50: 189-213.
[13]Syrett B C, Macdonald D D, Wing S S. Corrosion of copper-nickel alloys in sea water polluted with sulfide and sulfide oxidation products[J]. Corrosion, 1979, 35(4): 409-417.
[14]Milosev I, Metikos-Hukovic M. Passive films on 90Cu-Ni alloy: the mechanism of breakdown in chloride containing solutions[J]. Journal of the Electrochemical Society, 1991, 138(1): 61-65.
[15]�ܳ���. ��ʴ�绯ѧ[M]. ����: ��ѧ��ҵ������, 1990. 94.
CAO Chu-nan. Corrosion Electrochemistry[M]. Beijing: Chemical Industry Press, 1990. 94.
[16]Conway B E, Bockris J O, White R E, et al. Modern Aspects of Electrochemical Impedance Spectroscopy and Its Applications[M]. New York: Kluwer Academic/Plenum Publishers, 1999. 143-145.
������Ŀ: ������Ȼ��ѧ����������Ŀ(50271079); ����ʡ������A����л���������Ŀ(202112022)
�ո�����: 2005-05-23; ������: 2005-09-18
�����: ������(1965-), ��, ����, ��ʿ
ͨѶ����: ������, ����; �绰: 024-86593317; ����: 024-86592548; E-mail: caozhongqiu6508@sina.com


