���±�ţ�1004-0609(2009)03-0595-06
������Լ��Գ�ϸ���۷�ɢ���ܵ�Ӱ��
κ����1����ʢ��1, 2���� ��1��������1��������1
(1. �廪��ѧ ����������Դ�����о�Ժ������ 100084��
2. ���ϴ�ѧ ��ĩұ������ص�ʵ���ң�410082)
ժ Ҫ��
���Կ���Ѫ��Ϊ��ԭ�������������Ϊǰ���塢PVPΪ��������������Լ�Ϊ��ɢ����Һ�ѧ��ԭ��ϵ���Ʊ���ϸ���ۣ��о������ӡ������Ӻͷ����ӱ�����Լ��������Ʊ������еķ��ž����úͷ�ɢ���ã�������ɨ��羵(SEM)��X��������ȶԻ�ԭ���������ò�۲�ͽṹ���������������������Լ���������Ʊ���Ʒ�Ĵ��ȡ���ɢ�ԺͿ�����С������Ҫ��Ӱ�죬���������ӱ�����Լ��������ӱ�����Լ��ķ�ɢЧ�������ԣ������ӱ�����Լ��ķ�ɢЧ����á�������(TW)ϵ�з�ɢ�����о�������TW��Է��������Ĵ�С�����ۿ����ķ�ɢЧ������ò�ʹ�СҲ������Ӱ�죻����TW80��ɢ�����Ʊ����߷�ɢ��խ�����ij�ϸ���ۡ�
�ؼ��ʣ�
��ϸ������������Լ������ž�����ɢ��
��ͼ����ţ�TG 146.32; TB383; TF 832 ���ױ�ʶ�룺 A
Effects of surfactants on dispersive performance of ultrafine silver powder
WEI Li-li1, XU Sheng-ming1, 2, XU Gang1, CHEN Song-zhe1, LI Lin-yan1
(1. Institute of Nuclear and New Energy Technology, Tsinghua University, Beijing 100084, China;
2. State Key Laboratory of Powder Metallurgy, Central South University, Changsha 410083, China)
Abstract: The preparation of ultrafine silver powder was investigated by reducing Ag(NH3)2+ with ascorbic acid in the presence of poly-(vinylpyrrolidone) (PVP) as protective agent and surfactants as dispersant. The effects of cation, anion, and non-ion surfactants on aggregation-proof and dispersion of silver particles in the preparing silver powder were investigated, and the pattern and phase of reducing products were also characterized by scanning electron microscopy (SEM) and X-ray diffractometry (XRD). The results show that the surfactant species impact apparently on the purity, dispersion degree and particle size of the reducing sample. The non-ion surfactants can improve the dissemination of ultrafine silver particles, but both the dispersive effects of cation and anion surfactants are unapparent. Moreover, the results of reducing experiments with a series of TW surfactants show that the relative molecular mass of TW affects the dissemination, pattern and size of silver particles, and the well-dispersed ultrafine silver powder with narrow size distribution can be prepared in the presence of TW 80 surfactant.
Key words: ultrafine silver powder; surfactant; aggregation-proof; dispersion
��ϸ���۳�������ͨ�����ڵ硢�ȡ��ŵȷ�������������⣬������һ�㳬ϸ��������ʣ�����������С���ȱ��������ʣ���ɶࡢ����������λ�ȱ��ܸߵȡ�Ȼ������Щ��ϸ���ӵ�����ʹ������ϸ����������ѧ���������ڲ��ȶ�״̬�����³�ϸ���Ӽ���Է�����������ۣ����ž����������ӵ��Ʊ���������ÿһ�����������ж�������������ϸ�������ž�����ʽ����ʱ�������������������������ܱ�����Ӱ���˷���ļӹ����ܣ����һ������ص�Ӱ���Ʒ�����ܡ���ˣ����Ƴ�ϸ������ž�������߳�ϸ�����ķ�ɢ�Ƚ�����߳�ϸ�������ܵ�һ����Ч;������Ȼ��ϸ���۾��ж��صĵ�ѧ����ѧ��ѧ����[1]������θ������ɢ�ԡ��������ž���������Ŀǰ��δ��������⡣
�����ϵ���ʽ�ɽ��ž������Ϊ���žۺ�Ӳ�žۡ������»����������ϵļ���������ž۳�Ϊ���žۣ������žۿ��û�е������ɢ��������������������Ȼ�ѧ�ϵļ���������žۣ���ΪӲ�žۣ���Ӳ�ž��������û�е������ɢ�������Ʊ�������Ҫ�������ٻ��߱���Ӳ�ž۵ķ�������ϸ������ž���Ҫ�������Ӽ�������������ģ���Ҫ�����ž۾�Ҫ�������Ӽ���ų��������Ʊ���ϵ�еı�����Լ��ܹ������ڿ����ı��棬ͨ�������ų���߽����ռ�λ�������ṩ�ų������������Լ������������ɵĿ�������䵱����Ĥʹ��������룬���������͵ı�����Լ�ʹ����������ͬ�ĵ�ɣ������ų⣬�������ž�����ķ����Ӷ���ɢ���ã����ְ����������ƿ����������������ƿ����ijߴ����ò�����⣬��ӦҺ�е��ž����ڻ�е���������»����������ͨ�����������������ö����ϵ��죬������Լ����ӻ����Զ������뵽����/�����ڷ����ʹ�ѷ������ϣ�����ͨ�������Ӵ��ѷ��ʹ�ž�����ѳ���顣��˱�����Լ����ڳ�ϸ������Ʊ������г䵱���������߷�ɢ�����Ʊ���ɢ���ӻ��ɢ�Ѻϳɵ��ž۵ij�ϸ����[2?3]����Һ������У������о��߾ͱ�����Լ��Գ�ϸ�����Ʊ����̵�Ӱ����й��о�����ʹ�þ�����ϩ��[4]���л�����[5]�;۱���ϩ(PS)[6]��DBS[7]��Daxad 19[8]�ȱ�����Լ�����ɢ�������Ʊ�������ϸС����ɢ���ȵ����ۡ�
�������������PVPΪ���������ֱ��о������ӡ������Ӻͷ����ӱ�����Լ��ȹ�8�ֱ�����Լ��ڸ���ϵ�ж�Һ�ѧ��ԭ���Ʊ���ϸ���۹��̵�Ӱ�졣
1 ʵ��
��Ҫ�Լ����£�����������ˮ������ϩ������ͪ(PVP)������Ѫ�ᣬ�����Ʊ��и��ֳ��õı�����Լ����������ӱ�����Լ���ʮ����������廯�(CTAB)�;۱�ϩ����(PAM)�������ӱ�����Լ�����-(2-�һ��ѻ�)�ǻ���������(AOT)��ʮ�����������(SDS)�������ӱ�����Լ������Ҷ���(PEG)������ͨX-100 (Trion X-100)�����Ҵ���(TEA)������(TW)��
��Ҫ�������£��������Ļ�����ո����䣬���������ǣ�XRD �����ǣ�ɨ�����������
��������Ͳ��ȡ50 mL��0.02 mol/L��������Һ�������Ӱ�ˮ�Ƴ�������Һ���ٳ�ȡ0.17 g PVP���ڸ�������Һ�У��������һ�ձ��н�0.35 g����Ѫ������25 mLˮ����ɿ���Ѫ����Һ�����ڸ���Һ�м��������Լ�������ڳ����½����Ʊ���������Һ��εμӵ��ô�������Ŀ���Ѫ��ͱ�����Լ�����Һ�С�����ԭ��Ӧ����������»�3 h������Һ�������Ĺܽ��и������ķ��룬��������������¶�Ϊ40 �����ո������и�����ɫ��ĩ��Ϊ��ϸ���ۡ�
��ĩ��Ʒ�����������Rigaku D/Max?2000 ��X���߶ྦྷ��ĩ����������ɣ�����ͭ��(Cu K��)�����䲨������=1.541 8 ?����ѹ40 kV������100 mA��ɨ���ٶ�8 (?)/min��
��ĩ��Ʒ��XRD�� powderX ����У������Lorentz���������ð������۳�������İ���(0.107��)���õ��������ھ�������������Ŀ���ֵB������Scherer��ʽ���ƽ���������ȡ�Scherer��ʽΪD=k��/(��cos��)������ DΪ�ش�ֱ��{hkl}���淽���ƽ�������ߴ磻kΪScherer����(ͨ��ȡ0.9)����Ϊʵ����õ�X���߹Ⲩ������Ϊ��ѡ����{hkl}��������IJ�����Ƕȡ�
��Ʒ��SEM������Amary 1910FE�ͳ�����ɨ�������������ɣ��乤����ѹΪ10~15 kV����Ʒ��ϸ������ɢ���Ҵ����Ƴ�����Һ���Ѹ�����Һ���ڵ�����Ƭ�ϣ���ɨ��羵�¹۲���Ʒ�Ķ���������ò��
2 ���������
�������������Ϊǰ���塢����Ѫ����Ϊ��ԭ���Ʊ���ϸ���۵ķ�Ӧԭ��Ϊ
![]()
�������������Ϊǰ���壬����Ч�ؿ�����Һ�������ӵ��ͷ��ٶȣ����������ˮ���¡���ȩ��˫��ˮ�ȶ��Ի�ԭǿ�Ƚ�Ϊ�º͵Ŀ���Ѫ��Ϊ��ԭ�����������ڿ��Ʒ�Ӧ��ϵ�Ļ�ԭ��Ӧ�ٶȡ�
���⣬Ϊ�����������ӵ��ž۲��ȶ������������ӣ������ڷ�Ӧ��ϵ�м���һ��ˮ���Ը߷��Ӿۺ���PVP��Ϊ����������ΪPVP�����ں��м��Ե����� �����ͷǼ��Ե��Ǽ���PVP ����ӿ�ͨ����ԭ�Ӻ���ԭ���������ӱ����ԭ����λ���γɽϽ��ܵ������㣻����C��H �����������ܣ��γ��������ϣ���ֹ��Χ������������֮����žۡ�����ϵ�������ӵ�������������������3����ɣ�1) �����Ӻ�PVP���ã�2) �����ӱ���ԭΪ��ԭ�Ӳ��ҽ��������ԭ�������γ�����������ӣ��౻����Ϊһ�ο�����3) һ�ο�����PVP���û����븽����һ�ο��������γɶ��ο������ɴ˿ɼ���PVP�������������ӵĽ�һ���žۺ��ȶ���Һ�е������ӵ����á�
2.2.1 XRD����
X���������Dz����ܲⶨ����Ľṹ�����ҿɶ����Ƶ���Ʒ�Ĵ��Ƚ��г����жϡ���Ʒ��XRD����ͼ1 ��ʾ������ͼ1���Եõ���Ʒ��2��ֵ���ڱ�1��
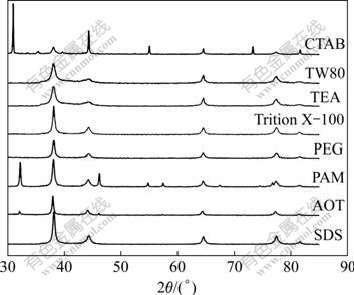
ͼ1 ���ò�ͬ������Լ�ʱ������Ʒ��XRD��
Fig.1 XRD patterns of samples prepared by different surfactants
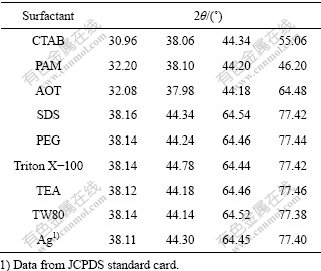
��1 ʹ�ò�ͬ������Լ�ʱ���Ƶ���Ʒ��2��ֵ��JCPDS ����Ƭ��Ag��2��ֵ
Table 1 2�� of Ag on JCPDS standard card and samples prepared by different surfactants
��ͼ1�ͱ�1���Կ���������CTAB��PAM��AOT��3�ֱ�����Լ��Ƶõ���Ʒ��2����������Ƭ�ϵ�2����ȣ����ӷ���֣�����������������Լ��Ƶõ���Ʒ��2����������Ƭ�ϵ�2�ȱ���һ�£����ӷ���֡����������CTAB��PAM��AOT��3�ֱ�����Լ��Ƶõ���Ʒ���Ǵ����ۣ�����������������Լ��Ƶõ���Ʒ�Ǵ����ۣ����������������ṹ�����۲쵽��5��������λ�÷ֱ������������ṹ�����۵�(111)��(200)��(220)��(311)��(222)��5���������Ӧ��
���������ӱ�����Լ�CTAB��PAM�������ӱ�����Լ�AOTʱ����Ʒ�о����������ࣻ�����÷����ӱ�����Լ�ʱ���Ƶô����ۡ���Ȼ���������Ʊ������У������ӱ�����Լ��ķ�ɢЧ�����������Ӻͷ����ӱ�����Լ��ġ����ñ�����Լ���Ŀ������ʹ��ӦҺ��һ��ɢ��ϵ�ȶ����Լ����ž۵ķ�������һ��ͨ���������ַ�ʽ���ﵽԤ�ڵ�Ч����һ�������Լ������ṩ����һ�������������֮�����������⣬������һ���ֿ��ž۵����������ٿ���֮����������������ų������Խ��Ϳ������ž��������ַ�ʽ���Բ��������ӱ�����Լ���ʵ�֣���һ�������Լ������ṩһ���ռ���ݣ��Ӷ������ž۵ķ���������Բ��÷����ӱ�����Լ���ʵ��[9?10]������CTAB�������ӱ�����Լ��д���±���ӣ��ʺ������γ�±�����������������۲�������ȻҲ�����������ӱ�����Լ��������ֱ�����Լ���������Ϊ��ɢ��������һ�㻹��Ϊ��ԭ��[11?14]��
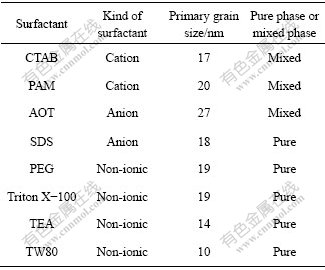
ͼ1��ʾ�ļ���������������������Ʒ�Ľᾧ�������ã���5�������������(111)����������Ϊ������˸���Scherrer ��ʽ��������ڴ�������ijߴ磬�������2���С��ɱ�2���Կ���������TW80����ɢ��ʱ������Ʒ��һ�ο�����С������TEA����ɢ��ʱ������Ʒ��һ�ο�����֮���������������Ȼ���ڱ���ԭ��ϵ������80��TEA��һ�ο����Ĵ�СӰ��ܴ��ܹ��Ϻõķ�ɢ���á�
��2 ������Լ���������Ƶõ���Ʒ��һ�ο�����ƽ��������С
Table 2 Kinds of surfactants and primary grain sizes
ͼ2��ʾ�ֱ�ΪSDS��PEG��Triton X?100��TEA��������Լ�ʱ�Ʊ�������Ʒ��SEM����ͼ2��֪����Ȼ���Ʊ������۾�Ϊ��״��������СҲ�������ɢЧ��ȴ������ͬ����������TEA�Ʊ������۷�ɢЧ����ã���Triton X?100��PEG�Ʊ��Ĵ�֮������SDS�Ʊ�����Խϲ��֮�����ڸ���ϵ�����½��г�ϸ���۵��Ʊ���������ӱ�����Լ��ķ�ɢ�����������������Ӻ������ӱ�����Լ���

ͼ2 ������Լ�ΪSDS��PEG��TritonX?100��TEAʱ�Ʊ�����Ʒ��SEM��
Fig.2 SEM images of as-prepared samples prepared by different surfactants: (a) SDS; (b) PEG; (c) TritonX?100; (d) TEA
���������ӱ�����Լ�����ɢ��ʱ��������������������ͬ��������ų���谭�˱�����Լ������������������õ������ӱ�����Լ������뻹ԭ��Ӧ��ϵʱ�������������Ӻ������������ӷ�Ӧ�����������ʣ��Ӷ��������ࡣ
���������ӱ�����Լ�����ɢ��ʱ�����������ӱ�����Լ�ͨ�������и���ɣ��������ӱ�����ʱ����ͨ�����������������ӽ�ϣ�Ȼ���ڻ�ԭ�����������ٰ������ӻ�ԭΪ�����ˡ������о����õ������ӱ�����Լ����������ǡ������ϵ���෴�������л�ѧ��ԭ��Ӧʱ�������������ϵ���涯��λ�½�ֱ���кͣ����������Ͷ������涨�����У���ϵ�����ھ۳������������γɵڶ��������Լ��ṹ����ˮ����ָ��ˮ��Һ��ʹ�����ɸı���ţ�ʹ��ɢ��ϵ�����ȶ������˹������������Լ����࣬��ɢЧ���
���ڷ����ӱ�����Լ�����������ˮ�в������Һ��н϶����ˮ����һ������ˮ������������������Լ���ȣ������ӱ�����Լ����ȶ��Ժ�ˮ���ԽϺã���������ϵ�ڵ���ʺ�����Ե�Ӱ�졣���⣬�����ӱ�����Լ������������֮�佨������������ã��Ƚ����������ڿ������棬���������ṩ���������ռ�λ������ã��Ӷ���ɢ����[15]��
�����������Լ���һ�ֳ��õķ����ӱ�����Լ���Ҳ��һ�ָ߷��Ӿۺ��ʵ���о��˲�ͬ��Է������������¶Գ�ϸ�����Ʊ����̵�Ӱ�졣ͼ3��ʾΪ�ڻ�ѧ��ԭ��ϵ�м����������TW40��TW65��TW80ʱ��XRD�ס�
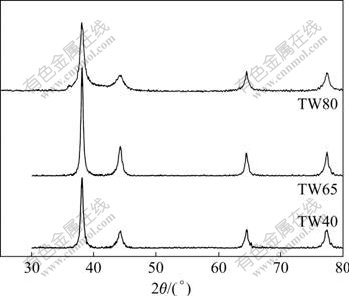
ͼ3 ���ò�ͬTW������Լ�ʱ�Ƶõ���Ʒ��XRD��
Fig.3 XRD patterns of samples prepared by different TW surfactants
��ͼ3��֪������4�ֲ�ͬ��Է������������·�ɢ��ʱ���ɻ�����������ṹ�Ĵ����ۣ���ͼ3�е����ݺ�Scherer��ʽ��������֪����һ�ο����Ĵ�С�ֱ�Ϊ19��22��10 nm����������Ʒ��SEM����ͼ4~6��ʾ����ͼ4~6���Կ��������ò�ͬ��Է���������������Ϊ������Լ�ʱ�����Ʊ������۾����нϺõķ�ɢ�ԣ����Բ���TW80�Ʊ�����ƷΪ���š���ˣ������ڶ�һ�ο����Ŀ��Ʒ��棬�����ڶԶ��ο����Ŀ��Ʒ��棬TW80������������Է���������С�ı�����Լ���������ͼ4(b)��ʾ��TW80��Ϊ������Լ�ʱ���Ʊ����������ȷֲ���խ������������140~160 nm�Ŀ���������ࡣ����������ڲ�ͬ�����ı�����Լ��ڹ�����������̶Ȳ�ͬ�������IJ��졣һ����ԣ����������ڱ���������ʹ����ҺŨ�Ƚϵ�ʱ��Ҳ�нϸߵ���������
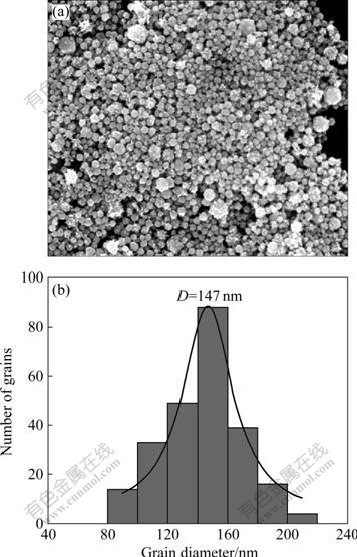
ͼ4 ������Լ�ΪTW80ʱ�Ƶõ���Ʒ��SEM�������ȷֲ�ͼ
Fig.4 SEM image (a) and size distribution histogram (b) of as-prepared sample prepared by TW80 surfactant

ͼ5 ������Լ�ΪTW65ʱ�Ƶõ���Ʒ��SEM��
Fig.5 SEM image of as-prepared sample prepared by TW40 surfactant

ͼ6 ������Լ�ΪTW40ʱ�Ƶõ���Ʒ��SEM��
Fig.6 SEM image of as-prepared sample prepared by TW40 surfactant
3 ����
1) ����PVPΪ�����������������Ϊǰ���塢����Ѫ��Ϊ��ԭ������Һ��ϵ�м�����ʵı�����Լ�ʱ���ܹ���Ч�ظ��Ƴ�ϸ���۵ķ�ɢ���ܡ��������Ӽ���ž�����
2) �����ӱ�����Լ��������ӱ�����Լ��Ŀ��ž�Ч���������ԣ��������ӱ�����Լ��Ŀ��ž�Ч���Ϻá�
3) �ڼ��ַ������Ա�����Լ��У�����ϵ�б�����Լ��ķ�ɢЧ��ȴ������Է��������IJ�ͬ���������죬��������Է��������ϴ��TW80�ķ�ɢЧ����á�
[1] �趦��. ���������[M]. ��ɳ: ���Ϲ�ҵ��ѧ������, 1991.
LI Ding-xin. Noble metal materials[M]. Changsha: Central South University of Technology Press, 1991.
[2] �� ��, �����, ۭӢ��. ������Լ����������Ʊ��е�Ӧ��[J]. �������Ͳ���, 2003, 31(7): 37?40.
LIU Jian, CAO Rui-jun, XI Ying-xin. Application of surfactants in preparation of nano-particles[J]. New Chemical Materials, 2003, 31(7): 37?40.
[3] �� ܿ, ������. ������Լ������ײ����о��е�Ӧ��(��)[J]. Ƥ���ѧ�빤��, 2004, 14(3): 33?38.
CHU Yun, MA Jian-zhong. Application of surfactants in nano-scale materials[J]. Leather Science and Engineering, 2004, 14(3): 33?38.
[4] ������, �� ��, �Ƹ�־, ������. ������ϩ�������Լ���ϵ�����������ĺϳ�[J]. ������ѧѧ��, 2001, 17(6): 537?541.
ZHANG Qing-min, LI Yan, HUANG Fu-zhi, GU Zhen-nan. Synthesis of silver nanoparticles in nonionic surfactant system[J]. Acta Physico-Chimica Sinica, 2001, 17(6): 537?541.
[5] TAN Yi-wei, LI Yong-fang, ZHU Dao-ben. Preparation of silver nanocrystals in the presence of aniline[J]. Journal of Colloid and Interface Science, 2003, 258: 244?251.
[6] WU Da-zhen, GE Xue-wu, HUANG Yu-hong, ZHANG Zhi-cheng, YE Qiang. ��-radiation synthesis of silver- polystyrene and cadmium sulfide-polystyrene nanocomposite microspheres [J]. Materials Letters, 2003, 57: 3549?3553.
[7] NERSISYAN H H, LEE J H, SON H T, WON C W, MAENG D Y. A new and effective chemical reduction method for preparation of nanosized silver powder and colloid dispersion[J]. Materials Research Bulletin, 2003, 38: 949?956.
[8] SONDI I, GOIA D V, MATIJEVI E. Preparation of highly concentrated stable dispersions of uniform silver nanoparticles[J]. Journal of Colloid and Interface Science, 2003, 260: 75?81.
[9] ������, �� ܿ, �ߵ���. ������Լ������ײ��������е�Ӧ��[J]. ���û�ѧ��ҵ, 2004, 34(6): 374?376.
MA Jian-zhong, CHU Yun, GAO Dang-ge. Application of surfactants in nano-scale materials[J]. China Surfactant Detergent & Cosmetics, 2004, 34(6): 374?376.
[10] �� ��, ��ѧ��. ������Լ��ڲ��Ϲ����е�Ӧ��[J]. ���Ͽ�ѧ�빤��, 1998, 16(4): 58?60.
CAO Jian, CAO Xue-feng. The application of surface active agent In materials technology[J]. Materials Science and Engineering, 1998, 16(4): 58?60.
[11] RANE S B, SETH T, PHATAK G J, AMALNERKAR D P, DAS B K. Influence of surfactants treatment on silver powder and its thick films[J]. Materials Letters, 2003, 57: 3096?3100.
[12] PAL T, SAU T K, JANA N R. Reversible formation and dissolution of silver nanoparticles in aqueous surfactant media[J]. Langmuir, 1997, 13: 1481?1485.
[13] LEE M H, OH S G, SUH K D, KIM D G, SOHN D W. Preparation of silver nanoparticles in hexagonal phase formed by nonionic Triton X?100 surfactant[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2002, 210: 49?60.
[14] LIZ-MARZA?N L M, LADO-TOURIN I. Reduction and stabilization of silver nanoparticles in ethanol by nonionic surfactants[J]. Langmuir, 1996, 12: 3585?3589.
[15] ���澴, ���´�, ���Ϸ�, ��ʤ. ������Լ��ڽ����Ʊ������е�����[J]. �й���ɫ����ѧ��, 1998, 8(2): 560?565.
XU Ke-jing, YANG Xin-chun, XU Yu-fen, KONG Fan-sheng. The effect of surfactants in preparation process of colloid[J]. The Chinese Journal of Nonferrous Metals, 1998, 8(2): 560?565.
������Ŀ��������Ȼ��ѧ����������Ŀ(50274045��50674060)�����ϴ�ѧ��ĩұ������ص�ʵ���ҿ��Ż���������Ŀ(2007)
�ո����ڣ�2008-03-08�������ڣ�2008-09-03
ͨѶ���ߣ���ʢ���������ڣ���ʿ���绰��010-89796082�����棺010-62773585��E-mail: smxu@tsinghua.edu.cn
(�༭ ��ѧ��)


