���±�ţ�1004-0609(2008)05-0884-06
S��������TiO2�Ŀɼ�����Ӧ����
���澴���г��壬�� ��
(ɽ��������ѧ ���Ͽ�ѧ�빤��ѧԺ���Ͳ� 255049)
ժ Ҫ��
������ΪS��Դ���ʣ������ᶡ��ΪTiO2��ǰ���壬�����ܽ�-�������Ʊ�S-TiO2�����������XRD��XPS��FTIR�ȼ�������S���Ӷ�TiO2����ṹ��Ӱ�죬��̽��Ԫ��S��TiO2�����еĻ�ѧ״̬�Լ����γɵĻ�ѧ�������͡�������������ӵ�S��S4+����TiO2������ȡ������Ti4+���γ�Ti1-xSxO2������S4+��TiO2�ļ۴����γ�1������ռ���ܼ����۴��ϵĵ���ռ���ܼ��ļ۴���λ��Ҫ��S3p̬���ɣ�ͬʱS3pҲ�������γ�1����Ti3d��O2p̬���ɵĵ�����S3p̬��۴��Ľ���ʹ�۴�����������ܴ���խ���Ӷ�����TiO2�Ĺ�����Ӧ��ʹ���ձ�Ե��չ���ɼ���������Ǽ����Ĺ⽵��ʵ����֤ʵ�������������˹�����ԡ�
�ؼ��ʣ�
S-TiO2����������ӻ�������ѧ״̬���ɼ��������ջ�����
��ͼ����ţ�O 643���� ���ױ�ʶ�룺A
Mechanism of sulfur-doping on TiO2
photo-response under visible light
XU Ke-jing, SHANG Chao-feng, LI Fang
(School of Materials Science and Technology, Shandong University of Technology, Zibo 255049, China)
Abstract: S-TiO2 photocatalysts, with thiourea as source substance of S and titanium tetrabutoxide (Ti(OC4H9)4 as precursor of titanium dioxide, were prepared by sol-gel method. The effects of sulfur-doping on TiO2 crystal structure, the chemical states of S atom in TiO2 crystals and the chemical bonds formed in TiO2 were analyzed by XRD, XPS and FTIR. The results show that S atom as the state of S4+ in TiO2 crystal lattices substitutes part of Ti atoms and form Ti1-xSxO2 catalyst, and S4+ forms an electron-occupied level in valence band (VB), and the electron occupies level above the VB consists of S3p states, at the same time, the S3p states contribute to the formation of a conduction band with Ti3d and O2p states, the chiasma of S3p states and the VB make VB broaden and result in energy gap narrow down, and then improve the optical response of TiO2 and extend its absorption edge into the visible-light region.
Key words: S-TiO2 photocatalyst; doping mechanism; chemical state; visible light; absorption activity
����TiO2�������������¾��к�ǿ�Ĺ�����Ժͻ�ѧ�ȶ��ԣ����Կɼ�������ջ��Ժܵͣ�����ͨ�����ӵķ�ʽ����TiO2�Կɼ�������ա���������ڶ��ֽ���Ԫ�صIJ��������о���Ϊ[1-4]������Ԫ�ز��ӵ�TiO2����������߱����ڵ��ȶ��ԣ����ڿ�����Ӧ�÷�Χ�ڲ��߱�����Ч�ĸ��ԣ�������(��)���ʵ�Ӱ��ܴ�[5-6]��Ҳ���о���Ϊ[7-9]�����ӷǽ���Ԫ���ܹ��������TiO2�ɼ������ջ��Բ��ܳ����ȶ�����Ҫ����Ϊλ��Ԫ�����ڱ���Ԫ��O��Χ�ķǽ���Ԫ��C��N��P��F��S�ȿ�����ΪTiO2�IJ���Ԫ�ض�������Կɼ�����Ӧ������C��N��P��FԪ�ش����Ը���Ԫ�ز��ӵ�TiO2�����У�ȡ�����ֵ�OԪ�أ��γ�TiO2-xYx��ʽ�Ĺ��������SԪ���Ƕ��Ԫ��(S2-��S4+��S6+)�����ò�ͬ�IJ����ֶΣ�S��TiO2�����л�ѧ״̬Ҳ��ͬ�����ӻ���Ҳ��ͬ��UMEBAYASHI��[10]����TiS2����ȴ�������þ��пɼ�����Ե�TiO2-xSx�������ZHANG��[11]���û�е��ѧ���ӷ�����˾��пɼ�����Ե�TiO2-xSx�������֤ʵS����S2-��ʽȡ����TiO2�����еIJ���O�γ�Ti��S����G?MEZ��[12-13]��������S����TiO2�����У��γ�S=O��O��S��O�����������ữ��SO4-TiO2��������е���ȱ�ݺ͵���������ص㣬�������TiO2�Ļ��ԣ�OHNO��[14]����ʪ��ѧ����õ�Ti1-xSxO2��ʽ�Ĺ�����Լ�����2-��������ǻ���������ȱ��ֳ���ǿ�Ľ���������
��������������ΪS��Դ���ʣ�����Sol-Gel���Ʊ�S-TiO2���������Ҫ�о�S���Ӷ�TiO2�������ܵ�Ӱ�죬����ʪ��ѧԪ�ط��Ʊ�S-TiO2�IJ��ӻ��ƣ�����ΪS�������TiO2�ɼ�����Ӧ�ṩ���ۻ�����
1 ʵ��
1.1 ����TiO2��S-TiO2��������Ʊ�
�����ᶡ�� (Ti(OC4H9)4) ΪTiO2��ǰ���壬������(NH2CSNH2)ΪS��Դ���ʣ������ܽ�-�������Ʊ���ͬ��S����TiO2��������һ���¶������պͷ�ĥ��õ���ͬ����������S����Ti(OC4H9)4��NH2CSNH2��Ħ���ȼƣ��ֱ�ȡΪ0��1?1��2?1��3?1��4?1�������¶�Ϊ500 �棬�����ٶ�Ϊ40 ��/min ������ʱ��Ϊ3 h��
1.2 UV-Vis������
����Cintra 10�ͷֹ������(�Ĵ�����GBC��)�������������չ��ס�
1.3 X����������
����INCA Energy�� X����������(Ӣ��OX Ford ��)��ΪSirion200��ɨ���������(����FEI��˾��)�ĸ����ɰ붨���ط���������Ԫ�سɷ֡�
1.4 XRD�������
����D8Advance�Ͷྦྷ������(�¹�Btuker��˾��)��Cu�У�����Ϊ2.2 kW��2����20? ~80? ��Χ�ڣ����������ľ��༰�����ߴ硣
1.5 XPS����
����PHI Quantera SXM��X���߹���������Ƿ���S��TiO2�����еĻ�ѧԪ��״̬�����õ��ǵ�ɫ����Al�����У������ֱ���Ϊ0.5 eV��������Ϊ3 mol/L CPS���Ƿֱ���Ϊ45?����������ն�Ϊ6.7��10-8 Pa������������ɨ��Ar+ǹ�����Ϊ1 mm��1 mm����������ԼΪ20 nm/min������Ϊ2.0 kV���������Ϊ20 mA��
1.6 FTIR����
����NicoletCentaurusTM����Ҷ���������(����Thermo��)����FTIRͼ������
1.7 �����Լ�����Һ�Ĺ⽵��ʵ��
����722�ͷֹ��ȼƲⶨ������Ĺ⽵�����ܡ���һ����(50 mmol/L)����������200 mLŨ��Ϊ10 mg/L�ļ�����Һ�У������д�������4 h��ʹ�����ﵽƽ����ٽ��й⽵�ⷴӦ����������300 W��ѹ������15~20 cm�����ڵ�����������ʼ��ʱ��ÿ30 minȡ��1�β���������ȡ���Һ��Ũ�Ⱥ������ct�����ȣ��併���ʿ��Ա�ʾΪ

2 ���������
2.1 ������UV-Vis������
Ϊ����������Ƚ�S�IJ��ӱ���ΪS��TiO2��Ħ����3?1���ս��¶�Ϊ500 �������(��ΪS-TiO2����)��Ϊ�������봿��TiO2�������бȽϡ����ݰ뵼������ܣ���TiO2��S-TiO2����϶(Eg)���Ը������¹�ʽ����[12]

����ʽ(2)����õ�TiO2��EgΪ3.32 eV����S-TiO2��Eg��СΪ3.03 eV��������Ӧ��UV-Vis ����������ͼ1��ʾ����ͼ1��֪��S-TiO2���������ձ�ԵǨ�Ƶ�400 nm����S-TiO2 �ڿɼ����¾������ջ��ԡ�
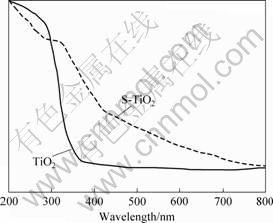
ͼ1 ��TiO2��S-TiO2 ������UV-Vis ����
Fig.1 UV-Vis spectra of TiO2 and S-TiO2 samples
2.2 S-TiO2������EDS����
ͼ2��ʾΪS-TiO2 ������SEMͼ��ͬ�ӳ��ڵ�ij�������ij�����XRD�ס����Կ��������ӳ��������SԪ�ؼ�����C�����S����Ϊ2.70%(ͼ2(a))�������ӳ��������֪��������Ҳ����SԪ�أ��Һ���ҲΪ2.70%(ͼ2(b))�����˵��SԪ�ش�����TiO2�����У��ҷֲ����ȡ�
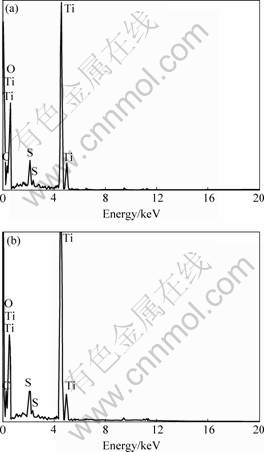
ͼ2 S-TiO2��ĩ��EDS��
Fig.2 EDS patterns of S-TiO2 powders: (a) Selected area; (b) Some point of selected area
����EDS���������֪����������������в���NԪ�أ�ֻ��������CԪ�أ�����ȼ�ղ���ȫ��ɵġ�
����������������Ϊ��S-TiO2 ���пɼ������ջ����Dz���S��Ե�ʡ�
2.3 ����S��TiO2����ѧ����Ӱ��
ͼ3��ʾΪ��ͬS��������TiO2��500 ��ʱ�ĺ�����ף�ͼ4��ʾΪS��TiO2Ħ����Ϊ3?1��TiO2��700 ��ʱ�ĺ�����ס���ͼ3���Կ�����4��S�������ĺ��������3 400~3 455 cm-1������ͬ�����շ壬���ɡ�OH ��������������ģ�һ����������ˮ(���������ˮ) �����ģ�2 854~2 975 cm-1�������շ������Ǽ���CH2�����������������ģ�1 639 cm-1�������շ��ӦH��O��H ����������ṹˮ�йأ�1 350~1 400 cm-1�������շ����Ϊ��CH2��CH3�����С�CH �ĶԳƱ�������ģ�1 079 cm-1�������շ���Ti��O��C ���ŵ�����������870~950 cm-1�������շ�����C��CH2��������450~700 cm-1������ڵķ���[TiO6]������λ�������ģ�˵��TiO2��������Ϊ������Ti��O���������ͱ�������Աȷ��֣�960~1 150 cm-1����3�����Ե����շ壬�ֱ���1 045��1 080��1 127 cm-1����ͼ3���Կ�����1 080 cm-1�������շ徭700 ���ȴ��� ������ʧ����S��O�����Գ����������շ����� ��1 000~1 300 cm-1֮�䣬������Ϊ1 045 cm-1��1 127 cm-1���ķ�ΪS��TiO2�������ϼ�˫��λ�������¡���ͬ��������960~1 300 cm-1���շ�Ҳ����ͬ�����Ų����������� 1 127 cm-1������Խ��Խ���ԣ�˵��S��O�����ࡣ
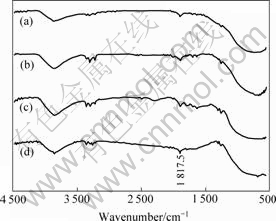
ͼ3 500 ���²�ͬ��S����TiO2�������
Fig.3 FTIR spectra of TiO2 with different amounts of S-doping at 500 ��: (a) 1?3; (b) 1?2; (c) 2?1; (d) 3?1
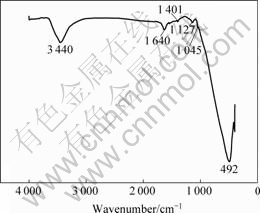
ͼ4 700 ����S��TiĦ����Ϊ3:1ʱTiO2�����ĺ��� ����
Fig.4 FTIR spectra of TiO2 with mole ratio of S to Ti of 3?1 at 700 ��
2.4 S��TiO2 �����еĻ�ѧԪ��״̬����
ͼ5~7��ʾΪS��TiĦ����Ϊ3?1��TiO2��Ʒ����500 ���ȴ���3 h��XPSȫ��ͼ��ͼ�г�����Ti2p1/2��Ti2p3/2��Ti2s��Ti3s��Ti3p��O1s��C1s��S2s��S2p��O2s�壬����C1s����У���ɵ�ЧӦʱ����Ⱦ̼ (������Ⱦ̼C1s��������ڱ�)�Ͳ��ֲ����л������¡�891 eV��741 eV���ķ�ֱ�ΪTi��Oԭ�ӵĶ�Ъ���ӷ壻459.4��465.1��562.5 eV���ķ�ֱ�ΪTi2p1/2��Ti2p3/2(��ͼ6��ʾ)��Ti2s��ΪTi4+�壬������������Ҫ�����ļ۴��ڣ�168 eV������1���Ͽ���S2p�壬��Ҫ�������������̬�����壬167.5 eV��168.2 eV���ķ�ֱ��ӦS4+��S6+���Ը���Ʒ��ȥ����ˮ��ϡ������ϴ���Ρ���ɺ�Ar+��ʴ���Է��֣�����S6+�Ѿ���ϴȥ��ʣ��S4+����������Ϊ2.70%����Ʒ��δ����ǰ������S2-���ڣ�������500 ���ȴ�����S��S4+����TiO2�����С���TiO2����ļ۴��͵�������Ti3d��O2p�����ɣ�Ti3d�������Ϊt2g��eg̬���������ֳ������֣��γɽϵ���ϸ�λ ̬���������TiO2���ڼ۴����γ�1������ռ���ܼ���ͬʱS3pҲ�������γ�1����Ti3d��O2p̬���ɵĵ������۴��ϵĵ���ռ���ܼ��ļ۴���λ��Ҫ��S3p̬���ɣ�S3p̬��۴��Ľ���ʹ�۴������������϶��խ���Ӷ��������ɼ���Ĺ�����Ӧ��
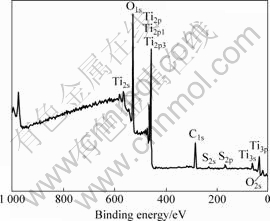
ͼ5 S-TiO2������XPSȫ��
Fig.5 XPS patterns of S-TiO2 sample
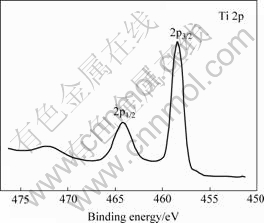
ͼ6 S-TiO2�������ӵ�XPS����
Fig.6 XPS pattern of titanium ion in S-doped TiO2
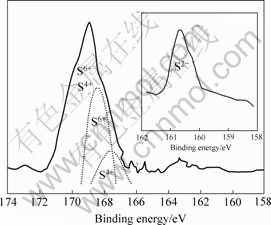
ͼ7 S-TiO2�������ӵ�XPS����
Fig.7 XPS pattern of sulfur ion in S-doped TiO2
Ϊ�˽�һ��ȷ�����������TiO2����ṹ�ı仯����TiO2��S-TiO2��XRD��(ͼ8)�е�(101)�����˷����������ͼ9��ʾ���ɼ��������TiO2��Ʒ�봿TiO2��(101)��������λ�û������䣬�������Կ�������������S4+����TiO2�����е��¾ֲ����䣬ƽ����������û�иı䡣ͨ��������������Ϊ�������ļ�������̬����TiO2����ṹȡ����Ti4+����λ �ã��γ�Ti1-xSxO2�����塣����S4+�뾶(0.037 nm)С��Ti4+�뾶(0.074 nm)����S4+ȡ�� Ti4+����TiO2����ṹ���Σ������������һ���ĸı䡣��TiO2�ľ������Ϊ��a=0.380 4 nm��c=0.953 1 nm����S4+���Ӻ��TiO2��Ʒ��500 ���ȴ�����ľ������Ϊ��a=0.379 6 nm��c=0.947 7 nm���ɴ˿ɼ���S4+���Ӻ�����TiO2���巢���˾ֲ����䣬�Ӷ����²���TiO2������������ܷ����ı䡣
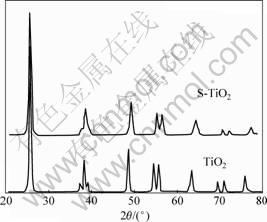
ͼ8 TiO2��S-TiO2��XRD��
Fig.8 XRD patterns of TiO2 and S- TiO2 samples
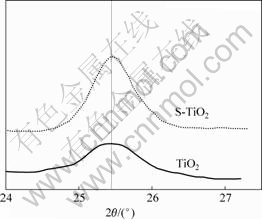
ͼ9 TiO2��S-TiO2��(101)��ķ�λͼ
Fig.9 XRD peaks of TiO2 and S-TiO2 samples
2.5 S��TiĦ���Ȳ�ͬʱTiO2��������Ǽ����Ľ�������
ͼ10��ʾΪS��TiĦ���Ȳ�ͬʱTiO2���� (500 ��/3 h) ���Ǽ����Ľ������ߡ������ԣ��������TiO2���Ǽ������Աȴ�TiO2�ĸߡ���S��Ti��Ħ����Ϊ3ʱ������Ч����ѣ���S��TiĦ����С��3ʱ����������Ǽ����Ľ�����������ӱ��������������S��TiĦ���ȴ���3ʱ��ǰ1.5 h�Ľ������ʱ�δ����TiO2���Դ��Ժ�����Ѹ�ٽ��͡�����������ڹ�������︲����TiO2���棬Ӱ�����������ܡ�
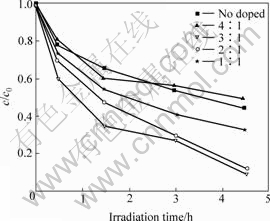
ͼ10 ��ͬS��TiĦ���ȵ�TiO2�������Ǽ����Ľ�������
Fig.10 Degradation curves of TiO2 with different S/Ti mol ratios
��֮������������ӿ����������TiO2�Ĺ�����ԡ�
3 ����
1) �����ܽ�-�����������Ʊ�S-TiO2������������IJ���S����ʹTiO2�����ձ�Ե�ƶ���400 nm���������TiO2�ڿɼ�������ջ��ԡ�
2) �������֤����S��TiO2�������γ���S��O��������������S���ӷ�Χ�ڣ����Ų�S������ ����TiO2�е�S��O�����ࡣ������������֤����S��S4+����TiO2����ṹ��ȡ������Ti4+����λ�ã����¾ֲ����䣬�ڼ۴����γ�1������ռ���ܼ���ͬʱ��S3pҲ�������γ�1����Ti3d��O2p̬���ɵĵ�����
3) �۴��ϵĵ���ռ���ܼ��ļ۴���λ��Ҫ��S3p̬���ɣ�S3p̬��۴�����ʹ�۴�����������ܴ���խ���Ӷ�����˿ɼ���Ĺ�����Ӧ�����Ǽ����Ĺ⽵��ʵ��֤ʵ������ӿ�������߹�����ԡ�
REFERENCES
[1] CHOI W K, TERMIN A, HOFFMANN M R. The role of metallic dopants in quantum-sized TiO2: correlation between photoreactivity charge carrier recombination dynamics[J]. J Phys Chem, 1997, 98: 13669-13679.
[2] PING Yang, CHEN Lu, NAN Ping-hua, YU Kou-du. Titanium dioxide nanoparticles co-doped with Fe3+ and Eu3+ ions for photocatalysis[J]. Materials Letters, 2002, 57: 794-801.
[3] �¿���, ���¾�, �� Ө, ������, ������. ϡ��Ԫ�ز��Ӷ�TiO2��Ĥ������ܵ�Ӱ��[J]. �й�ϡ��ѧ��, 2003, 21: 67-71.
CHEN Jun-tao, LI Xin-jun, YANG Ying, WANG Liang-yan, HE Ming-guang. Effect of RE doping for photocatalytic properties of TiO2 thin films[J]. Journal of the Chinese Rare Earth Society, 2003, 21: 67-71.
[4] RUPPERT A M, PARYJCZAK T. Pt/ZrO2/TiO2 catalysts for selective hydrogenation of crotonaldehyde: Tuning the SMSI effect for optimum performance[J]. Applied Catalysis A, 2007, 320: 80-90.
[5] ANPO M, TAKEUCHI M. The design and development of highly reactive titanium oxide photocatalysts operating under visible light irradiation[J]. Journal of Catalysis, 2003, 216: 505-516.
[6] OHNO T, AKIYOSHI M, UMEBAYASHI T, et al. Preparation of S-doped TiO2 photocatalyst and their photocatalytic activities under visible light[J]. Applied Catalysis A: General, 2004, 265(1): 115-121.
[7] MORIKAWA T, ASAHI R, AOKJ K, et al. Band-gap narrowing of titanium dioxide by nitrogen doping[J]. Japanese Journal of Applied Physics, Part: Letters, 2001, 40(6): 561-563.
[8] CHOI W Y, TERMIN A, HOFFMANN M R. The role of metal-ion dopants in quantum-sized TiO2: correlation between photoreactivity and charge-carrier recombination dynamics[J]. J Electroem Soc, 1994, 98: 13669-13679.
[9] ASAHI R, MORKAWA T, OHWAKI T, et al. Visible-light photocatalysis in nitrogen-doped titanium oxides[J]. Science, 2001, 293(13): 269-271.
[10] UMEBAYASHI T, YAMAKI T, YAMAMOTO S, MIYASHITA A, TANAICA S, SUMITA T, ASAI K. Journal of Applied Physics, 2003, 93(9): 5156-5160.
[11] ZHANG Qi-wu, WANG Jun, YIN Shu, SATO T, SAITO F. J Am Ceram Soc, 2004, 87(6): 1161-1163.
[12] G?MEZ R, L?PEZ T, ORTIZ-ISLAS E, NAVARRETE J, S?NCHEZ E, TZOMPANZTZI F, BOKHIMI X. Effect of sulfation on the photoactivity of TiO2 sol-gel derived catalysts[J]. Journal of Molecular Catalysis A: Chemical, 2003, 193: 217-226.
[13] MIAO L, TANEMURA S, TOH S, WATANABF H, TOH S, KANEKO K. Structural and compositional characterization of N2-H2 plasma surfae-treated TiO thin films[J]. Applied Surface Science, 2005, 244: 421-417.
[14] OHNO T, AKIYOSH I M, UMEBAYASHI T, ASAI K, MITSUI T, MATSUMURU M. Preparation of S-doped TiO2 phtocatalysts and their phtocatalytic activities under visible light[J]. Applied Catalysis A: General, 2004, 265: 115-121.
[15] ������, ����ҫ, ���´�, �� ��, ����ϼ, ���, ���沨. B/Fe2O3����������TiO2�ɼ����µĴ�����[J]. �й���ɫ����ѧ��, 2006, 16(12): 2098-2103.
LI Li-qing, LIU Zong-yao, TANG Xin-cun, TANG Lin, GUO San-xia, LI Hai-long, HE Yi-bo. Photocatalytic activity of nano-TiO2 codoped with boron and B/Fe2O3 in visible region[J]. The Chinese Journal of Nonferrous Metals, 2006, 16(12): 2098-2103.
������Ŀ�����Ҹ����о���չ�ƻ�������Ŀ(2001AA333040)
�ո����ڣ�2007-08-31�������ڣ�2007-12-25
ͨѶ���ߣ����澴�����ڣ��绰��0533-2782232-1��E-mail: xukj@sdut.edu.cn
ժ Ҫ��������ΪS��Դ���ʣ������ᶡ��ΪTiO2��ǰ���壬�����ܽ�-�������Ʊ�S-TiO2�����������XRD��XPS��FTIR�ȼ�������S���Ӷ�TiO2����ṹ��Ӱ�죬��̽��Ԫ��S��TiO2�����еĻ�ѧ״̬�Լ����γɵĻ�ѧ�������͡�������������ӵ�S��S4+����TiO2������ȡ������Ti4+���γ�Ti1-xSxO2������S4+��TiO2�ļ۴����γ�1������ռ���ܼ����۴��ϵĵ���ռ���ܼ��ļ۴���λ��Ҫ��S3p̬���ɣ�ͬʱS3pҲ�������γ�1����Ti3d��O2p̬���ɵĵ�����S3p̬��۴��Ľ���ʹ�۴�����������ܴ���խ���Ӷ�����TiO2�Ĺ�����Ӧ��ʹ���ձ�Ե��չ���ɼ���������Ǽ����Ĺ⽵��ʵ����֤ʵ�������������˹�����ԡ�


