���±�ţ�1004-0609(2013)10-2942-07
��������ʽ¯����¯������ұ�����̵�ͬʱƽ��
�� ��1��������1��̷ ��1���� ��1������Ԫ1���� ��2���� ��2����ƽ��1
(1. ���ϴ�ѧ ��ѧ����ѧԺ ��ɫ������Դ��ѧ�������ص�ʵ���ң���ɳ 410083��
2. ����ұ�����Źɷ�����˾������ 412000)
ժ Ҫ��
������Ǧ��������¯������ұ�����̵Ķ���ͬʱƽ��ԭ��������ƽ��Ħ���������������������¶ȡ���ʼ�����ͳ�ʼ��Ǧ����ƽ��������̬��������Ӱ�졣����������ڽϸ��¶��£���ʼ���������ӻ�ʹ����Ǧ�IJ������ӣ�����Ǧ�IJ������ͣ������������²���������Ǧ��������Ǧ�����Dz���ĺ���̼��ԭ��������ұ��������Ӧѡ����������������������״���������Ǧ�������ǽ��Ѵ�������Ǧ��
�ؼ��ʣ�
��������¯��ͬʱƽ����Ǧ������������Ǧ��
��ͼ����ţ�TF812 �� �� ���ױ�־�룺A
Simultaneous equilibrium about smelting process in functional area of Kivcet flash furnace
WAN Zi1, LIU Chang-qing1, TAN Jun1, LI Jie1, CHEN Qi-yuan1, WANG Hui2,
LIAO Zhou2, ZHANG Ping-min1
(1. Key Laboratory of Resources Chemistry of Nonferrous Metals, Ministry of Education,
School of Chemistry and Chemical Engineering, Central South University, Changsha 410083, China;
2. Zhuzhou Smelter Group Co., Ltd., Zhuzhou 412000, China)
Abstract: Based on the multiphase simultaneous equilibrium principle of lead sulfide minerals smelting process in the functional area of flash furnace, Moore balance method was used to investigate the effect of smelting temperature, initial oxygen content and initial lead sulfide content on the output of each condensed matter after reaching equilibrium. The results show that, under high temperature condition, the output of lead sulfate increases, while with the increase of initial of oxygen content, the output of lead sulfide decreases. In addition, lower oxygen input cann��t result in the generation of lead sulfate, but lead sulfide will emerge. Considering the subsequent treatment of the products, it is suggested that higher oxygen input should be chosen during the smelting process, in order to generate the tractable lead sulfate rather than unmanageable lead sulfide.
Key words: Kivcet furnace; simultaneous equilibrium; lead flash smelting; galena
Ŀǰ�����ڵ�Ǧұ�����հ�����ͳ��Ǧ���պ��۳������¹��ա���ͳǦұ������ʹ���ս�������乤�ռ��豸�����ƣ��ײ�����Ũ�ȵ�SO2�������ѶȴԻ�������Ⱦ�ϴ�[1-2]���۳������¹����ǽ������ҹ����ƹ�����������Ǧ��������������������ֱ����Ǧ����QSL��Ǧ��������������û����������������Ǧ���������״�-�ķ�¯��ԭ��Ǧ����[3-5]�����У���������ֱ����Ǧ���ķ�Ӧ����(�������̺ͻ�ԭ����)��Ҫ���ڻ�������¯�ķ�Ӧ������¯���������У������к������ŷ����͡����������ȶ����豸��������������С��SO2Ũ�ȸߡ����������ʸߡ����������ʸߡ��ܺĵ͡��ҵ�Ǧ��п�����״���������[6]��
�����ڻ�������¯ֱ����Ǧ��������ѧ����ƽ���о����Ľ��٣�Ϊ�ˣ�����������ͬʱƽ��ԭ����������Ǧ���ڻ�������ʽ¯�����������Ķ���ƽ����ѧģ�ͣ�����ƽ��Ħ�������о������¶ȡ���ʼ��������ʼ��Ǧ����ƽ����ɵ�Ӱ�죬Ϊ�ü����ķ�չ��Ӧ���ṩ�������ݡ�
1 ����¯������ұ�����̵Ļ�����Ӧ
CHANDHURI ��[7]�о�����Ǧ�����ڷ�Ӧ���ڵķ�Ӧ���������������ڸ��¡�����ǿ�����������µ�����¯�������ڣ���Ǧ�����������������Ӧ���ٶȷdz��죬�������ܶ���ѧ���ơ�SANNIKOV��[8]����Kivcet��Ӧ���ڷ�Ӧʱ�䡢�¶ȼ�����ɷֵı仯��Ҳ�õ������ƵĽ��ۣ��ɴˣ�Ǧ�����������̿���Ϊ�ﵽ������ﵽƽ��״̬���Ӷ����ԶԻ�������ʽ¯������¯��������ұ�����̽���ͬʱƽ���о�������¯�������ڵĻ�ѧ��Ӧ�϶࣬�������ɿ�֪��������Pb-O-S 3��Ԫ�������ɵķ�Ӧ��ϵ��ֻ��5����ӦΪ�����ģ�����Ǧұ�����̵Ļ���������Ӧ��ѡ[9]��
2PbS(s or l)=2Pb(l)+S2(g) (a)
S2(g)+2O2(g)=2SO2(g) (b)
2Pb(l)+O2(g)=2PbO(s or l) (c)
2SO2(g)+O2(g)=2SO3(g) (d)
PbO(s or l)+SO3(g)=PbSO4(s) (e)
2 ����¯�����������ɷ���
��������¯��������Ǧ-��-����ϵ���������ɹ�ʽ(f =C-��+2)��֪������ϵ������������棬��Ǧ-��-����ϵ���������������ޱ���״̬[10]����Ǧ-��-����ϵΪ�����ʱ������ϵΪ������״̬���ڻ�������ʽ¯�ڵ�����¯�������������������У���ȼ�Ϲ���̼�⣬���������ֻ��������棬��һ���������һ�����ࣻ�����ܴﵽ��Ҳ���ᳬ����4������(Һ���)���[11]�������ɷ�����֪����Ǧ-��-����ϵ���¶ȸ���������ƽ���¶�ʱ������¯�������ڿ��ܳ��ֵ���������Ƕ����ġ��е���Ӧ��ֱ����Ǧ���̣��е���Ӧ����Ǧ������������̣��е���Ӧ����Ǧ��ﳹ��̡�
����Ǧ-��-����ϵΪ���ࡢ���������棬���¶�ȷ����5��������Ӧ�ı�ƽ�ⳣ������ȷ��������Ǧ-��-����ϵ�ﵽ��Ԫ���෴Ӧƽ��ʱ������̬���ʵ�ƽ���ѹҲ����ȷ������ˣ�����ʼPbS������Ϊȷ��ֵʱ���ڲ�ͬ��ʼO2����������ĸ�������̬����IJ�������ͨ��ͬʱƽ���о��ļ�����á�
3 ͬʱƽ�������ѧ����ԭ��
ͬʱƽ����о�������Ҫ�з�Ӧ���ȷ�[12]��ƽ��Ħ������������������ַ����Ļ���ԭ����
3.1 ������Ӧ�ı�����˹�����ܱ仯�ͱ�ƽ�ⳣ��
������������ѧ���ݿ�����ø�����Ӧ�ı�����˹�����ܱ仯[13]
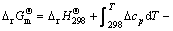
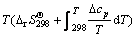 (1)
(1)
ʽ�У�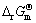 Ϊ��Ħ����Ӧ����˹�����ܣ�
Ϊ��Ħ����Ӧ����˹�����ܣ�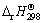 Ϊ298.15 K����ѹ���µ��ʱ䣻
Ϊ298.15 K����ѹ���µ��ʱ䣻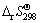 Ϊ298.15 K����ѹ���µ��ر䣻
Ϊ298.15 K����ѹ���µ��ر䣻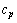 Ϊ��Ӧ����Ķ�ѹ�����ۡ�
Ϊ��Ӧ����Ķ�ѹ�����ۡ�
������Ӧ��ϵ�еĹ�̬������Ϊ�����ʣ�Һ̬�������γɵ�����Ϊ������Һ����Һ̬��̬���ʵĻ�Ⱦ�Ϊ1����Ӧ�ı�ƽ�ⳣ����ֻ��ƽ����ϵ�е���������ѹ�йء���Ӧ(a)��(b)��(c)��(d)��(e)�ı�ƽ�ⳣ������ʽ�ֱ�Ϊ
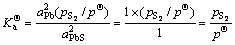 (2)
(2)
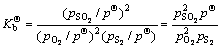 (3)
(3)
 (4)
(4)
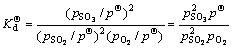 (5)
(5)
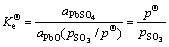 (6)
(6)
ʽ(2)~(6)�У�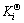 Ϊƽ��ʱ��Ӧi�ı�ƽ�ⳣ����
Ϊƽ��ʱ��Ӧi�ı�ƽ�ⳣ����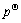 Ϊ������ѹ��ai��������i�Ļ�ȣ�pi����ƽ��ʱ����i�ķ�ѹ��ptΪϵͳƽ��ʱ����ѹ��
Ϊ������ѹ��ai��������i�Ļ�ȣ�pi����ƽ��ʱ����i�ķ�ѹ��ptΪϵͳƽ��ʱ����ѹ��
ƽ��ʱ�������ʵ�ƽ����ɻ������������ʵ�������yi��ʾ����Ӧ��ƽ�ⳣ��ΪKy��Ky����ƽ���ѹ��ʾ�ı�ƽ�ⳣ���Ĺ�ϵΪ
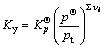
���¶�һ��ʱ��������Ӧ�ı�ƽ�ⳣ��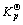 ȷ��������ƽ�ⳣ��Kp(��ѹ����ʾ��ƽ�ⳣ��)��Ky��Kc(�����ʵ���Ũ�ȱ�ʾ��ƽ�ⳣ��)Ҳ��ȷ����
ȷ��������ƽ�ⳣ��Kp(��ѹ����ʾ��ƽ�ⳣ��)��Ky��Kc(�����ʵ���Ũ�ȱ�ʾ��ƽ�ⳣ��)Ҳ��ȷ����
3.2 ͬʱƽ���о��ķ�Ӧ���ȷ�
���跴Ӧ(a)��(b)��(c)��(d)��(e)��ƽ�ⷴӦ���ȷֱ�Ϊ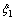 ��
��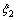 ��
��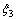 ��
��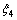 ��
��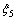 ��ni,eqΪƽ��ʱ����i��Ħ������ky,iΪ��Ӧi��Ħ������ƽ�ⳣ������ʼ��������Ϊ
��ni,eqΪƽ��ʱ����i��Ħ������ky,iΪ��Ӧi��Ħ������ƽ�ⳣ������ʼ��������Ϊ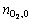 ����ƽ��ʱ�������Ħ���������������ʵ����ֱ�Ϊ
����ƽ��ʱ�������Ħ���������������ʵ����ֱ�Ϊ
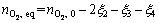 (7)
(7)
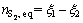 (8)
(8)
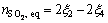 (9)
(9)
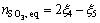 (10)
(10)
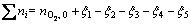 (11)
(11)
ƽ��ʱ������̬Ħ����Ϊ
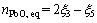 (12)
(12)
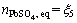 (13)
(13)
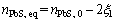 (14)
(14)
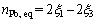 (15)
(15)
��Ӧ(a)��(b)��(c)��(d)��(e)��Ħ��������ƽ�ⳣ���ֱ�Ϊ
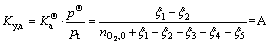 (16)
(16)
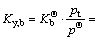
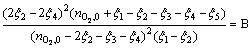 (17)
(17)
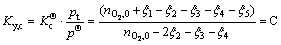 (18)
(18)
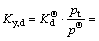
 (19)
(19)
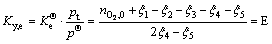 (20)
(20)
������5�����̵Ļ����ϣ�����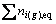 �����������ٽ���һ�����̣���
�����������ٽ���һ�����̣���
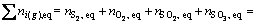
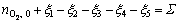 (21)
(21)
���������6�����̿ɹ����������Է����飺
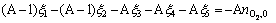 (22)
(22)
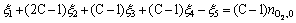 (23)
(23)
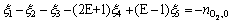 (24)
(24)
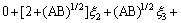
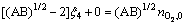 (25)
(25)
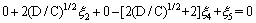 (26)
(26)
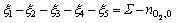 (27)
(27)
�����Ϻ�5��δ֪����6�����̵����Է�����������⣬���Եõ�ȷ���Ľ⣬���5��δ֪�ķ�Ӧ����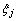 ����ֵ�����ɷ�Ӧ����
����ֵ�����ɷ�Ӧ����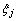 ���������������̬���ʵ�ƽ��Ħ��������
���������������̬���ʵ�ƽ��Ħ��������
3.3 ͬʱƽ���о���ƽ��Ħ������
����ƽ��Ħ������ֻ����ԭ�������غ��ԭ�����Բ�����ϵ�ķ�Ӧ�Ǻ��º�����������º�ѹ�����½��У�������ϵ�Ķ�����Ӧ�����ϣ�ƽ��Ħ����������Ӧ�á�����ʼ����Ǧ��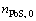 �ͳ�ʼ������
�ͳ�ʼ������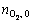 ��Ϊһ��ʱ������ԭ��������ƽ����
��Ϊһ��ʱ������ԭ��������ƽ����
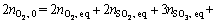
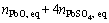 (28)
(28)
��Ǧԭ��������ƽ����
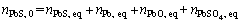 (29)
(29)
����ԭ��������ƽ����
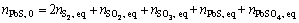 (30)
(30)
���ڷ���(20)��(21)���Թ���Ǧ�����ԭ�Ӿ���ԭ�Ӿ���ɵ�
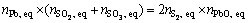 (31)
(31)
��Pb-O-S��ϵ��Ԫ���෴Ӧ��ƽ��ʱ��ʽ(28)~(31)�еĸ���̬����ƽ��Ħ�����ɸ���ǰ��ͬʱƽ������Խ������㡣��Ը���ϵ�Ķ�����Ӧ����ͨ�����������Ӧ�ı�ƽ�ⳣ������̬���ʵ�ƽ���ѹ��ϵ���̣��������ϵ����̬���ʵ�ƽ���ѹ����ѹ��Ȼ���趨��̬���ʵ���Ħ��������̬���ʵ����������ɽ�һ��ͨ��Ħ�������ļ�����õ���
���������̬����ƽ��Ħ���������������ʽ(28)~(31)�����������������̬Ħ��������̬Ħ�������������ѧʽ���£�
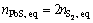 (32)
(32)
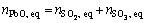 (33)
(33)
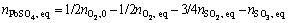 (34)
(34)
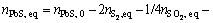
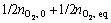 (35)
(35)
4 ����¯������ұ���������ݵ�ͬʱƽ�����
4.1 5�����ʱ��ƽ�����
��5����ƽ���ʱ������ʽ(2)~(6)�ɵ�
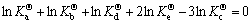 (36)
(36)
������
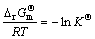 (37)
(37)
���Կɵ�
 (38)
(38)
���ݸ���Ӧ�����ı�Ħ���أ���Ħ�������ʣ�Ħ����ѹ���ݣ��ɵõ�����(a)~(e)������Ӧʽ�ļ���˹���������¶�T�Ĺ�ϵʽ������ʽ(38)�У�����������ƽ�����¶�ΪT=959.4 K����ʱ������ƽ����ƽ�ⳣ����ƽ���ѹ���������1��2���С�
�ɱ�2��֪��ƽ����������Ҫ�������������Ϊ�����������ѹ��������ѹ��
4.2 �����ʱ������̬Ħ�������ʼ��������nO2,0��ϵ�ļ���
������ƽ���ʱ����Ǧ����PbS�Ĺ��������㣬��������̬�������ʵ�Ħ���������ʼ����������nO2,0����ֵ�ı���仯����������ƽ�����¶��¸���̬���ʵķ�ѹ 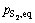 ��
��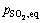 ��
��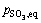 ��
��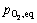 ������ı䡣
������ı䡣
����ǰ����ͬʱƽ���о���Ħ��������5�����¶�T =959.4 K�����趨��λʱ���ڵ���̬������Ħ����Ϊһ��ֵ����nt= 0.5 mol��������̬���ʵ�ƽ���ѹ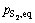 ��
�� 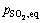 ��
��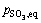 ��
��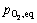 Ϊǰ��2��������ֵʱ������̬Ħ�������������������
Ϊǰ��2��������ֵʱ������̬Ħ�������������������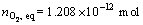 ��
��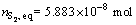 ��
��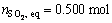 ��
��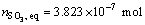 ��
��
���ô�ƽ��ʱ����̬Ħ�������������ʽ(32)~(35)��������ʼ�������ֱ�Ϊ1��3��5��7��9 mol��PbS��ʼ�������ֱ�Ϊ5��6��7 mol�������������̬��Ħ��������ɻ��������̬Ħ�������ʼ�����ı仯��ϵͼ1��������̬Ħ�������ʼPbS���ı仯��ϵ��ͼ2��ʾ��
��1 ����ƽ���ʱ����Ӧ�ı�ƽ�ⳣ��
Table 1 Standard equilibrium constant of reaction at state of five phase equilibrium

��2 ����ƽ���ʱ�������ʵ�ƽ���ѹ
Table 2 Equilibrium partial pressure of gases at state of five phase equilibrium
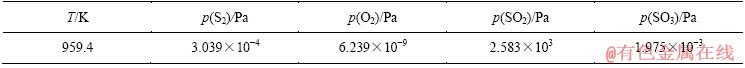
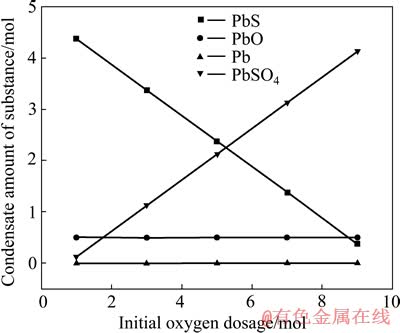
ͼ1 ��ʼPbS��Ϊ5 molʱ������̬Ħ�������ʼ�����Ĺ�ϵ
Fig. 1 Relationship between condensate amount of substance and initial oxygen at initial PbS dosage of 5 mol
��ͼ1���Կ�����Ǧ����������Ǧ���������ʼ�����ı仯���仯����Ǧ�����������������Ӷ����٣�����Ǧ�����������������Ӷ����ӣ�����Ǧ��Ϊ����¯����������Ҫ�����ͨ����������ﵽ9.750 molʱ����Ǧ�����ӽ���0�����ʱ������������棬�ѱ������档�ɴ˿�֪����ʼPbS�����ʼ������������ֵΪ5:9.750��
��ͼ2���Կ������ڳ�ʼ�������ı�������£�����̬��ֻ��PbS�������ų�ʼPbS�������Ӷ����ӣ���������̬Ħ�������䡣
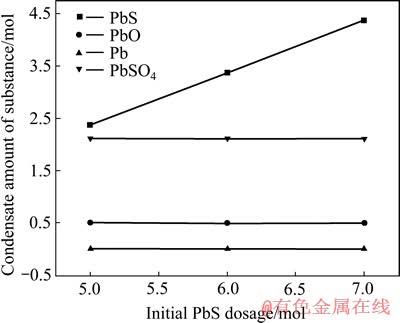
ͼ2 ��ʼ����Ϊ5 molʱ������̬Ħ�������ʼPbS���Ĺ�ϵ
Fig. 2 Relationship between condensate amount of substance and initial PbS at initial oxygen dosage of 5 mol
4.3 ��������ƽ����¶��µĸ��ֲ����������������ʼ������nO2,0�Ĺ�ϵ�ļ���
����ǰ������ѡ���¶�Ϊ1 100 K��1 273.5 K��ͬ�������÷�Ӧ(a)~(e)�ı�ƽ�ⳣ��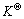 �����������3���С�
�����������3����
���¶�Ϊ1 100��1273.5 K�ı�ƽ�ⳣ������ʽ(2)~(6)�ɵó����������ڴﵽƽ��ʱ�ķ�ѹ�����4���С�
���趨��λʱ���������̬������Ħ����Ϊһ��ֵ��nt= 0.5 mol����ͬ�¶��£�ƽ���ʱ�������Ħ�������5���С�
��3 ��ͬ�¶��µķ�Ӧ��ƽ�ⳣ��
Table 3 Standard reaction equilibrium constant at different temperatures

��4 ��ͬ�¶���ƽ���ʱ�������ʵ�ƽ���ѹ
Table 4 Equilibrium partial pressure of gases at different temperatures

��5 ��ͬ�¶���ƽ���ʱ�������Ħ����
Table 5 Molar amount of gases in equilibrium coexistence at different temperatures
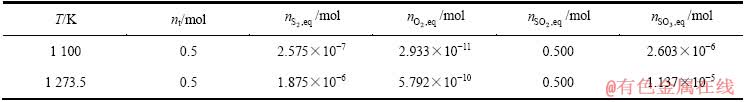
����ʽ(32)~(35)������ƽ��ʱ�������Ħ������PbS��ʼ��5 mol���������ֱ�Ϊ1��3��5��7��9 mol�������������̬��Ħ��������ɻ����ڲ�ͬ�¶�������̬��Ħ�������ʼ�����ı仯��ϵͼ����ͼ3��4��ʾ��
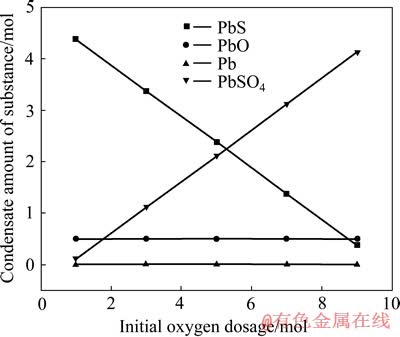
ͼ3 ��ʼPbS��Ϊ5 mol��1 100 Kʱ������̬��Ħ�������ʼ�����Ĺ�ϵ
Fig. 3 Relationship between condensate amount of substance and initial oxygen at initial PbS dosage of 5 mol and temperature of 1 100 K
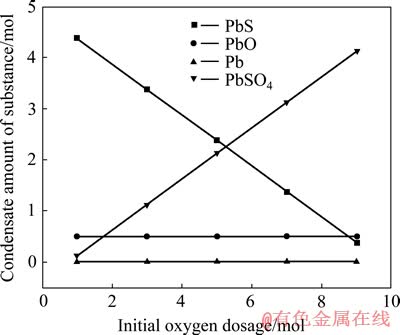
ͼ4 ��ʼPbS��Ϊ5 mol��1 273.5 Kʱ������̬��Ħ�������ʼ�����Ĺ�ϵ
Fig. 4 Relationship between condensate amount of substance and initial oxygen at initial PbS dosage of 5 mol and temperature of 1 273.5 K
��ͼ3��4���Կ�����������̬��Ħ�������ʼ�����ı仯��ϵ��������������¶�ʱһ�������¶ȷֱ�Ϊ1 100 K��1 273.5 K����λʱ���ڵ��������ʵ���Ħ������Ϊ0.5 molʱ����ʼPbS��ͬ��ʼ������������ֵ��Ϊ5:9.750���ɴ˿ɵã���������ֵͬǰ��������������ֵһ�¡�
5 ����
1) ����Ǧ�㹻��ʱ����̬���ʲ�����ҪΪ�����������Ϊ������������������ȫ������̬���ʲ����н���Ǧ������Ǧ������Ǧ��
2) Pb-S-O��ϵ�������¶�ΪT=959.4 K�����ڴ��¶ȣ���ϵ����̬��������٣���ϵ�������������������࣬���������ұ�����̵ĵ��ء�
3) �¶ȵ��������ϵ��ƽ�ⳣ������Ӱ�죬��Ӧ(a)�ı�ƽ�ⳣ������Ӧ(b)~(e)�ı�ƽ�ⳣ����С����Ӧ(a)��ƽ�ⳣ������������������Pb��S2���Է�Ӧ(b)��(c)��(d)��(e)�Ľ��ж�������
4) ��Ǧ�����������������������Ӷ����ͣ�����Ǧ�����������������������Ӷ�������ʹ������������ƽ�����������(�ɼ����������������ղ�����)Ϊ2:3�����·�Ӧ����������Ǧ��������Ǧ���Ӷ�����������¯��������Ǧ�����������ʵ�֡�
REFERENCES
[1] ������, ���, ��ѧ��, �Ŵ���. ����Ǧұ������״����չ˼��[J]. �й�����ͨ��, 2009(15): 34-37.
LI Wei-feng, YANG An-guo, GUO Xue-yi, ZHANG Chuan-fu. Status and opinion on the development of Henan��s lead smelting[J]. China Metal Bulletin, 2009(15): 34-37.
[2] ������. Ǧ��Ⱦ��״, ԭ�Բ�[J]. �й���Դ�ۺ�����, 2001(2): 26-28.
MA Yong-gang. Current situation��reasons and measures of lead pollution[J]. China Resources Comprehensive Utilization, 2001(2): 26-28.
[3] ������, ������, ��ѧ��, �Ŵ���. �ҹ�Ǧұ���ļ�����״����չ[J]. �й���ɫұ��, 2010, 39(2): 29-33.
LI Wei-feng, ZHANG Xiao-guo, GUO Xue-yi, ZHANG Chuan-fu. Status and progress of lead smelting technology in China[J]. China Nonferrous Metallurgy, 2010, 39(2): 29-33.
[4] ������. �ҹ�Ǧпұ����״�������չ[J]. �й���ɫ����ѧ��, 2004, 14(1): 52-62.
JIANG Ji-mu. Status and sustainable development of lead and zinc smelting industry in China[J]. The Chinese Journal of Nonferrous Metals, 2004, 14(1): 52-62.
[5] ������. �Ľ�����������Ǧұ��¯�ṹ���ͻ���ϵ�̽��[J]. �й���ɫұ��, 2007, 36(4): 42-44.
JIA Zhu-hong. Discussion on improvement structure and refractory material of oxygenenriched air &top-blown metallurgical furnace for lead smelting[J]. China Nonferrous Metallurgy, 2007,36(4): 42-44.
[6] �� ��. ��������ֱ����Ǧ������״���չ[J]. ������ɫ����, 1995, 8: 26-30.
WANG Hui. Status and progress of KIVCET lead smelting[J]. World Nonferrous Metals, 1995, 8: 26-30.
[7] CHAUDHURLK B, MELCHER G. Comparative view on the metallurgy of the KIVCET CS and other direct lead smelting processes[J]. Canadian Mining and Metallurgical Bulletin, 1978 (71): 126-130.
[8] SANNIKOV Y I, LIAMINA M, SHUMSKII V. A physical and chemical description of the Kivcet lead flash smelting process[J]. Canadian Mining and Metallurgical Bulletin, 1998, 91: 76-81.
[9] ������. Ǧұ��[M]. ��ɳ: ���ϴ�ѧ������, 2004: 65-66.
PENG Rong-qiu. Metallurgy of lead [M]. Changsha: Central South University Press, 2004: 65-66.
[10] ���ײ�, ����ϼ, Ҧ����. ������ѧ[M]. ����: �ߵȽ���������, 2005.
FU Xian-cai, SHEN Wen-xia, YAO Tian-yang. Physical chemistry[M]. Beijing: Higher Education Press, 2005.
[11] NERMES E O, TALONEN T T. Flash smelting of lead concentrates[J]. Journal of Metals, 1982, 34(11): 55-59.
[12] �켪��. ұ������ѧ[M]. ��ɳ: ���Ϲ�ҵ��ѧ������, 1995.
ZHU Ji-qing. Metallurgical thermodynamics[M]. Changsha: Central South University of Technology Press, 1995.
[13] ��ƽ��. ���ƴ�ѧ��ѧ[M]. ��ɳ: ���Ͻ���������, 2002.
ZHANG Ping-min. Advanced chemistry for engineering[M]. Changsha: Hunan Education Press, 2002.
[14] Ҷ����, ������. ʵ����������ѧ�����ֲ�[M]. ����: ұ��ҵ������, 2002.
YE Da-lun, HU Jian-hua. Practical inorganic thermo- dynamicdatamanual[M]. Beijing: Metallurgical Industry Press, 2002.
[15] BARIN I. �������Ȼ�ѧ�����ֲ�[M]. ������, ţ��ͨ, ��. ����: ��ѧ������, 2003: 1273-1306.
BARIN I. Thermochemical data of pure substances[M]. CHENG Nai-liang, NIU Si-tong, transl. Beijing: Science Press, 2003: 1273-1306.
(�༭ ����)
������Ŀ�����Ҹ����о���չ�ƻ�������Ŀ(2011AA061003)
�ո����ڣ�2012-06-20�������ڣ�2012-10-08
ͨ�����ߣ������࣬���ڣ���ʿ���绰��0731-88877365��E-mail: greenlcq@163.com
ժ Ҫ��������Ǧ��������¯������ұ�����̵Ķ���ͬʱƽ��ԭ��������ƽ��Ħ���������������������¶ȡ���ʼ�����ͳ�ʼ��Ǧ����ƽ��������̬��������Ӱ�졣����������ڽϸ��¶��£���ʼ���������ӻ�ʹ����Ǧ�IJ������ӣ�����Ǧ�IJ������ͣ������������²���������Ǧ��������Ǧ�����Dz���ĺ���̼��ԭ��������ұ��������Ӧѡ����������������������״���������Ǧ�������ǽ��Ѵ�������Ǧ��
[1] ������, ���, ��ѧ��, �Ŵ���. ����Ǧұ������״����չ˼��[J]. �й�����ͨ��, 2009(15): 34-37.
[2] ������. Ǧ��Ⱦ��״, ԭ�Բ�[J]. �й���Դ�ۺ�����, 2001(2): 26-28.
[3] ������, ������, ��ѧ��, �Ŵ���. �ҹ�Ǧұ���ļ�����״����չ[J]. �й���ɫұ��, 2010, 39(2): 29-33.
[4] ������. �ҹ�Ǧпұ����״�������չ[J]. �й���ɫ����ѧ��, 2004, 14(1): 52-62.
[5] ������. �Ľ�����������Ǧұ��¯�ṹ���ͻ���ϵ�̽��[J]. �й���ɫұ��, 2007, 36(4): 42-44.
[6] �� ��. ��������ֱ����Ǧ������״���չ[J]. ������ɫ����, 1995, 8: 26-30.
WANG Hui. Status and progress of KIVCET lead smelting[J]. World Nonferrous Metals, 1995, 8: 26-30.
[9] ������. Ǧұ��[M]. ��ɳ: ���ϴ�ѧ������, 2004: 65-66.
PENG Rong-qiu. Metallurgy of lead [M]. Changsha: Central South University Press, 2004: 65-66.
[10] ���ײ�, ����ϼ, Ҧ����. ������ѧ[M]. ����: �ߵȽ���������, 2005.
[12] �켪��. ұ������ѧ[M]. ��ɳ: ���Ϲ�ҵ��ѧ������, 1995.
[13] ��ƽ��. ���ƴ�ѧ��ѧ[M]. ��ɳ: ���Ͻ���������, 2002.
ZHANG Ping-min. Advanced chemistry for engineering[M]. Changsha: Hunan Education Press, 2002.
[14] Ҷ����, ������. ʵ����������ѧ�����ֲ�[M]. ����: ұ��ҵ������, 2002.
[15] BARIN I. �������Ȼ�ѧ�����ֲ�[M]. ������, ţ��ͨ, ��. ����: ��ѧ������, 2003: 1273-1306.


