DOI: 10.11817/j.ysxb.1004.0609.2020-39539
��������AlNˮ����Ϊ�����Ԫ�����Իع����
��˧˧���� �����ߺ����������
(��ͨ��ѧ ��е����ѧԺ����ͨ 226019)
ժ Ҫ��
ͨ����������ˮ�ⷴӦ��������ּ��京���仯���о��������������AlN������������ʽ������AlN����������ҺpHֵ�IJⶨ������ʱ�䡢�¶ȡ�ת�ٵ�ˮ�������AlNˮ�����ʵ�Ӱ�첢������ж�Ԫ�����Իع��������������������¶��ܽ�����������AlN��������������ҺpHֵ���ӳ�ʱ�����Ч�ٽ�AlN��ˮ�⣬ͬʱ��2h������ҺpHֵѸ����������λ��ת�ٶ�AlNˮ�����ʺ�����ҺpHֵ������Ӱ�졣������ԣ�AlN����������ҺpHֵ���ܿ۱�����������AlNˮ�����ʡ���ˮ���������������������AlN�������ж�Ԫ�����Իع���������μ���������ֵ��ʵ��ֵ������ܡ�8.65%��
�ؼ��ʣ�
��������AlN��ˮ������Ԫ�����Իع�������¶���ת����ʱ����
���±�ţ�1004-0609(2020)-04-0920-07���� ��ͼ����ţ�TF09 ���� ���ױ�־�룺A
�������������������в�����һ�ַ�������Ҫ��Դ������ʱƯ�������������IJ��ۼ���������P�������Ӽ�[1-2]���ݹ��ƣ�ÿ����1000 tԭ��Լ����25~50 t�����������ҹ�2018��ԭ������3365.9��t���㣬������������������ߴ�80~170��t���ҡ�
����Ŀǰ�������������д��ģ��Ч���õļ���ֻ�С�������һ�֣�����ȡ�������еĵ������Ի�ȡһ���ľ������棬ʣ���������ڹ�ҵ��ˮ�����ͻ���Ϻ�·�����ϵȷ���õ�һ������������[3-6]��Ȼ����Լ95%�����������õ���Ч���ã�ͨ������Ϊ�����������жѻ�������������Ⱦ��ռ���˴���������Դ���������г�Al��Al2O3��������д���AlN����ˮ������ˮ�Ⲣ�ͷų�����ǿ�Ҵ̱�����ζ[7-8]�����ǣ���������������������������AlN�Ĵ��ڣ���������Ʒ��ɲ������ܲ��ȶ�����ҺpHֵ�仯�����غ������Ϊ��̬��������Ա���������˼������š�
Ϊ��Ч����������������⣬�ڶ������Ա�����˴����о�������ΰ��[9]���ͨ��ˮ�������pHֵ����AlN��ˮ��̶ȣ����������¶ȵ����ߡ����ȵļ�С��AlNˮ�����Լӿ졣FUKUMOTO��[10]�о��˲�ͬ������ϵ��AlN��ĩ��ˮ����Ϊ������H3PO4��AlN��ĩ��ˮ������谭���ã��Ҵ���77�������²�����AlOOHΪ����С��77 �������²�����Al(OH)3Ϊ����������[11]�о���������������AlNˮ�������pHֵ���¶Ⱥ�ʱ������Ӷ����ˮ��̶������ӣ���373 K������ˮ��24 h����������AlN����ȫ��תΪAl(OH)3��LI��[12]��������ˮ����ϵ�е�pHֵ��NH3-NŨ�Ƚ��жԱȣ������ʾ��pHֵ�������ȶ���ʱ����Һ��NH3-N��Ũ���Բ���������˵��pHֵ��������������ˮ�����ʱ��������Ӧ���Dz���ѧ�ģ�ͬʱָ������������AlNˮ��������γ�Al(OH)3�ࡣ�ܳ����[13]ͨ���������-�к͵ζ����о��������¶���ʱ�������Լ�����������AlN�ķֽ⡣
�ɴ˿ɼ�����������ˮ�����ʵı����������������͵��о��г���һ�����硣
���Ķ���������AlNˮ��ʱ�¶ȡ�ʱ�䡢ת�ٵȲ�������ϵͳ�Է�������̽��pHֵ��AlN����������ʽ�ĺ����ԣ�ͬʱ���ڴ���ʵ�����ݵĻ����ϣ��Ը�ˮ���������������������AlN�������ж�Ԫ�����Իع�������ԴﵽԤ�⡢������������AlN��Ŀ�ġ�
1 ʵ��
1.1 ԭ�ϼ�Ԥ����
ʵ����������Դ�ڽ��պ����������˾������Ϊ��ȡ�������������������Ԥ��������з���������ʵ���о���Ԥ��������Ϊ���õ�Ŀ����ɸ�����������г�ɸ��ȥ������������ʣ�ಿ�ֽ�����ĥ�����Ȼ��������ø�Ŀ����ɸ����ɸ�֣�ȡɸ������Ϊʵ��ԭ�ϡ���XRD���������֤����ʵ����ԭ����Ҫ�ɷ�ΪAl��Al2O3��AlN��
1.2 ʵ���Լ�������
NaOH�������Ϊ�����������졢�μ�����Ϊָʾ�������ᣬ��ѧ��������ˮ����EPED-10TH�����õ�¯��DK-98-�����Խ�������JB60-SH��ˮԡ�䣬WB-4�����Ⱥ��¹ķ�����䣬101A-2��
1.3 ���Է���
1.3.1 ����ҺpHֵ
����ȼƽ��б궨��������Ӧ������500 mLȥ����ˮ����һ���¶�������ˮԡ���ȣ���Ӧ���ڼ���125 g����������ijת�������½��裻�̶�ʱ��κ�ֹͣ���裬�ʵ���������ȥ����ˮ�Ա�֤��Һ�Ȳ��䣬�������貢����ȼƼ������ҺpHֵ���ظ��������衣
1.3.2 ��������AlN����
1) ��������
����2 g������������װ��150 mL��20% NaOH��Һ����ƿ�У�Ѹ�ٸǽ�ƿ����������Ȳ����ַ���״̬2 h���ҽ���������200 mL��40 g/L��������Һ����������İ���������������Ա����졪�μ�����Ϊָʾ������0.05 mol/L��ϡ������Һ���еζ�����Һ����ɫͻ��Ϊ�Ϻ�ɫΪ�ζ��յ�[14]���������������հ�ʵ�顣
2) �������
ͨ�����ĵ���������������AlN������
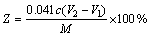 (1)
(1)
ʽ�У�cΪϡ����Ũ�ȣ�mol/L��V2Ϊ�ζ����������ĵ�ϡ���������mL��V1Ϊ�հ�ʵ�����ĵ�ϡ���������mL��MΪ����������g��ZΪֱ�Ӳ�õ���������AlN������%��
2 ���������
2.1 �ȶ���ѧģ��
ͨ���Բ������XRD��������ȷ����������AlNˮ�ⷴӦʽΪ
AlN+3H2O=Al(OH)3+NH3�� (2)
��ͬ�¶��·�Ӧ(2)�ļ���˹������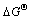 ���£�
���£�

 (3)
(3)
ʽ�У�viΪi���ʵĻ�ѧ�������������٣� Ϊi�������¶�T�����µ��ʣ�kJ/mol��
Ϊi�������¶�T�����µ��ʣ�kJ/mol��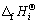 Ϊi���ʱ�Ħ�������ʣ�kJ/mol��cpΪ��ѹ���ݣ�J/(kg��K)��
Ϊi���ʱ�Ħ�������ʣ�kJ/mol��cpΪ��ѹ���ݣ�J/(kg��K)��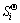 Ϊi�������¶�T�����µ��أ�kJ/mol������ʽ(3)��Ӧ�ĸ���������ѧ�������1���С�
Ϊi�������¶�T�����µ��أ�kJ/mol������ʽ(3)��Ӧ�ĸ���������ѧ�������1���С�
���������֪[12]���¶ȷ�Χ��298~373 K�䣬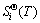 �ı仯���Ȳ���ͨ������298 K���������ƴ����������㣬��ͬ�¶������µ�
�ı仯���Ȳ���ͨ������298 K���������ƴ����������㣬��ͬ�¶������µ�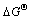 ��ֵ���2���С�
��ֵ���2���С�
�ɱ�2��֪����Ħ�����������ܱ���298~373 K���¶ȷ�Χ����ֵ��Ϊ����˵����������AlNˮ�ⷴӦ���ȶ���ѧ�Ƕ��϶��Կ��Է����У�����25 �����������¶���Ҳ�ɷ���ˮ�ⷴӦ��
��1 �����ʵ�����ѧ����
Table 1 Thermodynamic parameters of each substance

��2 ��ͬ�¶������� ��T�Ĺ�ϵ
��T�Ĺ�ϵ
Table 2 Relations between  and T at different temperatures
and T at different temperatures
2.2 ��ͬˮ��������AlN������Ӱ��
2.2.1 AlN������������ʽ
��������ˮ�ⷴӦ�����У�NԪ����NH3��ʽ���룬����Ԫ��λ�ø�OH-���ӣ��γɷ�����Ϊ78��Al(OH)3��Զ���ڷ�����Ϊ41��AlN�����⣬�������г�Al��Al2O3�������������⣬��������NaCl��KaCl�ȿ�������[15]����ֱ����ʽ(1)��ΪAlN�������Ⱥ�������ּ������ı仯��Ҳ����������������AlN���������ڸߵ��������IJ���ʱ������Ϊ��������⣬ͨ����ʽ(2)ˮ����̵��о�������AlN����Z��������
 (4)
(4)
ʽ�У�KΪԭʼAlN������%��MΪԭʼ��Ʒ������g��mΪˮ������з�Ӧ����AlN������g��YΪˮ�����Һ���ε�������g����ʵ����֤�������κ���Y/MΪ3.52%��

 (5)
(5)
ʽ�У�ZreΪ��������������AlN������%��
2.2.2 ʱ����ת�ٶ���������AlNˮ�����ʵ�Ӱ��
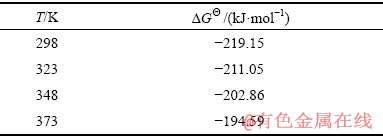
ͼ1��ʾΪ60 �桢��ͬת����������������������AlN�����仯����ͼ����ͼ1�ɼ��������ǵ�ת��(0 r/min��100 r/min��300 r/min)���Ǹ�ת��(600 r/min��1000 r/min)״̬�µĻ�е���裬��������������AlN�����仯���ƻ���һ�£��Ҹ�ʱ������������������AlN����ֵ����˵��ת�ٶ�������ˮ������������Ӱ�졣���ڴ�ˮ�������£�����24 hˮ�ⷴӦ����������������AlN������Լ����һ�룬��ԭʼ��12.7%����5.7%~7.0%����Ϊ���Եأ���0~4 h�Σ���������������AlN�����������12.7%�����С��9.0%~10.2%�����½�����Զ��������Ӧʱ��Σ�����ˮ��ʱ����ӳ���������ˮ�������Ż���20 h���������е�AlN�����������䡣

ͼ1 60 ��ʱ��ͬת����������������������AlN����
Fig. 1 Modified content of AlN in aluminum dross under different rotational speed at 60 ��
һ���棬�ڷ�Ӧ���ڽ������������ȼ��������ϴ���ˮ�Ӵ����������Ӧ�ϴ�����ͬˮ�������²μ�ˮ�ⷴӦ��AlN����Ը��࣬ˮ����������죻��һ���棬ˮ�ⷴӦ����Al(OH)3��һ��������ɫ��״����������ʱ����ӳ���������P�丽���ォ�������������������϶���谭AlN��ˮ�Ӵ�ͨ�����Ӷ�����������ˮ�����ʡ���������������������������ˮ����ϵ�У���ֹ��������ˮ����ϵ�ײ��ѵ�������ʱ�䡢�¶���ͬ�������£�ת�ٻ�����Ӱ����������AlN��ˮ�ĽӴ��������ˮ����̵�Ӱ��Ҳ��С��
2.2.3 �¶ȶ���������AlNˮ�����ʵ�Ӱ��
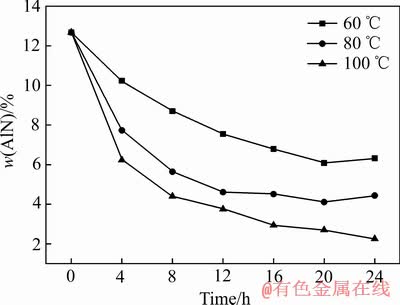
ͼ2 600 r/minת��ʱ��ͬ�¶���������������������AlN����
Fig. 2 Modified content of AlN in aluminum dross under different temperatures and speeds at 600 r/min
ͼ2��ʾΪ600 r/min����ͬ�¶���������������������AlN�����仯����ͼ����ͼ2�ɼ�������ˮ���¶ȵ���ߣ�����ͬˮ��ʱ���£�100 ���ˮ����ϵ����������������AlN�������Ե���60 ���80 �档���� 24 hˮ���100 ��ˮ����������������������AlN������ԭʼ��12.7%����2.3%���ң��Ҽ���ˮ�����������ζ��80 ��ʱ�½���4.5%���ң�����ˮ�����������ζ����60 ��ʱ������6.3%���ң��������ˮ������������ݼ���ζ������˵��60 ��������ˮ�����Զδ��������ˣ��¶ȵ����ӿ���Ч�ٽ���������AlN��ˮ�⡣
��ѧ��Ӧ�ڲ�ͬ�¶��µķ�Ӧ����Ҳ��ͬ���¶ȶԷ�Ӧ���ʵ�Ӱ����Ҫ����Ϊ�Է�Ӧ����ϵ����Ӱ�졣���ݰ�������˹��ʽ�ã�
 (6)
(6)
ʽ�У�kΪ��Ӧ����ϵ���������٣�EaΪ��Ӧ��ܣ�kJ/mol��TΪ�¶ȣ�K��RΪĦ�����峣����J/(mol��K)����������ͬ�¶ȵķ�Ӧ��ϵ�У�����T1~T2������(T1��T2)��Ea����Ϊ���������ڷ�Ӧ���Ea��0��R��0����k2/k1��1��������״̬�µķ�Ӧ����ϵ��һ����ڵ���״̬�µķ�Ӧ����ϵ�������ԣ������¶������������������AlN��ˮ�����ʡ�
2.3 ��ͬˮ������������ҺpHֵ��Ӱ��
2.3.1 ʱ����ת�ٶ�����ҺpHֵ��Ӱ��
ͼ3��ʾΪ60 �桢��ͬת������������ҺpHֵ�仯����ͼ����ͼ3�ɼ�����0~2 h�ķ�Ӧ�Σ���ת�������µ�����ҺpHֵ�������������ŷ�Ӧʱ����ӳ�����0 r/min��100 r/min�ĵ�ת�������£�����ҺpHֵ��������300 r/min��600 r/min��ת�������µ�����ҺpHֵ��������������ͬ�����µ�ת��״̬������NH3������Һ�е��������γɵ�NH3��H2O�������OH-Ũ�ȸ���������ҺpHֵ�Ըߣ�����ת�ٶ�����ҺpHֵ��Ӱ�첻���ر����ԡ�
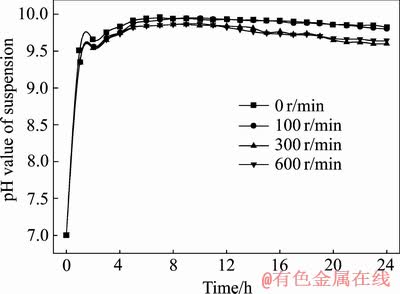
ͼ3 60 ��ʱ��ͬת������������ҺpHֵ
Fig. 3 pH value of suspension at different rotational speeds and 60 ��
2.3.2 �¶ȶ�����ҺpHֵ��Ӱ��
ͼ4��ʾΪ300 r/min����ͬ�¶������µ�����ҺpHֵ�仯����ͼ����ͼ4�ɼ�����0~2 h�ķ�Ӧ�Σ����¶������µ�����ҺpHֵ�������������ŷ�Ӧʱ����ӳ�������Һ�����pHֵ�����ڲ�ͬ�¶��±���һ��ʱ�䡣�������ڷ�Ӧ��������ά����ϵ�ı���״̬�����ŷ�Ӧ�ٶȵ��½��Ͱ����Ļ��ͣ�����ҺpHֵ������С�����У�60 ������������Һ���pHֵ�ϸߣ�Լ9.8��100 ��ʱ���pHֵ�ϵͣ���9.0���ҡ�

ͼ4 300 r/minת��ʱ��ͬ�¶�����������ҺpHֵ
Fig. 4 pH value of suspension at different temperatures and 300 r/min
������ҺpHֵ����Һ���빫ʽ�ɵã�
 (7)
(7)
ʽ�У�K1Ϊ��ˮ�ĵ��볣���������٣�K2Ϊˮ�ĵ��볣���������٣�c(H+)Ϊˮ�е������H+Ũ�ȣ�mol/L��c(NH3��H2O)Ϊ��Һ��δ�����NH3��H2OŨ�ȣ�mol/L��c(H2O)Ϊ��Һ��δ�����H2OŨ�ȣ�mol/L�����跴Ӧ��ϵ�ڰ�Ũ�ȱ��ͽΣ���ϵ��c(NH3��H2O)��c(H2O)ֵ�㶨������ҺpHֵ��Ҫ�백ˮ�ĵ��볣��K1��ˮ�ĵ��볣��K2�йء�����Ϊ��������¶�T��أ���������ʷ����Էֲ�����������ҺpHֵ�Ĵ�С��ȷ������ͬ�¶������µ�������ˮ�����ʡ�
2.4 ������ˮ������Ķ�Ԫ�����Իع����
��������ʵ�飬���¶ȡ�ת�١�ʱ��Ϊ�Ա�����������������Ϊ������������������[8]��չ����Ԫ���ζ���ʽ�ķ����Իع��������Ԫ�����Իع��������ģ��Ϊ
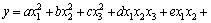
 (8)
(8)
ʽ�У�x1Ϊ������ˮ���¶ȣ��棻x2Ϊ������ˮ��ת�٣�r/min��x3Ϊ������ˮ��ʱ�䣬h��yΪ��������������%������Ϊ���������������١�����������֪���Ա�����ת�١��������������Ӱ�죬Ϊ��ģ�ͣ���ת��x2���С����㡱��������ģ�����£�
 (9)
(9)
��3��ʾΪʽ(8)��ʽ(9)�и���ع�ϵ����ֵ������ģ���еĶ����ж�ϵ��R2Ϊ0.93682��Fͳ����Ϊ570.37707��PֵΪ0����ģ���е�R2Ϊ0.94126��Fͳ����Ϊ1124.36109��PֵΪ0��˵����ģ�͵���������Ա���֮�����س̶ȸ��ߡ����Ч�����á�
����ģ�͵ľ������ʽ��
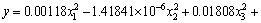
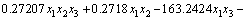

 (10)
(10)
��ģ�͵ľ������ʽ��
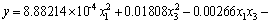
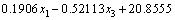 (11)
(11)
��4��ʾΪ����ģ�����ģ����ʵ��ֵ������ֵ�ĶԱ�������ɼ��������ܱ��ֽϺõľ��ȣ�������ֵ�������Կ����ڡ�8.65%���ڣ���ˮ��ʱ��������AlN������Ԥ������ƾ���һ��ָ�����塣
��3 �ع�ģ�͵���ֵͳ��
Table 3 Numerical statistics of regression model

��4 ��������������AlNˮ�������ʵ��ֵ������ֵ�Ա����(����)
Table 4 Comparison between experimental modified value and theoretical modified value of AlN hydrolysis process in aluminum dross (part)

3 ����
1) ͨ����������ˮ����̵��ȶ���ѧģ���о������ֱ�Ħ�����������ܱ�Ϊ��ֵ��˵����������AlNˮ�ⷴӦ������ѧ�Ƕ��϶��Կ��Է����С�ͬʱ�����ˮ�������������ּ������仯���о��õ�AlN������������ʽ����ǿ���ݴ����Ŀ�ѧ����ȷ�ԡ�
2) �¶ȵ������ܽ�����������AlN��������������ҺpHֵ��ʱ����ӳ�����Ч�ٽ���������AlN��ˮ�⣬ͬʱ��2 h��Ѹ�ٽ�����ҺpHֵ��������λ��ת�ٶ���������AlNˮ�����ʺ�����ҺpHֵ������Ӱ�졣������ԣ�ͨ��AlN����������������ˮ������������������ҺpHֵ��
3) ��ˮ�������AlN�������ж�Ԫ�����Իع���������μ��õ���ģ�ͣ���������������AlN����������ֵ��ʵ��ֵ�������ڡ�8.65%���ڣ���ˮ��ʱ��������AlN������Ԥ������ƾ���һ��ָ�����塣
REFERENCES
[1] �� ��. ���������ʼ����е�AIN�ڱ��պ�ˮ������е���Ϊ�о�[D]. ����: ������ѧ, 2008: 1-3.
LIU Ji. Study on the properties of aluminum dross and the behaviors of AlN in hydrolysis and roasting processes[D]. Shenyang: Northeastern University, 2008: 1-3.
[2] ��Զ��, �� ��, �� ��, �� ��, �� ʤ, ����ΰ. ���ҵ��ۺ�����[J]. �й���ɫұ��, 2008(6): 63-67.
LI Yuan-bing, SUN Li, ZHAO Lei, CHANG Na, ZHOU Sheng, LI Ya-wei. Utilization of aluminum ash[J]. China Nonferrous Metallurgy, 2008(6): 63-67.
[3] SINGH U, ANSARI M S, PUTTEWAR S P, AGNIHOTRI A. Studies on process for conversion of waste aluminium dross into value added products[J]. Russian Journal of Non-Ferrous Metals, 2016, 57(4): 296-300.
[4] SOOKSAEN P, PUATHAWEE P. Properties of unglazed ceramics containing aluminum dross as a major component[J]. Solid State Phenomena, 2017, 266: 182-186.
[5] ��ǿǿ. ��������������ש������[D]. ��: �㽭ʦ����ѧ, 2016: 15-48.
XU Qiang-qiang. Development of secondary aluminum ash unburned[D]. Jinhua: Zhejiang Normal University, 2016:15-48.
[6] MAILAR G, SUJAY R N, SREEDHARA B M. Investigation of concrete produced using recycled aluminium dross for hot weather concreting conditions[J]. Resource-Efficient Technologies, 2016, 2(2): 68-80.
[7] MURAYAMA N, MAEKAWA I, USHIRO H, MIYOSHI T, SHIBATA J, VALIX M. Synthesis of various layered double hydroxides using aluminum dross generated in aluminum recycling process[J]. International Journal of Mineral Processing, 2012, 110/111: 46-52.
[8] �� ��, ������, ��˶, ФϸԪ. ��Ӧ���淨��������AlN��ˮ����Ϊ[J]. �й���ɫ����ѧ��, 2016, 26(4): 919-927.
ZHANG Yong, GUO Zhao-hui, WANG Shuo, XIAO Xi-yuan. Hydrolysis behavior of AlN in aluminum dross with response surface methodology[J]. The Chinese Journal of Nonferrous Metals, 2016, 26(4): 919-927.
[9] �����, �� ��, ����ƽ, �� ��, �齨��, �ƽ���. ��������ĩ��ˮ����Ϊ�о�[J]. Ӧ�ÿƼ�, 2009, 36(9): 1-5.
XU Lin-wei, LIU Meng, HU Dang-ping, ZHANG Yu, HONG Jian-ming, TANG jian-cheng. Hydrolysis behavior of AlN powders[J]. Applied Science and Technology, 2009, 36(9): 1-5.
[10] FUKUMOTO S, HOOKABE T, TSUBAKINO H. Hydrolysis behavior of aluminum nitride in various solutions[J]. Journal of Materials Science, 2000, 35(11): 2743-2748.
[11] �� ��, ������, ���Ѷ�, �� �, Ҧ Ȫ. ������AlN��ˮ����Ϊ[J]. �й���ɫ����ѧ��, 2012, 22(12): 3555-3561.
JIANG Lan, QIU Ming-fang, DING You-dong, SU Nan, YAO Quan. Hydrolysis behavior of AlN in aluminum dross[J]. The Chinese Journal of Nonferrous Metals, 2012, 22(12): 3555-3561.
[12] LI Qi, YANG Qun, ZHANG Guo-fan, SHI Qing. Investigations on the hydrolysis behavior of AlN in the leaching process of secondary aluminum dross[J]. Hydrometallurgy, 2018, 182: 121-127.
[13] �ܳ���, �� ��, ���ľ�, �� ΰ. �������а����Ļ���[J]. �������������, 2012(3): 38-41.
ZHOU Chang-xiang, WANG Qing, ZHANG Wen-juan, ZHAO Wei. The recovery of ammonia nitrogen from aluminum slag ashes[J]. Conservation and Utilization of Mineral Resources, 2012(3): 38-41.
[14] GB 5009.5��2016. ʳƷ��ȫ���ұ� ʳƷ�е����ʵIJⶨ[S].
GB 5009.5��2016. National food safety standard determination of proteins in foods[S].
[15] SHINZATO M C, HYPOLITO R. Solid waste from aluminum recycling process: characterization and reuse of its economically valuable constituents[J]. Waste Management, 2005, 25(1): 37-46.
Hydrolysis behavior of AlN in aluminum dross and its multivariate nonlinear regression analysis
L�� Shuai-shuai, NI Wei, NI Hong-jun, ZHU Yang-yang
(School of Mechanical Engineering, Nantong University, Nantong 226019, China)
Abstract: The modified equation of AlN content in aluminium dross was put forward by studying the change of each component and its content in the process of aluminium dross hydrolysis reaction. The effects of hydrolysis parameters such as time, temperature and rotational speed on the hydrolysis rate of aluminium dross were investigated according to the measure of AlN content and pH of suspension. The hydrolysis parameters and the modified content of AlN in aluminium dross were analyzed by multivariate nonlinear regression analysis. The results show that the AlN content in the aluminum dross and the pH value of the suspension reduce with the increase of temperature. The hydrolysis of AlN can be effectively promoted with the prolongation of time, and the pH value of the suspension is simultaneously raised to a high level within 2 h. The rotational speed has no obvious effect on the hydrolysis rate of AlN and the pH value of suspension. Generally speaking, the way of the content of AlN is more objective than the pH value of suspension to characterize the hydrolysis rate of AlN in aluminum dross. Multivariate nonlinear regression analysis and secondary simplification on the hydrolysis parameters and the modified content of AlN in aluminium dross show that the relative error between the theoretical value and the experimental value is within ��8.65%, which has a certain guiding significance for the prediction and control of the modified content of AlN in aluminum dross during the hydrolysis process.
Key words: aluminum dross; AlN; hydrolysis; multivariate nonlinear regression analysis; temperature; rotational speed; time
Foundation item: Project(��2018��87) supported by the University Advantageous Discipline Construction Engineering Plan of Jiangsu Province, China; Project(BE2018093) supported by the Key Research and Development Plane of Jiangsu Province, China; Projects(201702, 201703) supported by the Wall Material Innovation Research Plan of Jiangsu Province, China; Projects(JC2018115, JCZ18024) supported by the Application Research Development Plan of Nantong City, China
Received date: 2019-05-20; Accepted date: 2019-11-19
Corresponding author: NI Hong-jun; Tel: +86-15962957962; E-mail: 949215056@qq.com
(�༭ ������)
������Ŀ�����ո�У����ѧ�ƽ��蹤��������Ŀ(��2018��87)������ʡ�ص��з��ƻ���Ŀ(BE2018093)������ʡǽ����ϸ��¿�����Ŀ(201702��201703)����ͨ��Ӧ���о��ƻ�������Ŀ(JC2018115��JCZ18024)
�ո����ڣ�2019-05-20�������ڣ�2019-11-19
ͨ�����ߣ��ߺ�������ڣ���ʿ���绰��15962957962��E-mail��949215056@qq.com
ժ Ҫ��ͨ����������ˮ�ⷴӦ��������ּ��京���仯���о��������������AlN������������ʽ������AlN����������ҺpHֵ�IJⶨ������ʱ�䡢�¶ȡ�ת�ٵ�ˮ�������AlNˮ�����ʵ�Ӱ�첢������ж�Ԫ�����Իع��������������������¶��ܽ�����������AlN��������������ҺpHֵ���ӳ�ʱ�����Ч�ٽ�AlN��ˮ�⣬ͬʱ��2h������ҺpHֵѸ����������λ��ת�ٶ�AlNˮ�����ʺ�����ҺpHֵ������Ӱ�졣������ԣ�AlN����������ҺpHֵ���ܿ۱�����������AlNˮ�����ʡ���ˮ���������������������AlN�������ж�Ԫ�����Իع���������μ���������ֵ��ʵ��ֵ������ܡ�8.65%��
[1] �� ��. ���������ʼ����е�AIN�ڱ��պ�ˮ������е���Ϊ�о�[D]. ����: ������ѧ, 2008: 1-3.
[2] ��Զ��, �� ��, �� ��, �� ��, �� ʤ, ����ΰ. ���ҵ��ۺ�����[J]. �й���ɫұ��, 2008(6): 63-67.
[5] ��ǿǿ. ��������������ש������[D]. ��: �㽭ʦ����ѧ, 2016: 15-48.
[8] �� ��, ������, ��˶, ФϸԪ. ��Ӧ���淨��������AlN��ˮ����Ϊ[J]. �й���ɫ����ѧ��, 2016, 26(4): 919-927.
[9] �����, �� ��, ����ƽ, �� ��, �齨��, �ƽ���. ��������ĩ��ˮ����Ϊ�о�[J]. Ӧ�ÿƼ�, 2009, 36(9): 1-5.
[11] �� ��, ������, ���Ѷ�, �� �, Ҧ Ȫ. ������AlN��ˮ����Ϊ[J]. �й���ɫ����ѧ��, 2012, 22(12): 3555-3561.
[13] �ܳ���, �� ��, ���ľ�, �� ΰ. �������а����Ļ���[J]. �������������, 2012(3): 38-41.
[14] GB 5009.5��2016. ʳƷ��ȫ���ұ� ʳƷ�е����ʵIJⶨ[S].
GB 5009.5��2016. National food safety standard determination of proteins in foods[S].


