��ѧ�ϳɷ��Ʊ�п����ظ�������п���
��ռ��1��������1��������2����С��1��������1
(1. ���ϴ�ѧ ��ѧ����ѧԺ������ ��ɳ��410083��
2. ������ɫ�����о�Ժ������ ������710016)
ժ Ҫ��
ժ Ҫ����Ħ����Ϊ1?2.02��Ca(OH)2��ZnOΪԭ�ϣ�ͨ����ѧ�ϳɷ��Ʊ�п��ơ�����X�������䡢���ط��������ȷ�����ѭ�������Լ�ģ���صij�ŵ�ȷ��������Ʊ�����Ʒ���б������о�������������Ƶ�п�����Ʒ�Ļ�ѧ���ΪCa(OH)2��2Zn(OH)2��2H2O����Ʒ�Ŀ��������ֲ����ȣ�ƽ������Ϊ23.18 ��m���Ը�п���Ϊ�����������ʵ�ģ��п����ؾ��кܸߵķŵ�ƽ̨���ﵽ1.686 V���Ƶõ�п��Ƶ�ʵ�ʱ�����Ϊ195.8 mA��h/g���ﵽ�����۱�������56.4%��
�ؼ��ʣ�
��ѧ�ϳɷ����ŵ�ƽ̨��п�����п�������ѭ����������
��ͼ����ţ�TM 912.2 ���ױ�ʶ�룺A ���±�ţ�1672-7207(2008)05-0918-05
Preparation of calcium zincate as negative electrode material for Ni/Zn battery by chemo-synthesis method
YANG Zhan-hong1, WANG Sheng-wei1, ZENG Li-hui2, WANG Xiao-hua1, LIU Dong-ren1
(1. School of Chemistry and Chemical Engineering, Central South University, Changsha 410083, China;
2. Northwest Institute for Non-ferrous Metal Research, Xi��an 710016, China)
Abstract: Calcium zincate was prepared by chemo-synthesis method from Ca(OH)2 and ZnO with the molar ratio of Ca(OH)2 to ZnO of 1?2.02. The sample was characterized by XRD, TGA, particle size analysis, cyclic voltammetry and charge-discharge test of simulated Ni/Zn battery. The results show that the chemical composition of sample is Ca(OH)2��2Zn(OH)2��2H2O. The sample consists of well dispersed particles with diameter about 23.18 ��m. The simulated Ni/Zn battery has very high discharge plateau of 1.686 V, as well as a discharge capacity of 195.8 mA��h/g, which approaches 56.4% of the theoretical specific capacity.
Key words: chemo-synthesis method; discharge plateau; calcium zincate; Ni/Zn battery; cyclic voltammetry
���Զ���п���������б�������ԭ���ϼ۸���ˡ��������ӵȶԻ����������Ⱦ�����������ǵĹ㷺��ע[1-2]���ر����ڵ綯�������綯���г��ͱ�Яʽ�����ȵ��ռ�Ӧ�ã�п������Ǿ��о�Ӧ��DZ��������ʹ�ü�ֵ�Ķ�����Դ�����ǣ�п�缫��֦���������ܽⸯʴ���缫���ε�����������Լ��п����صĿ�������[3-5]��
20����80��������Ƿ���п��ƶ�п�缫�������кܴ����[6-8]��֮��ʼ��п��Ƶ��Ʊ����������˴������о���Renuka��[9]ͨ��ѭ�����������о���п�缫�����Ӽ������������SnO��Ni(OH)2��Co(OH)2�ĵ绯ѧ���ԣ������͵�[10]ͨ����ѧ�ϳɷ��Ʊ���п��ƣ����о�����绯ѧ���ܣ�Zhang��[11]��NaOH��NH4OH�Ļ�ϼ�����Һ�У����û�ѧ���������ϳ���п��ƣ�Sharma��[12-13]�о���ͨ��������п���͵�KOH��Һ�л��������������Ʋ����Ͻ����Ƶ�п��ƣ�Zhu��[14-15]��ˮ��Һý���У����û�е��ĥ�Ʊ���п��ƣ������ܵ�[16]ͨ����ĥ���Ʊ�п��ƣ������˽���H2O��KOH��Ӱ�죻����ɽ��[17]ͨ��������п�κ����ڹ���������������Һ�й������Ʊ���п��ƣ�����Ⱥ��[18]ͨ����ѧ�ϳɵķ����Ʊ���п��ƣ�������˵�һ���п����Ʊ����ա�
���������Ʊ�п��Ƶķ������������ڴ��ģ�����������ȣ���ǿ�����Ʊ���п�����Ҫ����������ˮ��ϴ��ֱ�������ԣ��Ʊ����ϴ�ӹ���ķѴ�������������������Σ����û�е��ĥ�Ʊ�п��Ƶķ�����ÿ���Ʊ��������٣�����Ҫ��ʱ����ĥ��ֻ�ʺ���ʵ�����Ʊ���
Ϊ��Ѱ�Ҹ����ÿ��е�п����Ʊ����������������ڲ�������ǿ��������£�ͨ����ѧ��Ӧ���ϳ�п��ƣ����������ܽ����о���
1 ʵ ��
1.1 ��ѧ��Ӧ���ϳ�п���
��ѧ��Ӧ�ϳ�п��ư������·�Ӧ·�߽�����ƣ�
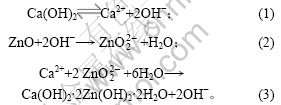
��Ӧ������������ˮ��Һ���ܽⲿ����ȫ���룬����ǿ�������������п����ǿ�����ܽ⣬ת��Ϊп�����������Һ�еĸ����ӽ�����ɳ������ʡ�������Ӧ��������Ӧ������С�ͬʱ����ʵ���У���Ӧ�ڼ�������½��У������˷�Ӧ�Ļ�ܣ���һ���ٽ��˷�Ӧƽ����������չ��
��������[19]����Ħ����Ϊ1?2.02�ı�����ȡCa(OH)2(��ѧ������¤����������)��ZnO(��ѧ������¤����������)�ڷ�Ӧ���У��������������ˮ����Ӧ�¶ȿ�����70~100 �档���Ͻ��裬������Ӧ12 h���õ����ɫ������Һ�������¾���12 h����ʹ��Ӧ���ɵ��»����ᄃ����г»���������ȥ�ϲ���Һ��Ưϴ1~2�μ���pHֵ���ڵ�7���پ������ˣ��õ������İ�ɫ���塣��50 ������и���5 h���õ����յĹ����ĩ��Ʒ��
1.2 X��������������ȷ��������ȷ���
X����������������ձ�Digaku D/max 2550VB+ 18KWת��X���������ǣ�ѡ��Cu��K�����䣬���ٵ�ѹΪ40 kV������Ϊ30 mA��ɨ���ٶ�Ϊ5 (?)/min������(TG)�������õ¹�NETZSCH STA449C�ۺ��ȷ����ǽ��У��������գ���������Ϊ10 ��/min����������Ϊ30 mL/min����������MICROTRAC S3500���������Ƕ���Ʒ�����Ƚ��з�����
1.3 п����Ƭ������
�����Ƶõ�п�����ʯī��PTFE��������(90?5?5)���л�ϣ�����һ����������ˮ�����Ƴɽ��ϣ�Ϳ���ڻ�ͭ���ϣ�����50 ������н��и��Ȼ�����ѹƬ���г�2 cm��2 cm�ij�Ʒ��Ƭ����Ʒп����Ƭ��п��Ƶľ�����Ϊ0.48 g��
1.4 ѭ����������
ѭ������ʵ������Ϻ�CHI-660b�绯ѧ����վ���в��ԣ�����װ�òο�����[13]�������缫Ϊ��п���Ϊ�������ʵķ�ĩ�缫����Hg/HgO�缫Ϊ�αȵ缫���������ƬΪ�����缫����Ĥ���þ���ϩ��֦Ĥ�����ҺΪ6 mol/L KOH��Һ��ɨ�跶ΧΪ-1.5~ -1.2 V��ɨ������Ϊ50 mV/s��
1.5 п��ģ���غ������ŵ�ʵ��
�Ƶõ�п����Ƭ����������Ĥ��ɵ�ؼ��飬���������л��������У�����һ������6 mol/L KOH���Һ��ģ���ؽṹ�ο�����[20]������BS-9300R���ε�����ܼ��װ�ý���ģ���صĺ������ŵ�ʵ�顣��ŵ��ƶ��������£������ܶ�Ϊ10 mA/cm2��������Ƶ�ѹΪ2.5 V���ŵ���ֹ��ѹΪ1.3 V��Ϊ�˱�֤���������ȫ�������������Զ���ڸ������������ʱ���趨Ϊ3 h��
2 ���������
2.1 п��Ƶ�X�����������
ͼ1(a)��ͼ1(b)��ʾ�ֱ�ΪCa(OH)2?2Zn(OH)2? 2H2O��ZnO�ı�X���߷�ĩ������ͼ�����Ƶõ�п��Ƶ�X����������������ͼ1(c)��ʾ���Ա�ͼ1(c)��ͼ1(a)���Կ�������2��Ϊ14.10?��28.48?��������1����ǿ������壬��Ӧ��п��ƾ���X��������<100><200>������������ա�ͨ����ѧ��Ӧ�ϳɵķ�ĩ���ϵ�����������Ļ�����������dz��Ǻϣ���������ϳɵ�п��Ʋ����Ǿ��е�б��ϵ�ṹ��Ca(OH)2?2Zn(OH)2?2H2O�����ͼ1(c)�д����������п��X���߷�ĩ�������Ӧ������壬����Ҫ����Ϊ�ڲ��û�ѧ��Ӧ�ϳɷ��Ʊ�п���ʱ��Ϊ��ʹ�������Ʒ�Ӧ��ȫ���������������п����ˣ����Ƶõķ�ĩ�д��������IJ�������п��ͬʱ����ͼ1(c)�в�û�з���Ca(OH)2������壬˵����ʵ����õĺϳɷ�����Ӧ�Ƚϳ�֡�
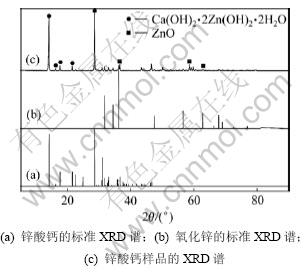
ͼ1 п��ƺ�����п��XRD���Լ�п�����Ʒ��XRD��
Fig.1 Standard XRD patterns of calcium zincate, zinc oxide and XRD pattern of calcium zincate sample
2.2 п�����Ʒ���ȷ���
п��Ƶ����ط��������ͼ2��ʾ���ɼ�����Ʒ��136 ���174 �� 2����������1��ʧ�����ȷ塣���ݡ���ѧ�����ٲ��ֲᡷ[21]��Zn(OH)2��ʧˮ�ֽ��¶�Ϊ125 �棬֣�Ľܵ�[22]������-Zn(OH)2�ķֽ��¶�Ϊ145 �档ͨ������õ�����2����ʧ��̨����������ʧ��Ϊ19.4%�����п��ƵĻ�ѧ��ɰ���Ca(OH)2��2Zn(OH)2��2H2O���з��������Լ������2���ᾧˮ���ѳ���Zn(OH)2ʧȥ1��ˮ���ӷֽ��������������ʧ��Ϊ23.38%������Ʒ�ڴ��¶������ʵ��������ʧ���Ըߡ���174 ����ֵ�ʧ�����ȷ��ǿ��ǿ��136 �洦��ǿ�ȣ�����Ҫ����Ϊ�ڴ˹����д���Zn(OH)2����ˮ�ֽⷴӦ��ͼ2����ʾ��415 ������˵�3��ʧ�����ȷ壬������ʧ��Ϊ5.1%������Ca(OH)2����ʧˮ�ֽ������������ʧ��5.84%�dz��ӽ������ǵ���Ʒ�д���δ��Ӧ��ȫ������п�Ͳ�����������Ϊ���������ض��ȷ��������Ӱ�죬���X����������������������Ϊ���Ʊ���п�����Ʒ�Ļ�ѧ�����Ca(OH)2��2Zn(OH)2��2H2O��
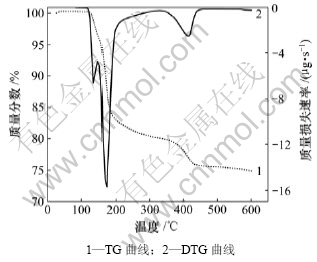
ͼ2 п��Ƶ����ط���
Fig.2 Thermogravimetric analysis of calcium zincate
2.3 п��ƹ����ĩ���ȷ���
ͼ3��ʾΪп�����Ʒ�����ȷ�������ͼ3�ɼ������Ʊ���п�����Ʒ�����ȳ�����̬�ֲ�������Ϊ23 ��m���ҵ�п�����Ʒռ�ı������d50 = 23.13 ��m��d90 = 35.28 ��m��������С�dz����ȣ�ƽ������Ϊ23.18 ��m��˵���Ʊ��������ƽϺá�
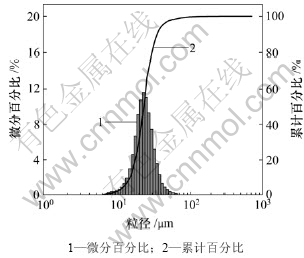
ͼ3 п�����Ʒ�����ȷ���
Fig.3 Particle size analysis of calcium zincate
2.4 ��ĩ�缫��ѭ���������Խ��
ͼ4��ʾΪп��Ʒ�ĩ�缫��ѭ�������� �ߡ��ɼ���п��Ƶ�������������ʾ�˱ȽϺõĶԳ��ԣ�����������Ϊ���ε�صĵ缫���ϡ�ͼ������������-1.33 V����1�������壬����������-1.42 V����1�������壬��Ϊп��Ƶ�������ͻ�ԭ�塣����-1.5 Vǰ��û�з������Եĵ����壬��˵��Ca(OH)2��ZnO�ķ�Ӧ�dz���֣����ʻ����ﵽ100%�����Ʊ���п�������������п�������٣���ˣ�����ZnO�������Ĺ���Ҳ�ɺ��ԡ�
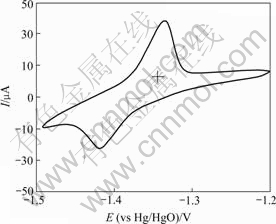
ͼ4 ��ĩ�缫��ѭ����������
Fig.4 Cyclic voltammogram of calcium zincate powder microelectrode
2.5 п��ģ���غ������ŵ�����
ͼ5��ʾΪ�����Ƶ�п���Ϊ�������ʵ�п��ģ���صķŵ����ߡ��ɼ����ŵ��ʼ��ѹΪ1.902 V��ģ���ؾ��зdz��ߵķŵ�ƽ̨���ﵽ1.686 V����������пΪ�����������ʵ�п����صķŵ�ƽ̨(1.65 V)��0.036 V����п�缫�ĵ缫��Ӧʽ���Ա�ʾΪ��
Ca(OH)2?2Zn(OH)2?2H2O+4e![]() Ca(OH)2+2Zn+
Ca(OH)2+2Zn+
4OH-+2H2O�� (4)
�ɷ�Ӧʽ(4)�ɼ����п��Ƶ����۵绯ѧ������Ϊ347 mA��h/g��ͨ����ģ���صķŵ����ݽ���ļ��㣬�Ƶõ�п�����Ʒ��ʵ�ʷŵ������Ϊ195.8 mA��h/g���ﵽ���۱�������56.4%��
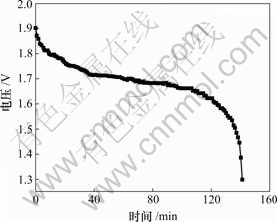
ͼ5 п��ģ���صķŵ�����
Fig.5 Discharging curve of simulated Ni/Zn battery
3 �� ��
a. ͨ����ѧ��Ӧ���ϳ�п��ơ��ϳɷ�Ӧ�¶ȿ�����70~100 �棬��Ӧʱ��Ϊ12 h�����ó»�12 h���˹��ձȼ�������ǿ����Ʊ����ղ��������и�ǿ�Ŀ����Ժ����õ������ɱ���
b. XRD���������ط������֤ʵ���ϳɵ���ƷΪп��ƣ��仯ѧ�����Ca(OH)2��2Zn(OH)2��2H2O��
c. ���ô˹����Ʊ���п�����Ʒ���ȳ���̬�ֲ������������ֲ����ȡ�
d. п��ƾ��нϺõĵ绯ѧ���ܣ���п���Ϊ�����������ʵ�ģ��п����ؾ��кܸߵķŵ�ƽ̨���ﵽ1.686 V���Ƶõ�п��Ƶ�ʵ�ʱ�����Ϊ195.8 mA��h/g��
�ο����ף�
[1] Jindra J. Progress in sealed Ni-Zn cells, 1991-1995[J]. Journal of Power Sources, 1997, 66(1): 15-25.
[2] ���ı�. �ܷ�п����ط�չ����[J]. ��Դ����, 2000, 24(3): 178-180.
ZHANG Wen-bao. Review of the progress in sealed nickel-zinc battery[J]. Chinese Journal of Power Sources, 2000, 24(3): 178-180.
[3] ������, ��ռ��, ɣ�̱�, ��. ���Һ���Ӽ����ܷ�п����ص�Ӱ��[J]. ��Դ����, 2007, 31(1): 45-48.
ZENG Li-hui, YANG Zhan-hong, SANG Shang-bin, et al. Influence of different electrolyte additives on sealed Ni-Zn battery[J]. Chinese Journal of Power Sources, 2007, 31(1): 45-48.
[4] Zhu J L, Zhou Y H, Gao C Q. Influence of surfactants on electrochemical behavior of zinc electrodes in alkaline solution[J]. Journal of Power Sources, 1998, 72(2): 231-235.
[5] ����ƽ. ����綯����п����ص��о�[J]. ��Դ����, 1995, 19(1): 37-40.
ZHAO Yun-ping. Studies on overseas rechargeable nickel-zinc batteries for electric vehicle applications[J]. Chinese Journal of Power Sources, 1995, 19(1): 37-40.
[6] Gagnon E G, Wang Y M. Pasted-rolled zinc electrodes containing calcium hydroxide for use in Zn/NiOOH cells[J]. Electrochem Soc, 1987, 134(9): 2091-2096.
[7] Gagnon E G. Effects of KOH concentration on the shape change and cycle life of Zn/NiOOH cells[J]. Electrochem Soc, 1986, 133(10): 1989-1995.
[8] Yuan Y F, Tu J P, Wu H M, et al. Effect of ZnO nanomaterials associated with Ca(OH)2 as anode material for Ni-Zn batteries[J]. Journal of Power Sources, 2006, 159(1): 357-360.
[9] Renuka R, Srinivasan L, Ramamurthy S, et al. Cyclic voltammetric study of zinc and zinc oxide electrodes in 5.3 M KOH[J]. Applied Electrochem, 2001, 31(6): 655-661.
[10] ������, ���, ������, ��. п��Ƶ��Ʊ���绯ѧ�����о�[J]. ���, 2001, 31(2): 65-67.
YU Jing-xian, YANG Han-xi, ZHU Xiao-ming, et al. Studies on preparation and electrochemical performance for calcium zincate[J]. Chinese Battery Bimonthly, 2001, 31(2): 65-67.
[11] Zhang C, Wang J M, Zhang L, et al. Study of the performance of secondary alkaline pasted zinc electrodes[J]. Applied Electrochem, 2001, 31(9): 1049-1054.
[12] Sharma R A. Physico-chemical properties of calcium zincate[J]. Electrochem Soc, 1986, 133(11): 2215-2219.
[13] YU Jing-xian, YANG Han-xi, Ai Xin-ping, et al. A study of calcium zincate as negative electrode materials for secondary batteries[J]. Journal of Power Sources, 2001, 103(1): 93-97.
[14] Zhu X M, Yang H X, Ai X P, et al. Structural and electrochemical characterization of mechanochemically synthesized calcium zincate as rechargeable anodic materials[J]. Applied Electrochem, 2003, 33(7): 607-612.
[15] ������, ���, ������, ��. п��Ƶ���ĥ���ϳɼ���绯ѧ����[J]. Ӧ�û�ѧ, 2003, 20(6): 528-531.
WANG Xiao-dan, YANG Hua-bin, MENG Xian-ling, et al. Electrochemical properties of calcium zincate synthesized by ball-milling method[J]. Chinese Journal of Applied Chemistry, 2003, 20(6): 528-531.
[16] ������, ��˩��, ����ɽ. ��ĥ���Ʊ�п����о�[J]. �绯ѧ, 2005, 11(1): 72-76.
LI Sheng-xian, TIAN Shuan-bao, ZHU Shao-shan. Calcium zincate prepared by ball mill method[J]. Chinese Electrochemistry, 2005, 11(1): 72-76.
[17] ����ɽ, ������. п��ƵĹ������Ʊ���[J]. ���, 2004, 34(2): 114-115.
ZHU Shao-shan, LI Sheng-xian. Preparation of calcium zincate by coprecipitation method[J]. Chinese Battery Bimonthly, 2004, 34(2): 114-115.
[18] ����Ⱥ, ������, ������. ��һ��п��Ƶ��Ʊ�[J]. ��Դ����, 2006, 30(8): 633-636.
ZHAO Yi-qun, ZHANG Zheng-fu, MA Ming-yi. Preparation of single-phase calcium zincate[J]. Chinese Journal of Power Sources, 2006, 30(8): 633-636.
[19] ɣ�̱�, ��ӳӨ, �ư���, ��. ���Ӽ�����п����������ˮ���Ʊ���Ӱ��[J]. ���Ϲ�ҵ��ѧѧ��: ��Ȼ��ѧ��, 2000, 31(4): 327-329.
SANG Shang-bin, GU Ying-ying, TANG Ai-dong, et al. The effect of additives on hydrothermal preparation of nanometer Mn, Zn ferrite particles[J]. Journal of Central South University of Technology: Natural Science, 2000, 31(4): 327-329.
[20] �¹�ƽ, �±���, ɣ�̱�, ��. ȫ��̬����Cd/Ni���ε�ص��Ʊ��Լ�����[J]. ���ϴ�ѧѧ��: ��Ȼ��ѧ��, 2004, 35(4): 604-608.
CHEN Guo-ping, CHEN Bao-ji, SANG Shang-bin, et al. Preparation of solid state alkaline Cd/Ni second cell and its properties[J]. Journal of Central South University: Science and Technology, 2004, 35(4): 604-608.
[21] ������. ��ѧ�����ٲ��ֲ�[M]. ����: ��ѧ��ҵ������, 2003.
LI Meng-Long. Concise handbook of chemical date[M]. Beijing: Chemical Industry Press, 2003.
[22] ֣�Ľ�, �� ��, ���λ�, ��. ��-Zn(OH)2������Ʊ��������о�[J]. ����ʦ����ѧѧ��: ��Ȼ��ѧ��, 2001(2): 20-23, 54.
ZHENG Wen-Jie, YANG Fang, ZENG Xin-Hua, et al. Preparation and charactrization of ��-Zn(OH)2 crystal[J]. Journal of South China Normal University: Natural Science, 2001(2): 20-23, 54.
�ո����ڣ�2007-12-17�������ڣ�2008-02-03
������Ŀ�����ҿƼ�֧�żƻ�������Ŀ(2006BAE03B03)
ͨ�����ߣ���ռ��(1969-)���У�����������, ����, ��ʿ����ʦ, ���µ绯ѧ�о����绰��0731-8879616��E-mail: zhyang@mail.csu.edu.cn


