DOI: 10.11817/j.ysxb.1004.0609.2021-39757
���⾫�����������
�� �1, 4�����γ�1���ڱ껪1��Ѧ����2���Ź���3�������4
(1. �人�Ƽ���ѧ ����ұ���¹��պ���ʡ�ص�ʵ���ң��人 430081��
2. �人�Ƽ���ѧ ʡ�������ͻ������ұ������ص�ʵ���ң��人 430081��
3. �����Ƽ���ѧ ����ұ���¼��������ص�ʵ���ң�����100083��
4. ��ɽ(����)�²����о�Ժ����ɽ 528200)
ժ Ҫ��
���������¶Ի��⾫�������������Ϊչ�������о�����������ģ����Ϸ���TG-DTA��SEM-EDS������ѧ����FactSage 7.3�ȷ������ֶζ�ʵ�������з��������������������723 K��773 K�²�����ȫ������Ȼ�����¶�����873 Kʱ����������ȫ����������������(MoO3)���ڽϸ��¶��£���873 K��773 Kʱ��������������չ����ɽ��滯ѧ��Ӧ���٣�Ȼ���ڽϵ��¶��£���723 Kʱ���滯ѧ��Ӧ���κ˳���ģ��ͬ�������á���Ӧ�����У������ɳ�ʼ������̬��ת��ɾ��в�״�ṹ��Ƭ״��ò�������ھ���ָ��(020)��(040)��(060)��(0100)�Ⱦ����������ǿ���������ӣ��������ɵ�MoO3����һ���ĸ������Ժ����ų��������⾫����������չ��̷��ϻӷ�-�����������ڼ�����������м�����������(MoO2)�����ɡ����չ����в������ս������Ǿֲ��¶ȵ����ߺ͵��۵㹲������γɹ�ͬ�������¡��������ѧ���ݱ��Ļ����۷�������Ҫ����Ԫ���ڱ��չ����е��ݱ���ɼ�����ս���Ϊ��Ӱ����ƣ��������Ч�����ս��������Ŀ��з�����
�ؼ��ʣ�
���⾫�������������������������ս�������
���±�ţ�1004-0609(2021)-07-1952-13���� ��ͼ����ţ�TF841���� ���ױ�־�룺A
���ĸ�ʽ���� �, ���γ�, �ڱ껪, ��. ���⾫�����������[J]. �й���ɫ����ѧ��, 2021, 31(7): 1952-1964. DOI: 10.11817/j.ysxb.1004.0609.2021-39757
WANG Lu, LI Meng-chao, QUE Biao-hua, et al. Oxidation roasting of molybdenite concentrate[J]. The Chinese Journal of Nonferrous Metals, 2021, 31(7): 1952-1964. DOI: 10.11817/j.ysxb.1004.0609.2021-39757
���⾫������������(MoO3)�Ʊ����������Ʒ��ӹ�����Ҫԭ����[1]��ʵ�ʹ�ҵ������һ����ö���¯���תҤ¯���������������[2]��������ʡ�����н�ѳ���ҵ�ɷ�����˾����8~12���ı��ն���¯[3]���������ֽα��ջ��⾫�����Ҫԭ�ϣ����չ����У�����ԭ�����ϲ����Ҫ����
������Ӧ���ɶ�������(MoO2)�����²��MoO2��������������MoO3���������չ��̺�ʱһ��ϳ������屺�չ��̴��¿�������ʽ(1)��(2)��ʾ[4]��
MoS2+3O2=MoO2+2SO2 (1)
MoO2+0.5O2=MoO3 (2)
������ҵ���棬�������ߴ����������ڸ�¯�������еõ��˹㷺Ӧ�ã�ұ��Ч�ʴ�����[5-6]�����ڴˣ�̽��һ���µı��չ��գ�ʹ���⾫���ڸ������������¿����������ճ�MoO3�ܵ�����ұ������ר�ҵĹ㷺��ע������о�Ҳ���������˱���[7-9]����ǰ�ڹ�����[10]����������ͬ���Դ��������»��⾫�������������Ϊչ�����о���Ȼ������ijЩ����Ľ��ͣ���ʱδ�ܸ����㹻��֤�ݡ��������ڽ�һ���������к�����̽��֮��ϴ��������ܵ�ɨ���������������ѧ���ݣ����۷�����������Ԫ�ڱ��չ����е��ݱ���ɼ�����ս����������Ӱ����ƣ��Ƕ�ǰ�ڹ���[10]���ݵ�һЩ��������ý��۵���֤��
1 ʵ��
1.1 ʵ��ԭ��
��������ʵ��ԭ��Ϊ��������ʡ�����н�ѳ���ҵ�ɷ�����˾�Ļ��⾫���仯ѧԪ���������(��������)��Mo��54.89%��S��33.27%��Si��1.83%��Fe��1.12%��Ca��0.28%��Al��0.19%��K��0.14%��Ti��0.04%��Pb��0.08%��Cu��0.07%��C��0.17%��P��0.01%������������Ԫ������Na��Mg�ȡ�ԭ�����ྭXRD�������ȷ������Ҫ�ɷ�Ϊ������(MoS2)����ò��ɨ����������۲��������̬�������ִ��ҷֲ�������[10]��
1.2 ʵ�鲽��
���⾫���ڴ����������������յ�ʵ�鲽����ǰ�ڹ���[10]�����й���ϸ���������ڴˣ����Ķ�����м�Ҫ������ԭ�Ͼ�383 K������12 h��ȡ3 g������Ʒ����ߴ��СΪ 50 mm��25 mm��20 mm(����������)�������������У����ԼΪ5 mm���˺�װ����Ʒ����������ʯӢ���ڣ��ܷ���ò�ͨ������ž����ڿ�����Ȼ��ʯӢ�ܻ���������������ָ����Ӧ�¶ȵ�Si-C��¯�ĺ����������¶��ȶ�������г�������ʼ��Ӧ��һ��ʱ��������л�������б�������ʯӢ��ȡ��¯����ȴ������Ʒ��ȴ������ʱ�ر������ȡ����Ʒ���г���������ʵ�����������ڲ�ͬ�¶����趨��ͬ�ķ�Ӧʱ����з������о��¶�Ϊ723 K��773 K��873 K��ʵ�����֮���ռ���Ʒ�������������ͺ��н���ṹ�۲��������������Է�Ӧ�����еĶ���ѧ��Ϊ�ͷ������ս������������������
2 ���������
2.1 ����ѧ����
���Ķ�723K��773K��873 K�»��⾫���ڲ�ͬ��Ӧʱ�䷴Ӧǰ��������ֱ�����˳�������ʽ(3)����������ʧ�ʽ��м��㣬�ó���ͬ��Ӧ�����»��⾫���������ʧ�����ߣ������ͼ1(a)��ʾ[10]��
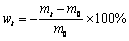 (3)
(3)
ʽ�У�mt��m0�ֱ�Ϊ����Ӧʱ��t��������ͳ�ʼ��������ʼ����Ϊ3 g����ͼ1(a)���Կ����������������ʧ�����ŷ�Ӧʱ����ӳ����������¶�Խ�ߣ���������Խ�졣�ڷ�Ӧʱ��ӽ�20 min(723 K��ԼΪ25 min)ʱ�����������������ʧ�ʾ���ƽ̨���¶�Խ�ߣ�ƽֵ̨Խ�����¶�Ϊ723 K��773 K��873 Kʱ����������������ʧ�ʵ�ƽ��ֵ�ֱ�Ϊ9.8375%��10.5865%��11.4330%��������������ǰ�ڹ���[10] XRD������������֪(����������ݼ�����[10])��������723 K��773 Kʱ��δ����ȫ����������ΪMoO3�Ͳ���δ����ȫ������MoS2����873 Kʱ������ȫ����������ΪMoO3���������չ����У�����������Ԫ��MoO2δ�ܲ��������������京���������³���XRD���������[10]��
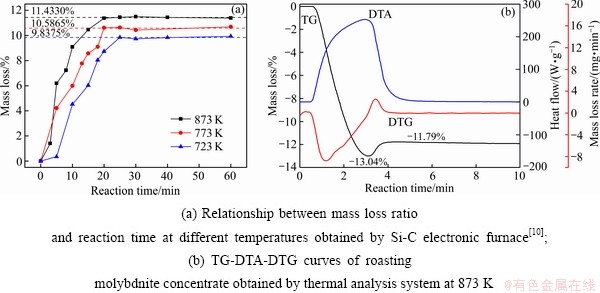
ͼ1 ���������»��⾫����������ն���ѧ����
Fig. 1 Kinetic curves of roasting molybdenite concentrate in oxygen atmosphere
Ϊ��һ���������⾫���������չ����е������������������873 KΪ�������˻��⾫�����������е��������ն���ѧʵ�飬�����ͼ1(b)��ʾ����Mo(54.89%)��S(33.27%)��Ԫ�ػ�ѧ�ɷֿ���֪������Mo��S��Ħ����1:2���л����γ�MoS2����S�������Բ��㣬Mo������������ʣ��Ϊ���ڷ��������ļ���Sȫ��MoS2��ʽ����(��ʵ��������ܲ�������Ϊ������������Ԫ��Ҳ�п����γ���Ӧ������)����ˣ���S�����Ʋ�Ļ��⾫��ľ���(MoS2�ĺ���)ԼΪ82.17%��������Mo�����������ʽ���ڡ��ٶ����⾫���е�����������ֲ�����������Ӧ������������ȫΪMoO3ʱ������ʧ��ԼΪ8.2%����������ȫΪMoO2ʱ������ʧ��ԼΪ16.4%������ͼ1(b)��TG����(��ɫʵ��)��֪�����ŷ�Ӧʱ��IJ����ӳ�����Ӧ���������ʧ�������ӣ���ʱ��ԼΪ3.15 minʱ������ʧ�ʴﵽ���Ϊ13.04%���˺����ŷ�Ӧʱ��ļ����ӳ���������ʧ�ʿ�ʼ��С����������ʧ��ԼΪ11.79%ʱ�ﵽƽ̨���������߽�����������⾫��ﵽƽ̨ʱ��������ʧ����ͼ1(a)��Si-C��¯ȡ�������ﵽƽ̨ʱ��������ʧ����ֵ�������Ȼ11.79%��11.43%��Ȼ��⾫����ȫ������MoO3ʱ��������ʧ����ֵ(8.2%)����ƫ��Ȼ�����ղ������ȴΪMoO3����������⾫���л������������ӷ���������֡���ʱ��11.79%����Ϊ�ǵ�ǰ����ԭ����ȫ����ʱ������������ʧ�ʡ���ͼ1(a)��773 K��723 K�¶���ԭ�ϵ�����������ʧ��ֵ�����ڴ���ֵ����Ҳ˵����773 K��723 K�»��⾫��δ����ȫ��������ͼ1(b)���ɿ��������������ʧ��(13.04%)������ȫ������MoO2��MoO3����������ʧ��֮�䣬˵����ʱ����Ⱥ���MoO2���ֺ���MoO3���ݴ˿�����֪������������ʧ�ʿ�ʼ��С�Dz���MoO2�������������¡���ˣ����⾫����ȫ������MoO3(�練Ӧʽ(4)��ʾ)����Ϊ�����η�Ӧ��ɣ�����MoS2����������������MoO2���緽��ʽ(1)��ʾ��������ɵ�MoO2������������MoO3���緽��ʽ(2)��ʾ��������ͬʱ���С�MoO2�ǻ��⾫���������չ��̵��м�������Ӧʱ��Ϊ3.15 min����ʱ��������ʧ�ʴﵽ���ʱ����ΪMoO2�����ɷ�Ӧ�����������˺�MoO2��������Ӧռ�����������⣬����ͼ1(b)�е�DTA����(��ɫʵ��)��֪�������������չ��̾�Ϊ���ȷ�Ӧ���ڷ�Ӧ���ڷ���ЧӦ��Ϊ�����Ҵﵽ���˵��MoO2��������Ӧ��MoO2�����ɷ�Ӧ����ЧӦ��Ϊ�������ų����������࣬�������ܹ���ʹ���չ����еľֲ���Ӧ�¶�Ѹ��������DTG���(��ɫʵ��)���������⾫��ԭ�ϵ�������ʧ�������ŷ�Ӧʱ��������ӿ죬��ʱ��ԼΪ1.12 minʱ�ﵽ��죬���������ʧ���ʻ�����Сֱ��Ϊ0(ʱ��ԼΪ3.15 min)���˺�MoO2��������Ӧռ��������Ʒ��������ʼ��������������������ͬ���������Ӻ��Сֱ��Ϊ0��
MoS2+3.5O2=MoO3+2SO2 (4)
�����������������ǰ�ڹ���[10]�������ο��о�[4]���й����֣�Ȼ����ȱ�����䷴Ӧ����ѧ��ϵͳ���������Ľ�Si-C��¯�ֶ�ȡ������ȡ�����¶��µ�ƽ��������ʧ�ʼٶ��ɸ����¶��¾�����ȫ����ʱ�����������ʧ�ʣ����ù�һ�������������䶯��ѧ���з��������з�Ӧ���ȿɱ�ʾ��һ��ʱ���ھ����ʵ��������ʧ�������������ʧ��֮�ȣ���ʽ(5)��ʾ��
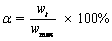 (5)
(5)
ʽ�У�wmaxΪ�����¶��¾�����ȫ����ʱ�����������ʧ�ʣ������Դ�ƽ̨ʱ��ƽ��������ʧ�ʽ��б�ʾ��
ͨ��ʽ(5)��ԭ�ϵķ�Ӧ�����뷴Ӧʱ��Ĺ�ϵ�ɱ�ʾ��ͼ2(a)��ʾ�����ò�ͬ�ķ�Ӧģ�Ͷ�ͼ 2(a)�е����ݽ��ж����ϣ�������ֻ�ѧ��Ӧģ��(��ʽ(6))�ܹ��ܺõض�ʵ�����ݽ��б�������ͼ2(b)~(d)��ʾ��
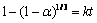 (6)
(6)
ʽ�У�kΪ��Ӧ���ʳ�������ͼ2(b)~(d)���Կ������ڽϸ��¶��£���873 K��773 K��ģ����Ͻ����ʵ���������ݾ������õ����Թ�ϵ��������ʱ��ѧ��Ӧģ�;���һ���ĺ����ԣ���873 K��773 K�¾�����������չ����ɽ��滯ѧ��Ӧ���١�Ȼ���ڽϵ��¶��£���723 K��ģ�ʹ��������ʵ���������ݵ����Թ�ϵ�����ɹۣ�����ʵ�����ݵ�ֲ������ֱ���·��������Ƿ�Ӧ��ʼ��(��ͼ2(b))���������¶���������Ӧ�����ɻ��ɻ�ѧ��Ӧ���١���ʵ�ϣ��ڽϵ��¶��µĻ�ѧ��Ӧ��������κ��볤�����ռ�ݺܴ�һ�����������ã������������㹻��ͳߴ��㹻��ʱ�����ٻ��ڲ��п��ܷ����ı䡣����723 K�£��������������ǰ�ڹ��̺��п���������������κ��볤����٣�֮������ת��ɾ���������֮��Ļ�ѧ��Ӧ���٣�����ʱ�ɺ��볤��ͻ�ѧ��Ӧ��ͬ�������á���ʵ�ʹ�ҵ����¯���תҤ¯�ڵ��������չ����У���Ӧ�¶�ͨ��ά����873 K���߸��ߣ��Ӷ���ѧ�Ƕȷ�����ѧ��Ӧ����ռ�����������ڻ������������ն���ѧ�������о����������ط���������������о�����������ù�������ά���滯ѧ��Ӧ���٣��뱾�Ľ�����[11]��
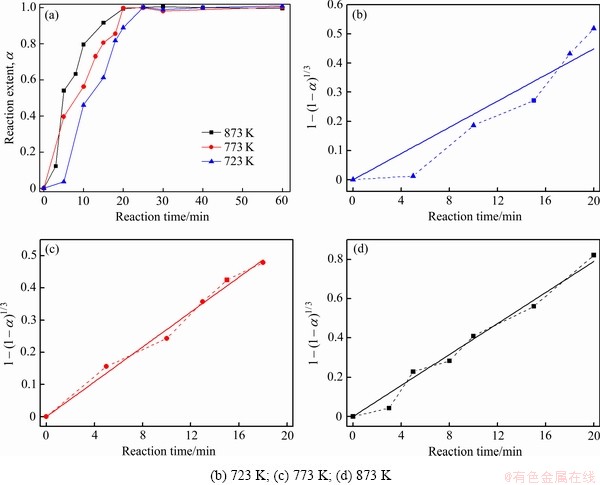
ͼ2 ��ͬ�¶��·�Ӧ�����뷴Ӧʱ��Ĺ�ϵͼ����ͬ�¶���1-(1-��)1/3�뷴Ӧʱ��Ĺ�ϵͼ
Fig. 2 Relationship between reaction extent with reaction time at different temperatures(a) and relationship between value of 1-(1-��)1/3 and reaction time at different temperatures((b)-(d))
2.2 ��Ӧ��������
��������[10]��������Ʒ�ķ�ĩ��ò���������䷴Ӧ����������������ŷ�Ӧʱ����ӳ�����Ʒ�ɿ���״��ת���ϸ���ı�Ƭ״�����ִִ��Ƭ״������������ž��嵱�����������γɵ������壬���ȿɴ�1 mm�����������ɼ���������ǰ�ڹ���[10]�����ϣ������Ʒ�ĺ��н���ṹͼ������ѧ���ݼ������䱺����Ϊչ�������������ƺ����������䷴Ӧ������
��Ʒ����������ĥ�������ɨ������������й۲죬�����ͼ3��ʾ������5 min����Ʒ��ض�����ִ���ϸС��(��ͼ3(a))������ǰ�ڹ���[10]�ķ�ĩ��ò����ͼ��δ�����֣���ʱ��������ɴ�����������SO2���ݳ����¡�10 min�����ɴ�����״�����֯��һ���γ�һ��������״�ṹ�ĺ��н���(��ͼ3(b))����ĥ��������ʱ��һЩ���ص����������ɼ�����������д���Ƭ״���γɣ�������֮�������(��ͼ3(c))����ЩƬ״���Ǵӵײ����ʵ��лӷ����������������ɡ���ͼ3(c)���ɷ��֣�����ϸС��С����ײ����ʽ�Ͻ��ܣ������ɴ�������ơ�����ЩϸС�����������(��ͼ3(d)��1)�������������ҪԪ�����ΪMo��O����Ħ���Ƚӽ�3:1��������������Ҫ�ɷ�ΪMoO3���������������������ɷֽ�Ϊ���ӣ��Ȱ���Mo��O��������S��Al��Ԫ�أ�Al������Դ��ԭ���е�������֣�S��Դ��δ����ȫ�����Ļ��⾫����Щδ�ӷ�����Ļ��ʻ���������������Ԫ�Ĵ����γɵĸ��۵������Ρ�40 min��������ȫ����(��ͼ1(a)����ʾ������ʧ�����ߺ�����[10])���������ɴ���ϸ�������(��ͼ3(e))�������н�����ƽ����ϸ������״����������ɼ�(��ͼ3(f))����ȿɴ������𣬳��ȿɴ�20 ��m�����Ҿ��ȷֲ�����ͼ���档��ĩ��òͼ��ʾϸ����״����ֵ��͵�����Ƭ״�ṹ(��ͼ4(a))���Ҵֲ�η�������Ե�⻬���ݶ����ԡ�XRD������(��ͼ4(b))������Щ����Ƭ״�������ⴿ�Ƚϸߣ���������嶼��Ӧ������������(PDF��Ƭ��5-508��a=3.962 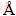 ��b=13.858
��b=13.858 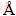 ��c=3.697
��c=3.697 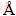 )�������ھ���ָ��Ϊ(020)��(040)��(060)��(0100)��������ر�ǿ�ң�˵����ʱ��õ�����Ƭ״��������ӵ��һ���ĸ������ԣ��������ų������ԡ�
)�������ھ���ָ��Ϊ(020)��(040)��(060)��(0100)��������ر�ǿ�ң�˵����ʱ��õ�����Ƭ״��������ӵ��һ���ĸ������ԣ��������ų������ԡ�
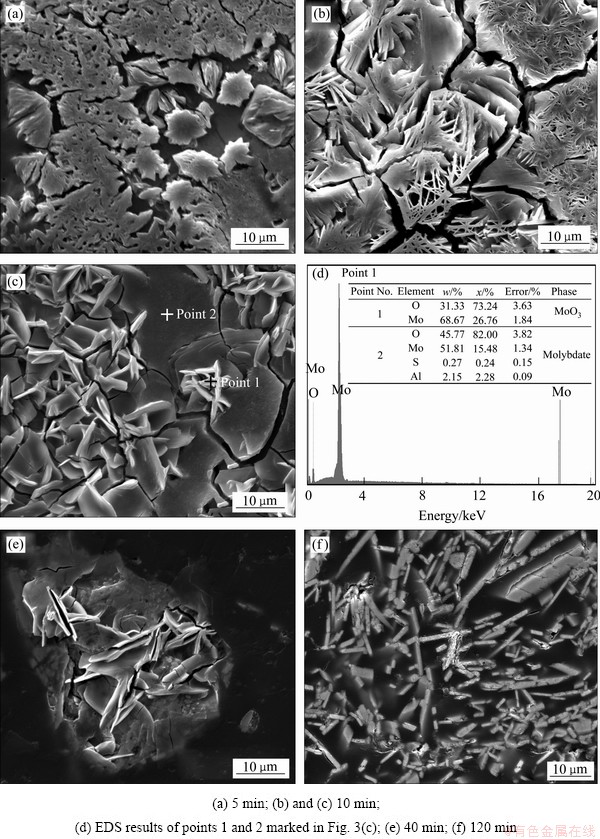
ͼ3 ���⾫����873 K���������б��ղ�ͬ��Ӧʱ������ĺ��н���ṹͼ
Fig. 3 Images of cross-section structure of samples obtained by roasting molybdenite concentrate roasted at 873 K for different time
ͼ5��ʾΪMo-S-O��Ԫ��ϵ��873 K�²���FactSage 7.3[12]���Ƶ�������ͼ(�����¶ȣ���773 K��723 K�������֮���ƣ����IJ����ṩ)�����Կ�����MoS2��������MoO3�Ĺ����У���Ҫ�����м����MoO2��һ���ڣ��÷�����ͼ1(b)�е��������߽��������ۺ����Ͻ�������⾫���������ճ�Ƭ״��������ķ�Ӧ���̿��������£��ڸ��»��������������У������ڷ�Ӧ�ij�ʼ�λ������������ɶ������⣬��ͼ1(b)��ͼ5��ʾ�����ڼ��ߵ�����ѹ�ͷ�Ӧ�¶ȣ������ɵĶ��������漴�������������������⣬������ͬʱ������ͬʱ���С����������о�[10]��֪����ʱ�����������������ӦС����������������ʣ�ʹ�伸�����ܵõ����ۣ�������Ӧ�������������ʼ�պܵͣ�����XRD���似���������ܽ�������������ɷ�Ӧ���̶������ⲻ�����ɵļ������ͬʱ��������������ϸߵĻӷ����Լ������������ձ����ķ������ԣ���ԭ�ϱ����γɵ��������⼫�ӷ�����Զ��(Զ�뷴Ӧ����)���������ڽϵ��¶��������������ص�����״̬���ӷ�Ӧ���������κ˴��γ�һ�����������ŵ�������������������������ſ�Ϊ������������Ļӷ�-�����ṩ�ݾ���Ϊ������������������ӵ����������ṩ����λ�㡣��Ӧ�����о���Ͷ�����������ϱ������京��Ҳ���٣��ų�������Ҳ��֮���Ϸ����仯�����º�����������Ļӷ�-����·�̲���ȫ��ͬ����ˣ��ں�����������ij���������γ�һ�����ƽ���״�ı���ṹ����Ӧ����Խ�࣬�¶�Խ�ߣ���������ӷ�-����·��Խ������Ӧ����Խ�٣��¶�Խ�ͣ��ӷ�-����·����Խ�̡����⾫���������յķ�Ӧ���̿ɼ�Ҫ����Ϊ�ӷ�-������������ͼ6��ʾ���ý��������[13]���о�������������

ͼ4 ���⾫����873 K���������б���20 min���õ���״�������ò��XRD��
Fig. 4 Powder micrograph(a) and XRD pattern(b) of needle-like product obtained by roasting molybdenite concentrate at 873 K for 20 min
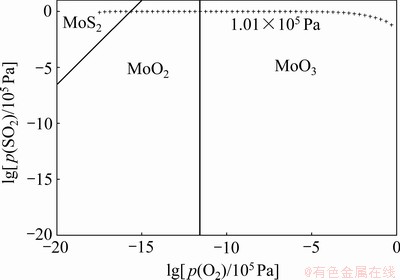
ͼ5 Mo-S-O��Ԫ��ϵ��873 K�µ�������ͼ
Fig. 5 Predominance phase diagram of Mo-S-O ternary systems at 873 K
2.3 �ս���Ϊ����
���⾫���ڴ��������б������ӽ���ȫʱ���ս�����Ҳ����֮�����������ֲ�������ν��ܵ��������ײ������һ���¶�Խ�ߣ��ս�����ԽΪ����[14-15]����ʵ�ʹ�ҵ����¯���չ����У��ս�����Ҳ��ʱ�����������¶���¯�ұ�ĥ�����أ�����豸ʹ������[16]����ˣ��о����չ����в�����ս���Ϊ�Ա����ս�����ķ��������ٲ���Ҫ���豸��ģ����;�����ʧ��Ϊ��Ҫ��Ϊ�ˣ�����������ǰ�ڹ���[10]�����ϣ���������������ѧ���ݼ��������ս���Ϊ�������������
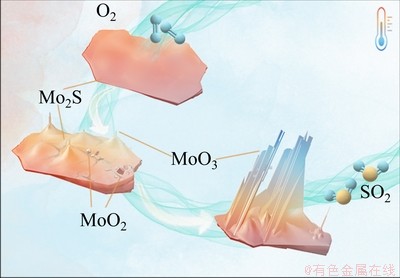
ͼ6 ����Ļ��⾫���������շ�Ӧ����ʾ��ͼ
Fig. 6 Schematic diagram of proposed possible oxidation roasting mechanism
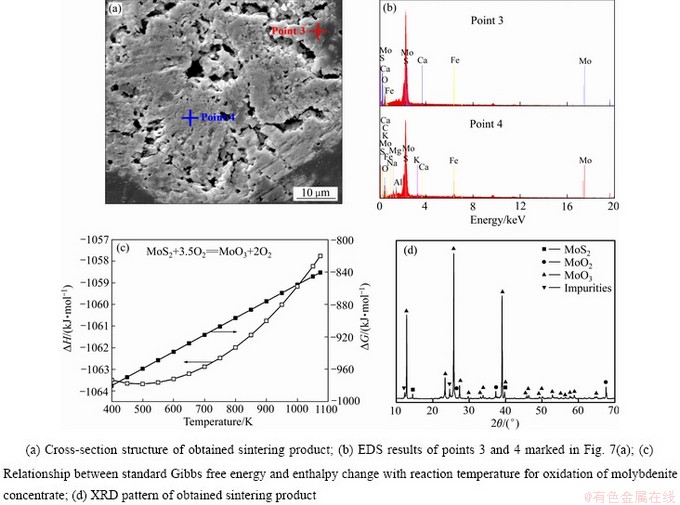
ͼ7 ���⾫����873 K���������б���40 min��ĵײ��ս����������
Fig. 7 Analysis results of sintering product obtained by roasting molybdenite concentrate in oxygen atmosphere at 873 K for 40 min
ͼ7(a)��ʾΪ�����ڴ��������б���40 min���ս����ĺ��н���ͼ�����Է��ֲ����������״̬����������Һ���Ѿ����ɡ�Һ������ɿ�������ǿ�ҵķ��ȷ�Ӧ����(��ͼ7(c))[12]����Ȼ�����¶Ȼ��⾫���ܵ�������Ӧ(��ʽ(4))���ʱ�ֵ�����������ƣ��������С��873 Kʱ�ʱ���Ϊ-1061 kJ/mol���������ȼ��࣬�ò��������ܹ�ʹ�ý����¶ȴ��������������������������۵��¶���ʹ���ڻ���XRD���������������ս�����г��˺������������⣬����������δ��ȫ������MoS2��MoO2(��ͼ7(d))����ʱMoO2�����ɻ��⾫��IJ�����������(��ʽ(1))��Ҳ������MoS2��MoO3�Ĺ��෴Ӧ����(��ʽ(7))�����⣬�������ʵ������Ҳ����������������ʱ�ս����ɷָ��Ӷ��������ʵõ��˸�����XRD�������״̬����һ���ľ����ԣ�������Ũ�ȵ���ijһ��ΧʱXRD���ܽ�������Ϊ�˸��õ�̽�������Ԫ����ɣ����Ļ�������������������������˼�⣬�����ͼ7(b)��ʾ������������ս���ﲻͬλ�õijɷ���ɾ���Ϊ���ӣ���������XRD�����ʾ��Mo��O��S��������Mg��Ca��Si��Al��Fe��Na��Ԫ�أ������⾫��Ĵ�������Ԫ�����ս���ﵱ�еõ��˸�����
MoS2+6MoO3=7MoO2+2SO2 (7)
����������Ԫ�ڱ��չ����е��ݱ���ɣ����Ľ�����������ѧ����FactSage 7.3[12]������з��������ڻ��⾫�����Ҫ���ΪMoS2����Ҫ������ԪΪMg��Ca��Si��Al��Fe�ȣ���˱�����Ҫ����⼸��������Ԫ������ѧ��ͼ�������۷�����
��������Ԫ��Mg(��873 KΪ��)����MoS2��������£���Ҫ��MgS��ʽ���ڣ��������������MgO������þ[(MgO)(MoO3)��MgMoO4]��������������ѹ��MoS2��ʼ�����������MoO2��MoO3����ʱMg��Ȼ��(MgO)(MoO3)����ʽ����(��ͼ8(c))��������ѹ�ӽ�1ʱ��Mg����Ҫ������ʽתΪ����þ(MgSO4)�����¶ȷ����ı�ʱ���Ա�723��773��873��973��1073 K��ȡ������ѧ���ݿ�֪��Mo-Mg-S-O��Ԫ��ϵ������ȶ����������������ƣ�����������ѹ���ߵķ����ƶ����¶�Ϊ723 K��773 K��873 K��973 Kʱ��Mg�����մ�����ʽ��ҪΪMgSO4��Ȼ�����¶�����1073 K������ʱ������Ҫ��(MgO)(MoO3)����ʽ����(��ͼ8)����˵����������������þ�������þ��Ϊ�ȶ�������þ�ڸ�������������ת�������þ�����ƣ�����������������ζ��Ը����ڸ������ȶ����ڡ�
����ʵ��������¶�Ϊ873 K����˱�����Ҫ��873 KΪ��������������Ԫ����Ԫ������ʽ�ݱ���ɵ�̽�֡���������Ԫ��Ca�����ݱ������Mg�������ƣ���MoS2�������������Ԫ��Ca��Ҫ��CaS����ʽ���ڣ���������ѹ�����ߣ�CaS�������������(CaSO4)�������[(CaO)(MoO3)��CaMoO4]��������������ѹ��MoO2��MoO3��(CaO)(MoO3)�Ļ����Ҳ��������ɣ�����ѹ�ӽ�1ʱ��Ca��Ҫ��CaSO4��ʽ���ڣ���ͼ9(a)��ʾ���������߷�Ӧ�¶ȣ�������Ԫ��Mg���ݱ���ɿ���֪��CaSO4���ջᱻ(CaO)(MoO3)��ȡ�����������ջ�ת��Ϊ(CaO)(MoO3)(����ѧ��ͼδ����)����������Ԫ��Si�������京������Ϊ�����������873 K�²���ͬ��Ϊ������������������ⷢ����Ӧ��������ڷ�Ӧ������ʼ����SiO2����ʽ���ڣ���ͼ9(b)��ʾ����ʱ��ʹ���������¶ȣ�Si�Ĵ�����ʽ��ȻΪSiO2(����ѧ��ͼδ����)����������Ԫ��Al����MoS2���ڵ�����£�Al��Ҫ��Al2O3����ʽ���ڣ���������ѹ�������ߣ�MoS2��������MoO2��Ȼ������MoO3����ͼ9(c)��ʾ��������ѹ�ӽ�1ʱ�����ղ���ΪMoO3��������(Al2(SO4)3)����Ȼ873 K������ѧ��ͼδ�ܷ���������(Al2(MoO4)3)���γɣ�����ʵ�ϸ���������MoO3��Al2O3�ᷢ����ѧ��Ӧ����������������������ǰ�ڹ���[17]�����Ժ�Ca��Al��Si��������Ԫ��ɵĹ�ҵ��������и��»ӷ�ʵ�飬�¶�Ϊ1273 K���������������������ȫ�ӷ�ʱ������Ԫ��Ca��Al��Si�ֱ���CaMoO4��Al2(MoO4)3��SiO2����ʽ���ڣ��뱾������ѧ����������������[17]ͬ����Ħ����Ϊ3:1�� MoO3��Al2O3�Ļ����1273 K�½����˸��±���ʵ�飬���ֵ���Ӧʱ���Ϊ10 minʱAl2(MoO4)3�ͻ����ɣ�����˵������������Al2(MoO4)3�ܹ��ȶ����ڡ���������Ԫ��Fe����Mo-Fe-S-O��Ԫ��ϵ��ͼ��֪������ѹ����ʱ����Ҫ�������ΪMoS2��FeS2����������ѹ�����ߣ�FeS2������������Fe3O4�����MoS2��������MoO2��������������ѹ��Fe3O4����������Fe2O3�����MoO2��MoO3����������(FeO)(MoO3)�Ļ����Ҳ������ɣ���һ����������ѹ������ΪMoO3��Fe2O3�����ۼ����������ڷ�Ӧ������Ӧ����������Ҳ�����ɣ���ͼ9(d)��ʾ���������Ԫ��Mg���¶ȱ仯���ݱ���ɿ���֪�����ŷ�Ӧ�¶ȵļ������ߣ�ͼ9(d)����������ڵ��ȶ�������ӦҲ�����ƣ��������γ���Ӧ�ĺ��������Ρ�
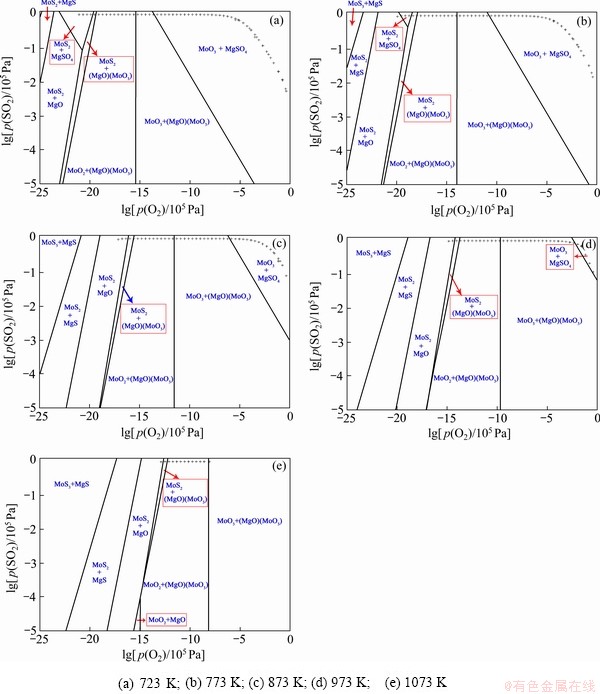
ͼ8 ��ͬ�¶���Mo-Mg-S-O��Ԫ��ϵ��������ͼ
Fig. 8 Predominance phase diagrams of Mo-Mg-S-O quaternary systems at different temperatures (��+��=1.01��105 Pa)
һ���棬������Ԫ���������չ������������ʽ��������ѹ���¶ȵı仯�ڲ��Ϸ����仯����һ���棬�ṹ�����仯��������Ԫ�������������ⷢ����Ӧ������Ӧ�����ε�����[18]���Ӷ��Ա�����Ϊ����Ӱ�죬�Ҳ�ͬ��������Ԫ��Ӱ��̶Ȳ�ͬ��Al��873 K�µ���Ҫ������ʽΪAl2(SO4)3����������������Ӧ��������������Al���������չ����м�������������Ӧ�ĵ��۵㹲����(�����������۵㹲����Ϊ��������������Ӧ�����η�����Ӧ���γɵ�һ�����)�����ս�����������Ӱ�죬����[19]Ҳ֤ʵ����һ�㡣Fe�ڷ�Ӧ�����л��γɲ����м���������Σ����������¶ȵ����ߣ������δ��ڵ��ȶ�����Ҳ�����ӣ�����Ca��Mg�Ľ�����ơ���ˣ��¶�Խ�ߣ�����Fe��MoO3���γɲ��ֵ��۵㹲���壬���ս��������һ��Ӱ�졣����Ca��Mg�������Ƶ�����ѧ��ͼ�����������չ����о���������Ӧ�������Σ��¶�Խ�ߣ�����������Խ�ȶ������۵㹲����Ҳ�����γɡ���MoO3��CaMoO4��999 K���Ҽ������ɵ��۵㹲���壬��Ӧ������ѧ��ͼ�μ�����[20]��MoO3��MgMoO4֮�������ѧ��ͼ��ͼ10��ʾ[21]����ͼ10���Է��֣�MoO3��MgMoO4�����γɵ��۵㹲���壬����MgMoO4����Ϊ19.5%ʱ���γɵĹ������۵��¶�ԼΪ1018 K����Ȼ���¶ȴ��ڱ��ĵ��о��¶�(873 K)������ǿ�ҷ��ȵı��շ�Ӧ�����£���Ӧ�����з�Ӧλ��ľֲ������¶ȼ��п��ܹ������ߣ��������ڸ��۵��¶ȼ�MoO3���۵�ֵ���ֲ���Ӧ�¶ȵ������ܹ���ʹ����(�����λ���������)�ۻ����γɵ�Һ����������ܱ߹���С���������������ܱ�δ��ȫ������MoS2�������У���ʹ����MoS2���ܽ�һ�����������ͬʱ��δ��ȫ������MoS2�ܹ���MoO3������Ӧ����MoO2������K��Na�����м��ߵķ�Ӧ���ԣ����շ�Ӧ�����У������γɵ������ξ�������MoO3������Ӧ�γ���Ӧ�ĵ��۵㹲���壬����MoO3��K2MoO4�γɵ��۵㹲������¶�ԼΪ753 K(MoO3��K2MoO4������ѧ��ͼ�μ�����[14])��MoO3��Na2MoO4�γɵĶ�Ԫ��ͼ��ͼ11��ʾ[22]����ͼ11��֪����MoO3����ԼΪ78%�������£�Na2MoO4��MoO3�γɵĹ������۵��¶�Ϊ813 K���ڴ������£���ʹ���չ��̷���ЧӦ�����ԣ���Ӧ�����ս�����Ҳ������������Ԥ�⣬�γɵ��۵㹲������¶�Խ�ͣ��ս�����Խ��������ϱ��Ľ���Ͳο�����[14, 19]��֪������K��Na�Ա��չ������ս������Ӱ����Ϊ���أ�Ca��Fe��Mg��֮��Al���ս�����Ӱ�첻�����ʺ�������Si���ս�����û��Ӱ�졣�ս���������ԭ�����ڸ�������Ԫ����MoO3֮���γɵĵ��۵㹲�����ڱ��չ����в����ۻ���Һ�壻ͬʱ�����ڻ��⾫����������ǿ�ҵķ���ЧӦ����Ӧ�����к������·�Ӧ�ֲ������¶����ߣ���ʹ����Ԫ�������κ�MoO3�γɵĵ��۵㹲�����ۻ������յ����ս������������������»��⾫������ȫ��������Na2MoO4��MoO3�ܹ��γ�813 K�ļ����۵㹲���壬��ˣ����ͷ�Ӧ�¶ȶ������ս�����ķ����ƺ���̫���롣һ����Ϊ���еķ����Ǿ����ܼ��پ����е�������ֺ���[23]�������Ƕ��������������γɵ��۵㹲�����Ԫ�أ���K��Na��Ca��Fe��Mg�ȡ����о���Ϊ��ҵ���⾫���չ����б����ս�����ķ�������߲��������Լ��ӳ�����¯���תҤ¯ʹ������������Ҫָ�����塣
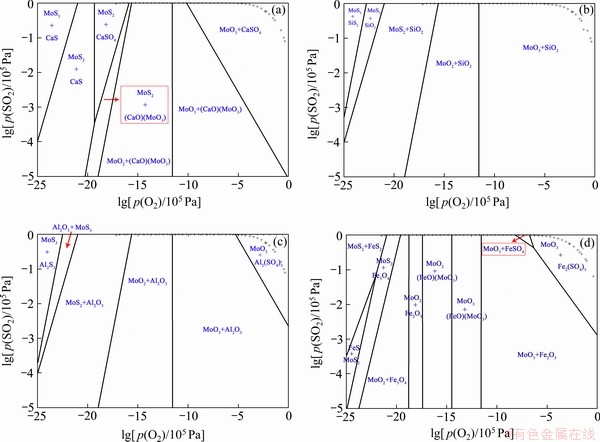
ͼ9 ��ͬ��Ԫ873 K��Mo-Me-S-O��Ԫ��ϵ��������ͼ(Me����Ca��Si��Al��Fe)
Fig. 9 Predominance phase diagram of Mo-Me-S-O quaternary systems at 873 K (Me represents Ca, Si, Al, and Fe) (��+��=1.01��105 Pa)
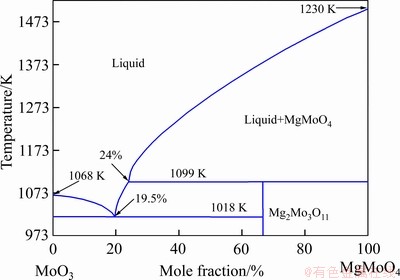
ͼ10 MoO3��MgO(MgMoO4)֮��Ķ�Ԫ��ͼ[21]
Fig. 10 Binary phase diagram of MoO3-MgO (MgMoO4) systems[21]
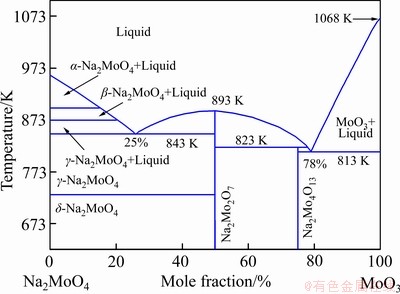
ͼ11 MoO3��Na2O(Na2MoO4)֮��Ķ�Ԫ��ͼ[22]
Fig. 11 Binary phase diagram of MoO3-Na2O (Na2MoO4) systems[22]
3 ����
1) 873 K�»��⾫���ܹ���ȫ��������Ƭ״MoO3���������̷��ϻ�ѧ��Ӧģ�ͣ�773 K��723 K�����£�������MoO3�Ͳ���δ��ȫ������MoS2��ɣ���Ӧ���ʷֱ��ɻ�ѧ��Ӧ�ͻ��ģ�Ϳ��ơ�
2) ���⾫���ճ���������Ĺ����а����������м���������������ɣ�������̬�ɿ�����״��ת���Ƭ״�ṹ�����ɵ����ղ������һ���ĸ������ԣ����ҷ��ֻ��⾫���ճ�Ƭ״��������Ĺ��̷��ϻӷ�-����������
3) ���ۼ���������������Ԫ�ڱ��չ������������ʽ����������ѹ���¶ȵı仯���Ϸ����仯��������Ϊ�ս�����ķ����Ǿֲ��¶ȵ����ߺ͵��۵㹲������γɹ�ͬ�������£���������Ԫ�غ�����������K��Na��Ca��Fe��Mg�ȣ��Ƚ��ͷ�Ӧ�¶��ڱ����ս�����ķ������������ʵ���С�
REFERENCES
[1] Ҧ Զ, ����, ���¿�. ���⾫���չ�������[J]. �й���ɫұ��, 2008, 37(2): 24-26.
YAO Yuan, LUO Dong-wei, FU Xin-ke. Comments on molybdenite concentrate roasting process[J]. China Nonferrous Metallurgy, 2008, 37(2): 24-26.
[2] WANG L, SUN W,ZHANG J, et al. A novel self-heated roasting technology for molybdenum concentrate[J]. Rare Metal Materials and Engineering, 2015, 44(11): 2618-2622.
[3] ������, ��ά��, �� �, ��. �����ұ������������չ��[J]. �й���ҵ, 2017, 41(6): 5-11.
BU Chun-yang, CAO Wei-cheng, WANG Lu, et al. Overview and prospect for the smelting process of molybdenite [J]. China Molybdenum Industry, 2017, 41(6): 5-11.
[4] ������, �ž���, �̾ž�, ��. �⾫���������ջ����о�[J]. �й���ҵ, 2011, 35(2): 17-19.
WANG Lian-yong, ZHANG Jing-fan, CAI Jiu-ju, et al. Study on mechanism of molybdenum concentrate roasting[J]. China Molybdenum Industry, 2011, 35(2): 17-19.
[5] �� ��, �� ��, �� ��, ��. �־���1�Ÿ�¯��������¯����ƥ�����[J]. �����о�ѧ��, 2020, 32(8): 720-726.
ZHANG Jian, WANG Kai, WANG Zhe, et al. Matching analysis of oxygen enrichment rate with furnace condition of No.1 blast furnace in ShougangJingtang[J]. Journal of Iron and Steel Research, 2020, 32(8): 720-726.
[6] ������. dz�������Ը�¯������Ӱ��[J]. ���ұ��, 2019(1): 18-20.
GUO Xiao-peng. Brief analysis on the effect of oxygen enrichment on ironmaking[J]. Tianjing Metallurgy, 2019(1): 18-20
[7] UTIGARD T. Oxidation mechanism of molybdenite concentrate[J]. Metallurgical and Materials Transactions B, 2009, 40(4): 490-496.
[8] PAUL R, THOMAS A. The oxidation kinetics of molybdenite at 525 �� to 635 ��[J]. Metallurgical Transactions, 1971, 2(3): 889-893.
[9] FU Y, XIAO Q, GAO Y. Pressure aqueous oxidation of molybdenite concentrate with oxygen[J]. Hydrometallurgy, 2017, 174: 131-139.
[10] WANG L, ZHANG G H, DANG J, et al. Oxidation roasting of molybdenite concentrate[J]. Transactions of Nonferrous Metals Society of China, 2015, 25(12): 4167-4174.
[11] SHIGEGAKI Y, BASU S, WAKIHARA M. Thermal analysis and kinetics of oxidation of molybdenum sulfides[J]. Journal of Thermal Analysis, 1988, 34(5): 1427-1440.
[12] BALE C, CHARTRAND P, DEGTEROV S. FactSage thermochemical software and databases[J]. Calphad- computer Coupling of Phase Diagrams and Thermochemistry, 2002, 33(2): 295-311.
[13] WILKOMIRSKY I, WATKINSON A, BRIMACOMBE J. Kinetics of oxidation of molybdenite[J]. Transactions of the Institution of Mining and Metallurgy Section C, 1997, 87: C16-C22.
[14] ������, ��ά��, �� �, ��. ������ս������о�[J]. �й���ҵ, 2018, 42(1): 8-11.
BU Chun-yang, CAO Wei-cheng, WANG Lu, et al. Study on the sintering phenomenon during the roasting processes of molybdenite by air[J]. China Molybdenum Industry, 2018, 42(1): 8-11.
[15] MARIN T, UTIGARD T, HERNANDEZ C. Roasting kinetics of molybdenite concentrates[J]. Canadian Metallurgical Quarterly, 2009, 48(1): 73-80.
[16] 袳���, ����. ����¯�����⾫����¶ȵ��������[J]. �й���ҵ, 2010, 34(5): 28-31.
JU Cheng-xin, GONG Yu-chuan. Temperature adjustment and control of roasting molybdenite in multi-hearth roaster[J]. China Molybdenum Industry, 2010, 34(5): 28-31.
[17] WANG L, ZHANG G H, SUN Y J, et al. Preparation of ultrafine ��-MoO3 from industrial grade MoO3 powder by the method of sublimation[J]. The Journal of Physical Chemistry C, 2016, 120(35): 19821-19829.
[18] �� ��, ������, �� ��, ��. ��Ʒλ�⾫���������չ��̵ķ�Ӧ��Ϊ[J]. �й���ɫ����ѧ��, 2014, 24(12): 3115-3122.
GAN Min, FAN Xiao-hui, ZHANG Lin, et al. Reaction behavior of low grade molybdenum concentrates in oxidation roasting process[J]. The Chinese Journal of Nonferrous Metals, 2014, 24(12): 3115-3122.
[19] WANG L, ZHANG G H, WANG J S, et al. Influences of different components on agglomeration behavior of MoS2during oxidation roasting process in air[J]. Metallurgical and Materials Transactions B, 2016, 47(4): 2421-2432.
[20] CHYCHKO A, TENG L, SEETHARAMAN S. MoO3 evaporation studies from binary systems towards choice of Mo precursors in EAF[J]. Steel Research International, 2010, 81: 784-791.
[21] ZHUKOVSKII V, YANUSHKEVICH T. Phase equilibria in the system MoO3-MgMoO4[J]. Physics of Metals and Metallography, 1968, 26(5): 959-960
[22] PETROSYAN Y, ZHUKOVSKII V, USTINOV O, et al. Phase equilibria in the system Na2MoO4-MoO3-NiO[J]. Russian Journal of Inorganic Chemistry, 1977, 22(10): 2841-2844.
[23] �� ��, ������, �����, ��. ��̼�������⾫�����ұ����������Ҫ����Ԫ�ص���Ϊ����[J]. �й���ɫ����ѧ��, 2020, 30(2): 438-446.
WANG Lei, GUO Pei-min, KONG Ling-bing, et al. Behavior analysis of main impurity elements in vacuum smelting of molybdenum concentrate with carbon[J]. The Chinese Journal of Nonferrous Metals, 2020, 30(2): 438-446.
Oxidation roasting of molybdenite concentrate
WANG Lu1, 4, LI Meng-chao1, QUE Biao-hua1, XUE Zheng-liang2, ZHANG Guo-hua3, LAN Wen-tao4
(1. Hubei Provincial Key Laboratory for New Processes of Ironmaking and Steelmaking, Wuhan University of Science and Technology, Wuhan 430081, China;
2. The State Key Laboratory of Refractories and Metallurgy, Wuhan University of Science and Technology, Wuhan 430081, China;
3. State Key Laboratory of Advanced Metallurgy, University of Science and Technology Beijing, Beijing 100083, China;
4. Foshan (Southern China) Institute for New Materials, Foshan 528200, China)
Abstract: The current work focus on the oxidation roasting behavior of molybdenite concentrate in high-purity oxygen atmosphere on the basis of the authors�� previous paper. The best modeling fit, TG-DTA, SEM-EDS and thermodynamic calculation method were adopted to analyze the experimental data. The results show that molybdenite concentrate cannot be reacted completely at 773 K and 723 K; when the temperature is increased to 873 K, however, the raw material can be oxidized to molybdenum trioxide (MoO3) completely. Combining the normalization and model fit methods, the work concludes that the rate-controlling step for the oxidization of molybdenite concentrate in the range of 773 K to 873 K is the interfacial chemical reaction. When the temperature is below 773 K, however, interfacial chemical reaction and nucleation and growth models both worked. It is also found that the morphology of obtained product transforms from previous particle shape to the final needle-like structure during the whole reaction process. XRD patterns show that the obtained needle-like product has an intense diffraction peak for the crystal indices of (020), (040), (060), and (0100), indicating its anisotropy and prior growth up tendency. Oxidation roasting processes of molybdenite concentration obey the vaporization- condensation mechanism with the formation of molybdenum dioxide (MoO2) as the intermediate product is also obtained. The study results also conclude that the occurrence of sintering phenomenon are due to the combined actions of the increase of local temperature and the formation of low-melting-point eutectics during the roasting process. With the help of FactSage 7.3 thermodynamic software, the transformation laws of the main impurities components and its effect on the sintering phenomenon during the roasting processes were also theoretically analyzed. The current work may play positive roles on understanding the roasting behavior of molybdenite concentrate and improve the service life of multiple heart furnaces.
Key words: molybdenite concentrate; oxidation roasting; molybdenum trioxide; sintering phenomenon
Foundation item: Project(2020CFB121) supported by the Natural Science Foundation of Hubei Province, China; Projects(2019A1515110361P) supported by the Guangdong Basic and Applied Basic Research Foundation, China; Project(2019ZYYD076) supported by the Central Government for Local Science and Technology Development of Hubei Province, China
Received date: 2019-09-28; Accepted date: 2020-12-20
Corresponding author: WANG Lu; Tel: +86-15600563937; E-mail: wanglu@wust.edu.cn
(�༭ ������)
������Ŀ������ʡ��Ȼ��ѧ����������Ŀ(2020CFB121)���㶫ʡ������Ӧ�û����о�������Ŀ(2019A1515110361P)�����������ط��Ƽ���չר��(2019ZYYD076)
�ո����ڣ�2019-09-28�������ڣ�2020-12-20
ͨ�����ߣ��� 责���ʦ����ʿ���绰��15600563937��E-mail��wanglu@wust.edu.cn
ժ Ҫ�����������¶Ի��⾫�������������Ϊչ�������о�����������ģ����Ϸ���TG-DTA��SEM-EDS������ѧ����FactSage 7.3�ȷ������ֶζ�ʵ�������з��������������������723 K��773 K�²�����ȫ������Ȼ�����¶�����873 Kʱ����������ȫ����������������(MoO3)���ڽϸ��¶��£���873 K��773 Kʱ��������������չ����ɽ��滯ѧ��Ӧ���٣�Ȼ���ڽϵ��¶��£���723 Kʱ���滯ѧ��Ӧ���κ˳���ģ��ͬ�������á���Ӧ�����У������ɳ�ʼ������̬��ת��ɾ��в�״�ṹ��Ƭ״��ò�������ھ���ָ��(020)��(040)��(060)��(0100)�Ⱦ����������ǿ���������ӣ��������ɵ�MoO3����һ���ĸ������Ժ����ų��������⾫����������չ��̷��ϻӷ�-�����������ڼ�����������м�����������(MoO2)�����ɡ����չ����в������ս������Ǿֲ��¶ȵ����ߺ͵��۵㹲������γɹ�ͬ�������¡��������ѧ���ݱ��Ļ����۷�������Ҫ����Ԫ���ڱ��չ����е��ݱ���ɼ�����ս���Ϊ��Ӱ����ƣ��������Ч�����ս��������Ŀ��з�����
[1] Ҧ Զ, ����, ���¿�. ���⾫���չ�������[J]. �й���ɫұ��, 2008, 37(2): 24-26.
[3] ������, ��ά��, �� �, ��. �����ұ������������չ��[J]. �й���ҵ, 2017, 41(6): 5-11.
[4] ������, �ž���, �̾ž�, ��. �⾫���������ջ����о�[J]. �й���ҵ, 2011, 35(2): 17-19.
[5] �� ��, �� ��, �� ��, ��. �־���1�Ÿ�¯��������¯����ƥ�����[J]. �����о�ѧ��, 2020, 32(8): 720-726.
[6] ������. dz�������Ը�¯������Ӱ��[J]. ���ұ��, 2019(1): 18-20.
[14] ������, ��ά��, �� �, ��. ������ս������о�[J]. �й���ҵ, 2018, 42(1): 8-11.
[16] 袳���, ����. ����¯�����⾫����¶ȵ��������[J]. �й���ҵ, 2010, 34(5): 28-31.
[18] �� ��, ������, �� ��, ��. ��Ʒλ�⾫���������չ��̵ķ�Ӧ��Ϊ[J]. �й���ɫ����ѧ��, 2014, 24(12): 3115-3122.


