�й���ɫ����ѧ�� 2003,(01),229-233 DOI:10.19476/j.ysxb.1004.0609.2003.01.042
Cu2+��Fe2+��T.f�����η�ĩ�缫��������Ϊ��Ӱ��
������ɫ�����о���Ժ,���ϴ�ѧ���﹤��ϵ,���ϴ�ѧ���﹤��ϵ,������ɫ�����о���Ժ,������ɫ�����о���Ժ ����100088 ,��ɳ410083 ,��ɳ410083 ,����100088���ϴ�ѧ���﹤��ϵ,��ɳ410083 ,����100088
ժ Ҫ��
Fe2 + ��������ϸ����������о�����Ҫ���� ,ϸ����ͭ������ ,Cu2 + �Ĵ��ڶ�T .f����������л��������Fe2 + ��������һ��Ӱ�졣�Ʊ���T .f������̼�۷�ĩ�缫 ,�о���Cu2 + ������Fe2 + ��T .f�����η�ĩ�缫�������ĵ绯ѧ��Ӧ���� ,���ⶨ����Ӧ�ĵ缫���̶���ѧ������ѭ�������о����� ,Cu2 + �Ĵ��ڲ�Ӱ��Fe2 + ��T .f�����η�ĩ�缫�ϵ�������Ӧ�Ŀ����ԡ��Ե缫��̬����̬�����о����� ,��Cu2 + Ũ���� 12mmol/L����ʱ ,Cu2 + �Ĵ��ڲ�������Fe2 + ��T .f�����η�ĩ�缫�ϵ����� ,����Cu2 + ��ǿT .f������Fe2 +��������������ӿ��˵�ɴ�������
�ؼ��ʣ�
ϸ������;T.f�����η�ĩ�缫;�绯ѧ����;
��ͼ����ţ� TF18
����飺�����(1971),��,������ʦ,��ʿ;
�ո����ڣ�2001-12-24
����������Ȼ��ѧ����������Ŀ (5 0 2 0 40 0 1);
Influence of Cu2+ on oxidation of Fe2+ on thiobacillus ferr oxidans modified powder microelectrode
Abstract��
The oxidation of Fe 2+ plays a v er y important role in bio-leaching, the exist of Cu 2+ has a un-excluded in fluence on the oxidation of Fe 2+ and the growth of thiobacillus ferrooxidans. Using the thiobacillus ferroxidans modified carbon powder microelectrode, the electrochemical mechanism of the i nfluence of Cu 2+ on the oxidation of Fe 2+ was studied. The Cyclic vo ltammetry study shows that the presence of Cu 2+ can not change the reversi bility of Fe 2+ oxidation reaction. Steady potentiodynamic and transient st air-step measurement demonstrate that the presence of Cu 2+ can not suppre ss the oxidation of Fe 2+ on the thiobacillus ferroxidans modified powder microelectrode. However when the concentration of Cu 2+ is under 15 mmol/L , it can enhance the mass transfer coefficient and accele rate the charge transfer rate of oxidation reaction
Keyword��
bio-leaching; thiobacillus ferroxidans modified powder microelectrode; electrochemistry mechanism;
Received�� 2001-12-24
T.f��Ϊ����ұ�������̵���������, T.f������Ѹ������������Fe2+�Ի��������ά��������������л�� ��ϸ�����������, ���Fe2+���������������������: һ����, Fe2+������ΪT.f���������ṩ�����������������л, �ٽ�T.f����������ֳ, ����ϸ������, Ϊϸ�������ṩ����
1ʵ��
1.1 T.f�����롢 �����������η�ĩ�缫�Ʊ�
������������T.f�����ɹ㶫��ɽ���Կ��ˮ�з��롢 �����õ�, ������������Ҫѱ���� T.f���������ñ�9 K������, �����Ϊ(g/L):(NH4)2SO4 3.0, KCl 0.1, K2HPO4 0.5, MgSO4��7H2O 0.5, Ca(NO3)2 0.01, Fe2+ 9�� �����Լ���Ϊ������, ��������ȥ����ˮ����, ������pH������Ҫ��6 mol/L��H2SO4���ڡ�
�Ʊ����̵缫ʱ, �������ˮ���丯ʴ��һ��d 0.1 mm��20��50 ��m���ס� ȡ���״�ʯī��, ����һ������T.f��Һ, �����, �Ƴ�ϸ���������η�ĩ, T.f����ͨ��ϸ��������ڳ��ĵ�����ճ����̼������, ��һ��ʱ���, ѹ�벬���缫��, ѹ��ʱ����ĩ����ƽ����, ������ѹ�Ա�֤�缫����ƽ�����
1.2�绯ѧʵ��
��̬�������ߡ� ѭ���������ߡ� ��λ��Ծ���ߵȵIJⶨ�����õ��͵����缫��ϵ, ��T.f�����η�ĩ�缫Ϊ�����缫, �����Ȼ��ظʹ��缫Ϊ�αȵ缫, ��Ƭ�缫Ϊ�Ե缫, �αȵ缫�����缫֮���ɴ���³��ëϸ�ܵ��������ӡ� ��500 mL�ĵ�����, ��Ӣ��Solartron��˾��S1-1287 �绯ѧ����ϵͳ(�������λ�ǡ� �źŷ������� ������¼�ǡ� P�������� Corrware��Corrview��������)���в���, �����Ϊ������Cu2+������Fe2+��9KҺ�� ����9K����Һ�������õĻ�ѧҩƷ��Ϊ������, ������Һ��ϴ�Ӿ���ȥ����ˮ��
2���������
2.1Fe2+�����η�ĩ�缫������������
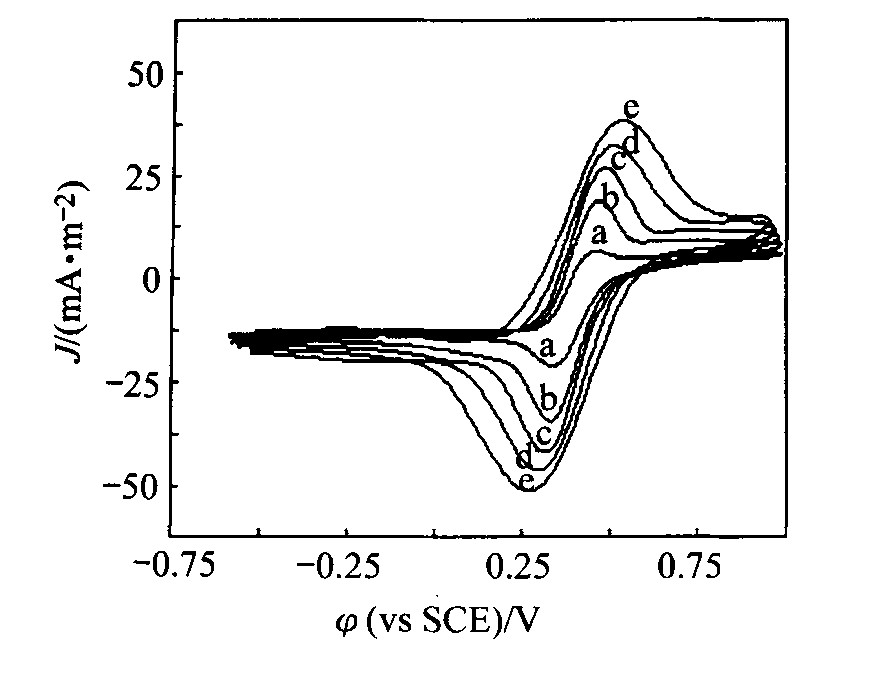
��ͬɨ���ٶ���, Fe2+��T.f������̼���缫��ѭ������������ͼ1��ʾ, ��ͼ��֪, ����ɨ���ٶȵ����ӷ��������, ���������ʼ��������������������, ���ݷ�ĩ�缫���ۼ���Fe2+��T.f�����η�ĩ�缫�������������о�, �����ƶϸ÷�ӦΪһ���淴Ӧ
ͼ1 Fe2+��T.f������̼���缫�ϵ� ѭ������ͼ
Fig.1 Cycle voltammograms of Fe2+ on T.f modified carbon micro electrode under different scan rates
(pH=2.0; ��=25 ��; c(FeSO4)=0.16 mol/L; Initial sweep: anode) a��1 mV/s; b��2 mV/s; c��3 mV/s; d��4 mV/s; e��5 mV/s
2. 2Cu2+��Fe2+��T.f���缫��������Ӧ��Ӱ��
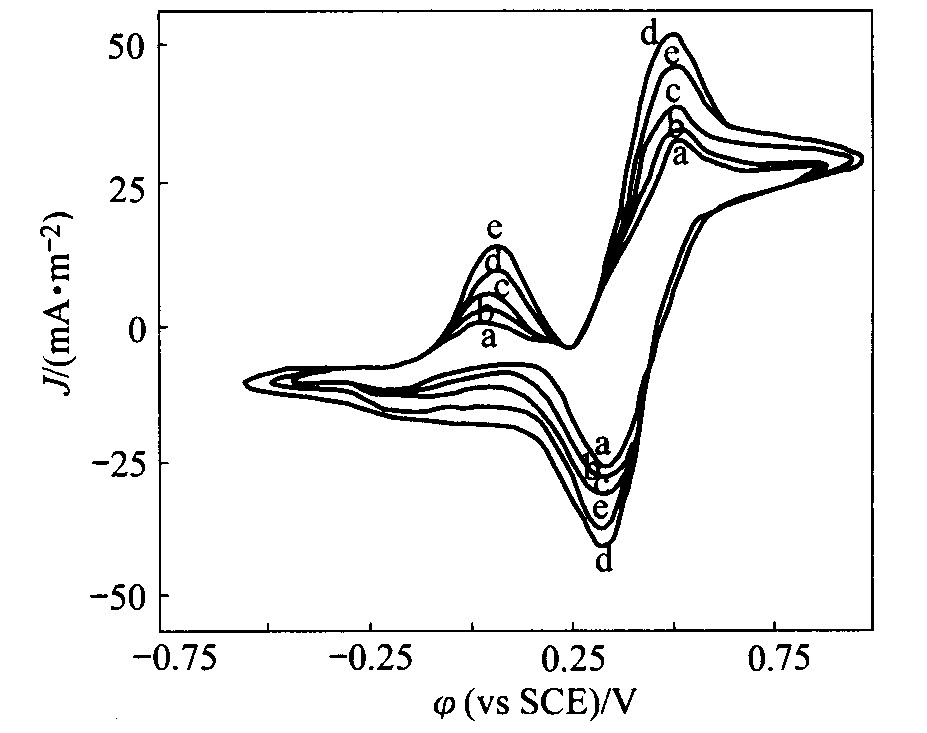
���벻ͬŨ�ȵ�Cu2+����, FeSO4Ϊ0.16 mol/Lʱ, T.f������̼���缫ѭ������������ͼ2��ʾ�� ��ͬCu2+����Ũ����ѭ���������߸������Ĺ�ϵ����1��
�����ʾ, ��ͬCu2+����Ũ��ʱ���������ʼ�պ�������������, �Ҧ� ��p���ֲ���, �ɼ�Cu2+���ӵļ��벻Ӱ�췴Ӧ�Ŀ����ԡ� ͬʱ�Ա�Cu2+���Ӽ���ǰ��Fe2+�����ķ����, ��֪��Cu2+С��12 mmol/Lʱ, ����Cu2+Ũ�ȵ�����, Fe2+���������������, ����Cu2+����12 mmol/Lʱ, Cu2+��Fe2+�����Ĵٽ������½�, ���뵱Cu2+Ũ�ȴﵽһ���̶�ʱ, T.f����л���Խ���, ����Fe2+�������½��йء�
����ͼ2��֪, ����=0.25 V����, ����Cu+����ΪCu2+�ķ�, ������Cu2+����Ũ�ȵ�����, ���������������, �˹���Ϊһ��������̡�
��1 ��ͬCu2+����Ũ����ѭ���������߸������Ĺ�ϵ
Table 1 Relation between sweep data and Cu2+ concentration
c( Cu2+)/ (mmol��L-1) |
Jp(Fe2+)/ (mA��m-2) |
Jp(Cu2+)/ (mA��m-2) |
�� ��p (Fe2+)/ V |
1.5 |
37.2 | - | 0.18 |
4.0 |
37.7 | 2.80 | 0.18 |
8.0 |
38.7 | 5.13 | 0.18 |
12 |
51.1 | 9.93 | 0.19 |
15 |
45.5 | 16.0 | 0.18 |
ͼ2 ��ͬCu2+Ũ����Fe2+��T.f������̼�� �缫�ϵ�ѭ������ͼ
Fig.2 Cycle voltammograms of Fe2+ on T.f modified carbon micro electrode in different Cu2+ concentration solution
(v=5 mV/s; pH=2.0; ��=25 ��; c(FeSO4)=0.16 mol/L; Initial sweep: anode) a��c(Cu2+)=1.5 mmol/L; b��c(Cu2+)=4 mmol/L; c��c(Cu2+)=8 mmol/L; d��c(Cu2+)=12 mmol/L; e��c(Cu2+)=15 mmol/L
2.3Cu2+����̬���̵�Ӱ��
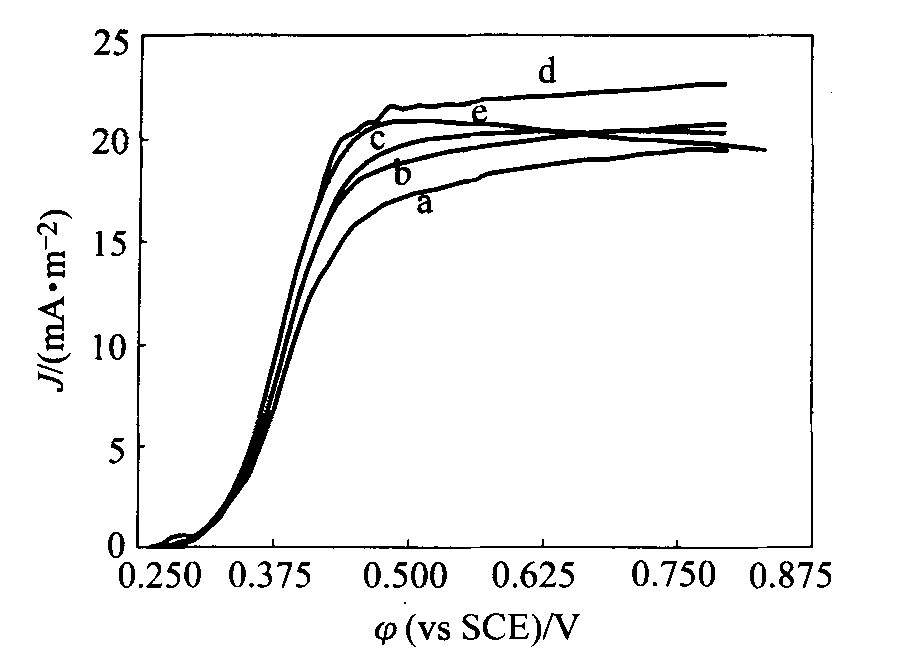
���벻ͬŨ��Cu2+��, T.f�����ε缫��̬���̼���������ͼ3��ʾ�� ��ͼ3��֪, ����Cu2+�ļ���, ��̬���� JL����, ˵��Cu2+��ϸ������FeSO4�м�ǿ����, ��Cu2+�ﵽһ��Ũ�Ⱥ�JL�½�, �������ڹ��ߵ�Cu2+��ϸ�������������������á� ��Cu2+Ũ����12 mmol/L����ʱ, Cu2+��ϸ������Fe2+���������ò�������, ����ѭ�������о����һ��, ΪT.f���ڽ���ͭ����ʱ, �Խ���Һ�е�Cu2+����һ�������������ṩ��һ��֤����
���ݵ缫��̬���̶���ѧ����
ͼ3 ��ͬCu2+Ũ����Fe2+��T.f������̼�� �缫�ϵ���̬��������
Fig.3 Steady-state polarization curves of Fe2+ on T.f modified carbon micro electrode in different Cu2+ concentration solution
(v=5 mV/s; pH=2; ��=25 ��; c(FeSO4)=0.16 mol/L) a��c(Cu2+)=1.5 mmol/L; b��c(Cu2+)=4 mmol/L; c��c(Cu2+)=8 mmol/L; d��c(Cu2+)=12 mmol/L; e��c(Cu2+)=15 mmol/L
2.4Cu2+����̬���̵�Ӱ��
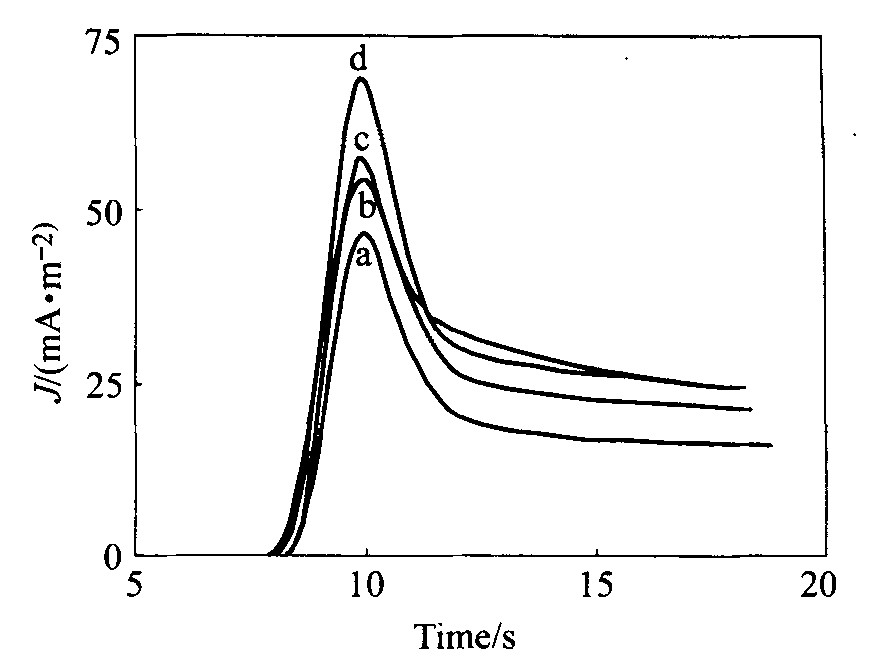
��FeSO4��Һ�м���Cu2+���ӵ�Ũ�Ȳ�ͬʱ, ��ϸ������̼���缫��λ��Ծ��ʱ��������õĵ缫��Ӧ�����ܶ�J��ʱ��t�ı仯��ͼ4��ʾ, ���ݵ绯ѧ�о�����
��2 Cu2+����Ũ���뼫����ɢ��������ɢϵ��D0�Ĺ�ϵ
Table 2 Relation between JL and D0 under different concentrations of Cu2+
c(Cu2+)/ (mmol��L-1) |
JL/(mA��m-2) | D0/(10-10m2��s-1) |
1.5 |
16.6 | 5.74 |
4.0 |
18.8 | 6.30 |
8.0 |
21.0 | 7.28 |
12 |
21.6 | 7.56 |
15 |
20.7 | 7.15 |
ͼ4 ��ͬCu2+Ũ��ʱ��λ ��ԾJ��t��ϵ
Fig.4 Potential stair step relation between J and t under different concentration of Cu2+
(��=200 mV; pH=2.0; ��=25 ��; c(FeSO4)=0.16 mol/L) a��c(Cu2+)=4 mmol/L; b��c(Cu2+)=8 mmol/L; c��c(Cu2+)=12 mmol/L, d��c(Cu2+)=15 mmol/L
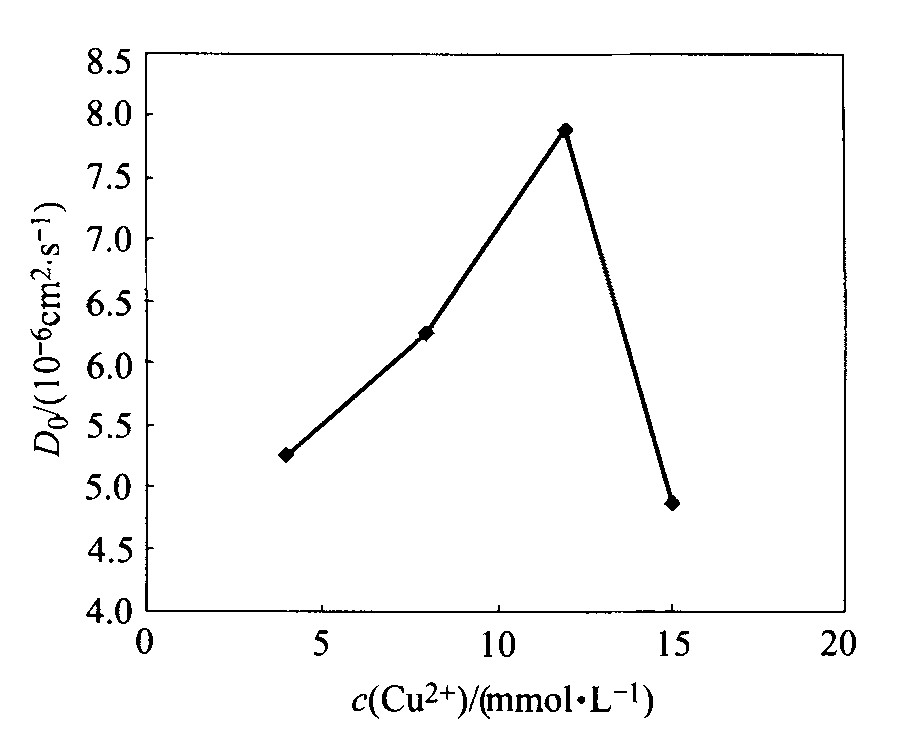
ͼ5 Cu2+Ũ�ȶ�D0��Ӱ��
Fig.5 Effect of Cu2+ concentration on D0
�����Ե缫��̬����̬���̵��о���֪, Cu2+��Fe2+��T.f�����η�ĩ�缫�������ļ�ǿ���������������Fe2+������Ӧ���̵�ɵĴ��ݡ�
3����
Ӧ��T.f�����η�ĩ�缫��ʾϸ������Fe2+��������Ӧ������������ ѭ�������о�����, Fe2+��T.f�����η�ĩ�缫�ϵ�������Ӧ��һ���淴Ӧ�� ��Cu2+Ũ����12 mmol/L����ʱ, Cu2+�Ĵ��ڲ�������Fe2+��T.f�����η�ĩ�缫�ϵ�����, ����4��12 mmol/L��Χ��, ����Cu2+������, ������Ӧ��ǿ, ��Ӧ�Ŀ���̶Ȳ��䡣 �Ե缫��Ӧ��̬����̬���̵��о�����, һ��Ũ��Cu2+�ļ����ʹFe2+��T.f�����η�ĩ�缫�ϵ�������Ӧ������ɢϵ������, ���Ʋ�����Cu2+��ǿT.f������Fe2+������������ӿ��˵�ɴ������ʡ�
�����