���±�ţ�1004-0609(2008)S1-0416-06
пұ���������������Ƽ������¼���
����ΰ������Ԫ�������࣬������
(���ϴ�ѧ ұ���ѧ�빤��ѧԺ����ɳ410083)
ժ Ҫ��
���пұ����ҵ����Ũ�ȶ����ؽ������������ԣ����������Ƽ����-ˮ���¹��ս��д�������ҵ�������й����ж����ἰ�������ˮ�и��ؽ����������ȵ�Ũ�Ƚ��м�⣬���Բ������������з���������������ؽ���Ũ�ȷֱ��ɹ�14.78~56.70 mg/L����13.71~40.15 mg/L��п20.50~58.90 mg/L��Ǧ12.8~64.2 mg/L����2.1~13.6 mg/L��ͭ0.54~1.44 mg/L����339~512 mg/L����472~3400 mg/L�ѳ�����0.029~0.049 mg/L����0.029~0.065 mg/L��п0.11~0.37 mg/L��Ǧ0.1~0.43 mg/L���ӵ���0.01 mg/L��ͭ����0.1 mg/L����0.054~4.99 mg/L����29.5~43.7 mg/L���������ˮ�и��ؽ��������������Ⱥ�����Զ���ڡ���ˮ�ۺ��ŷű���(GB8978��1996)��������еĹ������ߴ�29.95%������Ϊ��ԭ�Ͻ��л��գ�ˮ�������ؽ��������ͣ��������ƴ����ʹ��á�
�ؼ��ʣ�
��ͼ����ţ�X 703.1���� ���ױ�ʶ�룺A
Novel technology for treatment of acidic wastewater containing Hg by biologics in zinc smelter
WANG Qing-wei, CHAI Li-yuan, WANG Yun-yan, LI Qing-zhu
(School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China)
Abstract: Acidic wastewater with high concentration of heavy metals discharged from zinc smelter industry was treated by the novel technology of biologics complex-hydrolyzation, and the removal effect of heavy metals(Hg, As, Zn, Pb, Cd, Cu) and F-, Cl- was examined. During stable industrial experiments heavy metals and F-, Cl- of acidic wastewater are removed from 14.78-56.70 mg/L Hg2+, 13.71-40.15 mg/L As, 20.50-58.90 mg/L Zn2+, 12.8-64.2 mg/L Pb2+, 2.1-13.6 mg/L Cd2+, 0.54-1.44 mg/L Cu2+, 339-512 mg/L F- and 472-3400 mg/L Cl- to 0.029-0.049 mg/L Hg2+, 0.029-0.065 mg/L As, 0.11-0.37 mg/L Zn2+, 0.1-0.43 mg/L Pb2+, 0-0.01 mg/L Cd2+, 0-0.1 mg/L Cu2+, 0.054-4.99 mg/L F- and 29.5-43.7 mg/L Cl- respectively, which are all lower than those required in ��Integrated Wastewater Discharge Standard�� (GB8978��1996). Sediment from stable industrial experiments was analyzed. The result shows that mercury in complexing sediment reaches 29.95% and low concentration of heavy metals in hydrolytic sediment makes it easier to dispose and treat.
Key words: acidic wastewater; biologics; complexing; hydrolyzation
пұ���ճ�ϵͳ�ų��ĸ��������������ᳵ��ǰ���ھ�������Ŀ����б�����������ȴ��ϴ�ӳ��ӡ�����ϡ��ѭ��ϵͳ��Ϊ��������ˮ�з���������Ũ�ȹ��߶��ŷų���һ���ַ��ᣬ��Ϊ���ᡣ���ڸ��������к��д�����ϸ�����̳�������������SO2��SO3�ȣ���ϴ�ӹ�������Щ���ʽ������ᣬ������������ʷdz����ӣ����������¼��㣺1) �ɷָ��ӡ������к���ͭ��Ǧ��п���ӡ��顢�����ؽ������ӡ�2) ��ȸߡ����������������������1%~4%֮�䣬�����д�����SO2���塣3) �ؽ���Ũ�ȸ��Ҳ������������ؽ�����Ũ������Сʱ���ɼ������˲���������������ǧ���ˡ�4) ��������״̬���ӡ��Թ�Ϊ�����о����������еĹ�������������̬��������̬��������̬��[1-2]��
������ˮ�Ĵ�ͳ����������Ҫ�л�ѧ��������������ԭ���������������ӽ���������ⷨ�������[3-9]����ͳ������ͬ��ȱ���ǣ����ڴ�����������Ũ��1~100 mg/L�ķ�ˮʱ�����������ú�ԭ���ϳɱ���Թ��ߣ���Լ����㷺�Ĺ�ҵӦ�ã�������ˮ��Ȼ�ǻ�������Ҫ��ȾԴ֮һ[10-11]���������������һ�������Ե�����[12-14]����ˣ�������Ҫ����һ�ָ�Ч�ļ�������������ˮ�������Ǵ������Ӷ�����������ᣬ�Ը��´�ͳ�����ᴦ������������ؽ�������ˮ�����Ⱦ����֤��ˮ��ȫ��
�����������ԣ����������״��������Ƽ�����������������¼���������������Һ�����(30 m3/h)�о�����ȡ���˺ܺõĴ���Ч�������¼���ͨ����ר����ļ������϶��ﵽ�˹�������ˮƽ�����������������һ���������⣬Ϊȷ������ˮ��ȫ�ṩ�˼���֧�š����о��������ص�̽�ֹ�ҵ�����������й����������и��ؽ����������ȵ��ѳ�Ч�������������и����ؽ����ķֲ������
1 ʵ�鷽��
�ɷ��ڱ����ճ�����������20 m3/h�������һ����Ϸ�Ӧ�ۣ��������Ƽ����ѹ���������Ϸ�Ӧ�����������������Ϸ�Ӧ�ۼ�����Ӧ���ڴ˹����У�ԭ��̬�����ѹ�����Ӧ�����γɡ����š�������̬����ͭ��Ǧ��п���ӡ�����������Ƽ�����γ�����塣��Ϸ�Ӧ����������һ��ˮ��ۣ������ʯ�ཬ��pH��10~11����һ��ˮ�ⷴӦ��������ˮ�ⷴӦ��ɺ�������PAM�����Ũ����ʵ��Һ�̷��룬����Һ�������š�����������ͼ1��ʾ��
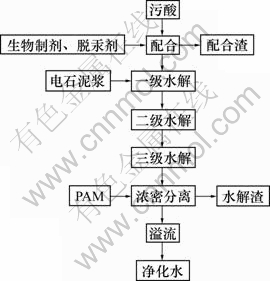
ͼ1 �����Ƽ��������Ṥҵʵ������
Fig.1 Flowchart of industrial experiment of acidic wastewater treated by biologics
ʵ���ڼ���������Ϊ20 m3/h���ѹ���������Ϊ20 g/m3�������Ƽ����������й�Ũ�ȵ�40������Ͷ�ӣ����õ�ʯ�����pHֵ��һ��ˮ��pHֵ������10~11֮�䣬PAM�ļ�����Ϊ5 g/m3 ��
ʵ���ڼ�ί�к���ʡ���վ����48 h��������⣬���й�ÿ2 hȡ�����һ�Σ�ͭ��Ǧ��п���ӡ��顢������ÿ4 hȡ�����һ�Ρ�
ͭ��Ǧ��п���Ӳ���ԭ�����շֹ��ȷ��ⶨ�������ͺ�VARIAN220�������ԭ��ӫ��ֹ��ȷ��ⶨ�������ͺ�AFS2201��������USEPA7473���з������������Ϊ0.05 ?g/L����������Ȼ����������ɫ���ⶨ�������ͺ�HJ/T84-2001��
2 ���������
ͼ2��3��ʾ�ֱ�Ϊ���ἰ�������ˮ�й������Ũ�ȡ���ͼ2��ͼ3��֪��ʵ������������й�Ũ����14.78 mg/L��56.70 mg/L֮�䲨������Ũ����13.71 mg/L��40.15 mg/L֮�䲨�������������Ƽ�������ˮ�й�Ũ����0.029 mg/L��0.049 mg/L֮�䣬��ˮ����Ũ����0.029 mg/L��0.065 mg/L֮�䣬�����ڹ��ҡ���ˮ�ۺ��ŷű���������������Ƽ��������еĹ����鶼�кܺõ�ȥ��Ч����
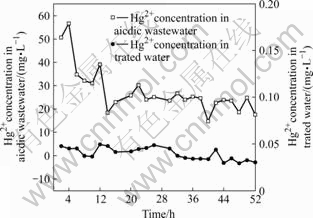
ͼ2 �����Ƽ����������й���ȥ��Ч��
Fig.2 Removal effect of Hg2+ from acidic wastewater by biologics
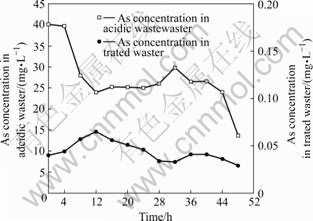
ͼ3 �����Ƽ��������������ȥ��Ч��
Fig.3 Removal effect of As from acidic wastewater by biologics
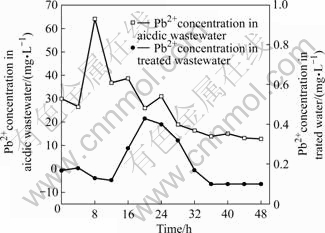
ͼ4~7�ֱ�Ϊ�����Ƽ���������п��Ǧ���ӡ�ͭ��ȥ�������Ӱ�졣�ɼ��������и��ؽ�����Ũ�Ȳ����ܴ�ʵ�������������пŨ����20.50 mg/L��58.90 mg/L֮�䲨����ǦŨ��12.8~64.2 mg/L����Ũ��2.1~13.6 mg/L��ͭŨ��0.54~1.44 mg/L�����������Ƽ�������ij�ˮ��пŨ��0.11~0.37 mg/L��ǦŨ��Ϊ0.1~0.43 mg/L����Ũ��һֱ���ڼ����0.01 mg/L��ͭŨ��һֱ���ڼ����0.1 mg/L�������ڹ��ҡ���ˮ�ۺ��ŷű���������������Ƽ����������й���40��Ͷ�Ӷ������и��ؽ������кܺõ�ȥ��Ч����
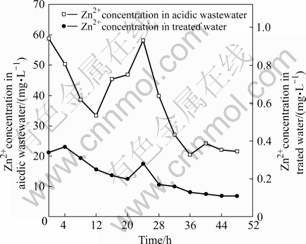
ͼ4 �����Ƽ�����������п��ȥ��Ч��
Fig.4 Removal effect of Zn2+ from��acidic wastewater by biologics
ͼ5 �����Ƽ���������Ǧ��ȥ��Ч��
Fig.5 Removal effect of Pb2+ from acidic wastewater by biologics
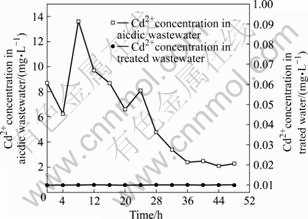
ͼ6 �����Ƽ������������ӵ�ȥ��Ч��
Fig.6 Removal effect of Cd2+ from acidic wastewater by biologics
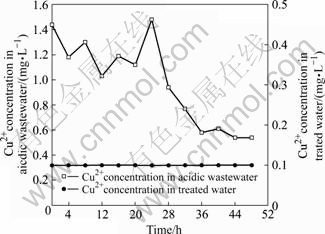
ͼ7 �����Ƽ�����������ͭ��ȥ��Ч��
Fig.7 Removal effect of Cu2+ from acidic wastewater by biologics
ͼ8��9�ֱ�Ϊ�����Ƽ��������з����ȵ�ȥ�������Ӱ�졣ʵ������������еķ�Ũ�Ⱦ�����339 mg/L����ߴﵽ��512 mg/L��ͨ�������Ƽ���ȴ�����ˮ�з�Ũ����0.054 mg/L��4.99 mg/L֮�䣬���ڹ��ҡ���ˮ�ۺ��ŷű�����ʵ���ڼ������������ӵ�Ũ�Ȳ����������Ũ��Ϊ472 mg/L�����Ũ�ȴﵽ��3.4 g/L�����������Ƽ�������ij�ˮ������Ũ��29.5~43.7 mg/L��ȥ�����ȶ���98%���ϡ�����������Ƽ��������еķ������кܺõ�ȥ��Ч����
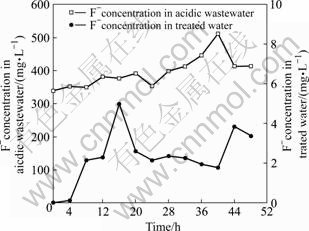
ͼ8 �����Ƽ����������з���ȥ��Ч��
Fig.8 Removal effect of F- from��acidic wastewater by biologics
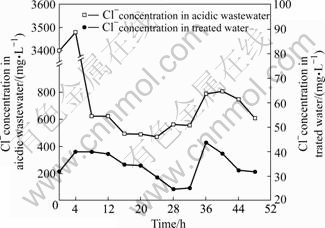
ͼ9 �����Ƽ������������ȵ�ȥ��Ч��
Fig.9 Removal effect of Cl- from��acidic wastewater by biologics
�����Ƽ�������������л���������������������ˮ�������������Ҫ���������е��̳�����������������ͱ��ƻ��˽ṹ�Ľ��������ˮ����������ͨ����ʯ�����pH�����������Ƽ����ؽ����γ�������ˮ����ؽ���������ѳ�������������ʵ����������������������������������ͼ10��ͼ11��ʾ��
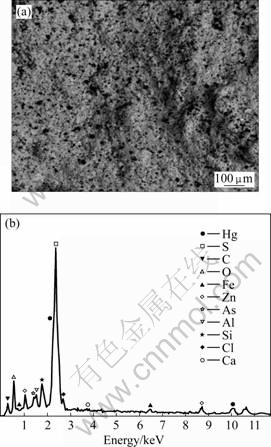
ͼ10���������SEM��EDXͼ
Fig.10 SEM image(a)and EDX pattern(b) of bio-complexing sediment
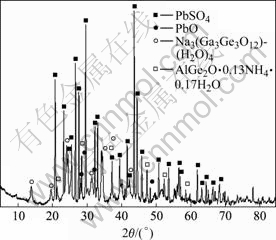
ͼ11 �������XRD��
Fig.11 XRD pattern of bio-complexing sediment
��ͼ10���Կ�����������к���Pb��Hg��S��C��O��Fe��Zn��As��Al��Si��Cl��Ca��Ԫ�أ��ɸ�Ԫ�صĺ���������֪��������й������ߴ�29.95%��Ǧ27.72%�����Ϊ��11.64%, ̼9.61%����9.53%��п4.22%���ٴ�Ϊ��0.45%����1.49%����1.21%����2.38%����1.46%����0.36%(��������)��������еĹ���Ҫ���������е���������̬�ͽ���̬����ͼ11����������еĹ��ԷǾ�̬��ʽ���ڣ�������е�Ǧ��Ҫ������Ǧ������Ǧ����ʽ���ڡ�
��ˮ����������������ķ����������ͼ12��13��ʾ����ͼ12���Կ�����ˮ�����иƺ����ߴ�37.68%����37.37%��̼12.79%����3.28%����2.52%�����Ϊ��1.30%, ��0.80%����0.63%����0.72%����0.47%����0.11%����1.74%��п0.58%����ͼ12���Կ�����ˮ��������Ҫ�ɷ�ΪCaCO3��CaSO4��CaF2�����ؽ�����ˮ�����еĺ������ϵͣ��Ҿ�������״̬���ڣ�����С�����ڴ����봦�á�
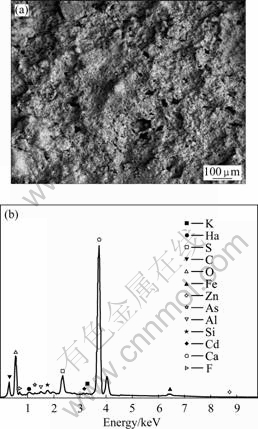
ͼ12 ˮ������SEM��EDXͼ
Fig.12 SEM image (a) and EDX pattern (b) of hydrolytic sediment
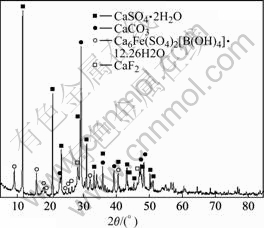
ͼ13 ˮ������X����������
Fig.13 XRD pattern of hydrolytic sediment
3 ����
1) ���������ڼ���������20 m3/h���ѹ�������20 g/m3�������Ƽ��������й�Ũ�ȵ�40��Ͷ�ӣ�ˮ�����pHֵ������10����ʱ�����ᾭ�������������Һ�й�0.029~0.049 mg/L����0.029~0.065 mg/L��п0.11~0.37 mg/L��Ǧ0.1~0.43 mg/L���ӵ���0.01 mg/L��ͭ����0.1 mg/L����0.054~4.99 mg/L����29.5~43.7 mg/L���������ˮ�и��ؽ����������ܴﵽ����ˮ�ۺ��ŷű���(GB8978��1996)��
2) ʵ��������ռ���������й������������ﵽ��29.95%��������Ϊ��ұ����ҵ��ԭ�ϻ������е��ؽ�����ˮ�������ؽ��������͡�����С�����ڰ�ȫ�����ʹ��á�
3) �����Ƽ����ѹ���������Ⱦ�������Ѻá�������࣬����ˮ����̲��õ�ʯ��Ϊ�кͼ���Ϊ��ʯ���ʹ�ÿ�����һ����;�������������ᴦ���ɱ�����ﵽ�ˡ��Է��ηϡ���Ŀ�ġ�
REFERENCES
[1] Ԭپ��, �� ��, ������. ������̬�����о���չ[J]. �ҿ����, 1999, 18(2): 150-156.
YUAN Zhuo-bin, ZHU Min, HAN Shu-bo. Progress in speciation anslysis of mercury[J]. Rock and Mineral Analysis, 1999, 18(2): 150-156.
[2] �� �D, ��־��, ����Ƽ, ������. ˮ�й������о���չ[J]. �����뽡��, 2005, 12(5): 399-400
LI Yang, DUAN Zhi-min, SHEN Qi-ping, WANG Jian-hua. Research advances in analysis of trace mercury in water[J]. Environment and Health, 2005, 12(5): 399-400
[3] �� ��, ����Ԫ, ��С��. ������ˮ�����������о���չ[J]. ��ҵˮ����, 2004, 24(8): 5-8
TANG Ning, CHAI Li-yuan, MIN Xiao-bo. Research development in the treatment of mercury-wastewater[J]. Industrial Water Treatment, 2004, 24(8): 5-8.
[4] ����÷, ������. �ȿǻ�����ˮ�й�������̽��[J].���ջ����Ƽ�, 1999, 12(4): 4-6.
ZHANG Song-mei, LI Li-qing. Discussion of experiment on the adsorption of mercury in water by rice husk ash[J]. Jiangshu Environmental Technology, 1999, 12(4): 4-6.
[5] ���ִ�, �ֽ���, ����ǿ, �� ʤ. ��س�������ˮ������[J]. �����뼼��, 1999, 3: 12-14.
ZHU You-chun, LIN Jian-ming, LIN Mei-qiang, ZENG Sheng. Micro-electrolysis treatment of mercury-contained wasterwater discharged from battery factory[J]. Engineering and Technology, 1999, 3: 12-14.
[6] ANSARI M H, DESHKAR A M, KELKAR P S, DHARMADHIKARI D M, HASAN M Z. Mercury removal from wastewater by steamed hoof powder[J]. Water Science and Technology, 1999, 40(7): 109-116.
[7] LARSON, KAREN A, WIENCEK J M. Liquid ion exchange for mercury removal from water over a wide pH range[J]. Industrial & Engineering Chemistry Research, 1992, 31(12): 2714-2722.
[8] NAVARRO R R, SUMI K, FUJII N, MATSUMURA M. Mercury removal from wastewater using porous cellulose carrier modified with polyethyleneimine[J]. Water Research, 1996, 30(10): 2488-2494.
[9] KAPOOR A, VIRARAGHAVAN T. Adsorption of mercury from wastewater by fly ash[J]. Adsorption Science and Technology, 1992, 9(3): 130-147.
[10] ZHANG Fu-shen, NRIAGU J O, ITOH H. Mercury removal from water using activated carbons derived from organic sewage sludge[J]. Water Research, 2005, 39(3): 389-395.
[11] DI N F, LANCIA A, DI N M, KARATZA D, MUSMARRA D. Capture of mercury ions by natural and industrial materials[J]. Journal of Hazardous Materials, 2006, 132(3): 220-225.
[12] BARRON Z J, LABORIE S, VIERS P, RAKIB M, DURAND G. Mercury removal and recovery from aqueous solutions by coupled complexation-ultrafiltration and electrolysis[J]. Journal of Membrane Science, 2004, 229(2): 179-186.
[13] LEONHAUSER J, ROHRICHT M, WAGNER D I, DECKWER W D. Reaction engineering aspects of microbial mercury removal[J]. Engineering in Life Sciences, 2006, 6(2): 139-148.
[14] MEENA A K, MISHRA G K, KUMAR S, RAJAGOPAL C, NAGAR P N. Low-cost adsorbents for the removal of mercury (��) from aqueous solution��A comparative study[J]. Defence Science Journal, 2004, 54(4): 537-548.
������Ŀ�����ҿƼ�֧�żƻ��ص�������Ŀ(2007BAC25B01)������ʡ�ش�Ƽ�ר��(2006SK1002)������ʡ�Ƽ��ƻ��ص���Ŀ(2007SK2006)
ͨѶ���ߣ�����Ԫ�����ڣ���ʿ���绰��0731-8836921��E-mail: lychai@mail.csu.edu.cn
(�༭ �� ��)


