���±�ţ�1004-0609(2011)01-0214-06
��Ʒλ����п����MACA��ϵ�е�ѭ������
������, �ż���, �� ��, ������, �� ��, �Ƴ���, ���
(���ϴ�ѧ ұ���ѧ�빤��ѧԺ����ɳ 410083)
ժ Ҫ��
�о�Me(��)-NH4Cl-NH3-H2O(MACA)��ϵ������ƺ��Ʒλ����п��Ľ������̣������ѭ������������������Һ��пŨ�ȵĹ��ռ������������������ѭ���������Ż�����ΪҺ�̱�4:1�����¡������ٶ�300 r/min������ʱ��3 h��ͨ��ѭ�������ֱ�Ϊ14��15��10��3���ε�ѭ���������飬�������п�����ʡ�69%������ҺпŨ�ȡ�33 g/L�ĽϺý�����ù��վ������̼�̡��ܺĵ͡��������ס������Ѻõ��ŵ㣬�Ե�Ʒλ������ʯ��ѡ����п��Ŀ������þ�����Ҫ���塣
�ؼ��ʣ�
пұ���� ��Ʒλ����п���� MACA��ϵ�� ѭ��������
��ͼ����ţ�TF813���� ���ױ�־�룺A
Cycle leaching of low grade zinc oxide ores in MACA system
TANG Mo-tang, ZHANG Jia-liang, WANG Bo, YANG Sheng-hai, HE Jing, TANG Chao-bo, YANG Jian-guang
(School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China)
Abstract: The leaching processes of the low grade zinc oxide ores from Lanping in the system of Me(��)-NH4Cl-NH3-H2O(MACA) were studied. The technical process of enriching the concentration of zinc in lixivium by cycle leaching was proposed. The results show that the optimal conditions are found, including the ratio of liquid to solid to be 4, stirring speed to be 300 r/min, leaching time to be 3 h and at ambient temperature. Three-stage experiments of cycle leaching were carried out, and the results indicated that the zinc-leaching rate is more than 69% and the zinc concentration of leaching solution is more than 33 g/L. This process has lots of advantages, including a simple flow sheet, low energy consumption, easy purification, being environment-friendly and so on. Therefore, it is to be significant in exploitation and utilization of low-grade zinc oxide ores, which contain high-alkaline gangues and are also difficultly treated by beneficiation.
Key words: zinc metallurgy; low grade zinc oxide ores; MACA system; cycle leaching
�ҹ�����п��Ĵ�������ḻ[1]�����Ǿ�������п��Ʒλ�ͣ�������ʯ�����ߣ���ʯ��ɸ��ӣ��俪��������Ŀǰһؽ�����������[2]�����ô�ͳ��������մ������ָ��Եĵ�Ʒλ����п�������Ĵ����ʶࡢ�������Ӹ����ص�ȱ��[3]����˹�����ѧ��Խ��Խ��ע�����ü�����ϵ�����ÿ���,��Ŀǰ�о��϶�ļ�����ϵ��ҪΪǿ������ϵ[4-6]�Ͱ�����ϵ[7-9]������NaOH��ǿ�������Ʒλ����п��ʱ����������ߴ�����NaOH����Pb��Si������Ҳ��ͬʱ���������Ӷ�Ӱ�������������ˣ��ù����в��߱���ҵӦ��ǰ������֮��������ϵ��ǿ������ϵ��������ϵ�����ŵ��ǽ���ѡ���Ժã�����п���д������ڵļ�����ʯ�������Ρ������������ʶ������뷴Ӧ���Լ�������[10]�����⣬������ϵ�н���Һ�����������ף�һ��������������п�ۼ��ɽ���Һ�е�Cu��Cd��Ni��Co�����ʽ������������������Ҫ�������ֵ���¡��ű�ƽ��[11]���������[12]����Me(��)- NH4Cl-NH3-H2O(MACA)��ϵ������Ʒλ����п�������������£�������п�����ʾ��ﵽ93%���ϡ�����Һ������������������õ�п�������1#��п��������������ֻ������п��������15%������п�����ڴ������п����Ϊ5%~15%�ĵ�Ʒλ��������ƺ��Ʒλ����п��һ�ν���Һ�е�пŨ��Զ���ڵ��ϵͳ��Ҫ���п�ٽ�Ũ�ȣ������ڽ�����Խ���Һ��пŨ�Ƚ��и����ɽ��е����
һЩѧ�߿�չ�˴�п���Һ����ȡп�Ĺ����о�����ѡ�õ���ȡ����Ҫ��P204[13]��Lix54[14]��Cyanex923[15]��Cyanex272[16]�ȡ�P204��п����Ҫ��������ȡ�����д��������븺���л��࣬���·���ʱ��ĺܸߣ���֮��淋�����п����Һ��������пʱҲ����������������[17]��������������ȡ����пʱ�������ż۸��ղ������ѿ��ơ���ȡ������С�����ȱ�ݣ���ˣ�������ȡ����пŨ�ȵĹ���Ҳû�еõ��㷺��Ӧ�á��ڴ˱����£�����������MACA��ϵ�в���ѭ�������ķ�������п��������10%�ĵ�Ʒλ����п���Դﵽ����пŨ�ȵ�Ŀ�ġ�
1 ʵ��
ʵ������ԭ��ȡ��������ƺ��пҵ����˾��
ԭ�Ͼ��������ĥ�����Ժ�����95%������С��150 ��m������Ҫ��ѧ�ɷ���������ɷֱ����1��2���С��ɱ�1�ͱ�2��֪��������п�����ͣ���Ϊ6.59%�����ɽ���п(ZnO+ ZnSO4)Ϊ4.93%��
��1 ��Ʒλ����п��Ļ�ѧ�ɷ�
Table 1 Chemical composition of low grade zinc oxide ores (mass fraction,%)
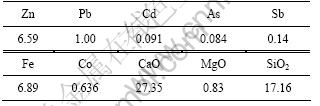
��2 ��Ʒλ����п����п���������
Table 2 Phase composition of zinc in low grade oxide ores (mass fraction, %)

MACA��ϵѭ��������Ʒλ����п���ԭ��������ͼ1��ʾ����ͼ1��֪�������̵������ص��Ǵֽ���Һ���ؽ������̣��Ӷ�ʵ�ֽ���Һ��пŨ�ȵĸ�����������п��Ҫ��
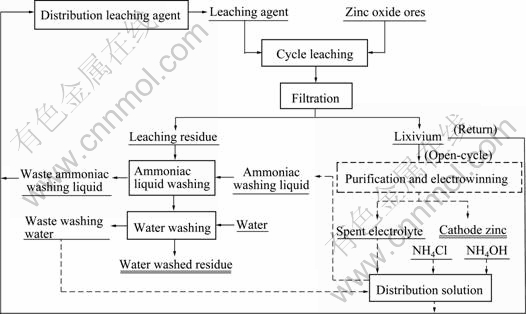
ͼ1 MACA��ϵѭ��������Ʒλ����п���ԭ��������
Fig.1 Principle flow sheet of cycle leaching of low grade zinc oxide ores in MACA system
1.3.1 ������������
��������������500 mLƽ����ƿ�н��У����ú��´�����������������ʪ��ұ�����鷽���������������ʵ���ģΪ100 g����/�Σ���������ֱ���а�ϴ��ˮϴ��������һ����������������ͬ�İ�ϴҺ��5��ϴ�ӣ���ϴ����������ˮ��5��ϴ�ӣ�ˮϴ��Һ�������������´ν����İ�ϴҺ����ϴ��Һ�����Һ�ֱ������ȫ����ϴ��Һ�뷵�صĽ���Һ�ϲ��������´ν����������صĽ���Һ��Ϊ����������ȥ��ϴ��Һ��֮����ν��������벽�����ͬ�����ѭ������5�Ρ�
1.3.2 ѭ�������ۺ�����
ѭ�������ۺ������ѭ����ʽ�Ͳ�������������ͬ���ۺ������3���ν������Ż��������ɷֺͽ���Һ��·������3�ε���������������ʾ��
��. �������ɷ�3 mol/L NH4OH+3 mol/L NH4Cl����·����25%��Һ�̱�4:1�����¡������ٶ�300 r/min������ʱ��3 h��ʵ���ģ100 g����/�Ρ�
��. �������ɷ�3 mol/L NH4OH+4 mol/L NH4Cl����·����25%���������������ͬ��
��. �������ɷ�3 mol/L NH4OH+4 mol/L NH4Cl����·����28.75%���������������ͬ��
п��Ũ����EDTA�������ⶨ����������Ľ�������Һ��Ϊ���ۺ�����Ľ�����������Ϊ��Һ�ƽ�����R1�����ƽ�����R2�ļ���ʽ�ֱ�������ʾ��
![]()
![]()
ʽ�У�wL(Zn)�ǽ���Һ�е�п������wA(Zn)�ǰ�ϴ��Һ�е�п������wT(Zn)��ԭ���е�п������wR(Zn)��ˮϴ���е�п������
����Һ�е����ʲ���ICP-AES���з�����
2 ���������
���ǵ����Ļӷ��Ժͽ���Ч�ʣ���������[18]���о��������3 mol/L NH4OH+3 mol/L NH4Cl�Ļ����Һ��Ϊ������������Ʒλ����п���õ��������鷽����������Һ�̱ȡ��¶ȡ������ٶȺ�ʱ��4��������ѭ������������ƽ�������ʵ�Ӱ�죬��������ͼ2~5��ʾ��

ͼ2 Һ�̱ȶ�ƽ�������ʵ�Ӱ��
Fig.2 Effect of ratio of liquid to solid on average leaching rate

ͼ3 �¶ȶ�ƽ�������ʵ�Ӱ��
Fig.3 Effect of temperature on average leaching rate
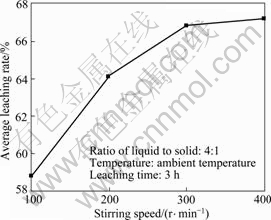
ͼ4 �����ٶȶ�ƽ�������ʵ�Ӱ��
Fig.4 Effect of stirring speed on average leaching rate

ͼ5 ����ʱ���ƽ�������ʵ�Ӱ��
Fig.5 Effect of leaching time on average leaching rate
�ɼ�Һ�̱ȡ��¶ȡ������ٶȡ�����ʱ���ѭ������������п�Ľ���Ч�����в�ͬ�̶ȵ�Ӱ�졣��ͼ2��֪��Һ�̱ȶ�ѭ�������������Ž�Ϊ������Ӱ�졣��Һ�̱�С��4:1ʱ��ƽ������������Һ�̱ȵ�������������ߣ�����Һ�̱ȴ���4:1ʱ�������ٶ�����ƽ������ˣ��ۺϿ�������Һ�̱�Ϊ4:1����ͼ3���Կ������������¶ȴ�20 �����ߵ�30 ��ʱ��ƽ�������ʱ仯���������������¶�ʱ��ƽ�������ʼ����½�������Ҫ�������¶ȵ�����ʹ�ý������а��ӷ��Ӿ磬��������ϵ��NH3Ũ�ȡ���ˣ�ȷ�����Ž����¶�Ϊ20~30 �棬�����¡���ͼ4��֪���������ٶ�С��300 r/minʱ��пƽ�����������Ž����ٶȵļӿ���������������ٶȴ�300 r/min���ߵ�400 r/minʱ��ƽ�������ʱ仯������ˣ�ȷ�����Ž����ٶ�Ϊ300 r/min����ͼ5��֪��������ʱ��С��3 hʱ��ƽ���������������ǵ�����ʱ���3 h����4 hʱ��ƽ�������ʱ仯�������ѡ�����Ž���ʱ��Ϊ3 h��
Ϊ��һ���Ż�ѭ�������ý������ɷּ�ȷ���Ϻ����Ľ���Һ��·������������3���ε�ѭ�������ۺ����顣�����ͼ6��7��ʾ����ͼ6��֪��3����ѭ�������ۺ��������Һ��пŨ�ȵı仯���������ͬ����ǰ5�ν��������У�пŨ������ѭ�����������Ӷ��������ߡ��˺�����ѭ�������Ľ��У�пŨ�����ߵķ�������ƽ���������ձ����ȶ����ﵽһ�����ƽ���״̬���������Ͽ��Ը��ݽ���Һ��·��������ﵽƽ�������ѭ��������������ʵ����3��������пҺ�ﵽƽ�������ѭ�������ֱ�Ϊ9��11��8�Σ���ƽ����п����Һ��ƽ��Ũ�ȷֱ�Ϊ32.72��39.03��33.93 g/L����ͼ7���Կ�����3����ѭ�������ۺ�ʵ��п�����ʵı仯���Ҳ������ͬ���ڴﵽƽ��ǰ������������ѭ�����������Ӷ���С��ƽ������ʻ������ֺ㶨��ƽ���Ľ����ʵ�ƽ��ֵ�ֱ�Ϊ62.72%��67.88%��69.08%��

ͼ6 ѭ�������ۺ�ʵ���н���ҺпŨ�ȵı仯
Fig.6 Zn2+ concentration of lixivium in integrated cycle leaching experiments: ��. Leaching agent of 3 mol/L NH4OH+ 3 mol/L NH4Cl, open-cycle fraction of 25%; ��. Leaching agent of 3 mol/L NH4OH+4 mol/L NH4Cl, open-cycle fraction of 25%; ��. Leaching agent of 3 mol/L NH4OH+4 mol/L NH4Cl, open-cycle fraction of 28.75%
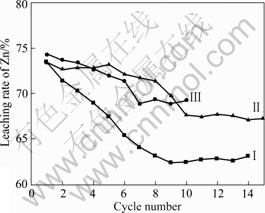
ͼ7 ѭ�������ۺ�ʵ����п�����ʵı仯
Fig.7 leaching rate of Zn in integrated cycle leaching experiments: ��. Leaching agent of 3 mol/L NH4OH+3 mol/L NH4Cl, open-cycle fraction of 25%; ��. Leaching agent of 3 mol/L NH4OH+4 mol/L NH4Cl, open-cycle fraction of 25%; ��. Leaching agent of 3 mol/L NH4OH+4 mol/L NH4Cl, open-cycle fraction of 28.75%
�����������������ijɷֺͿ�·������ѭ���������̵�Ӱ��������һ���棬�ڱ��ֿ�·��������ʱ���ʵ�����߽����������Ũ�ȣ������Ե����ƽ������Һ��пŨ�Ⱥ�п�����ʣ���һ���棬�ڽ������ɷֲ���ʱ���ʵ�������·������п�������������ߡ�
�ɴˣ�ȷ��ѭ������ʵ��������������£��������ɷ�Ϊ3 mol/L NH4OH+4 mol/L NH4Cl����·����Ϊ28.75%��Һ�̱�Ϊ4:1�����£������ٶ�Ϊ300 r/min������ʱ��Ϊ3 h���ڴ������£�ƽ������Һ��п��ƽ��Ũ��Ϊ33.93 g/L��пƽ��������Ϊ69.08%��
������ѭ����������Ľ���Һ����Ҫ����Ũ�ȵı仯�����ͼ8��ʾ����ͼ8��֪����Ҫ����Ũ�ȵı仯���ɻ�����ͬ����ǰ5�ε�ѭ�������У�����һ���̶ȵ����ӣ�֮���ﵽ�ȶ�״̬�����ڽ�С�ķ�Χ�ڲ���������Cd��Ũ�Ƚϸߣ�ƽ�����320~350 mg/L�ķ�Χ�ڡ���������Ԫ��Ũ�Ⱦ��ϵͣ�������Fe��Ca��Mg��As����20 mg/L���£���Щ���ٴ���֤�˰�����ϵ����ѡ���Ժõ��ŵ㡣
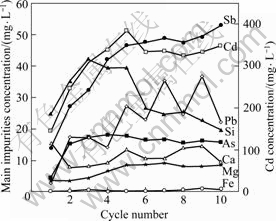
ͼ8 ������ѭ�������ۺ�ʵ�����Һ����Ҫ����Ũ�ȵı仯
Fig.8 Main impurities concentration of lixivium in third integrated cycle leaching experiment
3 ����
1) �������ѭ������������������Һ��пŨ�ȵĹ��ռ���������ȷ����ѭ����������������£�Һ�̱�4:1�����¡������ٶ�300 r/min������ʱ��3 h��
2) ���������ɷ�Ϊ3 mol/L NH4OH+4 mol/L NH4Cl����·����Ϊ28.75%ʱ��ƽ������Һ��п��ƽ��Ũ��Ϊ33.93 g/L��п��ƽ��������Ϊ69.08%��������Ԫ�ؽ������Һ�������١�
3) MACA��ϵ��ѭ��������Ʒλ����п��ʱ���ɸ�������Һ��пŨ�ȣ�ʹ֮���ϵ����Ҫ��
References
[1] ����ϣ, �ż��. ����Ǧп��Դ�Ϳ���������״[J]. ������ɫ����, 2004, 32: 22-29.
DAI Zi-xi, ZHANG Jia-rui. Present situation of development and utilization of lead and zinc resources in the world[J]. World Nonferrous Metals, 2004, 32: 22-29.
[2] ����÷, �� ��, ����Ԫ, ������. �������Ե�Ʒλ����п����Ϊ��Ӱ��[J]. �й���ɫ����ѧ��, 2009, 19(5): 960-966.
ZHANG Yu-mei, LI Jie, CHEN Qi-yuan, DING Hong-qing. Influence of ultrasonic irradiation on ammonia leaching of zinc from low-grade oxide zinc ore[J]. The Chinese Journal of Nonferrous Metals, 2009, 19(5): 960-966.
[3] MENG X, HAN K. Principles and applications of ammonia leaching of metals�DA review[J]. Mineral Processing and Extractive Metallurgy Review, 1996, 16(1): 23-61.
[4] FRENAY J. Leaching of oxidized zinc ore in various media[J]. Hydrometallurgy, 1985, 15(2): 243-253.
[5] ZHAO Y, STANDFORTH R. Production of Zn powder by alkaline treatment of smithsonite Zn-Pb ores[J]. Hydrometallurgy, 2000, 56(2): 237-249.
[6] CHEN A, ZHAO Z, JIA X, LONG S, HUO G, CHEN X. Alkaline leaching Zn and its concomitant metals from refractory hemimorphite zinc oxide ore[J]. Hydrometallurgy, 2009, 97(3/4): 228-232.
[7] FENG L, YANG X, SHEN Q, XU M, JIN B. Pelletizing and alkaline leaching of powdery low grade zinc oxide ores[J]. Hydrometallurgy, 2007, 89(3/4): 305-310.
[8] QIN W, LI W, LAN Z, QIU G. Simulated small-scale pilot plant heap leaching of low-grade oxide zinc ore with integrated selective extraction of zinc[J]. Minerals Engineering, 2007, 20(7): 694-700.
[9] WANG Rui-xiang, TANG Mo-tang, YANG Sheng-hai, ZHANG Wen-hai, TANG Chao-bo, HE Jing, YANG Jian-guang. Leaching kinetics of low grade zinc oxide ore in NH3-NH4Cl-H2O system[J]. Journal of Central South University of Technology, 2008, 15(5): 679-683.
[10] HARVEY T. The hydrometallurgical extraction of zinc by ammonium carbonate: A review of the Schnabel Process[J]. Mineral Processing and Extractive Metallurgy Review, 2006, 27(4): 231-279.
[11] �ű�ƽ, ������, ������. ������������п����ȡ��п[J]. ���Ϲ�ҵ��ѧѧ��: ��Ȼ��ѧ��, 2003, 34(6): 619-623.
ZHANG Bao-ping, TANG Mo-tang, YANG Sheng-hai. Treating zinc oxide ores using ammonia-ammonium chloride to produce electrolysis zinc[J]. Journal of Central South University of Technology: Nature Science, 2003, 34(6): 619-623.
[12] ������, ������, ��ά, ������, ���ĺ�. NH3-NH4Cl-H2O��ϵ������Ʒλ����п����ȡ��п[J]. ���̹���ѧ��, 2008, 8(S1): 219-222.
WANG Rui-xiang, TANG Mo-tang, LIU Wei, YANG Sheng-hai, ZHANG Wen-hai. Leaching of low grade zinc oxide ore in NH3-NH4Cl-H2O system for production of electrolytic zinc[J]. The Chinese Journal of Process Engineering, 2008, 8(S1): 219-222.
[13] AMER S, FIGUEIREDO J, LUIS A. The recovery of zinc from leach liquors of the CENIM-LNETI process by solvent extraction with di(2-ethylhexyl) phosphoric acid[J]. Hydrometallurgy, 1995(37): 323-337.
[14] ALGUACIL F, ALONSO M. Effect of ammonium sulphate and ammonia on the liquid-liquid extraction of zinc using LIX54[J]. Hydrometallurgy, 1999, 53(2): 203-209.
[15] ALGUACIL F, MARTINEZ S. Solvent extraction equilibrium of zinc(II) from ammonium chloride medium by CYANEX923 in Solvesso 100[J]. Journal of Chemical Engineering of Japan, 2001, 34(11): 1439-1442.
[16] AMER S, LUIS A. Extraction of zinc and other minor metals from concentrated ammonium chloride solutions with D2EHPA and Cyanex272[J]. Revista de Metalurgia (Madrid), 1995, 31(6): 351-372. (in French)
[17] DEEP A, de CARVALHO J. Review on the recent developments in the solvent extraction of zinc[J]. Solvent Extraction and Ion Exchange, 2008, 26(4): 375-404.
[18] ������. MACA��ϵ�д�����Ʒλ����п����ȡ��п�������빤���о�[D]. ��ɳ: ���ϴ�ѧ, 2009: 87-91.
WANG Rui-xiang. Study on theory and technology for treating low-grade zinc oxide to prepare cathode zinc in the MACA system[D]. Changsha: Central South University, 2009: 87-91.
(�༭ ��ѧ��)
������Ŀ�������ص�����о���չ�ƻ�������Ŀ(2007CB613604)��������Ȼ��ѧ����������Ŀ(50674104)
�ո����ڣ�2010-01-11�������ڣ�2010-05-08
ͨ�����ߣ������ã����ڣ���ʿ���绰: 0731-88830470��E-mail: mttang@mail.csu.edu.cn


