�ȴ��������ʯ��������﮵绯ѧ���ܵ�Ӱ��
�� ����������
(���ϴ�ѧ ұ���ѧ�빤��ѧԺ������ ��ɳ��410083)
ժ Ҫ��
ժ Ҫ�� ��FeSO4?7H2O��NH4H2PO4Ϊԭ�ϣ�H2O2Ϊ��������ͨ��Һ��������Ʊ�ǰ����FePO4��Ȼ��ͨ��̼�Ȼ�ԭ���ϳ�LiFePO4���о������ٶȶԲ��ᄃ�ͽṹ����ò�Լ��绯ѧ���ܵ�Ӱ�졣��LiFePO4��ɨ����Ƭ���Կ��������Ž����ٶȵı�������Ʒ�����������绯ѧ�����о������������ٶȲ��˹�����С�������˵Ľ����ٶ�Ϊ2 ��/min���������ºϳɵIJ�����0.1C���ʳ�ŵ�ʱ���״ηŵ�����Ϊ153 mA?h/g����1C���ʳ�ŵ�ʱ���״ηŵ�������136 mA?h/g����ѭ�����ܺá�
�ؼ��ʣ�
LiFePO4��Һ�������̼�Ȼ�ԭ���������ٶ���
��ͼ����ţ�TM912.9 ���ױ�ʶ�룺A ���±�ţ�1672-7207(2007)06-1106-04
Effect of heat treatment on electrochemical performance of
olivine type lithium iron phospho
ZHANG Bao, PENG Chun-li
(School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China)
Abstract: LiFePO4 was prepared by carbothermal reduction of FePO4, which was synthesized by aqueous precipitation from FeSO4?7H2O and NH4H2PO4 and hydrogen peroxide as the oxidizing agent. The effect of cooling rate on the structure, morphology and electrochemical performance was investigated. Scanning electron microscope images show that the particle size of LiFePO4 becomes bigger as cooling rate gets slower. The optimum performance of sample is synthesized at cooling rate of 2 ��/min, with the discharge capacity of 153 mA?h/g at rate of 0.1C and 136 mA?h/g at rate of 1C and good cycling performance is obtained.
Key words: LiFePO4; aqueous precipitation; carbothermal reduction; cooling rate
1997��Padhi��[1]������LiFePO4���г�ŵ����ܣ������۱�����Ϊ170 mA?h/g���ŵ�ƽ̨Ϊ3.4 V���������õ�ѭ������[2]�����ȶ�����[3]���������۸���˵��ص�ʹ��������Ϊ��һ��������ӵ���������ϡ������ֲ���Ҳ����һЩ�����谭������ʵ��Ӧ ��[4-6]��һ�Ǻϳ���Fe2+��������Fe3+�����õ������LiFePO4������LiFePO4�����Բ���������ŵ����ܲ���е��о�ͨ�����¼����������LiFePO4������[7-9]��a. ���ö�������������Fe2+��b. �ϳ�С������LiFePO4�������ӵ���ɢ������c. �ӵ絼������ߵ絼�ʡ����⣬�ϳɷ����Բ��ϵ����ܼ�ʵ��Ӧ���кܴ��Ӱ�죬���еķ�����Ҫ�й��� ��[10-12]���ܽ�-������[13-14]��̼�Ȼ�ԭ��[15]��̼�Ȼ�ԭ������Ϊ�Ƚ���ǰ;��һ�ַ�������Ϊ�ϳɵIJ��ϵ绯ѧ���ܺ���ʵ����������
�������߲���̼�Ȼ�ԭ���ϳ�LiFePO4������FeSO4?7H2O��NH4H2PO4Ϊԭ�ϲ���Һ��������Ʊ�FePO4ǰ���壬Ȼ��ǰ���塢Li2CO3����Ȳ�ڻ�Ͼ��Ȳ���560 ������12 h����Ҫ�о������ٶȶ�LiFePO4���Ͻṹ�����ܵ�Ӱ�졣
1 ʵ ��
1.1 LiFePO4���Ʊ�
��ȡ�����ʵ�����FeSO4?7H2O��NH4H2PO4���ֱ���ȥ����ˮ�ܽ������Һ��Ȼ��2����Һ��ϼ��뷴Ӧ���У����跴Ӧ30 min�����H2O2�������д�����FePO4��ɫ������������Ӧ��ȫ��������ķ�����ϴ�ӣ�Ȼ���ɡ�����ɺ����������̼��﮼���Ȳ�ڰ���ѧ������(��Ȳ�ڹ���10%)��Ͼ��ȣ�Ȼ����Ar���ı�������560 ������12 h��Ȼ��ֱ�����¯��ȴ(ƽ�������ٶ�Ϊ3~4 ��/min)�������ٶ�Ϊ2 ��/min�������ٶ�Ϊ1 ��/min�õ�3����Ʒ����Ϊ��Ʒa��b��c�����ϲ��ϵĽ��·�Χ������560~ 250 �档
1.2 �� ��
���� CS800����̼������(Eltar��˾, �¹�)�Ժϳɲ�����̼�ĺ������з�������������SDT Q600���ȷ�������������������ٶ�Ϊ10 ��/min����ǰ��������ȷ���������X����������(XRD) (Rint-2000��Rigaku)��ɨ��羵��(SEM)(JEOL��JSM-5600LV)�ֱ������Ʒ�ľ���ṹ�ͱ�����ò��
1.3 �����װ�Ͳ���
��ԭ�ϰ�m(LiFePO4)?m(��Ȳ��)?m(PVDF)=8?1?1��Ͼ��Ⱥ�ͿƬ������120 ����ո���10 hѹƬ����������Խ����Ƭ��������1 mol/L LiPF6/(̼�������(EC)+̼����ϩ��(DMC) (�����1?1))Ϊ���Һ��������������װ��CR2025�Ϳ�ʽ��ء��������������Dz��Ե�صij�ŵ����ܣ��ڵ�ѹΪ2.3~4.1 Vʱ���г�ŵ����顣
2 ���������
ͼ1��ʾΪǰ����������������-���ȷ���(TG-DTA)���ߡ��ɼ�����150 �����ҳ������Ե����ȷ壬ͬʱ��������������ʧ���˷�ӦΪǰ����ʧȥ�ᾧˮ�Ĺ��̣�����580 ���710 �����ҳ���2�����ȷ����û����������ʧ������ֱܷ��Ӧ��������������ת��Ϊ�����ͣ����Ӧ�����ת��Ϊ�¾��͵�2������[5]����TG���߿��Կ�������20~500 ��֮�䣬ǰ����������ʧ��Ϊ19%�������ظ���صζ�ǰ�������ĺ���������京��Ϊ29.88%����Щ����������[13]�б���������������2���ᾧˮ���Ǻϡ�ͼ2��ʾΪǰ����FePO4��ɨ��羵��Ƭ����ͼ2���Կ������ϳɵ�ǰ�������������״���ֲ��dz����ȣ�ƽ������Ϊ0.1 ��m���ң��ұȱ������
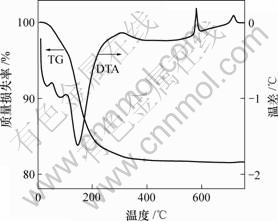
ͼ1 FePO4��TG-DTA����
Fig.1 TG and DTA curves for precipitated FePO4

ͼ2 FePO4��ɨ��羵��Ƭ
Fig.2 SEM image of FePO4
ͼ3��ʾΪ��ͬ��ȴ�ٶ����õ�LiFePO4��XRD�ס���ͼ3���Կ���������Ʒ��Ϊ��һ��LiFePO4���࣬����ͼ����û�г���̼�壻������ȴ�ٶȵļ�С����Ʒ����������������խ����˵����Ʒ�ľ���������ȴ�ٶȵļ�С����������ͼ4��ʾΪ��ͬ��ȴ�ٶ����õ�LiFePO4��SEM��Ƭ����ͼ4���Կ��������Ž����ٶȵļ�С�����õ�LiFePO4�Ŀ���������ٶ�Ϊ1 ��/minʱ����������������0.6 ��m�������ٶ�Ϊ2 ��/minʱ������������ԼΪ0.5 ��m���������ٶ�����3~4 ��/minʱ������������ԼΪ0.3 ��m��
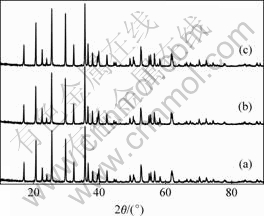
�����ٶ�/(��?min-1): (a) 3~4; (b) 2; (c) 1
ͼ3 ��ͬ�����ٶ��µõ�LiFePO4��XRD��
Fig.3 XRD patterns of LiFePO4 prepared at different cooling rates

�����ٶ�/(��?min-1): (a) 3~4; (b) 2; (c) 1
ͼ4 ��ͬ�����ٶ��µõ�LiFePO4��SEM��Ƭ
Fig.4 SEM images of LiFePO4 prepared at different cooling rates
ͼ5��ʾΪ��ͬ��ȴ�ٶȵõ���LiFePO4��0.1C�����µij�ŵ����ߡ���ͼ5���Կ���������Ʒ�ij�ŵ����߶��dz�ƽ�ȣ����ƽ̨��3.47 V���ң���Ʒa��b�ķŵ�ƽ̨��3.41 V���ң���Ʒc�ķŵ�ƽ̨���н��͡����⣬��ȴ�ٶȵĿ�����С�����ŵ������û��̫���Ӱ�졣�����ٶ�Ϊ3~4��2��1 ��/min����Ʒ����ŵ������ֱ�Ϊ151��153��150 mA?h/g��
ͼ6��ʾΪ�ڲ�ͬ�����ٶ��µõ���LiFePO4��1C�����µij�ŵ����ߡ����Կ�������Ʒa��b��c�ķŵ������ֱ�Ϊ129��136��126 mA?h/g��ͬʱ����Ʒc�ķŵ�ƽ̨��������Ʒ�ķŵ�ƽ̨����ƫ�ͣ���

�����ٶ�/(��?min-1): 1��3~4; 2��2; 3��1
ͼ5 ��ͬ�����ٶ��µõ���LiFePO4��0.1C�����µ��״γ�ŵ�����
Fig.5 The first charge-discharge curves of LiFePO4 synthesized at different cooling rates recorded at rate of 0.1C
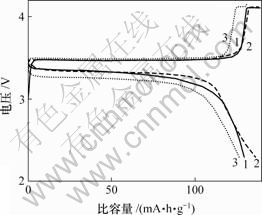
�����ٶ�/(��?min-1): 1��3~4; 2��2; 3��1
ͼ6 ��ͬ�����ٶ��µõ���LiFePO4��1C�����µ��״γ�ŵ�����
Fig.6 The first charge-discharge curves of LiFePO4 synthesized at different cooling rates recorded at rate of 1C
Լ���0.1 V����˵�������ٶ�Ϊ2 ��/min�Ƚ����룬�������ٶȹ��죬��Ȼ�õ���������﮿����Ƚ�ϸС�������Ͽ��ܴ��ںܶ�ȱ�ݣ�����ŵ����������������ģ����������ٶȹ�������Ȼ������﮽ᾧ�Ƚ����ƣ������ڿ����ϴ���ŵ�������ͣ��Ҽ�����
ͼ7 ��ʾΪ��ͬ�����ٶ��ºϳɵ�LiFePO4��1C���ʷŵ�ʱ��ѭ������ͼ�����Կ�������Ʒa��b��c���������õ�ѭ�����ܡ�������ŵ�������ѭ��30�Σ���ŵ������������䡣��������������ٶ�Ϊ2 ��/min����Ʒ��绯ѧ���ܱȽ����롣��0.1C���ʷŵ�ʱ����������153 mA?h/g����1C���ʷŵ�ʱ���������ﵽ136 mA?h/g����ѭ���������á�
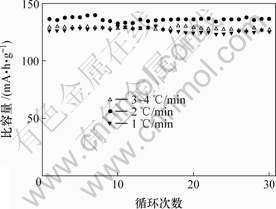
ͼ7 ��ͬ�����ٶ��µõ���LiFePO4ѭ������ͼ
Fig.7 Electrochemical cycling performance of LiFePO4 synthesized at different cooling rates
3 �� ��
a. ͨ��̼�Ȼ�ԭ�������ò�ͬ���ȴ�����ʽ�ϳ���LiFePO4�����Ž����ٶȵı�������Ʒ���������
b. �����ٶ�Ϊ2 ��/minʱ���õ���Ʒ������ƽ������ԼΪ0.5 ��m���ҷֲ��ȽϾ��ȣ���0.1C���ʳ�ŵ�ʱ���״ηŵ�����Ϊ153 mA?h/g����1C���ʳ�ŵ�ʱ���״ηŵ�������136 mA?h/g����ѭ������ ���á�
�ο����ף�
[1] Padhi A K, Nanjundaswamy K S, Goodenough J B. Phospho-olivines as positive-electrode materials for rechargeable lithium batteries[J]. J Electrochem Soc, 1997, 144(4): 1188-1194.
[2] Anna S A, Beata K, Lennart H, et al. Lithium extraction/insertion in LiFePO4: An X-ray diffraction and mossbauer spectroscopy study[J]. Solid State Ionics, 2000, 133(1/2): 41-52.
[3] Macneil D D, Lu Z, Chen Z, et al. A comparison of electrode/electrolyte reaction at elevated temperature for various Li-ion battery cathodes[J]. J Power Sources, 2002, 108: 8-14.
[4] Prosini P P, List M, Scaccia S, et al. Synthesis and characterization of amorphous hydrated FePO4 and its electrode performance in lithium batteries[J]. J Electrochem Soc, 2002, 149: A297-A301.
[5] Prosini P P, List M, Zane D. Determination of the chemical diffusion coefficient of lithium in LiFePO4[J]. Solid State Ionics, 2002, 148(1/2): 45-51.
[6] Iucheu N, Chen Y, Okada S, et al. LiFePO4 storage at room and elevated temperature[J]. J Power Sources, 2003, 119/121: 749-754.
[7] Cho T, Chung H. Synthesis of olivine-type LiFePO4 by emulsion-drying method[J]. J Power Sources, 2004, 133: 272-276.
[8] Doeff M M, Hu Y, Mclaron F, et al. Effect of surface carbon structure on the lectrochemical performance of LiFePO4[J]. Electrochem and Solid State Lett, 2003, 6(10): A207-A209.
[9] Herstedt M, Stjerndahl M, Nyten A, et al. Surface chemistry of carbon-treated LiFePO4 particles for Li-ion battery cathodes studied by PES[J]. Electrochem and Solid State Lett, 2003, 6(9): A202-A206.
[10] Andersson A S, Thomas J O. The source of first-cycle capacity loss in LiFePO4[J]. J Power Sources, 2001, 97/98: 498-502.
[11] Yamada A, Chung S C, Hinokuma K. Optimized LiFePO4 for lithium battery cathodes[J]. J Electrochem Soc, 2001, 148(3): A224-A229.
[12] Huang H, Cyin S, Nazar L F. Approaching theoretical capacity of LiFePO4 at room termperature at high rates[J]. Electrochem and Solid State Lett, 2001, 4(5): A170-A172.
[13] �� ��, ������, ��־��, ��. ��̼��ʽ��������﮶���ѧ���绯ѧ���ܵ�Ӱ��[J]. ���ϴ�ѧѧ��: ��Ȼ��ѧ��, 2007, 38(5): 863-866.
ZHANG Bao, PENG Chun-li, WANG Zhi-xing, et al. Effect of adding carbon modes on kinetic and electrochemical performances of LiFePO4[J]. Journal of Central South University: Science and Technology, 2007, 38(5): 863-866.
[14] Hu H Q, Doeff M M, Kostecki R, et al. Electrochemical performance of sol-gel synthesized LiFePO4 in lithium batteries[J]. J Electrochem Soc, 2004, 151(8): A1279-A1285.
[15] �� ��, ���º�, ���ı�, ��. LiFe(1-x)MgxPO4����ӵ���������ϵĵ绯ѧ����[J]. ���ϴ�ѧѧ��: ��Ȼ��ѧ��, 2006, 37(6): 1094-1097.
ZHANG Bao, LI Xin-hai, LUO Wen-bin, et al. Electrochemical properties of LiFe(1-x)MgxPO4 for cathode materials of lithium ion batteries[J]. Journal of Central South University: Science and Technology, 2006, 37(6): 1094-1097.
�ո����ڣ�2007-02-05�������ڣ�2007-03-28
������Ŀ��������Ȼ��ѧ����������Ŀ(50302016)
����飺�� ��(1971-)���У����������ˣ���ʿ���²��ϼ��绯ѧ������о�
ͨ�����ߣ��� �����У���ʿ�绰��0731-8836357��E-mail: csuzb@vip.163.com


