���±��: 1004-0609(2006)02-0268-05
����Ni��Һ��Zn�е��ܽ����
�� ��, ¬����, �����
(����������ѧ ���Ͽ�ѧ�빤��ѧԺ, ���� 510640)
ժ Ҫ��
ͨ���о�����Ni�ھ�ֹ��Һ��Zn�е��ܽ���Ϊ, ��������Ȼ�����µ��ܽ�����ģ��, ȷ���˲�ͬ�¶���Ni��Һ��Zn�е��ܽ���Ʋ��衣 �������: 450��ʱ����Ni��Һ��Zn�е��ܽ��ɽ��淴Ӧ������ԭ���ںϽ�����е���ɢ�����ؿ���; 550���650��ʱ, ����Niԭ��ͨ��Һ��Zn��Ũ�ȱ߽�����ɢΪ�ܽ����Ҫ���ƻ���; 650��ʱ, ����ӺϽ���а��������Ni��Һ��Zn�е��ܽ⡣
�ؼ���: ����Ni; Һ��Zn; �ܽ�; ��ɢ
��ͼ�����: T174.4 ���ױ�ʶ��: A
Dissolution mechanism of solid nickel in liquid zinc
KONG Gang, LU Jin-tang, XU Qiao-yu
(School of Materials Science and Engineering,
South China University of Technology, Guangzhou 510640, China)
Abstract: The dissolution behavior of solid nickel in static liquid zinc was studied and a natural convection model considering intermetallic compound layers formation was established to determine the rate-determining step of dissolution rate of solid nickel in liquid zinc. The results show that the dissolution process is governed by a mixed control mechanism involving diffusion of nickel atom in Ni-Zn alloy layers and the chemical reaction between solid nickel and liquid zinc at 450��. At above 550��, the dissolution rates are controlled by diffusion of nickel atom across a concentration boundary layer in liquid zinc, and the dissolution process seems to be accelerated as �� phase peeled off at 650��.
Key words: solid nickel; liquid zinc; dissolution; diffusion
������Һ��Zn�ķ�Ӧ�ڲ��ϱ��洦����ұ����̾�������, ������Ƚ���п�� ��п�۲��ϵ�ѡ�á� �����۵������п���Ͻ������ȡ� ���ڹ�̬������Һ��Zn�еķ�Ӧ�� �ܽ��ѧ�ȷ���, ���в��ٵ��о�����, ��Fe��Һ��Zn�е��ܽ���ɢ[1]�� Co��Zn�еķ�Ӧ����ѧ[2]�Լ�Һ��Zn��Cu���ܽ�[3]��, ��Щ�о��Ļ������۾�Ϊ: ���������Һ���е��ܽ�������Ҫ��Һ�������ʵ���ɢ�����ơ� ����Ni-Znϵ, Dybkov��[4]�Թ�̬��ɢ��Ni/Zn�����Ϧúͦ����������������о��� ���ڹ���Ni��Һ��Zn�е��ܽⷽ����о���δ��������
������, Zn-Ni�Ͻ���ΪʵʩTechnigalva�����Ĺؼ��Ͻ����, �������ȶ�п����ȡ���˹㷺Ӧ��[5]�� ����, Zn-Ni�Ͻ���Ϊ����������Zn-Ni�Ͻ���������[6]��Ӧ��, ���漰������Ni��Һ��Zn���ܽ�����⡣ �������߶���Ȼ���������¹���Ni��Һ��Zn�е��ܽ���̽����о�, �������н����仯����������Ĺ���Ni��Һ��Zn�е��ܽ�ģ��, ��̽�����ܽ���ơ�
1 ʵ��
ʵ����ϲ��ú�99.5%Ni(��������)��Բ������˿����, ԭʼֱ��Ϊ1.000mm; ��п����99.995%п���� ����ʵ����SG2-1.5-6����������¯�зֱ����, ��100g��Zn����30mL����������, ���Ȳ��������¶ȷֱ�㶨��450�� 550��650�档 ȡ50mm����˿����, ��������֬�����80���ܼ�(ZnCl2+NH4Cl)��, ȡ����ɺ��������벢�̶����Ѻ���������, �������Ϊ30mm�� һ��ʱ���, ����һ��ʵ���ǽ���Zn�����˿ȡ����Ѹ��ˮ�䡣 �ö��������������ж�п�����˿�����в����²�(����˿�ײ�20mm��10mm��)��ֱ���仯; ��һ��ʵ�����ǽ�������ͬ��˿����������һ���ˮ��ȴ, �ھ�С���ײ�15mm���ĺ������ȡ���������� ��˿λ���������ġ� �ô��̶�Ŀ���Ľ���������SEM�۲�Ͻ�����������, ��EDS����������, �����ݦ��ࡢ �����(�����ü���1)�ͦ�1��ijɷַ�Χ(��������)�ֱ�Ϊ10%~11%�� 14%~25%(���Ц�Ϊ14%~20%, ��1Ϊ20%~25%)��45%~52%[4, 10], ��ȷ���Ͻ�������ɡ�
2 ���������
2.1 Ni������Һ��Zn�е�ֱ���仯
���о��漰���й����������ݼ���1��
ͼ1��ʾΪ��ͬ�¶��½�Znһ��ʱ���Ni�����в����²�ֱ���ı仯�� ��ͼ�ɼ�, ����450��пԡ�е�Ni����ֱ����ʱ�����������Ӷ����С; ������550��650��пԡ�е�Niֱ����ʱ�����Ӷ���С�� �����Ni��������450��пԡ����ʱ�����γɵĽ����仯������Ȼ���ڱ��ܽ�Ľ����仯�������Zn/Ni��Ӧ���ĵ�������֮��, �ʴ��ж�п���Ni����ֱ�������ԭʼ������
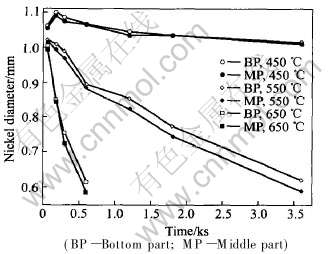
ͼ1 ��ͬ�¶�Һ��п��Ni������ͬ��λֱ����ʱ��ı仯
Fig.1 Variation of reacted nickel diameter as function of reaction time in liquid zinc under different temperatures
��ͼ1�л��ɿ���, Ni����450~650��Һ��Znʱ, �����в�ֱ����С�ñ��¶˸��졣 ��������пԡ�е�Ni �����в����ܽ����ʱ��¶˴� ���� ������������Һ�̽���Һ����������ܶ��ݶȶ��������Ȼ������ɵ�[15]�� ��Ȼ�����ij̶ȿ��ɸ���ϵ������������, ����ϵ������Խ��, ����Ȼ����Խǿ�ҡ� ���帡��ϵ������Ϊ[12]
![]()
�ɱ�1���йص��ܶ�������ò�ͬ�¶���Ni����Һ��Zn�еĸ���ϵ������, ����2�� �ɱ�2�ɼ�, �¶�Խ��, ����Խ��, ����Ȼ����Խǿ�ҡ� ���ڱ�ʵ�������¿���Ni��Һ��Zn�е��ܽ����, ʵ��������Ȼ���������µ��ܽ���ơ�
2.2 ��Ȼ������������������������
����������ԭ��, ��Ȼ����������Բ����ģ����������������̿�����Ȼ�������ȵ�������[8]��Ȼ��, ��ֱ��ʵ���õ�������[12]��
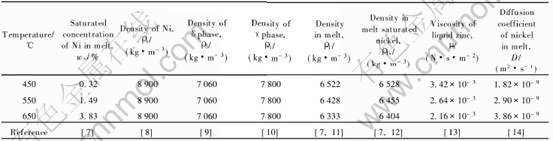
��1 �����������
Table 1 Values of physical properties
��2 ��ͬ�¶���Ni��пԡ�ܽ�ʱ�ĸ���ϵ��
Table 2 Buoyancy coefficient (����) for dissolution of Ni in liquid Zn

��һ��, �ɱ�ʾΪ
![]()
ʽ�� Sh�� Grm��Sc�ֱ��Ӧ�����������Sherwood���� Grashof����Schmit����
��ʽ(2)���Ƶ���������ϵ��kmΪ
![]()
ʽ�� kmΪ��������ϵ��, m/s, ����Ȼ���������¹�Һ�����ϵ�λŨ�Ȳ�ʱ�������ʵ�����ͨ��; lΪ����Һ���е������߶�, m; gΪ�������ٶ�, m/s2�� ��Ȼ, ��ʽ�Ľ�������Ȼ�������ܽ�������������Ƶ�������, ��������ϵ��km����Һ��Zn���й�������������, �������ǹ�������������ɵĽ����仯�ϲ��Ӱ�졣
2.3 ����Ni��Һ��Zn�е��ܽ����ʷ���
SEM�۲켰EDS�����������, Ni����450��Һ��Zn�л��γɦ���ͦ����(��ͼ2(a)); ����550���650��Һ��Znʱ, ���γɦ���, ����ʱ�������Ϊ������ò, ���ı�ʾΪ�úͦ�1��, ����Һ��Zn�¶ȸ�, �ڹ�Һ���渽�����ڵĸ�NiҺ�������ȴ������������������(��ͼ2(b)�� (c)), ���¶�Խ��, �ø�NiҺ����е�NiŨ��Խ��, ������������Խ�ࡣ

ͼ2 Ni���벻ͬ�¶���Znԡ��300s�γ�Ni-Zn�Ͻ���SEM��Ƭ
Fig.2 SEM photos of Ni-Zn phase layers in liquid zinc at different temperarues for 300s
���������Һ��������ܽ�ʱ, ���������غ㶨��, ���Ƴ�����ܽ����ʷ���Ϊ[12]
![]()
ʽ�� SΪ��/Һ�������; VΪ�������; ![]() Ϊ������������������w��ʱ��仯����, ����Ӧ�ڹ���Ni��Һ��п�е��ܽ�����; kdΪ�ܽ����ʳ���, ���ܽ��ɹ��������Һ���е���������������ʱ, kd��Ϊk [12]m��
Ϊ������������������w��ʱ��仯����, ����Ӧ�ڹ���Ni��Һ��п�е��ܽ�����; kdΪ�ܽ����ʳ���, ���ܽ��ɹ��������Һ���е���������������ʱ, kd��Ϊk [12]m��
��ͼ2�ɼ�, Ni��Һ��Zn�е��ܽ������, ��/Һ������γɽ����仯����㡣 ��Ni����ֱ�����ٵ�Ni���ĵ�һ������Ϊ����������ʽ���Һ��, ��һ�������ڽ����仯�������, ���ܽ�ʾ��ͼ��ͼ3�� ��ͼ�ɼ�, Ni��������������msΪ
![]()
ʽ�� hΪ����Һ��Zn�е������߶�, m; r0��r�ֱ�ΪNi������ԭʼ�뾶�͵�ǰ�뾶ֵ, m��
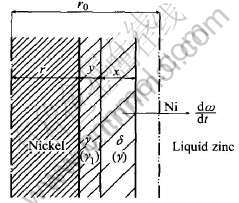
ͼ3 Ni��Һ��Zn���ܽ�ʾ��ͼ
Fig.3 Schematic illustration of nickel
���ڦ���ͦ������ƽ��Ni����ԼΪ10%��20%[4, 10]�� ���ࡢ ������к�Ni��m���� m���ֱ�Ϊ
![]()
![]()
ʽ�� m����m���ֱ�Ϊ����ͦ���㺬Ni��, kg; x��y�ֱ�Ϊ����ͦ����ĺ��, m��
��ʽ(5)��ȥʽ(6)��(7), ���ɵõ�����Һ��Zn��Ni��m(Ni):
![]()
��Һ����Ni����������wΪ
![]()
ʽ�� m0Ϊп����ԭ������, kg��
����r�� x�� y��Ϊʱ��t�ĺ���, ��
![]()
ͨ����ѧ�ɵ�:
![]()
ʽ�� R=��sr+0.1����x+0.2����y
![]()
ʽ�� X=0.1����(r+x+y)
![]()
ʽ�� Y=0.1����x+0.2����(x+y)
����/Һ��������S=2��rh, Һ��Zn����� ![]() , ��ͬʽ(9)~(13)����ʽ(4)����������ܽ����ʳ���kd�ı���ʽΪ
, ��ͬʽ(9)~(13)����ʽ(4)����������ܽ����ʳ���kd�ı���ʽΪ
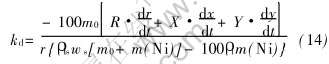
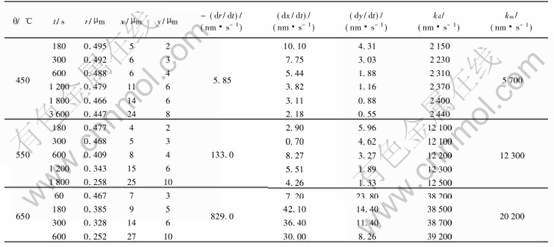
ʽ�� Һ��Zn����m0Ϊ0.1kg; Ni��������߶�hΪ0.03m, r�� x�� y������ʵ����; (dr/dt)�� (dx/dt)��(dy/dt)�ɾ�����������, ��������������1�� 550���650���¦������, ���ʽ(14)�����˱�Ҫ����, ��ʽ�����漰�Ħ����æ�����桢 �����æ�1�����, ����ͦ�1�����ƽ����Ni�����ֱ�Ϊ17%��22%[4, 10]�� ���й����ݷֱ����ʽ(3)��ʽ(14), �������450~650����kd��km, �������3��
��3 ��ͬ�¶��¹���Ni��Һ��Zn�е��ܽ����ʳ�������������ָ��
Table 3 Dissolution rate contant(kd) and mass transfer coefficient(km)of solid nickel into liquid zinc at different temperatures
2.4 �ܽ����ʿ��Ʋ���ķ���
����Һ�������Ӧ�γɺϽ����Ĺ��������Һ������е��ܽ�, ͨ���������²���: 1) �ڹ��������Ͻ��������ϵķ�Ӧ; 2) �Ͻ�����е���ɢ������; 3) �Ͻ������Һ�������Ľ��淴Ӧ; 4) �������ԭ��ͨ����Һ���渽����Ũ�ȱ߽����������䡣 ͨ���ܽ����ʿ���������һ����������ơ� ���ܽ����ʳ���kd����������ϵ��km���бȽ�, ��kd�dz��ӽ������kmʱ, ���4��Ϊ�ܽ����ʵĿ��Ʋ���; ��kdС��kmʱ, ���1~3���е�һ������������Ҫ���á�
�ɱ�3����ɼ�, ��450��ʱ, kdС��km, �������¶��µ��ܽ�������ɽ��淴Ӧ�ͺϽ�����е���ɢΪ��Ҫ���ƻ��ơ�
��550��ʱ, kd����km, ����Ni��Һ��Zn�е��ܽ�������Ҫ��Niԭ��ͨ��Һ��Zn��Ũ�ȱ߽�����ɢ������, �����仯�������γɼ������������谭�ܽ⡣
��650��ʱ, kd����km�� �������¶����ܽ����ʵĿ��Ʋ���Ҳ��������Niԭ��ͨ��Һ��Zn��Ũ�ȱ߽���������������� ����kd�����ۼ���ֵkm���ԭ������������ڸ����ºϽ�����������Ӷ�������Niԭ����Һ��Zn�е���ɢ�� ��ͼ2(c)�ɼ�, ��650�������, ������漫��ƽ��, Ե�����ܽ������������, ����㸽��������ȴ�����������Ħ���������, �����ڦ�����, ��������Ӧ���ǽ�пʱ�Ӧ�����ϰ��������, ���ְ��뽫����Ni��Һ��Zn�е��ܽ�, �����ܽ�ģ����δ�ܿ��ǵ������ء�
REFERENCES
[1]Giorgi M L, Durighello P, Nicolle R, et al. Dissolution kinetics of iron in liquid zinc[J]. J Materials Science, 2004, 39(18): 5803-5808.
[2]Duchenko O V, Vereshchaka V M, Dybkov V I. Phase formation and reaction kinetics in Co-Zn diffusion couples[J]. Journal of Alloy Compounds, 1999, 288: 164-169.
[3]S��rensen O B, Maahn E. The reaction between copper and liquid zinc[J]. Metal Science, 1976, 11: 23-26.
[4]Dybkov V I, Duchenko O V. The homogeneity ranges of �� and �� phase of Ni-Zn system grown by the reaction couple method[J]. Journal of Phase Equilibria, 1998, 19(5): 434-440.
[5]¬����, �½���, �����, ��. пԡ�������ȶ�п����֯��Ӱ��[J]. �й���ɫ����ѧ��, 1996, 6(4): 87-100.
LU Jin-tang, CHEN Jin-hong, XU Qiao-yu, et al. Influence of adding Ni in zinc bath on the microstructure of hot dip galvanized coating[J]. The Chinese Journal of Nonferrous Metels, 1996, 6(4): 87-100.
[6]�����, ��ؾ�, �����, ��. �����п���Ͻ����������Ƽ�Ӧ��[J]. ����, 2002, 51(9): 554-556.
GUO Ling-jun, LI He-jun, LI Ke-zhi, et al. Research and practice on Zn-Ni alloy anoid used in electroplating[J]. Foundry, 2002, 51(9): 554-556.
[7]Nash P, Pan Y Y. The Ni-Zn system[J]. Bulletin of Alloy Phase Diagrams, 1987, 8(5): 422-429.
[8]������, ���, ������. ұ����ԭ������[M]. ����: ұ��ҵ������, 2000. 292.
SHENG Yi-shen, LI Bao-wei, WU Mao-ling. Basic Theory of Metallurgical Transfer[M]. Beijing: Metallurgy Industry Press, 2000. 292.
[9]Critchley J K, Denton S. The crystal structure of ��-Ni-Zn[J]. Joural of Institute Metals, 1971, 99: 26-99.
[10]Vassilev G P, Acebo T G, Tedenac J C. Thermodynamic optimization of the Ni-Zn system[J]. J Phase Equilibria, 2000, 21(3): 287-300.
[11]Crawley A F. Densities and viscosities of some liquid alloys of zinc and cadmium[J]. International Metal Review, 1974, 19: 32-48.
[12]Ishida T. Rate of dissolution of solid nickel in liquid Tin under static conditions[J]. Metallurgy Transactions, 1986, 17B(2): 281-289.
[13]Dell S ��, Chales J, Vlot M, et al. Modelling of iron dissolution during hot dip galvanizing of strip steel[J]. Materials Science and Technology, 2004, 20(2): 251-256.
[14]Roy A K, Chhabra R P. Prediction of solute diffusion coefficients in liquid metals[J]. Metallurgy Transactions A, 1988, 19A(2): 273-279.
[15]Shiah S W, Yang B C, Cheung F B, et al. Natural convection mass transfer along a dissolution boundary layer in an isothermal binary metallic system[J]. Inter Journal of Heat and Mass Transfer, 1998, 41(23): 3759-3769.
(�༭�°���)
�ո�����: 2005-06-20; ������: 2005-11-14
�����: �� ��(1971-), ��, ��ʦ, ��ʿ
ͨѶ����: �� ��, �绰: 020-85511540; E-mail: konggang@scut.edu.cn
[5]¬����, �½���, �����, ��. пԡ�������ȶ�п����֯��Ӱ��[J]. �й���ɫ����ѧ��, 1996, 6(4): 87-100.
[6]�����, ��ؾ�, �����, ��. �����п���Ͻ����������Ƽ�Ӧ��[J]. ����, 2002, 51(9): 554-556.
[7]Nash P, Pan Y Y. The Ni-Zn system[J]. Bulletin of Alloy Phase Diagrams, 1987, 8(5): 422-429.
[8]������, ���, ������. ұ����ԭ������[M]. ����: ұ��ҵ������, 2000. 292.


