DOI: 10.11817/j.ysxb.1004.0609.2020-37635
̼���Ƴ����ᾧ���̼���Ӱ������
�߹���1��������1����С��3���δ���1��������2��Ф���1, 2
(1. ����������ѧ ����ұ��ѧѧ�������� 341000��
2. ϡ�����Źɷ�����˾������ 341000��
3. ���пƼ���������˾������ 100088)
ժ Ҫ��
���̼���Ƴ������ѻ�þ���̼���Ƶ����⣬������̼����Ϊ��������ͨ���������̽����FBRM-PVM�����о��¶ȡ�pH���»������ֵ����ض�̼���ƾ��ͳ�����Ӱ�죬����̼���Ƴ����ᾧ���̽�����������������������(80 �棬pH 5.9~6.0)�����£��ɵõ��������ܽ��Ų�����һ���ᾧ�ȵij��������ʱ̼���ƵĽᾧ�������յ��ɺˡ�����������Ostwald�컯�Ķ�̬ƽ����̣������½���»����̶�̼���ƵĽᾧû������������ã�������гɺ˺ͽӴ��ɺ����ÿ���ʹ���������нϴ������ת��Ϊ��С������ʹ��ϵ�ڿ���ƽ�����ȼ�С�����⣬���ֵĴ��ڿ��Դٽ���������ᾧת�����Ҽ���Ostwald�컯���ھ���ѭ�������У����������Ĺ����dzɺˡ���״��Ƭ״��������״��Ƭ״����ۼ���������ˮ������̼���ƾ��塣ʵ����1�ξ���ѭ���������¼��ɵõ�����12.0 ��m�ҷ�ɢ�Ծ��ȵľ���̼���ơ����Ľ�Ϊ̼���Ƴ����Ʊ�����̼�����ṩ����ָ����
�ؼ��ʣ�
̼������FBRM-PVM���ᾧ��̼������Ostwald�컯��
���±�ţ�1004-0609(2020)-10-2457-18���� ��ͼ����ţ�O614.33��TF845.3���� ���ױ�־�룺A
��������һ����Ҫ�ĸ�������Ϳ�������̼Ϳ�����[1-2]��ͬʱҲ�㷺Ӧ�����մɲ���[3]���������[4]����������[5]������̼������Ϊ�Ʊ������Ƶ���Ҫǰ���壬�������Ʋ�Ʒ���Ʊ�����������ҪӰ�졣
���ڳ��������о�ȷ�������ϻ�ѧ��ɡ�ԭ�ϳɱ��͡����ռ�����������ŵ㣬���Թ�ҵ���ձ���ó������Ʊ�̼��ϡ�����������ջ��ϡ�������Ŀǰ�Ʊ�̼��ϡ���ij�������̼����李�̼�����ơ�̼���Ƶȣ�����̼����麟����������ã��Ƽ������ߴ�������ᾧ����[6-10]����ҵ��Ӧ��[11-12]�����˺ܶ���о���ʵ����̼����林��ģ�����Ʊ�����̼��ϡ���IJ�ҵ������̼����淋�ʹ�û���������İ�����ˮ��Ҫ����ˮ���������Ҫ�����ܴ�Ĵ��ۡ���ˣ����Ź��ҶԻ������ӳ̶ȵ����ӣ���������̼���ƻ�̼�����ƴ���̼�������Ϊ��������ҵ�ڹ�ͬ��ע��һ���ȵ㡣Ȼ��̼���ƻ�̼��������Ϊ����������ϡ����Һ�������γ�������״�������ᾧ�ȵ�[13-15]��Ϊ���������⣬ϡ������������һϵ�е��о������罹С���[13]��̼�����Ƴ�����Ľᾧ���̽������о����õ���̼����ᾧ����������˾���̼���磻�������[14]��̼��������������ͨ�������������ƣ�������׳��������˵�̼�����ϣ���������[15]���������Ϸ�ʽ����̼�������������Ʊ����˵���Ƭ״̼���磻��ϰ���[16]�Թ�ҵ̼����������������ͨ�����뾧�ּ����������ĵ��أ��õ�����̼�����ϣ�NAGASHIMA��[17]�ֱ���̼���ƺ�̼������Ϊ����������ϡ��̼���ε��Ʊ��ͽṹ�������о����������¶ȶ�ϡ��̼�����γ�Ӱ�졣Ȼ���������о�����IJ����ڳ���Ч�����շ�����ֻ�����˳������̵ķ�Ӧ����δ��̼��ϡ���Ľᾧ���̽����о�����Ϊ��Ҫ���ǣ�������Щ�о���Եĸ�������ϡ��Ԫ�أ���û���漰�Ƶ���ϡ��Ԫ�صĽᾧ���̺��ա�
�����̼�����ƣ�̼���Ƴ���1 molϡ�����������̼�����Ƶ�һ��[14]���ɱ����ͣ�����̼������Һ�ļ�ȸ�����ᾧ���̱�̼�����Ƹ��ѡ����ǵ������Ƶ���Դ���ƺ�̼���Ƶijɱ����ƣ��������Ȼ�����ҺΪ�о�������̼����Ϊ����������ϸ�о����¶�-pH���»������ֵ����ض�̼���Ƴ������̵�Ӱ�죬��ͨ��FBRM-PVM��̼���Ƴ����ᾧ���̺ͻ���������̽�֣����ջ���˽ᾧ���õ�̼���ơ����ĵ��о���Ϊ̼���Ƴ����Ʊ�����̼�����ṩ����ָ������ϡ���������յ���������������Ҫ���塣
1 ʵ��
1.1 ʵ��ԭ��������
ʵ��ԭ�ϣ�Ũ��Ϊ1.5 mol/L���Ҹߴ��Ȼ�����Һ���ɸ���տ���²��ϿƼ��ɷ�����˾�ṩ�����⣬EDTA����ˮ̼���Ƶ��Լ���Ϊ��������������¤��ѧ�ɷ�����˾��
ʵ��������������(Rw20��IKA)�����ӷ�����ƽ(AL204��Mettler-Toledo)���䶯��(BT300-2J�������������������˾����)��pH��(FE20K������0.01��Mettler-Toledo)��ˮѭ����ձ�(SHB-B95A��֣�ݳ��ǿƹ�ó����˾����)������ˮԡ��(DF-101S����������������������˾����)������������(Mastersizer 3000E��Malvern Panalytical)��ɨ��羵(SEM��Quanta250/MLA650F�� ThermoFisher Scientific)��X���߶ྦྷ������(XRD�� Empy-rean��PANalytical Co., Ltd.)���۽��������������(Focused Beam Reflectance Measurement(FBRM)�������ߴ磺0.5 ��m~2.0 mm���¶ȷ�Χ��-90~300 �棬ѹ����Χ����1��103 Pa��Mettler-Toledo)������¼Ӱ����(Particle video microscope(PVM))�������ߴ磺2 ��m~1 mm���¶ȷ�Χ��-80~120 �棬ѹ����Χ����1��103 Pa��Mettler-Toledo)��
1.2 ʵ�����
1) �����ᾧ���̣��Ըߴ��Ȼ�����Һ��̼����Ϊԭ�ϣ�����0.1 mol/L YCl3��Һ��0.15 mol/L Na2CO3��Һ�������䶯�÷ֱ����YCl3��Һ��Na2CO3��Һ�ļ����ٶȣ��Բ����ķ�ʽ��������Һ������һ����ˮΪ��Һ���ձ��У�ʵ��ͨ������������Һ�ļ����ٶ���������ϵpH��ͨ��ˮԡ�����Ʒ�Ӧ�����¶ȣ�ͨ�����������ƽ����ٶȣ�����ʹ������Ӧ��һ���¶ȡ�pH�������ٶ��½��С�
2) �»����̣���һ�����������µõ��ij�������Ϊԭ�ϣ��ڲ�ͬ�¶��½��н���»�����ó»����
3) ����ѭ�����̣���һ�����������µõ��ij�������Ϊ��Һ������������ͬ�����µij������̷�Ӧ��������Ӧ��������һ��������Һ����Һ���Դ����ƣ�����3��ѭ����
���ն�������ͬ�λ�õIJ���������ȡ����ࡢ��ò�ȷ��������⣬��Ҫע����ǣ���ʹ��FBRM��PVM��������ϵ��ʵ������У����������ķ�Ӧ��������ϳ������ʵ���С������ʹ��FBRM��PVM���Է�����ʵ�鷴Ӧʱ���볣�����ʵ�鷴Ӧʱ���в�𣬵�������ᾧ���̾���һ���Ĵ����ԡ�
1.3 ���Է���
��������ᾧԽ�ã��������������ҲԽ��[6, 14]�����ʵ������ͨ���۲����ij������ܣ��Գ����жϲ�ͬ�β���Ľᾧ������������Ϊ��ȡ100 mL���������100 mL��Ͳ���Դ˹۲��¼����һ���������ʱ�䣻��ͬ�λ�õIJ������X���߷�ĩ�����Dz��������࣬����ɨ��羵�����侧����ò�����ü��������Dzⶨ̼���Ƶ�ƽ������(D50)�����ȷֲ�((D90-D10)/2D50)������ʵʱ���߿�������ϵͳFBRM��PVM�Գ����ᾧ���»�������ѭ�����̽������ȼ�ʵʱͼ�������
ͨ��FBRMʵʱԭλ�����ٿ������ȼ��ֲ��ı仯��������ԶԽᾧ��������ָ����ͨ��PVMʵʱ����¼������ͼ����Ϣ�����Խ��ᾧ���̿��ӻ�����һ����ʾ�ᾧ������
2 ���������
2.1 �¶�-pH��̼���Ƴ����ᾧ���̵�Ӱ��
2.1.1 �����ᾧ��������¶�-pH��ȷ��
��̼���ƹ�������Һ�У�Y3+��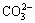 ���ײ�۶���ɾ���[18]�������˳�����ٶȴ��ھ������ɵ��ٶ�ʱ����Խ�����γ�̼���ƾ��ͳ����������Ч��ҲԽ�á��¶Ⱥ�pH������������ɢ�ٶȺ���Һ�����Ͷ�Ӱ��ܴӶ��������������ɺͳ�������Ϊ�Ʊ�����̼���ƣ�ѡ����ʵ��¶Ⱥ�pH��Χ��Ϊ�ؼ�[6, 19]��
���ײ�۶���ɾ���[18]�������˳�����ٶȴ��ھ������ɵ��ٶ�ʱ����Խ�����γ�̼���ƾ��ͳ����������Ч��ҲԽ�á��¶Ⱥ�pH������������ɢ�ٶȺ���Һ�����Ͷ�Ӱ��ܴӶ��������������ɺͳ�������Ϊ�Ʊ�����̼���ƣ�ѡ����ʵ��¶Ⱥ�pH��Χ��Ϊ�ؼ�[6, 19]��
���Ʋ�ͬ��Ӧ�¶�-pH����̼���Ƴ���ʵ�飬�۲��������ij������ܣ������ͼ1��ʾ����ͼ1�п��Կ��������ų�����Ӧ�¶����ߣ���������������Ӧ�����pHֵ��Χ��Լ�С���統�����¶�Ϊ60 ��ʱ��pH 6.4~6.5�����³�����죬�������¶�Ϊ80 ��ʱ��pH 5.9~6.0�����³�����졣���⣬�ڲ�ͬ�¶ȺͶ�Ӧ���pH��Χ�����£���������ij���Ч��Ҳ�нϴ�������(60 �棬pH 6.4~6.5)��(70 �棬 pH 6.0~6.1)��(90 �棬pH 5.7~5.8)�����£�����50 mL����ʱ��ֱ�Ϊ190 s��163 s��186 s������(80 �棬pH 5.9~6.0)�����£�����50 mL����ʱ��Ϊ138 s��С�����������µij���ʱ�䣬�����������죬����������ѣ�˵��(80 �棬pH 5.9~6.0)�����»�õij�������ᾧ����ߡ�������Ϊ�¶�Խ�ߣ��ṩ������Խ�࣬����Խ���˷�����������ݶ��ᾧ����pH������Ӱ��̼���ƵĹ����Ͷȣ�ֻ���ڽϵ͵Ĺ����Ͷ��£�̼���Ƶijɺ����ʲ���С���������ʣ��Ӷ���ýϴ��̼���ƾ��塣
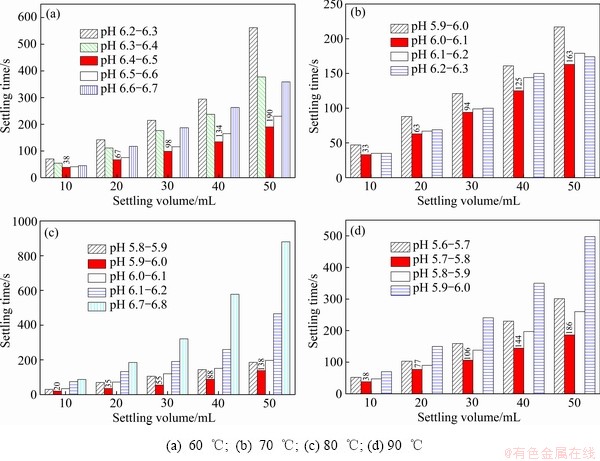
ͼ1 ��ͬ�¶Ⱥ�pH��Χ���������ó�������ij�������
Fig. 1 Settling properties of precipitate product obtained under different temperatures and pH ranges
ѡȡ(60 �棬pH 6.4~6.5)��(80 �棬pH 5.9~6.0)�����»�õij����������XRD��SEM�����������ͼ2��ʾ����ͼ2(a)�п��Կ�������Ӧ�¶�60 ��ʱ���ó��������XRD����û�����Ե�����壬������80 �������£������������з�ǿ�Ƚ�С������ϴ������壬�������������Y2(CO3)3��2H2O��ͼ��(PDF#24-1419)���Ǻϡ�ͬʱ��ͼ2(c)��Ҳ���Կ�������80 ����������������״�������ɣ�������80 �����в��ֽᾧ̼�����������������������ܵ�������һ���ԡ�
2.1.2 �����ᾧ���̵�ԭλ���ȼ�ʵʱͼ�����
Ϊ��̽��(80 �棬pH 5.9~6.0)�����µ�̼���Ƴ����ᾧ���̣�����FBRM-PVM�Գ����ᾧ���̽������ȼ�ʵʱͼ������������ͼ3��4��ʾ��һ������£��ᾧ���̿��Է�Ϊ�ɺ˺������������̣����о����ǹ�������Һ�������ɵ�С�������ӣ��Ǿ���������������Ҫ�ĺ��ġ���û�о��֡����������ʻ����Ӱ�������£��ɺ˹���Ϊ��������ɺˣ��ھ����յ������£��ɺ˹���Ϊ���γɺˡ���������ɺ�[20]�������������ӿ����˶����������һ���γ����壻Ȼ������ĵ�Ԫ������ij���ȣ����Գ�Ϊ���ߣ��������;��������������ñ˴�֮��Ѹ�پۼ������������ٽ�ɺ˳ߴ��Ϊ������Һ��������ѧƽ��ľ��ˡ��ӹ����ͶȽ�������������֮���һ��ʱ��Ϊ�յ��ڡ�ͼ3��ʾΪ�����ᾧ���̵�FBRMͼ������˳����ᾧ�����в�ͬ����������������߱仯��ƽ���������߱仯�Ͳ�ͬʱ�����ȷֲ�����ͼ3(a)�ɼ���ǰ10 minʱ������Ŀ������������������ʱ�����ҪΪ�յ��ɺ���(��1��)����Ҫ������С�����������ӣ����Ҵ�ͼ3(b)Ҳ���Կ�������ǰ10 min�ڣ������յ��ɺ��ھ��˽��٣�����FBRM�豸�����Ķ�Ϊ��������;����γɵĴ�Χ��״�������ƽ�������нϴ����յ��ɺ��ںᾧ���̽����2�Σ���ͼ3(a)�ɼ������ų�����Ӧ���У���ϵ�ڲ����������(100~1000 ��m)����С����(��10 ��m)��Ŀ���еȿ���(10~100 ��m)��ĿѸ�����ӣ������ܿ�����(��1000 ��m)Ѹ�����ӣ������еȿ�����Ŀ�����С������Ŀ���������ʸ�������ζ�Ŵ�ʱ��δ��ھ��������ڣ���ͼ3(b)��(c)Ҳ���Կ�����10~40 min��ƽ�����������ӣ����ȷֲ��������ҷ�ƫ�Ʋ�Ѹ���������ڵ�3�Σ���ͼ3(a)�Ŀ��������߱仯����б��������С��������������ƽ�Ⲣ���еȿ�������������С��������ΪС������������Ŀ�����ʵ��Է��ɺ���Ŀ����ƽ�⣬�����������еȿ�����ͬʱ����һ������ԭ���еȿ��������ϳ���ʱ��û�г���100 ��m������ȻΪ�еȿ����������������ʼ�С������ζ�Ŵ˽���Ҫ����С���������ںͽϴ��еȿ����ij���[21]���ᾧ������ת�뵽Ostwald�컯����[21-23]����ͼ3(b)��(c)Ҳ���Կ�����ƽ�����Ȳ������ӣ����ȷֲ�������������Ҳ��С��ֹͣƫ�ƣ�˵�����ȷֲ������У�������ΪС�����������Լ����γɺ����ý�ʹС����ƽ�����ȼ�С�ķ��Ƚϴ��еȿ����ļ��������볤��ʹ�еȿ���ƽ�����ȵ����ӵķ��Ƚ�С������ʹ��ƽ�����ȱ仯����ƽ�⡣
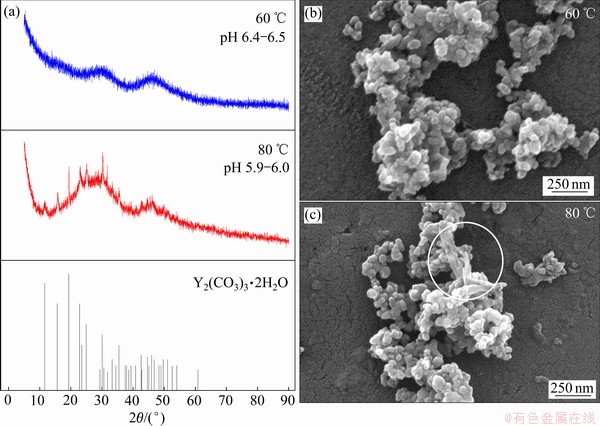
ͼ2 ��60 ���80 ��-���pH�µõ��ij��������XRD��SEM��
Fig. 2 XRD patterns(a) and SEM images((b), (c)) of precipitate product obtained at 60 �� and 80 �� with optimal pH ranges
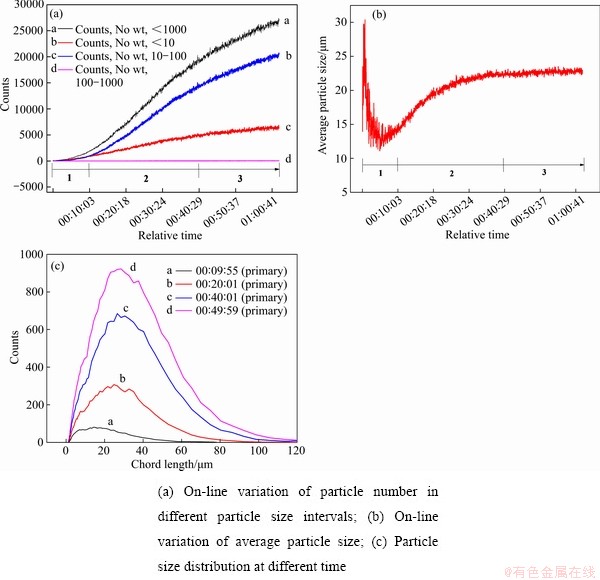
ͼ3 �����ᾧ�����в�ͬ����������������߱仯��ƽ���������߱仯�Ͳ�ͬʱ�����ȷֲ���FBRMͼ
Fig. 3 FBRM images during precipitation crystallization process (80 ��, pH 5.9-6.0)
ͼ4��ʾΪ�����ᾧ�����в�ͬʱ�̵�PVMͼ����10 minʱ����������Ҫ������״�����۲쵽�����ر���ò�Ŀ�������(��ͼ4(a))�����ŷ�Ӧ���У�Ũ������״�����е�С�������еȿ������࣬����Խ��Խ�����ɼ�(��ͼ4(b)��(c))����40 min��С�������еȿ���״�����������������Dz�������̬������������ͼ������ʾ����̬��С����Ŀ���������DZ仯(��ͼ4(d)~(f))����Ҳ��֤������̼���ƿ��������ᾧ���̷�����

ͼ4 �����ᾧ�����в�ͬʱ�̵�PVMͼ
Fig. 4 PVM images at different time during precipitation crystallization process (80 ��, pH 5.9-6.0)
2.1.3 �����ᾧ���̲����XRD��SEM�����ȱ仯����
Ϊ�˽�һ����֤̼���Ƴ����ᾧ���̣���(80 �棬 pH 5.9~6.0)�ij���ʵ��Ϊ���Բ�ͬ��Ӧʱ���µõ��ij������������XRD��SEM�����ȱ仯�����������ͼ5��6��ʾ����ͼ5(a)�пɿ�������150 minʱ���ɵij���������ǿ�Ƚ�С������ϴ������塣��ͼ5(b)~(f)�п��Կ������ڷ�Ӧ��ʼ�Σ������͵�̼�����յ��������������ˣ���Щ���˴����žۣ������ŷ�Ӧ���У����Կ�����Щ���������������壬��ʱ������������������˾������ܽ��ɢ���̣�������ʱ��ʵ���ٽᾧ����������״�������ɣ����������ɴ˿ɼ�����Ӧ�ᾧ�������յ��ɺˡ�����������Ostwald�컯�Ķ�̬ƽ����̡�
ͼ6��ʾΪ��ͬ��Ӧʱ�����ó�����������ȼ����ȷֲ��仯ͼ����ͼ6�п��Կ��������ų���ʱ�������������ƽ���������������ȷֲ�����1���ң��ֲ����ȡ������������ᾧ�����о����ڲ���������
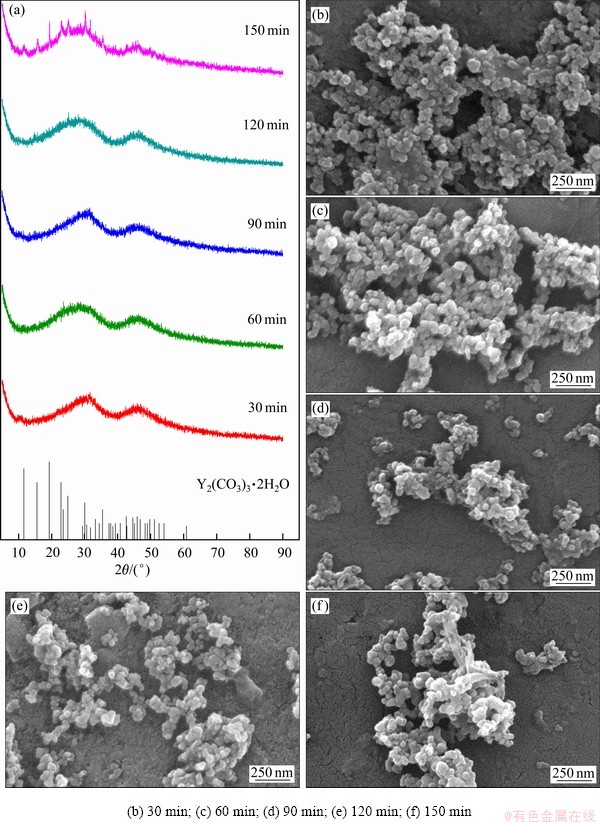
ͼ5 ��ͬ��Ӧʱ�����ó��������XRD��SEM��
Fig. 5 XRD patterns(a) and SEM images((b)-(f)) of precipitate product obtained at different reaction time (80 ��, pH 5.9-6.0)
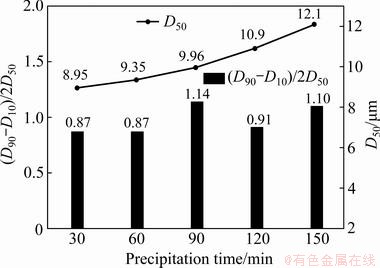
ͼ6 ��ͬ��Ӧʱ�����ó�����������Ⱥ����ȷֲ��仯ͼ
Fig. 6 Particle size and particle size distribution of precipitate product obtained at different reaction time (80 ��, pH 5.9-6.0)
2.2 �»����̶�̼���ƽᾧ���̵�Ӱ��
2.2.1 ��������»�����̽��
һ������£��»����̻ᵼ��С���Ӳ����ܽ�������Ӽ�������ʹ�����������������������ȣ�ͬʱҲ�ı侧������ȷֲ���ʹ���ȷֲ�����խ�����ҳ»��¶Ⱥ�ʱ��ֱ��Ӱ������ᾧ���̶�[6, 24-25]����ˣ�ʵ����(80 �棬pH 5.9~6.0)�����»�õij�������Ϊ�о������о��˳»��¶Ⱥ�ʱ���̼���ƽᾧ���̵�Ӱ�죬ͼ7��ʾΪ��ͬ�¶Ⱥ�ʱ�����������ó»�����ij������ܡ���ͼ7�п��Կ��������ų»��¶ȵ����ߣ��»�����ij���ʱ�併�ͣ�����ͬ�»��¶��£����ų»�ʱ������ӣ��»�����ij���Ч��Խ�����80 �������£��»�1��2��4��6 h����50 mL����ʱ��ֱ�Ϊ162��189��192��267 s���ɴ�˵����������������������ºͶ�ʱ��ij»��Գ»�����Ľᾧ�Կ�����һ����������á�
2.2.2 �»����̵�ԭλ���Ⱥ�ʵʱͼ�����
Ϊ�˽�һ��̽��80 �������µij�������(̼����)�»����̣�����FBRM-PVM�Գ»����̽������Ⱥ�ʵʱͼ������������ͼ8��9��ʾ��ͼ8��ʾΪ�»�������FBRMͼ����ͼ8(a)�ɼ������ų»���Ӧ���У���ϵ�ڲ����ڴ����(100~1000 ��m)��С����(��10 ��m)��Ŀ���еȿ���(10~100 ��m)��Ŀ�������ӣ������ܿ�����(��1000 ��m)���ӣ�����С�������������ʽϴ�������Ϊ�»������д��ڴ����Ķ��γɺ�[26-27]������Ҫ��������Դ��һ����Һ�����������ľ���֮���������˶��ٶȣ�������߽���д��ڵļ�Ӧ��ʹһЩ�����ھ����ϵ�С�������䣻���ǵ����������ľ�������轰�����ڻ��������巢���Ӵ�ʱ�����������Ƭ�������������ӻ��߽ϴ�ľ�����Ƭ�����ȴ����ٽ����ȣ��Ϳ��Գ�Ϊ�µľ��ˣ���������������л��߿�����ײ���ö������Ķ��γɺ˿ɳ�Ϊ���гɺ˺ͽӴ��ɺˡ���һ���棬����Ҳ�����ƻ������ľ۽�����[6, 28-29]��������ϵ�ڿ������ı仯���»������У����ڼ��гɺ˺ͽӴ��ɺˣ�С�������ϲ�����Ȼά����10 ��m���������ȸ�С�Ŀ��������еȿ����ڲ��ϲ���С������ͬʱ��Ҳ���ܲ��������ά��10~100 ��m��Χ���еȿ��������磬һ��80 ��m���еȿ������ܲ���5 ��mС������20/25/30 ��m���еȿ���������С������Ŀ�����Ͽ죬�еȿ�����Ŀ��������������������Ŀ�仯�����µĽ����ͼ8(b)��ʾ���ڳ»��Σ�����ƽ��������С��ͼ8(c)Ҳ���������ų»�ʱ������ƣ����ȷֲ�����������ƫ�ƣ��������ߣ���������ƽ��������С����Ҳ������������Ŀ�仯��ƽ�����ȱ仯���������
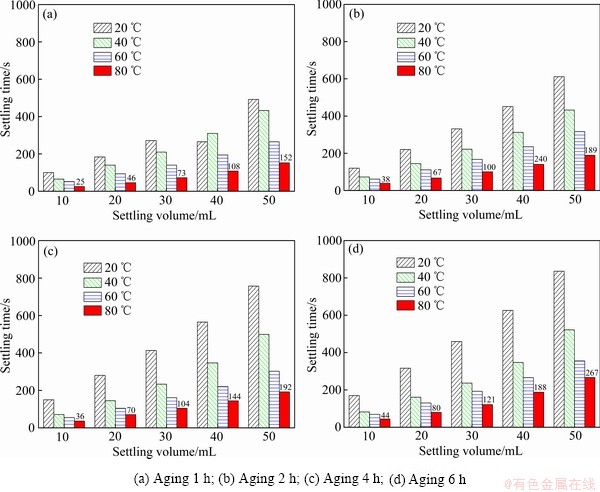
ͼ7 ��ͬ�¶Ⱥ�ʱ�����������ó»�����ij�������
Fig. 7 Settling properties of aged product obtained under different temperature and time
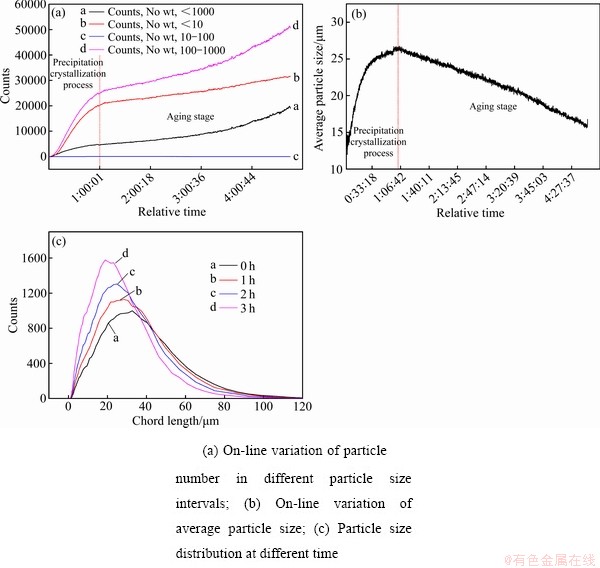
ͼ8 �»�������FBRMͼ
Fig. 8 FBRM images during aging process
ͼ9��ʾΪ�»������в�ͬʱ�̵�PVMͼ����ͼ9�п��Կ��������ų»���Ӧ�Ľ��У�С�����������࣬�ϴ��еȿ�������Ŀ���ٲ�������С�еȿ������»�3.5 hʱ�����Ѿ��dz��ܼ����ⶼ��֤�������������߱仯���ɣ����֤����ϵ�ڴ��ڴ����Ķ��γɺˡ�
2.2.3 �»����̲����XRD��SEM�����ȱ仯����
Ϊ��һ����֤̼���Ƴ»���Ӧ���̣���80 �������³»���ͬʱ�����ó»����������XRD��SEM���������ȱ仯�����������ͼ10��11��ʾ����ͼ10�п�֪�������δ�»��ij��������XRD�ף���ͬ�»�ʱ���µij»����ﶼ�����͵ģ��ɼ��ڳ»������п�����û�о�������������Ϊ�����Ķ��γɺˣ������ƻ��ᾧ�����á�ͼ11��ʾΪ��ͬ��Ӧʱ�����ó»������SEM��ͼ11�п�֪���»������в�û�нᾧ�����������ɽϴ������ɽ�С��������Ϊ�����������[6]��Ҫ���ʷ�����������ɢ�������ھ�������̶����������ڳ»������У���Һ�м����Ѳ�����Y3+��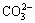 ��������ϵ�ڴ��ڵ��ٲ�������;���Ҳ�����ṩ�㹻�Ĺ�����֣�ȱ���˾��������ı�Ҫ���������Գ»���û��ʹ�����������Ϊ���塣�෴�����ڳ»���������ϵ��ϵ�ھ��������Ķ��γɺ˹��̣�������ƽ�����ȵļ�С��
��������ϵ�ڴ��ڵ��ٲ�������;���Ҳ�����ṩ�㹻�Ĺ�����֣�ȱ���˾��������ı�Ҫ���������Գ»���û��ʹ�����������Ϊ���塣�෴�����ڳ»���������ϵ��ϵ�ھ��������Ķ��γɺ˹��̣�������ƽ�����ȵļ�С��
ͼ12��ʾΪ��ͬ��Ӧʱ�����ó»���������Ⱥ����ȷֲ�ͼ�����ų»�ʱ�������ƽ��������С�����ȷֲ�����1���ң��ֲ����ȡ�����������»����������ڴ��ڴ����Ķ��γɺ˶�ʹƽ�����ȼ�С�Ľ��ۡ�

ͼ9 �»������в�ͬʱ�̵�PVMͼ
Fig. 9 PVM images at different time during aging process
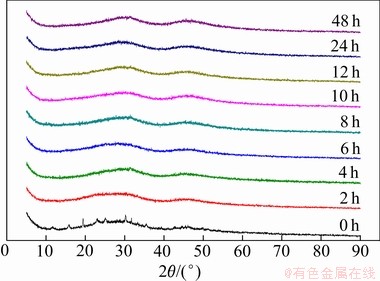
ͼ10 ��ͬ��Ӧʱ�����ó»������XRD��
Fig. 10 XRD patterns of aged product obtained at different reaction time
2.3 ����ѭ����̼���ƽᾧ���̵�Ӱ��
2.3.1 ����ѭ������̽��
���������ᾧ���̵��о���Ȼ�õ�����ѳ����ᾧ�¶Ⱥ�pH�����dz���������̼���ƽᾧ����Ȼ���ߣ����ҳ»��Գ�������ľ���Ҳ�����á����ǵ����־���ʹ�ᾧ����������������[7]��Ϊ�õ��ᾧ�Ϻõ�̼���ƣ�ʵ����(80 �棬pH 5.9~6.0)�ij��������£��о��˾���ѭ���Խᾧ���̵�Ӱ�졣ͼ13��ʾΪ��ͬ����ѭ���������ó����������50 mL�ij���ʱ�䡣��ͼ13�ɼ���ÿ��ѭ�����ó�������ij���ʱ�䶼Ҫ����δѭ���ij���������������ѭ��ʹ̼���ƵĽᾧ����ߡ�
ͼ14��ʾΪ��ͬ����ѭ���������ó��������XRD��SEM��ͼ14(a)�п��Կ�����ѭ������������ʹ̼������������խ��ǿ���������������ѭ����ʹ̼���ƾ������������Ч����һ�¡����ҵ�1��ѭ���ѿɵõ�����̼���ƣ�δ�����������࣬�������������Y2(CO3)3��2H2O��ͼ��(PDF#24-1419)���Ǻϡ���ͼ14(b)~(e)�п��Կ������ھ���ѭ�������У�̼���Ƴ�����������״���壬Ȼ��������Ƭ״�ᾧת�����ڶ���ѭ����̼�����ѱ������״��Ƭ״�ۼ��������ξۺϾ��壬�����ˮ������[6-7]̼���Ƶ���̬�ṹ����������ˮ�������е�C(1) ��ϡ�����ӹ���(002)ƽ�����λ��ʽ����ʹ̼�������ȳ�һά��������γʶ�ά���������Ծ���ѭ��ʵ��õ���ˮ������̼���Ƴ���״��Ƭ״�������ξۺϾ��塣��ˣ�̼���Ƴ�������̼���Ƶij���������ѭ�������У�����������һ���ɺˡ���״��Ƭ״��������״��Ƭ״����ۼ��������ξ���Ĺ��̣�ʾ��ͼ��ͼ15��ʾ��
��ϡ�����ӹ���(002)ƽ�����λ��ʽ����ʹ̼�������ȳ�һά��������γʶ�ά���������Ծ���ѭ��ʵ��õ���ˮ������̼���Ƴ���״��Ƭ״�������ξۺϾ��塣��ˣ�̼���Ƴ�������̼���Ƶij���������ѭ�������У�����������һ���ɺˡ���״��Ƭ״��������״��Ƭ״����ۼ��������ξ���Ĺ��̣�ʾ��ͼ��ͼ15��ʾ��

ͼ11 ��ͬ��Ӧʱ��ij»������SEM��
Fig. 11 SEM images of aged product at different reaction time
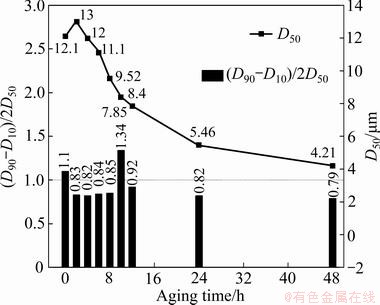
ͼ12 ��ͬ��Ӧʱ�����ó»���������ȼ����ȷֲ��仯ͼ
Fig. 12 Particle size and particle size distribution of aged product obtained at different reaction time
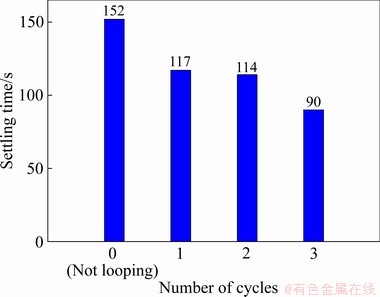
ͼ13 ��ͬ����ѭ���������ó����������50 mL�ij���ʱ��
Fig. 13 Settling time of precipitate product sedimentation of 50 mL obtained at different number of cycles of seed crystals
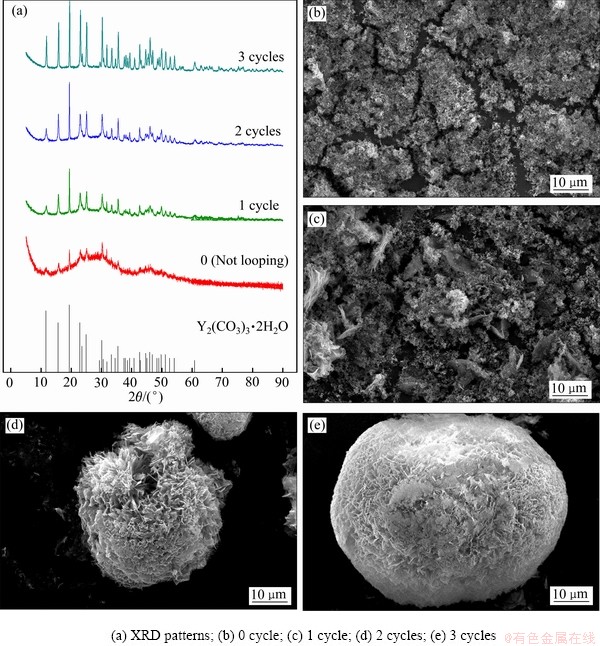
ͼ14 ��ͬ����ѭ���������ó��������XRD��SEM��
Fig. 14 XRD patterns(a) and SEM images((b)-(e)) of precipitate product obtained at different number of cycles of seed crystals
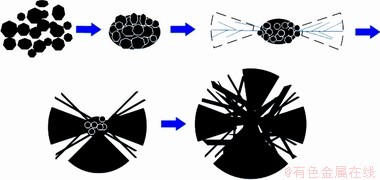
ͼ15 ������������̬�ݱ����ʾ��ͼ
Fig. 15 Schematic diagram of morphological evolution of crystals growth
ͼ16��ʾΪ��ͬ����ѭ����������̼�������Ⱥ����ȷֲ��仯ͼ����ͼ16�ɼ�������ѭ�����������ӣ���Һ�е�ϡ�����Ӻ�̼������ӳ����ھ��ֱ�������������̼���Ƶ�������������ѭ������Ϊ3��ʱ������̼����ƽ�����ȴﵽ22.9 ��m��������������������������̾���һ���ԡ�
2.3.2 ����ѭ�����̵�ԭλ���Ⱥ�ʵʱͼ�����
Ϊ�˽�һ��̽������ѭ����Ӧ�ᾧ����������FBRM-PVM��ѭ�����̽������Ⱥ�ʵʱͼ������������ͼ17��18��ʾ��ͼ17��ʾΪ����ѭ��������FBRMͼ��ͼ17(a)��ʾΪ��ͬ��������̼���ƿ��������߱仯ͼ����1�ξ���ѭ��������С����(��10 ��m)��Ŀ�����ޱ仯���еȿ���(10~100 ��m)��Ŀ��ԭ�л����ϻ������ӣ������ܿ�����(��1000 ��m)Ҳ����������������Ϊ�ڵ�1��ѭ���У������ٲ���С�������ܽ⣬С�����ܽ�������������ӡ����塢�����Լ������Y3+��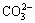 ��Ϊ������ݣ��佫�ھ��ֱ������������һ���ֽ���10 ��m��С��������Ϊ�еȿ��������еȿ�������������ʱ��ϵ��Ҳ�����������ӵ��Է��ɺˣ��Է��ɺ��γɵ�С������Ŀǡ�ú�����С��������Ŀ�����������С������Ŀ�仯����ƽ�⣬���еȿ�����Ŀ���ࡣ����������Ŀ�����ȱ仯��������ϵ��ƽ�����ȳ������ӣ���ͼ17(b)��ʾ���ڵ�2�ξ���ѭ�������У���ͼ17(c)��ʾ����ϵ����С����(��10 ��m)��Ŀ��С�����еȿ���(10~100 ��m)��Ŀ�������仯������ܿ�����(��1000 ��m)Ҳ�������١�������Ϊ��2��ѭ���У�С�������ܽ���Y3+��
��Ϊ������ݣ��佫�ھ��ֱ������������һ���ֽ���10 ��m��С��������Ϊ�еȿ��������еȿ�������������ʱ��ϵ��Ҳ�����������ӵ��Է��ɺˣ��Է��ɺ��γɵ�С������Ŀǡ�ú�����С��������Ŀ�����������С������Ŀ�仯����ƽ�⣬���еȿ�����Ŀ���ࡣ����������Ŀ�����ȱ仯��������ϵ��ƽ�����ȳ������ӣ���ͼ17(b)��ʾ���ڵ�2�ξ���ѭ�������У���ͼ17(c)��ʾ����ϵ����С����(��10 ��m)��Ŀ��С�����еȿ���(10~100 ��m)��Ŀ�������仯������ܿ�����(��1000 ��m)Ҳ�������١�������Ϊ��2��ѭ���У�С�������ܽ���Y3+��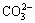 �ļ�����ҪΪ�еȿ����ļ��������ṩԭ�ϣ����������Է��ɺˣ������еȿ�������ԭ�л����������������20 ��m������30 ��m��������������Ŀû�����࣬����С������Ŀ���٣����еȿ�����Ŀ�仯����ƽ�⡣����ѭ�����̵ı仯�����µĽ����ͼ17(d)��ʾ����ϵ�ڿ���ƽ������һֱ�����ӡ���ͼ17(e)��ʾ����3��ѭ����ϵ��С����(��10 ��m)��Ŀ��Ȼ��С�����еȿ���(10~100 ��m)��ĿҲ�������䣬��Ҳ�����ܿ�����(��1000 ��m)���м��١�������Ϊ��3��ѭ���У�С�������ܽ���Y3+��
�ļ�����ҪΪ�еȿ����ļ��������ṩԭ�ϣ����������Է��ɺˣ������еȿ�������ԭ�л����������������20 ��m������30 ��m��������������Ŀû�����࣬����С������Ŀ���٣����еȿ�����Ŀ�仯����ƽ�⡣����ѭ�����̵ı仯�����µĽ����ͼ17(d)��ʾ����ϵ�ڿ���ƽ������һֱ�����ӡ���ͼ17(e)��ʾ����3��ѭ����ϵ��С����(��10 ��m)��Ŀ��Ȼ��С�����еȿ���(10~100 ��m)��ĿҲ�������䣬��Ҳ�����ܿ�����(��1000 ��m)���м��١�������Ϊ��3��ѭ���У�С�������ܽ���Y3+�� �ļ������Ϊ�еȿ����ij����ṩԭ�ϣ�����ͬ�������еȿ�����ԭ�л���������������������Ŀ�������࣬����С������Ŀ��Ȼ���٣����еȿ�����Ŀ�仯����ƽ�⡣������ͼ17(f)��ʾ��ƽ������û�г������ӣ�����������һ���̶Ⱥ����䡣�������ڿ���Խ�����Խ�������������ӡ����塢���ߵȾ���������ݵ�λ��ҲԽ�࣬������������Ĺ�����ݹ�Ӧ���㣬����ʹ���еȿ������������dz����������Ҽ����ޱ仯����������ƽ�����ȱ仯����ƽ�⡣��������ѭ��������һֱ����С���������ںͽϴ��еȿ����ij�����������ֵĴ���Ϊ������Ostwald�컯���̿��ٽ����ṩ�˱�Ҫ����[7]��
�ļ������Ϊ�еȿ����ij����ṩԭ�ϣ�����ͬ�������еȿ�����ԭ�л���������������������Ŀ�������࣬����С������Ŀ��Ȼ���٣����еȿ�����Ŀ�仯����ƽ�⡣������ͼ17(f)��ʾ��ƽ������û�г������ӣ�����������һ���̶Ⱥ����䡣�������ڿ���Խ�����Խ�������������ӡ����塢���ߵȾ���������ݵ�λ��ҲԽ�࣬������������Ĺ�����ݹ�Ӧ���㣬����ʹ���еȿ������������dz����������Ҽ����ޱ仯����������ƽ�����ȱ仯����ƽ�⡣��������ѭ��������һֱ����С���������ںͽϴ��еȿ����ij�����������ֵĴ���Ϊ������Ostwald�컯���̿��ٽ����ṩ�˱�Ҫ����[7]��
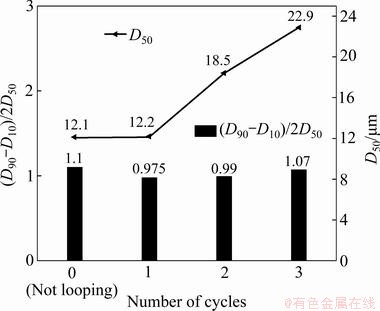
ͼ16 ��ͬ����ѭ����������̼�������ȼ����ȷֲ��仯ͼ
Fig. 16 Particle size and particle size distribution of yttrium carbonate obtained at different number of cycles of seed crystals
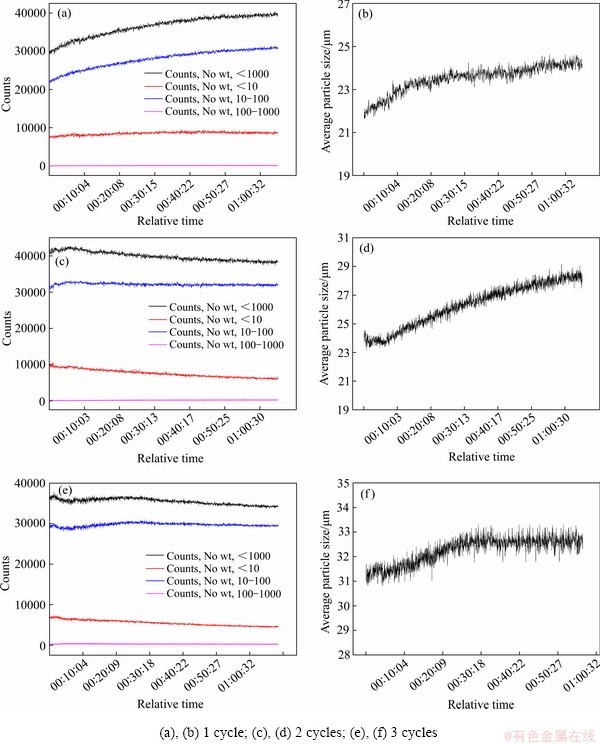
ͼ17 ����ѭ��������FBRMͼ
Fig. 17 FBRM images during cycle of seed crystals process
ͼ18��ʾΪÿ��ѭ����Ӧ����30 min(��ͼ 18(a))��60 min(��ͼ18(b))ʱ��̼�������ȷֲ�ͼ����ͼ18�ɼ�������ѭ�����������ӣ����ȷֲ�����������������ƫ�ƣ�����̼����ƽ��������ѭ�������������������һֱ�������������������������̵ķ���һ�¡�
ͼ19��ʾΪÿ��ѭ����Ӧ�յ��PVMͼ.��ͼ19�пɿ�����δѭ���IJ��ᄃ��������٣�������ѭ�����������ӣ��ϴ������еȿ����������࣬С�������٣���û�г���100 ��m�Ĵ������������Ҳ�������������߱仯���ɷ�����һ�£���֤�˾���ѭ��������Ҫ����Ostwald�컯�;����������̡�
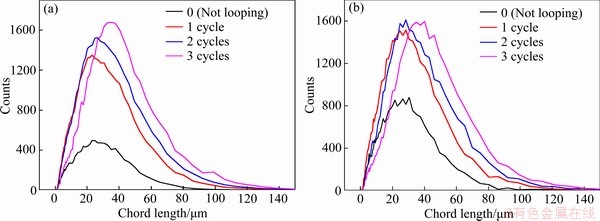
ͼ18 ÿ��ѭ����Ӧ����30 min��60 minʱ��̼�������ȷֲ�ͼ
Fig. 18 Yttrium carbonate particle size distribution of each cycle of reaction for 30 min (a) and 60 min (b)

ͼ19 ÿ��ѭ����Ӧ�յ��PVMͼ
Fig. 19 PVM images of each cycle reaction at end
2.3.3 ����1��ѭ����������̼���Ƶ�XRD��SEM�����ȱ仯����
������������֪����1��ѭ���������ԵĽᾧ��Ϊ��һ����֤����ѭ����Ӧ�ᾧ������ʵ���ظ��˾���1��ѭ�����̣���������̼���ƽ�����XRD��SEM�ֺ����ȱ仯�����������ͼ20��ʾ����ͼ20(a)�п������ھ��������£����ŷ�Ӧʱ������ӣ�̼������������խ��ǿ���������������ѭ����ʹ̼���ƾ������������������Y2(CO3)3��2H2O��ͼ��(PDF#24-1419)���Ǻϡ����⣬��С����������������״��Ƭ״���壬������״��ת��ΪƬ״����仯���Ʒ�����������ѭ������̼���Ƶ���ò�仯���������ֵĴ��ڶԽᾧת�������ԵĴٽ��� �ã�������Ostwald�컯����ɹ����ھ��ֵĺ˾�����[6]��
ͼ21��ʾΪ����1��ѭ����Ӧ��ͬʱ������̼���Ƶ����ȼ����ȷֲ�ͼ����ͼ�ɼ���1��ѭ�������У����ŷ�Ӧʱ������ӣ�̼���Ƶ��������������ھ��������£��ᾧ��Ѹ����ɣ��������ϳ������������������һ�¡�
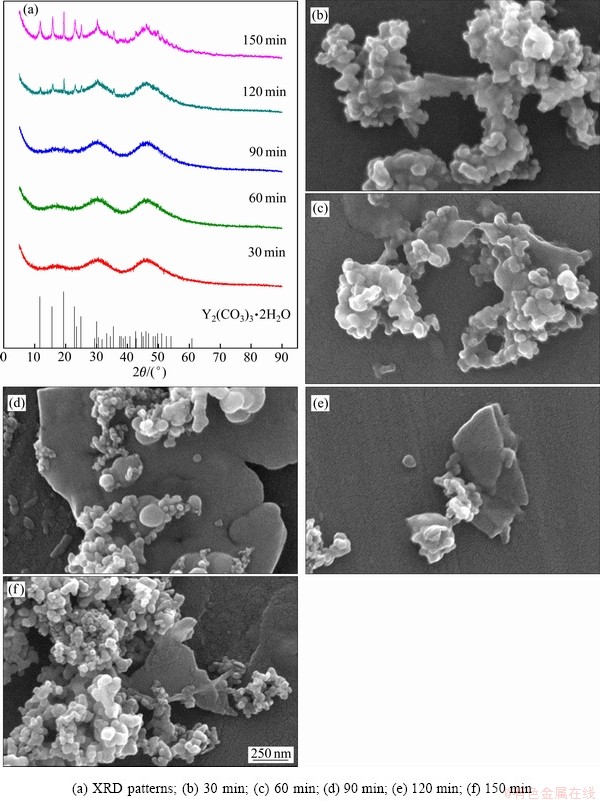
ͼ20 ����1��ѭ����Ӧ��ͬʱ������̼���Ƶ�XRD��SEM��
Fig. 20 XRD patterns(a) and SEM images ((b)-(f)) of yttrium carbonate obtained at different reaction time by first cycle of seed crystals
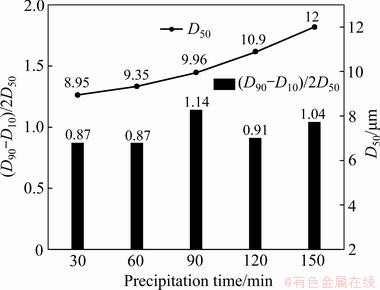
ͼ21 ����1��ѭ����Ӧ��ͬʱ������̼���Ƶ����ȼ����ȷֲ�ͼ
Fig. 21 Particle size and particle size distribution of yttrium carbonate obtained at different reaction time by first cycle of seed crystals
3 ����
1) �¶�Խ�ߣ��ṩ������Խ�࣬����Խ���˷�����������ݶ��ᾧ������ϵpH������Ӱ��̼���ƵĹ����Ͷȡ���(80 �棬pH 5.9~6.0)�����£�̼���ƵĽᾧ�������յ��ɺˡ�����������Ostwald�컯�Ķ�̬ƽ����̣���ʱ���ó����������50 mL����ʱ���Ϊ138 s���������ܽ��ţ������������һ���ᾧ�ȡ�
2) �ڸ��½���»������д��ڼ��гɺ˺ͽӴ��ɺˣ�����ʹ���������нϴ������ת��Ϊ��С������������ϵ�ڿ���ƽ�����ȼ�С�����ҳ»�ʱ��Խ����ƽ�����ȼ�С����Խ���ԣ��Գ�������ĽᾧԽ������
3) �ھ���ѭ���У����ھ��ֵĺ˾����ã����ٽ��ᾧת�����Ҽ���Ostwald�컯��ʹ������������������״���壬��������Ƭ״�ᾧת�������տ�������Ϊ����״��Ƭ״�ۼ���ˮ������̼���ƾ��塣ʵ����1�ξ���ѭ����(80 �棬pH 5.9~6.0)�������¼��ɵõ�����12.0 ��m�ҷ�ɢ�Ծ��ȵľ���̼���ơ�
REFERENCES
[1] YOU S K, WEON H K. Optical loss mechanism in yttria thin film waveguides[J]. Optical Materials, 2000, 14(3): 229-234.
[2] PAILLOUX F, IMHOFF D, JUBLOT M, PAUMIER F, GABORIAUD R J, JAOUEN M. HRTEM and EELS study of Y2O3/MgO thin films[J]. Micron, 2006, 37(5): 420-425.
[3] JIN Ling-ling, ZHOU GUO-hong, SHIMAI Shun-zo, ZHANG Jian, WANG Shi-wei. ZrO2-doped Y2O3 transparent ceramics via slip casting and vacuum sintering[J]. Journal of the European Ceramic Society, 2010, 30(10): 2139-2143.
[4] ZHAO Shi-hua, CUI Dan-dan, YIN Nai-qiang, CHENG Wen-jing. Preparation and luminescent properties of Y2O3:Eu3+ nanocrystal via a homogeneous precipitation method[J]. Nanoscience and Nanotechnology Letters, 2018, 10(1): 145-148.
[5] BEECHER S J, PARSONAGE T L, MACKENZIE J I, SLOYAN K A, GRANT-JACOB J A, EASON R W. Diode-end-pumped 12 W Yb:Y2O3 planar waveguide laser[J]. Optics Express, 2014, 22(18): 22056-22061.
[6] �� ��. ̼���ơ�̼���ϵĽᾧ����ؼ����о�[D]. �ϲ�: �ϲ���ѧ, 2005.
HUANG Ting. Crystallization of yttrium carbonate and neodymium carbonate and the relative technologies[D]. Nanchang: Nanchang University, 2005.
[7] �� ΰ, ����, �����, ף�IJ�, �� ��, ������, �ƽ, ����ľ, ������. Y2(CO3)3�ij����ᾧ�����뾧����С����[J]. �й�ϡ��ѧ��, 2016, 34(2): 180-188.
ZHU Wei, QIU Dong-xing, PEI Hao-yu, ZHU Wen-cai, LI Jing, LIU Yan-zhu, LI Dong-ping, ZHOU Xing-mu, LI Yong-xiu. Precipitation crystallization process of yttrium carbonate and size controlling synthesis of ytterium oxide particles[J]. Journal of the Chinese Society of Rare Earths, 2016, 34(2): 180-188.
[8] ������, �� ��, ��С��, ����Ӣ, ��ƽ��, ��ѩ��. ̼��������Ȼ��Ʒ�Ӧ���ᾧ�������ɺ;�������[J].����ѧѧ��, 2002,18(11):1138-1142.
LI Yong-xiu, LI Ming, HE Xiao-bin, GU Zi-ying, HU Ping-gui, ZHONG Xue-zhen. The composition and crystalline phase type of products obtained by precipitating yttrium ion with ammonium bicarbonate[J]. Chinese Journal of Inorganic Chemistry, 2002, 18(11): 1138-1142.
[9] ������, �� ��, ��С��, ��ƽ��, ����Ӣ. ̼��ϡ���ij�����ᾧ����[J]. �й���ɫ����ѧ��, 1999, 9(1): 165-170.
LI Yong-xiu, LI Ming, HE Xiao-bin, HU Ping-gui, GU Zi-ying. Precipitation and crystallization process of rare earth carbonate[J]. The Chinese Journal of Nonferrous Metals, 1999, 9(1): 165-170.
[10] LIU Song, MA Rong-jun, JIANG Rong-ying, LUO Fang-cheng. Synthesis and structure of hydrated neodymium carbonate[J]. Journal of Crystal Growth, 1999, 203(3): 454-457.
[11] ������, ������, �� ��, �ܺ��. ̼����麟������Ʊ���ϸY2O3��Ӧ���������ȵ�Ӱ��[J]. ϡ��, 2010, 31(2): 31-33.
LIU Ling-sheng, XIONG Xiao-bai, JIA Tao, CAO Hong-zhang. Effects of reaction conditions on the particle size of ultra-fine Y2O3 prepared by NH4HCO3 precipitation method[J]. Chinese Rare Earths, 2010, 31(2): 31-33.
[12] �� Ө, ������, �� ��, ����Ƽ, ���ȿ�, �� ��. ̼��ϡ�����������Ż�[J]. �й�ϡ��ѧ��, 2002, 20(S2): 149-151.
MA Ying, WANG Xiu-yan, QIAO Jun, ZHANG Li-ping, HAO Xian-ku, CHANG Shu. New process of producing rare earth carbonates[J]. Journal of the Chinese Society of Rare Earths, 2002, 20(S2): 149-151.
[13] ��С��, ������, ���, ����Ӣ, ������. ̼�����Ƴ����缰̼����Ľᾧ�����о�[J]. ϡ�н�����Ӳ�ʺϽ�, 2001, 145(2): 4-8.
JIAO Xiao-yan, LUO Xian-man, YANG Yu-jun, GU Zi-ying, LI Yong-xiu. Study of crystallization process during La and La2(CO3)3 precipitation with sodium bicarbonate[J]. Rare Metal and Cemented Carbides, 2001, 145(2): 4-8.
[14] ������, �� ��, �̸���, �� ��, �δ���. ̼�������������Ʊ�̼��ϡ�����о�[J]. ��ұ, 2015, 24(2): 44-46..
WANG Song-ling, LIU Yan, CHENG Fu-xiang, WU Sheng, LIAO Chun-sheng. A study on preparation of rare earth carbonate by using sodium carbonate[J]. Mining and Metallurgy, 2015, 24(2): 44-46.
[15] ������, �½���, ����ɽ, ɣ����, ��ȫ��, ����ǿ. ��̼�������������Ʊ�����̼����[J]. ϡ��, 2015, 36(6): 118-122.
JIANG Xiao-li, CHEN Jian-bo, GUO Shu-shan, SAGN Xiao-yun, XING Quan-sheng, ZHANG Sheng-qiang. Preparation of low sodium lanthanum carbonate with precipitant of sodium carbonate[J]. Chinese Rare Earths, 2015, 36(6): 118-122.
[16] ��ϰ��, ������, ����ϼ, �����, �����. �������鷨��ѡ̼�������Ʊ�̼�����ϵ��о�[J]. �й���Դ�ۺ�����, 2019, 37(5): 17-19.
GAO Xi-gui, SUN Ming-hua, SUN Ming-xia, FENG Chang-fa, SUN Jiu-zhou. Study on preparation of barium carbonate by orthogonal test methodand sodium bicarbonate[J]. China Resources Comprehensive Utilization, 2019, 37(5): 17-19.
[17] NAGASHIMA K, WAKITA H, MOCHIZUKI A. The synthesis of crystalline rare earth carbonates[J]. Bulletin of the Chemical Society of Japan,1973, 46(1): 152-156.
[18] �컪��, �����, ������, �κ��. �������Ʊ��������ӵ��о� ���� ��ѧԭ����Ӱ������[J]. ������չ, 1996(5): 29-31
XU Hua-rui, LI Feng-sheng, CHEN Shu-lin, SONG Hong-chang. Precipitation process of nanometer particles: Chemical principles and effects of operation parameters[J]. Chemical Industry and Engineering Progress, 1996(5): 29-31.
[19] ���컪, ���Ȱ�. ����̼��ϡ�����γɼ���Ӱ������[J]. �й�ϡ��ѧ��, 1993, 11(2): 171-173.
YU Qing-hua, LI Xian-bai. Formation of crystalline rare earth carbonate and its influencing factors[J]. Journal of the Chinese Society of Rare Earths, 1993, 11(2): 171-173.
[20] SUN Yu-zhu, SONG Xing-fu, WANG Jin, LUO Yan, YU Jian-guo. Seeded induction period and secondary nucleation of lithium carbonate[J]. The Chinese Journal of Process Engineering, 2009, 9(4): 652-660.
[21] VENGRENOVICH R D, IVANSKIIA B V, PANKOA I I, FESIVA I V, KRYVETSKYIA V I, STASYK M O. To the mechanism coarsening of Ostwald ripening of Pt, Pd catalysts and their compounds[C]// Proceedings Volume 9809, Twelfth International Conference on Correlation Optics. Chernivsti, Ukraine: SPIE, 2015: 98090P.
[22] ����ϼ. �ೡ����ģ��Ostwald�컯�ݱ�[D]. ����: ������ѧ, 2014.
ZHU Tina-xia. Phase field formulations for modeling the evolution of the Ostwald ripening[D]. Nanning: Guangxi University, 2014.
[23] YEC C C, ZENG Hua-chun. Synthesis of complex nanomaterials via Ostwald ripening[J]. Journal of Materials Chemistry A, 2014, 2(14): 4843-4851.
[24] ������, ��ƽ��, ��С��, ����Ӣ, �� ��. ̼����笠��νᾧ���γɼ�Ӱ������[J]. �й�ϡ��ѧ��, 2000, 18(1): 79-81.
LI Yong-xiu, HU Ping-gui, HE Xiao-bin, GU Zi-ying, LI Min. Formation process of crystalline ammonium yttrium carbonate double salt[J]. Journal of the Chinese Society of Rare Earths, 2000, 18(1): 79-81.
[25] �� ��, ����ƽ, ����Զ. �»�ʱ����������ƹ������ܵ�Ӱ��[J]. ��ѧ��ҵ�빤��, 2018, 35(6): 62-66.
CHEN Cheng, DANG Le-ping, WEI Hong-yuan. Influence of aging time on the solid performance of tricalcium phosphate[J]. Chemical Industry and Engineering, 2018, 35(6): 62-66.
[26] RANDOLPH A D, LARSON M A. Theory of particulate processes[M]. 2nd ed. San Diego: Academic Press Inc., 1988: 123-128.
[27] MYERSON A S. Handbook of industrial crystallization[M]. 2nd ed. Oxford: Butterworth Heinemann Press, 2002: 46-50.
[28] NORE P, MERSMANN A. Batch precipitation of barium carbonate[J]. Chemical Engineering Science, 1993, 48(17): 3083-3088.
[29] KONISHI Y, NODA Y, ASAIS. Precipitation stripping of yttrium oxalate powders from yttrium-loaded carboxylate solutions with aqueous oxalic acid solutions[J]. Industrial & Engineering Chemistry Research, 1998, 37(6): 2093-2098.
Precipitation crystallization process of yttrium carbonate and its influencing factors
GAO Guo-hua1, LAI An-bang1, ZHOU Xiao-fang3, LIAO Chun-fa1, LIU Jun-yun2, XIAO Yan-fei1, 2
(1. Faculty of Materials Metallurgy and Chemistry, Jiangxi University of Science and Technology, Ganzhou 341000, China;
2. Qiandong Rare Earth Group Co., Ltd., Ganzhou 341000, China;
3. General Research Institute for Nonferrous Metals, Beijing 100088, China)
Abstract: In view of the difficulty in obtaining crystalline yttrium carbonate by sodium carbonate precipitation process, the sodium carbonate was used as precipitant, the effects of temperature, pH, aging and seed crystals on the crystalline precipitation of yttrium carbonate were studied by conventional precipitation experiment and FBRM-PVM, and the precipitation crystallization process of yttrium carbonate was analyzed as well. The results show that the precipitation crystallization process of yttrium carbonate is a dynamic equilibrium process of induced nucleation��crystal particles growth��Ostwald ripening at 80 �� and pH 5.9-6.0. Under this condition, the precipitate product with better settling properties and certain crystallinity is obtained. In addition, the high temperature stirring aging process has no positive effect on the crystallization of yttrium carbonate. But the shear nucleation and contact nucleation in the aging process can gradually transform the larger particles into smaller particles, leading to a decrease in the average particle size in the system. Moreover, seed crystals can promote crystallization transformation and accelerate Ostwald ripening. In the seed cycle process, the crystal growth process is a process of nucleation��needle-like and sheet-like growth��needle-like and sheet-like crystals aggregated into spherical crystals of tengerite type yttrium carbonate. Finally, crystalline yttrium carbonate with a particle size of 12.0 ��m and uniform dispersion can be obtained under the conditions of the first cycle of seed crystals. The research in this paper will provide theoretical guidance for the preparation of crystalline yttrium carbonate by sodium carbonate precipitation.
Key words: sodium carbonate; FBRM-PVM; crystallization; yttrium carbonate; Ostwald ripening
Foundation item: Project(51964018) supported by the National Natural Science Foundation of China; Project (2018T110661) supported the by China Postdoctoral Science Foundation; Project (20171ACE50008) supported by the Key Research and Development Plan of Jiangxi Province, China; Project(��2018��50) supported by the Science and Technology Innovation Talents Program of Ganzhou City, China; Project([2017]179) supported by the Key R&D Projects of Science and Technology Program of Ganzhou City, China; Project(2018KY01) supported by the Preferential Funding for Postdoctoral Research Projects in Jiangxi Province, China
Received date: 2019-11-07; Accepted date: 2020-04-28
Corresponding author: XIAO Yan-fei; Tell: +86-18379727723; E-mail: xiaoyanfei0906@163.com
(�༭ �� ��)
������Ŀ��������Ȼ��ѧ����������Ŀ(51964018)���й���ʿ���ѧ����������Ŀ(2018T110661)������ʡ�ص��з��ƻ�������Ŀ(20171ACE50008)�������пƼ������˲żƻ�������Ŀ(���пƷ���2018��50��)�������пƼ��ƻ���Ŀ�ص��з��ƻ�������Ŀ(���вƽ���[2017]179 ��)������ʡ��ʿ�������Ŀ����һ��������Ŀ(2018KY01)
�ո����ڣ�2019-11-07�������ڣ�2020-04-28
ͨ�����ߣ�Ф��ɣ������ڣ���ʿ���绰��18379727723��E-mail��xiaoyanfei0906@163.com
ժ Ҫ�����̼���Ƴ������ѻ�þ���̼���Ƶ����⣬������̼����Ϊ��������ͨ���������̽����FBRM-PVM�����о��¶ȡ�pH���»������ֵ����ض�̼���ƾ��ͳ�����Ӱ�죬����̼���Ƴ����ᾧ���̽�����������������������(80 �棬pH 5.9~6.0)�����£��ɵõ��������ܽ��Ų�����һ���ᾧ�ȵij��������ʱ̼���ƵĽᾧ�������յ��ɺˡ�����������Ostwald�컯�Ķ�̬ƽ����̣������½���»����̶�̼���ƵĽᾧû������������ã�������гɺ˺ͽӴ��ɺ����ÿ���ʹ���������нϴ������ת��Ϊ��С������ʹ��ϵ�ڿ���ƽ�����ȼ�С�����⣬���ֵĴ��ڿ��Դٽ���������ᾧת�����Ҽ���Ostwald�컯���ھ���ѭ�������У����������Ĺ����dzɺˡ���״��Ƭ״��������״��Ƭ״����ۼ���������ˮ������̼���ƾ��塣ʵ����1�ξ���ѭ���������¼��ɵõ�����12.0 ��m�ҷ�ɢ�Ծ��ȵľ���̼���ơ����Ľ�Ϊ̼���Ƴ����Ʊ�����̼�����ṩ����ָ����
[6] �� ��. ̼���ơ�̼���ϵĽᾧ����ؼ����о�[D]. �ϲ�: �ϲ���ѧ, 2005.
[9] ������, �� ��, ��С��, ��ƽ��, ����Ӣ. ̼��ϡ���ij�����ᾧ����[J]. �й���ɫ����ѧ��, 1999, 9(1): 165-170.
[14] ������, �� ��, �̸���, �� ��, �δ���. ̼�������������Ʊ�̼��ϡ�����о�[J]. ��ұ, 2015, 24(2): 44-46..
[19] ���컪, ���Ȱ�. ����̼��ϡ�����γɼ���Ӱ������[J]. �й�ϡ��ѧ��, 1993, 11(2): 171-173.
[22] ����ϼ. �ೡ����ģ��Ostwald�컯�ݱ�[D]. ����: ������ѧ, 2014.
[24] ������, ��ƽ��, ��С��, ����Ӣ, �� ��. ̼����笠��νᾧ���γɼ�Ӱ������[J]. �й�ϡ��ѧ��, 2000, 18(1): 79-81.
[25] �� ��, ����ƽ, ����Զ. �»�ʱ����������ƹ������ܵ�Ӱ��[J]. ��ѧ��ҵ�빤��, 2018, 35(6): 62-66.


