���±�ţ�1004-0609(2008)S1-0407-05
��ú���������ж��������ڸ�Ũ�ȼ�Һ�е��ܽ���Ϊ
�� �ޣ�����IJ�������� ��
(������ѧ ����ұ��ѧԺ������ 110004)
ժ Ҫ��
��ú���ᷨ��ȡ�����������ж������躬���ӽ�85%�����Ʊ�������ˮ����������ԭ�ϡ�������ڳ�ѹ���ø�Ũ�ȼ�Һ������ú���������ж�������Ĺ��գ��о��˶���������Ũ����ϵ�еĽ�����Ϊ��ʵ�������������¶�Ϊ110 �桢��Ũ��Ϊ50%��Һ�̱�Ϊ2.2?1��ʱ��Ϊ60 min�����·�Ӧ��ѣ��������XRD�������������������ж��μ��������SiO2������ȫ����Ҫ����Ϊ�ƹ�����̼���Ρ�
�ؼ��ʣ�
��ú��������������Ũ����������������������
��ͼ����ţ�TQ 110.3���� ���ױ�ʶ�룺A
Dissolving behavior of SiO2 in residue of fly ash detached Al2O3 in highly concentrated alkali solution
WU Yan, ZHAI Yu-chun, MU Wen-ning, SUN Yang
(School of Materials and Metallurgy, Northeastern University, Shenyang 110004, China)
Abstract: The concentration of SiO2 in the residue of fly ash detached Al2O3 was 85%. It is the excellent material to prepare Na2SiO3. A new method of leaching SiO2 from the residue was studied in atmosphere and highly concentrated alkali solution. The optimum conditions are: reaction temperature 110 ��, alkali concentration 50%, ratio of liquid to ore 2.2?1 and reaction time 60 min. The XRD was used to analyze the residue after alkali leaching. The result shows that SiO2 is leached completely and the main phases are Na-Al silicate slime and carbonate.
Key words: fly ash; residue; leaching; highly concentrated alkali solution; Na2SiO3; SiO2
��ú����ȡ���������侫ϸ�����õ�һ����Ҫ�о����������ᷨ�ӷ�ú������ȡ���������յ��ս����죬�ᷨ���������Ĵ����Ѿ���ΪĿǰ�ᷨ���չ�ҵ���ƹ����Ҫ���⡣��ú���ᷨ�Ʊ���������ʣ����������ӽ���ú��ԭ�ϵ�60%�����ж������躬���ߴ�85%����ֱ������ˮ�࣬��������Ч����Ʒ����ֵ��[1-6]���������ڲ���������ȫ�����ã��������ʵ�ַ�ú�ҵ���ȫ��ϸ���ۺ����á�
��ú�����������ж������躬���ϸߣ������������ͣ������Ƴɹ�����[7-8]���ټӹ��Ʊ�SiO2��Ʒ��Ŀǰ��������ˮ�������������ɷ�Ϊ�ɷ���ʪ�����ɷ������ܺĸߡ�ԭ�����ĸߡ��ɱ��ߵ�ȱ�㣻ʪ���ܺĽ�Ϊ�ɷ���1/6~1/3����Ҫ��ԭ���еĶ���������нϸߵĻ���[9]��Ϊ�ˣ���ʵ����ʪ�����յĻ����Ͻ��иĽ������ø�Ũ���ʷе�����ԭ�����ڳ�ѹ�����ø��¡���Ũ��������ǿ��Ӧ������������ͨʪ���ѷֽ�ĺ��������������ʡ�Ϊ��֤���������н�����Ũ�ȸߣ��ֲ�ʹ�����������϶������˷ѣ������ղ��õ�Һ�̱������·�Ӧ��������и���Ĺ�ҵ����ֵ��ͨ��ʵ�鿼���˷�Ӧ�¶ȡ���ʼNaOHŨ�ȡ�Һ�̱Ⱥͷ�Ӧʱ���SiO2�����ʵ�Ӱ�죬�����XRD����������ԭ�Ϻͷ�Ӧʣ���������ɷ֡�
1 ʵ��
ʵ������ԭ�Ϸ�ú������ɽ�����Ƶ糧������Ũ���������õ��������(�����������FAS��ʾ)������Ҫ��ѧ�ɷּ���1�����Կ�����SiO2�����ﵽ84.900%��Al2O3������Ϊ8.400%�����л���Fe2O3��CaO��TiO2�����ʡ�
��1 ��������Ļ�ѧ�ɷ�
Table 1 Composition of FAS (mass fraction, %)

ʵ���ڲ���ֲ��ʵķ�Ӧ�����н��С��������Ƹ�Ũ��NaOH��Һ���ڿ���ϵͳ��Ԥ�ȵ�ʵ���¶ȣ��ٳ�ȡ�����ķ�ú����������NaOHŨҺ�У���100 r/min���ٶȽ��裬��Ӧһ��ʱ�䣻��Ӧ��Ϻ�����80 �沢����5������������ˮ�������ܳ�30 min����Һ�����õ���������Һ���˱������˱���ϴ3�Ρ�
ʹ���ձ���ѧD/max-RB X���������Dzⶨ��������ɷ֣��õ¹�˹����X����ӫ������Ƿ�����ĩ��Ʒ�е�Ԫ�غ�������EDTAֱ�ӵζ���������Һ�����ĺ���[10]���÷������������������Һ�й�ĺ���[11]��
2 ���������
ͼ1��ʾΪ��ú�Ҽ���������XRD�������ͼ������ͼ1(a)Ϊ��ú�ҵ�XRD�ף�ͼ1(b)Ϊ������XRD�ס���ͼ1�ɼ�����ú���ᷨ��ȡ��������������Ԧ�-SiO2��Ϊ������ú�Һ�������XRD������20?~25?�������˽Ͽ�����������壬����������Ĵ��ڡ�ԭ���еĿ���û�������еĿ������ԣ������������в������в����࣬�����ڷ�Ӧ�����з��������SiO2��ǿ���˿��塣��ˣ������е���Ҫ�ɷ�SiO2�Ĵ�����̬��3�֣�һ���Բ��������ʽ���ڣ����������δ��ڣ������Ԧ�-SiO2�������[1]������3�ִ�����̬�У�������̬���ڵ�SiO2������ߣ����Ϊ�����࣬�ٴ�Ϊ��-SiO2��
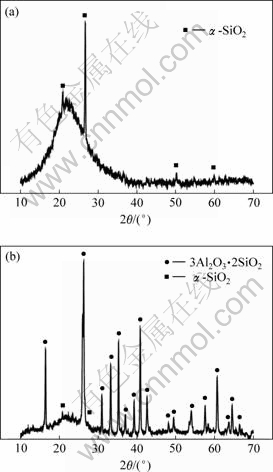
ͼ1 ��ú�Ҽ����������X����������
Fig.1 XRD patterns of fly ash and FAS: (a) Fly ash; (b) FAS
2.2.1 �����Ӧ�¶ȶ�SiO2��ȡ�ʵ�Ӱ��
ͼ2��ʾΪ��Ӧ�¶ȶ�������SiO2��ȡ�ʵ�Ӱ�졣���ŷ�Ӧ�¶ȵ����ߣ�SiO2��ȡ�����������¶����ߵ�110 ������ʱ���������¶ȣ���ȡ�����Խ��͡��ڷ�Ӧ�Ŀ�ʼ�Σ���Ӧ���ң��з�����������Ҫ����Ϊ���д��ڲ��ֻ���SiO2���ڸ�Ũ�ȼ�Һ�������£�Ѹ�ٷ�Ӧ����ϵ�¶������������е㣬���������������ŷ�Ӧ�¶ȵ���ߣ��ǻ���SiO2Ҳ����Ũ��Һ��Ӧ���¶����ߣ���Ӧ���������������SiO2�����ʡ�����Ӧ�¶ȸ���110 ��ʱ�����ڷ�Ӧ���ڷ���ʱ��ϳ���ʧˮ���࣬��ɷ�Ӧ��ϵճ�����������Բ��ɢ�ٶȼ�����������������ɢ�ٶ�Ӱ������½�����[12]�����⣬����ˮ���������죬�����ײ������ϳ��ֽ�������ʹ�����ʽ��͡�
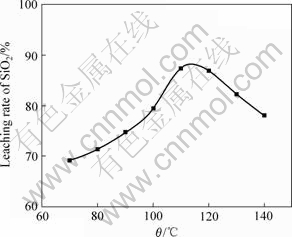
ͼ2 �¶ȶ�SiO2��ȡ�ʵ�Ӱ��
Fig.2 Effect of temperature on leaching rate of SiO2 (Concentration of NaOH: 50%; Mass ratio of alkali to ore: 2.2?1.0; Time: 60 min)
��ͼ2���Կ������¶ȹ�����Ͷ�SiO2�Ľ������Dz����ġ���������SiO2��NaOH�ķ�ӦʹNaOHŨ�Ƚ��͡�һ����������NaOH����������ģ���һ���������ڷ�Ӧ��������ˮ�����ɡ�����Ӧ������ͬʱ����ˮ�ֵ�����������ά����NaOH��Ũ�ȡ�ʵ�������������Ʒ�Ӧ�¶���110 ��ʱ��SiO2�Ľ����ʽϸߣ����¶�ǡ����ά����Һ��ˮ��ƽ�⣬�ȱ�����NaOH��Ũ�ȣ���ʹ��Һ����ˮ�ֵ������������������ԡ�
2.2.2 NaOHŨ�ȶ�SiO2��ȡ�ʵ�Ӱ��
NaOHŨ��(��������)��SiO2��ȡ�ʵ�Ӱ���ͼ3����NaOHŨ�Ƚ�Сʱ����ȡ�ʽϵͣ�����NaOHŨ�ȵ����ӣ���ȡ�ʲ������ߣ���Ũ�ȴ�30%����40%ʱ�������ʴ������ߣ���NaOHŨ�ȴ���60%ʱ������ˮ�������٣���Һճ�ȸߣ������������ں������ײ����裬�����Ӧ�ﲻ���������ԣ���ɢ���ѣ����·�Ӧ���ʽ��ͣ���������ʲ������ӡ�
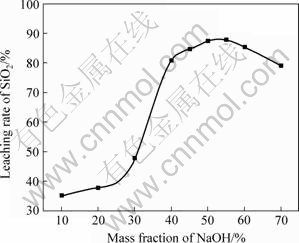
ͼ3 NaOHŨ�ȶ�SiO2��ȡ�ʵ�Ӱ��
Fig.3 Effect of mass fraction of NaOH on leaching rate of SiO2 (Temperature: 110 ��; Mass ratio of alkali to ore: 2.2?1.0; Time: 60 min)
���⣬��NaOHŨ�ȴ���60%ʱ�����ڿ����ܽ��Na2SiO3���״ﵽ�����ͣ������������Һ���������ӷ�Ӧ�����ƹ��������ķ�Ӧ[13]�����ƹ���Ҳ���ڷ�Ӧ������γɱ����������SiO2�Ľ�������ˣ�NaOHŨ��ѡȡ50%Ϊ�ˡ�
2.2.3 Һ�̱ȶ�SiO2��ȡ�ʵ�Ӱ��
Ϊ��֤�ڽϵ͵�Һ�̱�(������)������NaOHҲ�������ģ��ڱ�����ʵ����NaOHŨ��Ϊ60%����Һ�̱ȴ���1.9?1.0ʱ��NaOH��Թ�����ͼ4��ʾΪҺ�̱���SiO2��ȡ�ʵĹ�ϵ����Һ�̱�С��2?1ʱ����Һ�̱ȵ�����������ߺܿ죻��Һ�̱ȴ���2?1ʱ����������Һ�̱ȵ��������������NaOH��ҺŨ��һ���������£��ϵ͵�Һ�̱ȿ��Լ��ټ�ģ����ͳɱ������ǣ���Һ�̱Ƚϵ͵�����£���ճ�� �����ڷ�Ӧ�Ĵ��ʹ��̣��Ӷ������ʽ��͡�����Һ�̱ȿ�����߿������ԣ���ߴ����ٶȣ�������߷�Ӧ�ٶȡ����Ա���ϵ���ԣ����ڼ��Ũ�Ⱥܸߣ��ڽϵ͵�Һ�̱��¼��ɵõ��ϸߵĽ����ʡ����ԣ��ۺϾ������أ�ѡȡҺ�̱�Ϊ2.2?1.0��
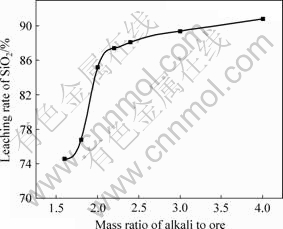
ͼ4 ��Һ�ȶ�SiO2��ȡ�ʵ�Ӱ��
Fig.4 Effect of mass ratio of alkali to ore on leaching rate of SiO2 (Temperature: 110 ��; Concentration of NaOH: 50%; Time: 60 min)
2.2.4 ��Ӧʱ���SiO2��ȡ�ʵ�Ӱ��
��Ӧʱ����SiO2��ȡ�ʵĹ�ϵ��ͼ5���ڷ�Ӧ���е�30 min��ǰ����������ʱ�����Ӻܿ죻�ڷ�Ӧ���е�30~60 min�ĽΣ������������ٶȼ���������Ӧ���е�60 min�Ժ����ʵ����Ӹ�Ϊ��������ʵ���������ɹ۲쵽�ڿ����Ũ���ϳ��ڣ���Ӧ�dz����ң���Һ���ݣ��ʷ���״̬���������Ӧ��ϵ�¶�����5~7 �棬��Ӧ30 min����ϵ����ƽ����������Ϊ�����к��в��ֻ��������裬�����еIJ�����Ҳ����������Ĺ������γ��˴����Ŀ��ͱ���ȱ�ݣ����ȵ�ŨNaOH��Һ���к�ǿ�ķ�Ӧ�� �����뱩¶������Ļ���SiO2�Ӵ���������Ӧ��������ַ�������Ӧ60 min����Һ�е�SiO2��AlO3�ﵽһ��Ũ�ȣ������ƹ�������������ʹ��Һ��SiO2Ũ�Ƚ��ͣ������ڷ�Ӧ������γɱ���������Ʒ�Ӧ�Ľ��У�����������淴Ӧʱ����ӳ����������Եı仯����ˣ���Ӧʱ����60 minΪ�ˡ�
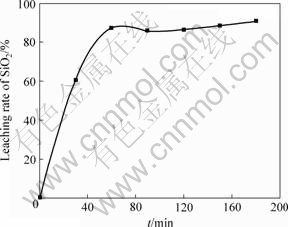
ͼ5 ��Ӧʱ���SiO2�����ʵ�Ӱ��
Fig.5 Effect of reaction time on leaching rate of SiO2 (Temperature: 110 ��; Concentration of NaOH: 50%; Mass ratio of alkali to ore: 2.2?1.0)
Ϊʹ�����Ӧ��ֽ��У��۲������ڼ����Ӧ�����еķ�Ӧ������������������η��������ʹ���е�SiO2��ַ�Ӧ�����������ʾΪ��Ӧ����Ͳ��ܷ�Ӧ���ʡ��������XRD������ͼ6���ڱ���ϵ�У�����������ԭ��Ϊ��ú��������IJ������Ũ�Ӧ�����Ϊ���η�Ӧ���������Ӧ����Ƚϸ��ӡ���ͼ6�����Կ������ƹ����ྦྷ�����ʣ��仯ѧʽ���ɱ�ʾΪ��Na8(Al6Si6O24)X?yH2O[14]����Ũ�Ӧ�����У�һ����Al2O3��SiO2��Ũ���������ܽ������Һ����һ���������Һ�е�����������Һ�е��ƺ����Ԫ�ط�Ӧ���ɳ���������ʱ�����������ӷ�Ӧʱ��������������ԵĽ�������Ǻϵġ����⣬�ڼ�����л���þ�Ƶ�̼���γ�����
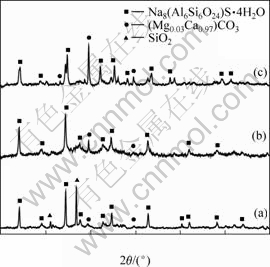
ͼ6 �������X����������
Fig.6 XRD patterns of residue of alkali leaching: (a) Leaching once; (b) Leaching twice; (c) Leaching three times
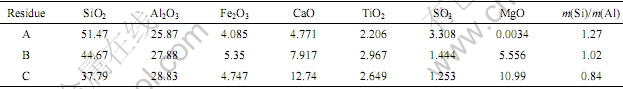
��ͼ6�����Կ�����һ�μ����Ӧ�����л��������Ե�SiO2���࣬�����μ�����е�SiO2����ʧ��˵��������κ������еĦ�-SiO2��Ӧ�Ƚ��� ȫ�����⣬̼��ƺ�̼��þ�ķ��������ԣ����μ����Ӧ���ƹ��������ʲ�������巢����ƫ�ƣ�̼��ƺ�̼��þ�Ļ�������ǿ�ҡ���������������Ӧ���������ӣ��������ʵĺ��������仯������������ǿ�ȱ仯���ɼ�������ijɷַ���(����2)�ɼ������ż�����������ӣ�����SiO2�������ͣ�Al2O3�������ߣ������Ƚ��͡�һ�μ�����ܽ��е�����Ҫԭ��Ϊ����Ӧʱ�䲻��֣���Ӧ���е�һ���̶Ⱥ�����NaOH���Ķ��ﲻ����������Ũ�ȣ����ڷ�Ӧ��ϵ��Һ�̱Ƚϵͣ���Ӧ���е�һ���̶Ⱥ���ﲻ�ܼ�ʱ���뷴Ӧ����棬�γɲ�������ڷ�Ӧ����棬�Ӷ�������NaOH��Ӧ����ɢ���Ѷȡ�
��2 ��������Ļ�ѧ�ɷ�
Table 2 Compositions of residue leached by alkali (mass fraction, %)
3 ����
1) ����˳�ѹ�����ø�Ũ�ȼ�Һ��ȡ��ú���ᷨ��������SiO2�Ĺ��գ��о��������ж���������Ũ����ϵ�еĽ�����Ϊ��
2) ���¶�Ϊ110 �桢��Ũ��Ϊ50%��Һ�̱�Ϊ2.2?1.0����ӦΪ60 min�������·�Ӧ��ѡ���Ӧ���������ɵ��ƹ�������������ڷ�Ӧ����棬�����ڷ�Ӧ�Ľ��У��Ӷ�����Ӱ��SiO2�Ľ��������Ӽ����Ӧ�������ԴﵽSiO2��ֽ�����Ŀ�ģ���������е���Ҫ����Ϊ�ƹ�����̼�����ࡣ
REFERENCES
[1] ����Ԫ, ������. ��ú���ۺ�����[M]. 2��. ����: �й�����������, 2004: 545.
WANG Fu-yuan, WU Zheng-yan. Fly ash utilization handbook[M]. 2nd ed. Beijing: China Electric Power Press, 2004: 545.
[2] SEIDEL A, SLUSZNV A, SHELEF G, ZIM MELS Y. Variation in fly ash properties with milling and acid leaching[J]. Fuel, 2005, 84(1): 89-96.
[3] ������. ��ú���ᷨ�������Ʊ�������ˮ����о�[J]. ��ú���ۺ�����, 2002(2): 40-41.
HUANG Shao-wen. Study on preparing Portland cement from the residue of fly ash detached Al2O3[J]. Fly Ash Comprehensive Utilization, 2002(2): 40-41.
[4] PARK H C, PARK Y J. Synthesis of alumina from high purity alum derived from coal fly ash[J]. Materials Science and Engineering A, 2004, A367: 166-170.
[5] ����ʱ, ����, �ؽ���, �� ��. �Է�ú��Ϊԭ���Ʊ��ߴ�������[J]. ����ѧ��, 2006, 57(9): 2189-2193.
LI Lai-shi, ZHAI Yu-chun, QIN Jin-guo, WU Yan.Extracting high-purity alumina from fly ash[J]. Journal of Chemical Industry and Engineering, 2006, 57(9): 2189-2193.
[6] MATJIE R H, BUNT J R, van HEERDEN. Extraction of alumina from coal fly ash generated from a selected low rank bituminous South African coal[J]. Minerals Engineering, 2005, 18(3): 299-310.
[7] ����ʱ. ��ú�Ҹ߸���ֵ�ۺ����á���ȡ������[D]. ����: ������ѧ, 2007.
LI Lai-shi. High added value utilization of coal fly ash��Extracting alumina from it[D]. Shenyang: Northeastern University, 2007.
[8] ���ľ�, ������, �̽���, ������. �ᷨ��ȡ��ú����������������ѡ��[J]. ��Դ��������, 2003, 17(4): 17-19, 47.
WANG Wen-jing, HAN Zuo-zhen, CHENG Jian-guang, FANG Jian-guo. The withdrawing of oxidize the aluminum from the fly ash[J]. Energy Environment Protection, 2003, 17(4): 17-19, 47.
[9] ղ ��. ��ˮ��������������Ӧ��[J]. ��ѧ��ҵ�빤�̼���, 1995, 16(2): 52-56.
ZHAN Qin. The production and application of sodium soluble glass[J]. Journal of Chemical Industry and Engineering, 1995, 16(2): 52-56.
[10] ������. �����ұ�����[M]. ����: ұ��ҵ������, 1990: 43-62.
CHANG Fa-xian. Metallurgy of light metals analysis[M]. Beijing: Metallurgical Industry Press, 1990: 43-62.
[11] ������. �����������ⶨ������[J]. �Ĵ��ữ��ѧԺѧ��, 2001, 14(1): 21-23.
DU Li-cheng. Volumetry analysis natrium silicate[J]. Journal of Sichuan Institute of Light Industry and Chemical Technology, 2001, 14(1): 21-23.
[12] ������. ��������������ѧ[M]. ����: ұ��ҵ������, 1982: 85.
YANG Chong-yu. The technology of alumina production[M]. Beijing: Metallurgical Industry Press, 1982: 85.
[13] ����, ��С��, ��־��. Ũ��߿��Ա���������Һ��ˮ�����������γɵĶ���ѧ�о�[J]. �ߵ�ѧУ��ѧѧ��, 1999, 20(8): 1262-1265.
LIU Gui-hua, LI Xiao-bin, PENG Zhi-hong. The kinetics of formation of sodium aluminosilicate hydrate in strong caustic solutions[J]. Chemical Journal of Chinese Universities, 1999, 20(8): 1262-1265.
[14] ��С��. ��������Һ�������Ļ����о�[D]. ����: ������ѧ, 2000.
LI Xiao-bin. Study on technology and mechanism of separating silica and alumina in aluminate solution[D]. Shenyang: Northeastern University, 2000.
������Ŀ�������ص�����о���չ�ƻ�������Ŀ(2007CB613603)
ͨѶ���ߣ��������ڣ��绰��024-83687731��E-mail: wuy@smm.neu.edu.cn


