���±�ţ�1004-0609(2010)07-1339-07
Mg������������ĭ��������Ϊ��Ӱ��
�� ��1, 2��Ҧ�㴺1, 2�����1, 2������˹1, 2����־��1, 2
(1. ������ѧ ������ұ��ѧԺ������ 110819��
2. ������ѧ �����������Ƚ��Ʊ����������о����ģ����� 110004)
ժ Ҫ��
���÷�ĩұ���Ʊ���ͬMg���������Ĵ����տ���ĭ�����ϣ�����Mg������������ĭ��������Ϊ����ĭ�ȶ��Ե�Ӱ������о������������Mg�۵����ӵ���ǰ���������ʵ������������ĭ���ݿṹ�ľ��Ȼ������ӵ�Mg��ͬ��������Al�۱����Al2O3��Ӧ������ͬ��������������ʪ�Ե�MgAl2O4�࣬����ԭ�����۱����������ṹ�����ɵ�MgAl2O4����ȵطֲ����ݿIJ����±߽���ݱ��ϣ���ʪ��MgAl2O4��ij�����������ı����ȣ�������������Һ��ëϸ���ú��������������ĸ���Ӱ�죬�Ӷ������ĭ���ȶ��ԣ��ڿ���������ҵ��Al�ۺ�����(��������)Ϊ(0.34��0.01)%��Mg��������Ϊ(0.6%~1.0)%�������£����Ի����ѵ������ʺ;��ȵ��ݿṹ��
�ؼ��ʣ�
��ĭ������ĩұ����Mg����������Ϊ����ĭ�ȶ�����
��ͼ����ţ�TG 146.21���� ���ױ�־�룺A
Effect of addition of Mg powders on foaming behaviors of Al foams
WANG Lei1, 2, YAO Guang-chun1, 2, LUO Hong-jie1, 2, LIANG Li-si1, 2, ZHANG Zhi-gang1, 2
(1. School of Materials and Metallurgy, Northeastern University, Shenyang 110819, China;
2. Engineering and Researching Center of Advanced Preparation Technology of Materials, Ministry of Education, Northeastern University, Shenyang 110004, China)
Abstract: Closed-cell pure aluminum (Al) foams with Mg powders were prepared by powder metallurgy route. The effects of addition of Mg powders on the foaming behaviors and foam stability were discussed. The results show that the expansion rate of the precursor increases significantly with addition of Mg powders and uniform cell structures of Al foams are obtained; MgAl2O4 phases with good wettability with Al melt are formed due to the reaction between Mg powders and Al2O3 on the surface of Al powders; original oxide structures on surfaces of Al powder are destroyed and MgAl2O4 phases locate uniformly into the plateau borders and cell walls; the apparent viscosity of melt is enhanced due to the present of MgAl2O4 phases. Negative impacts caused by gravity drainage��capillarity and bubble flow are weakened greatly and hence foam stability is improved. The optimum expansion rate and uniform cell structures are achieved as oxygen content for air-atomized Al powder is (0.34��0.01)% (mass fraction) and addition of Mg powder is (0.6%-1.0) %.
Key words: Al foams; powder metallurgy; Mg powder; foaming behaviors; foam stability
��ĭ����һ�ּ��ṹ�빦��Ϊһ��������ϲ��ϣ��������ʡ��߱ȸնȡ������������Լ�������κ����������ŵ�[1-3]�����ڶ���ĭ���Ʊ�����(����ֱ�ӷ��ݷ���ע�����ͷ�ĩұ��)�У���ĩұ�����ھ��н�������[4-6]���ص㣬�����Ʊ�������״���ӵ���ĭ���㲿����Խ��Խ�ܵ���ĭ���о��ߵ����������ø÷������Ʊ���������ĭ����ƷҲ�㷺Ӧ������������ͺ��պ��������[7-8]��
����ĭ�����Ʊ������У�������Һ��ëϸ���ú����������Dz��ɱ���ġ����������µ�Һ̬�����������ݱںͲ����±߽��γɵ�ͨ����������ֱ���µķ�������������ʵ����ij��֣���ëϸ����ʹ���Ѿ��γɵ�Һ̬�ݱ����ڲ����±߽����������ø�ϸ����������ʹ����γɵ��������ѹ��ͬ�����������ݺϲ��ĸ��ʡ���˼�С������Һ��ëϸ�����Լ������������ȶ����ݵĹؼ����ڡ�Ŀǰ��������ĭ����Ҫ���ȶ���������DUDKA��[9]����Ŀ����ȶ���������ͨ�������մɿ����������������Ϸ�Ӧ�Ŀ������ʵ�����������߷�ĩұ���Ʊ���ǰ�����У�ͨ���մɿ�������-�̽��洦�ĸ�������������ı����ȣ���С�����±߽����ݱ�֮���ѹ����ȶ���ĭ��Һ̬�������ݷ����ǽ��մɿ������ӵ����ڽ����У������ձ����Ϊ��Һ̬�����кܺ���ʪ�Ե��մɿ����ܹ�������ĭ���ȶ���[10-11]���ڲ��÷�ĩұ���Ʊ���ĭ���Ĺ����У�Al�۱��������Dz��ɱ���ģ��������ۼ�������������������أ���������[12]�����˹�����������Al�ۻᵼ����ĭ�IJ��ȶ������ʹ���ʵ���������Al���DZ���ġ���������������������������֮������ʪ��[13]��������Щ���۱���������������������ȶ���ĭ������[14]������Mg���������ս�ʵ���еĹؼ����ã���ͨ������������Mg�ۣ���ЩMg��ͬAl�۱��������Ĥ��Ӧ�γ�MgAl2O4���ƻ���ԭ����������ṹ���ٽ������۵��սᡣ��ˣ�ͨ��������Mg�����ӵ���ĩұ����ĭ����ǰ�����У���Ȼ���ƻ����۱����������ṹ��Ŀǰ���������ټ�������ױ���ϵͳ�о�Mg�۶Է�ĩұ����ĭ���ݿṹ����ĭ�ȶ��Ե�Ӱ�졣
��������ͨ�����Ӳ�ͬ����Mg�۵�ǰ�����У��������ݺ���ĭ��������Ϊ�ͱ�����ò��ȷ�������Mg�ۺ�����������ԭλ��Ӧ���ɵ���ʪ�Կ����ȶ�����[9]̽��Mg�۵����Ӷ���ĭ�ȶ��Ե�Ӱ�졣
1 ʵ��
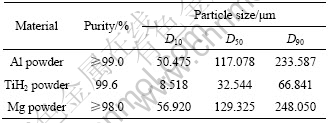
����Malvern Mastersizer2000�������ȷ����Ƿ�����������ʹ�õķ�ĩ����ĩԭ�ϵ��������1���С�
����LECO��˾������TC-436�������ⶨ�Dz�ÿ�������Al����������(��������)Ϊ(0.34��0.01)%��
��1 ʵ���÷�ĩԭ�ϵ���������
Table 1 Physical characteristics of powder materials used in experiment
���÷ֱ���Ϊ300dpi��ɨ���ǶԷ��ݺ�δ�и���Ʒ���������òɨ�衣�������и������ĭ���ظ߶ȷ����п������п�����ݿ�����ú�ɫ������������ᴦ�������Ӳ����±߽���ݱ�ͬ�ݿײ�֮��ĶԱȶȣ�����������ɵ���Ʒ��ɰֽ��ĥ���⣬��Ʒ�������ݿױ�����ò����ɨ�衣����������Mg�۵�ǰ������һ���¶��¼��ȣ�����XRD��������������Ƿ����µ��������ɡ����ù�ѧ����(OM)��ɨ���������(SEM)���������±߽���ݱ��ϵ����ʷֲ��������SEM�е��������EDSԪ�ط���������ȷ����������ɡ�
����ҵ��Al�ۡ���ͬ��������Mg�ۺ�0.6%(��������)���⻯����KQM-X4B/B������ʽ��ͷ������ĥ���ϻ���2 h���������YES-2000������ʽѹ���������ͨ����������ѹѹ�Ƴ�ֱ��Ϊ50 mm���߶�Ϊ20 mm�Ŀɷ���ǰ������ϡ����õ�ѹ��ѹ��Ϊ400 MPa����ѹʱ��Ϊ10 min����ѹ�ƺ��ǰ�������Ԥ�ȼ��ȵ�1 073 K�ĵ���¯�ڽ��з���ʵ�顣����ʱ�������100~160 s������û������Mg�۵�ǰ���壬����ʱ��Ϊ140~150 s��������Mg�۵�ǰ���巢��ʱ�������100~110 s��ʵ�鹤������ʾ��ͼ��ͼ1��ʾ��
2 ���������
��ʵ���в��õ�Mg��������Ϊ0��0.2%��0.6%��1.0%��1.4%��1.8%��Ϊ�˸���ȷ��������ĭ��������Ϊ�����������ʼ��㹫ʽ��
![]() (1)
(1)
ʽ�У�REΪ�����ʣ�hPΪ��ĭ�巢��ǰ�߶ȣ�hFΪ��ĭ�巢�ݺ�߶ȡ�
ͼ2��ʾΪ���в�ͬMg������ĭ�����ݺ�������Ƭ����ʵ������У���Mg�۵�ǰ����ķ���ʱ��Ϊ105 s��û��Mg�۵ķ���ʱ��Ϊ145 s(����������105 s������£�����ʱû��Mg�۵�ǰ������ϱ����������ض����²��ܳ������Ե����ͣ���ͼ2(a)������ʾ)����ͼ2���Կ���������Mg�ۺ��������ӣ�������Ҳ��������Mg�������ﵽ0.6%ʱ������������ﵽ1.0%ʱ��������С���ȵļ�С������ֳ�����С��������Mg��������Ϊ0.6%ʱ������ʽ(1)�ɼ��������������ʴ�ԼΪ472%����ˣ���������Ϊ�Ͽ���Mg����������0.2%���ϾͿ����ˡ�
ͼ3��ʾΪ��ͬMg��������ĭ������������Ƭ�����Է�������Mg���������ӣ��ݿṹ���������Ըı䡣��ͼ3(a)�п��Է����ݿṹ�������ȣ������γ��˵ײ�ʵ���㡣ͼ3(b)��ʾ���ݿṹ�������ƣ����ǵײ�ʵ���㻹�DZȽ����ԡ���˵��������Mg������û����Ч����ֹ������Һ��Ȼ������ͼ3(c)��(d)���Է��֣���Mg����Ϊ0.6%~1.0%ʱ��ĭ����������Ϊ��ǿ���ݿṹ��Ծ��ȣ����Ҹ�Ϊ��Ҫ���ǵײ�ʵ���������ʧ�ˣ���Ҳ�Ƿ�ĩұ���ܹ��Ʊ�����������ĭ��������ԭ��֮һ����������Mg�ۣ�����Mg��������1.0%֮�����ݴ����غϲ���������Ϊ����Mg��ͬ������֮���γɲ���þ���Ͻ��࣬�����˻�����ϵ��۵㡣��ˣ�����ͬ�����¶��ºϽ�����ı����Ⱦͻή�ͣ������������¼Ӿ��˽���Һ�����Ų����±߽���ݱ��γɵ�ͨ����ֱ����������ʹ�ײ�ʵ�������Ա�����ӹ���Mg�ۻ��ᵼ�ºϽ�����ı����������ӣ�ʹ�����±߽���ݱڵ�˱��������ǿ�����������ݱڱ䱡�����������������Ѻͺϲ���������ͼ3(e)��(f)��ʾ�����ݺϲ���ʵ����ij��֡�
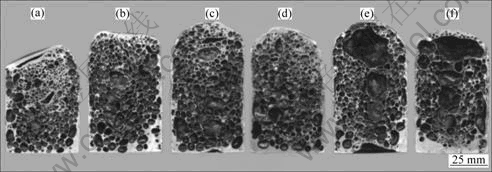
����ǰ�����϶����ڷ��ݹ�������ȫ���ڿ����У�����϶�����ǰ����Ӵ���������Ҳ����Ũ����ߵĵط������Է��ݺ���ĭ�嶥����ò�ܹ���Ӧ��ĭ��ı��������̶ȡ����ڼ����������������������̶Ⱦ�������ĭ�����͵ĸߵ͡�ͼ4��ʾΪ6�ֲ�ͬMg������Ʒ���ݺ�û���и�Ķ�����ͼ�����Է�������Mg���������ӣ�����ͬʱ����(����û������
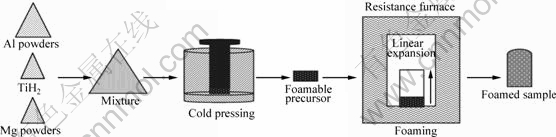
ͼ1 ��ĩұ���Ʊ���ĭ������ʾ��ͼ
Fig.1 Schematic diagram of preparation of Al foams by powder metallurgy route

ͼ2 ��ͬMg��������ĭ�������Ƭ(�����¶�Ϊ1 073 K)
Fig.2 Macrographs of Al foams with different mass fractions of Mg at foaming temperature of 1 073 K: (a) Without Mg; (b) 0.2% Mg; (c) 0.6% Mg; (d) 1.0% Mg; (e) 1.4% Mg; (f) 1.8% Mg
ͼ3 ��ͬMg��������ĭ�����ݿױ�����ò
Fig.3 Surface morphologies of cell walls of Al foams with different mass fractions of Mg: (a) Without Mg; (b) 0.2% Mg; (c) 0.6% Mg; (d) 1.0% Mg; (e) 1.4% Mg; (f) 1.8% Mg

ͼ4 ��ͬMg����������ĭ���Ķ�����ͼ
Fig.4 Top views of Al foams with different mass fractions of Mg: (a) Without Mg; (b) 0.2% Mg; (c) 0.6% Mg; (d) 1.0% Mg; (e) 1.4% Mg; (f) 1.8% Mg
Mg���ſ鷢��ʱ��Ϊ145 s��)���������̶���С������Mg������������0.6%ʱ�ᷢ�ֶ�����ò�Ѿ�û��̫��仯��ͼ4(a)��ʾ����Ʒ���������Ƚ����أ�����������û��Mg������£�Al�۱������������ܸ���Һ������ʪ��ֻ����������Һ����ž��γɴ����������߱��ų��ĭ��ı��档��ˣ��� 1 073 K��¯�������£�û������Mg�۵�ǰ�����ϲ����ڴ��ڿ����У��ų�����������ϱ����Ѿ����ڸ����µı��棬ʹ��������ø������ף��ټ��ϴ����������ų���������������ʹ������ĭ�嶥���γ������������㡣��ͼ4(b)��ʾ������0.2%Mg�۵���ĭ���ϲ��Ѿ�û�г���ͼ4(a)��ʾ�Ĺ����������㣬ֻ���ֺ����������㣬˵������Mg��Ч�ؼ����˶�����ĭ���������
ͼ5��ʾΪû������Mg��������1.0%Mg���ݿ�SEM���ÿ�Բ�ζ�������ͼ5�е��ݿ���ò����Բ�ζȶ���Ϊ[15]
![]() ��
��![]() ��2��
��2��
ʽ�У�cΪ��Բ�ζ�ci��ƽ��ֵ��liΪ�ݿױ߽糤�ȣ�
ͼ5 ��ͬMg������ĭ�����ݿIJ����±߽��SEM��
Fig.5 SEM images of Al foams with different mass fractions of Mg at Plateau borders: (a) Without Mg��(b) With 1.0% Mg
AiΪ�ݿ������nΪ�ݿ���Ŀ��ci=1���ݿ���Բ�ס�cԽ����ƫ��Բ�εij̶�Խ��
Ŀǰ���������������ȶ���Һ̬�����ݿṹΪ���ʮ������[16]����ˣ�Բ�����������Ͷ��Ǽ����ȶ��ġ���ͼ5(a)������û������Mg�۵���ĭ�������ݱڽϺ��ݿ�С�������±߽缸������һƬ�����ֶദ�ֲ�ṹ���ݱں��ͬ�����±߽��ȼ����൱���ݱڱ�Ե�ʲ�������״���ɹ�ʽ(2)��֪Բ�ζ�c�ӽ�1����ͼ5(b)��ʾ�����ڵ��͵Ľ�����ĭ�����±߽磬��Ҫ�γɵ��Ǿ�����������Ľ���������� �ݿ�[16]��
��ԭλ��Ӧ�����ȶ���������֪����ͨ�����Ӹ߷�ӦԪ��ͬ��������е����ʷ�Ӧ���γɵ�ϸС���������ͬ����֮�����ʪ�Ժû����൱��Ҫ�ġ���ʪ�Բ�Ŀ�������������ų����ý����Ի�е���Ľ�Ϸ�ʽ�������ݿ��ڱ�������ų������棬���ȶ���ĭ�����ã�ֻ����ȫ��ʪ�ԵĿ������ܹ��ӻ����ݱڱ䱡����С������Һ��ëϸ���õĸ���Ӱ����ȶ���ĭ��ͼ6(a)��ʾΪû������Mg�IJ����±߽��ϵ�������ֲ��������û������þ������£�ǰ������ֻ�п�������Al�۱������γɵ������������㡣�ڷ����ڼ䣬��Щ������ͬ������Һ֮������ʪ�Ե����˴�����������֮�����ž۲���飬������������︻���������������������Ĵ���ʹ����ĭ�����ȶ�������ֻ�����������ڵ�ǰ���巢�ݺ��������е�����ȴ���̹����б���������ĭ���У��е������������ǿ���ų����ö��ﵽ��ĭ��ı��档�����ų�������Ϊ���Եı��־���ǰ�����϶����������ֽӴ��IJ��ַ��ݺ��γ������ܵ��������(��ͼ4(a))��ͼ6(b)��ʾΪ����1.0%Mg�۵IJ����±߽��ϵ�������ֲ���������Կ���Mg�����ӵ���ԭ���ž۽�����������ȷ�ɢ����ǰ��ʵ�����֪��������1.0%Mg�ۺ�Һ̬��ĭ���ȶ��Եõ���Ч��ߣ�����������Ҳ�������ӣ�ͬʱ��������ĭ�嶥�������̶ȡ�
������һ���̶�������Mg�����ӵ�����һ����������Al���У����ܻ�������·�Ӧ��
MgO+Al2O3![]() MgAl2O4 (3)
MgAl2O4 (3)
3Mg+Al2O3![]() 3MgO+2Al (4)
3MgO+2Al (4)
3Mg+4Al2O3![]() 3MgAl2O4+2Al (5)
3MgAl2O4+2Al (5)
ͼ7��ʾΪ����3����Ӧ����ʽ�ļ���˹�����ܱ仯����ͼ����ͼ7�п��Կ�����3����Ӧ���������뷴Ӧ��ļ���˹�����ܵIJ�ֵ��1 000 K���¶��Ǹ�ֵ����ʵ����õķ����¶�Ϊ1 073 K��ǰ�����������¶�һ����973 K���ң����˵����3����Ӧ������ѧ�϶��ǿ��еġ���1 073 K�ķ����¶��£�������������Mg�����ӵ�����������Al���У�Mg�۱����MgO���ȸ�Al2O3��Ӧ����þ���⾧ʯ������Ӧ���е��е���Mg����ʱ����Ӧ(4)��ʼ������MgO�����ɵ�MgO��������ͬAl�۱����Al2O3��Ӧ�γ�þ���⾧ʯ�����Կ�����Ϊ��Ӧʽ(3)��(4)��(5)���� �䷴Ӧ���̡����������ԭ���Ƕȣ�����˹�����ܵIJ�ֵԽС˵����Ӧ�Ŀ�����Խ��ͼ7�����Է��ַ�Ӧʽ(5)�����������·���˵������������ͷ�Ӧ���DG��С��ʽ(5)���γ�MgAl2O4����Ҫ��Ӧ��

ͼ6 ��ͬMg��������ĭ���IJ����±߽��ѧ��Ƭ
Fig.6 Optical photographs of Al foams at Plateau borders: (a) Without Mg��(b) With 1.0%Mg
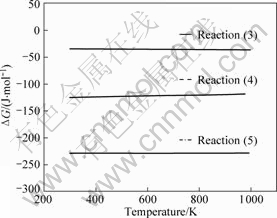
ͼ7 ��Ӧ(3)��(4)��(5)�ļ���˹�����ܱ仯
Fig.7 Changes of Gibbs free energies for reaction equations (3), (4) and (5)
Ϊ�˽�һ��֤��þ���⾧ʯ�Ĵ��ڣ���������1.0%Mg�۵�ǰ����(û�����ӷ��ݼ���ǰ����)�� 793 K�������ս�1 h��Ȼ�����XRD��������ͼ8��ʾ����ͼ8���Կ��������˻���Al���⣬��Ҫ������MgAl2O4�⾧ʯ�࣬˵������Ӧʽ(5)�����ı�Ȼ�ԡ�
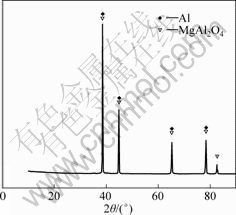
ͼ8 ����1.0%Mg�۵�ǰ������793 K�ս�1 h��� XRD��
Fig.8 XRD pattern of precursor with 1.0% Mg annealed at 793 K for 1 h
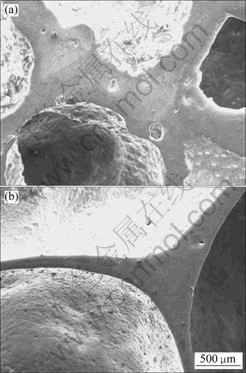
����1.0%Mg�۵�ǰ���巢�ݺ��ݱ��ϵ�SEM����ͼ9(a)��ʾ��ͼ9(a)�е�״�Ϳ�״���ʵ�EDS����ͼ9(b)��ʾ����ͼ9���Եó�����Щ��ɫ���ȷ�ɢ�ĵ�״���߿�״����Ϊþ���⾧ʯ��þ���⾧ʯ�ܱ���������ȫ��ʪ�����ҹ㷺�طֲ��ڲ����±߽���ݱ��ϡ�ͼ9(a)�������İ�ɫ����Ϊ������������Ҫ�������ڿ����з��ݣ����������������ͬ����Ӧ�γɵ����������Щ���ʵĴ��ڶ����ȶ�Ҳ����һ���ĸ������á�
���ӵ�Mg��ͬ���۱���������ﷴӦ����þ���⾧ʯ��þ���⾧ʯ�ij����ƻ������۱����������ṹ����������������֮��Ľ�飬�γɹ㷺�ֲ��ڲ����±߽���ݱ��ϵľ��ȷ�ɢ��ϸС������������⾧ʯ������ɻ������������ͬ������֮�����ʪ�ԣ�������һ���̶�������������ı����ȣ�ʹ�����������Ա�������Һ��ëϸ���ú����������������IJ���Ӱ�����һ���̶��ϵõ����ƣ��Ӷ��ӳ�����ĭ�����������Һ̬����ĭ���ȶ��ԡ�

ͼ9 ����1.0% Mg����ĭ���ݱ�SEM��EDS��
Fig.9 SEM image (a) of cell walls in Al foam with 1.0%Mg and EDS spectrum (b) of MgAl2O4 phases
3 ����
1) û������Mg�۵�ǰ���巢�ݺ���Ʒ�����������ز����γ������ܵ������㣬ʹ��ǰ�����ڸ߶ȷ����ϵ����������ܵ��谭����Ӧ���ӳ��˷���ʱ�䡣����Mg�������������ӣ����ݺ���Ʒ���������̶����ᣬ��������������
2) ���ӵ�Mg����Al�۱����Al2O3��Ӧ����������������������ʪ�Ե�MgAl2O4�ࡣMgAl2O4����ȷ�ɢ����ĭ��IJ����±߽���ݱ��ϣ����ֻ���ȫ������������������ʪ�Ե�MgAl2O4������������ı����ȣ�������������Һ��ëϸ���ú������������ӻ������ݱڱ䱡���ȶ���Һ̬��ĭ��
3) ��Al�ۺ�����Ϊ(0.34��0.01)%�������£�Mg����������(0.6%~1.0%)�������£��ܹ���Ч����������Һ��ëϸ���ò����Ի����ѵ������ʺ;��ȵ��ݿṹ��
REFERENCES
[1] BANHART J. Manufacture, characterization and application of cellular metals and metal foams[J]. Prog Mater Sci, 2001, 46: 559-632.
[2] LEHMHUS D, BANHART J. Properties of heat-treated aluminium foams[J]. Mater Sci Eng A, 2003, 349: 98-110.
[3] DUARTE I, BANHART J. A study of aluminium foam formation-kinetics and microstructure[J]. Acta Mater, 2000, 48: 2349-2362.
[4] BANHART J. Metal foam: Production and stability[J]. Adv Eng Mater, 2006, 8(9): 781-794.
[5] KENNEDY A R, ASAVAVISITHCHAI S. Effect of ceramic particle additions on foam expansion and stability in compacted Al-TiH2 powder precursors[J]. Adv Eng Mater, 2004, 6(6): 400-402.
[6] �� ��, ����, �� ��, Ҧ�㴺, ����ʤ. ��ĭ���Ʊ����������ݲ���γ������[J]. �й���ɫ����ѧ��, 2008, 18(7): 1268-1273.
LI Bing, CAO Zhuo-kun, WANG Yong, YAO Guang-chun, HUA Zhong-sheng. Formation and control of bubble-free layer during preparation of Al foam by foaming in melt[J]. The Chinese Journal of Nonferrous Metals, 2008, 18(7): 1268-1273.
[7] SCHWINGEL D, SEELIGER H W, VECCHIONACCI C, ALWES D, DITTRICH J. Aluminium foam sandwich structures for space applications[J]. Acta Astronaut, 2007, 61: 326-330.
[8] FUGANTI A, LORENZI L, HANSSEN A G, LANGSETH M. Aluminium foam for automotive applications[J]. Adv Eng Mater, 2002, 2(4): 200-204.
[9] DUDKA A, GARCIA-MORENO F, WANDERKA N, BANHART J. Structure and distribution of oxides in aluminium foam[J]. Acta Mater, 2008, 56: 3990-4001.
[10] KAPTAY G. Interfacial criteria for stabilization of liquid foams by solid particles[J]. Colloids Surf A, 2002, 230: 67-80.
[11] SUN Y Q, GAO T. The optimum wetting angle for the stabilization of liquid-metal foams by ceramic particles: Experimental simulations[J]. Metall Trans A, 2002, 33: 3285- 3292.
[12] K?RNER C, ARNOLD M, SINGER R F. Metal foam stabilization by oxide network particles[J]. Mater Sci Eng A, 2005, 396: 28-40.
[13] LANDRY K, KALOGEROPOULOU S, EUSTATHOPOULOS N. Wettability of carbon by aluminum and aluminum alloys[J]. Mater Sci Eng A, 1998, 254: 99-111.
[14] LUMLEY R N, SERCOMBE T B, SCHAFFER G B. Surface oxide and the role of magnesium during the sintering of aluminum[J]. Metall Trans A, 1999, 30: 457-463.
[15] BONACCORSI L, PROVERBIO E. Powder compaction effect on foaming behavior of uni-axial pressed PM precursors[J]. Adv Eng Mater, 2006, 8(9): 864-869.
[16] GERGELY V, CLYNE T W. Drainage in standing liquid metal foams: Modeling and experimental observations[J]. Acta Mater, 2004, 52: 3047-3058.
(�༭ �� ��)
������Ŀ�����Ҹ����о���չ�ƻ�������Ŀ(2008AA03Z512)��������Ȼ��ѧ����������Ŀ(50774021)
�ո����ڣ�2009-05-19�������ڣ�2010-04-25
ͨ�����ߣ�Ҧ�㴺�����ڣ���ʿ���绰��024-83686462��E-mail��gcyao@mail.neu.edu.cn


