���Ӽ���Ca(OH)2���������õ�Ӱ��
��ƽ�����ڣ����ػ�����ɭ�֣������̣�����
(����������ѧ ������ѧ�빤��ѧԺ������ ������650500)
ժ Ҫ��
ȼ�ջ���β��, ��ZnO��Fe2O3��MgO��Ϊ���Ӽ�����Ca(OH)2�����ƻ���β������Ϊ1 m3/h����������Ϊ3.6 m3/h��ʹ¯���¶ȱ�����960~980 �棬���첻ͬ���Ӽ���Ca(OH)2���������õ�Ӱ�죬�����ռ�����XRD��SEM��EDS�����������Ԫ�ط������о����������ZnO���Ӽ���ʹ���ռ������γ�һ�����ܵ�Ca19Zn2(PO4)14���������ռ��ڶ�ʱ����ʧ�Fe2O3���Ӽ���ͬCaO��Ӧ�γ�Ca2Fe2O5������SO2��ȥ���ʣ���Ca2Fe2O5�����ɻ�ʹP2O5��ȥ������ߡ�MgO���Ӽ��ɴٽ�SO2��P2O5���������ռ����е���ɢ���ӿ캬����������γɣ��Ӷ�������ռ���SO2��P2O5��ȥ���ʡ���120 min�ķ�Ӧʱ���ڣ�MgO������Ϊ25%ʱ�����ռ���SO2ȥ����ƽ�����7.5%��P2O5��ȥ����ƽ�����19.5%��
�ؼ��ʣ�
��ͼ����ţ�X511 ���ױ�־�룺A ���±�ţ�1672-7207(2013)10-4342-08
Effects of additives on Ca(OH)2 sorbent for sulfur- and phosphorus-fixing
NING Ping, WANG Lei, WANG Zhonghua, TIAN Senlin, QIN Yangsong, JIANG Ming
(Faculty of Environment Science and Engineering, Kunming University of Science and Technology, Kunming 650500, China)
Abstract: Premixed combustion of yellow phosphorus tail gas was performed in fluidized bed. ZnO, Fe2O3 and MgO were used as additives of Ca(OH)2 sorbent. The effect of additives on the retention of P2O5 and SO2 in Ca(OH)2 was examined at 960-980 ��, with yellow phosphorus tail gas flowed being controlled at 1 m3/h, and air flowed at 3.6 m3/h. XRD, SEM and EDS techniques were used to analyze and characterize sorbent. The results show that ZnO additive can induce Ca19Zn2(PO4)14 cover sorbent surface and result in the inactivation of sorbent within a short reaction time. Fe2O3 additive can react with CaO to from Ca2Fe2O5, which reduces removal rate of SO2, but improves removal rate of P2O5. MgO additive can promote the spreading of gaseous SO2and P2O5in sorbent, accelerate phosphorus crystal particle formation, and consequently improve the removal rate of absorbent toward SO2 and P2O5. When 25% of MgO is presented in sorbent, the removal efficiencies of SO2 and P2O5 increase to about 7.5% and 19.5%, respectively, during 120 min.
Key words: sulfur-fixing; phosphorus-fixing; premixed combustion; yellow phosphorus tail gas
�й��Dz��״��������ռ�����ܲ��ܵ�80%[1]��ÿ����1 t���ף���������β��Ϊ2 500~3 000 m3��β���к�CO 87%~92%(��������)������0.8~8.0 g/m3������0.5~1.5 g/m3������һЩ���ʣ�����ֵΪ10.5~11.0 MJ/m3 [2]�����ڻ���β�����нϸߵ���ֵ��������ҵ���Բ��û���β����������¯��������β��ȼ�պ������P2O5��SO2�ḯʴ¯���ڻ������ͻ��ȹܱڣ�7~90 d֮�ھ��ܵ��´��ף���¯ͣ��[3]��Ŀǰ���ڶԻ���β�������ʲ���30%��������ҵ����ȼ�պ�ֱ���ŷ�[4]�������������Դ�˷ѣ��Դ�������Ҳ�������Ⱦ��Ca�����ռ��������ۺͲ��������ѱ��㷺����SO2�Ĺ̶��������������ռ������ʵͺ����¹���Ч�ʵ͵�����[5-6]�����о�����[7-9]�����Ӽ��ܹ�����Ca����������۽ṹ����С��ɢ��������߱ȱ�������Ӷ�������ռ��Ĺ���Ч�ʺ������ʡ�ͬʱ����Ca�����ռ������о�����[10-11]�����ռ�����ȥ�������¶ȳ����ȣ��¶�Խ�����ռ����Ĺ̶�Ч��Խ�á�Ŀǰ�������ڵ�[10-11]���о��⣬��δ���������Ӽ�����Ca�����ռ���ͬʱ��߹�����Ч������ر������������߲���������Ԥ��ȼ�ջ���β������Ca(OH)2���ռ��зֱ����ZnO��Fe2O3��MgO���о���3�����Ӽ���Ca(OH)2���������õ�Ӱ�졣������X�������ɨ��羵�Է�Ӧǰ������ռ����з�����̽�����Ӽ���Ca(OH)2���ռ��ɷֺͱ�����̬��Ӱ�졣
1 ʵ��
1.1 ʵ��ԭ��
1.1.1 β������Դ�����
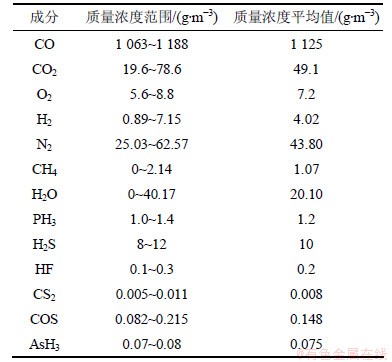
ʵ�����û���β��Ϊij���׳���¯������װ�ò�����¯������3��ˮ��������������پ�3��ˮϴ���õ�β����������λ�ھ���װ�����ǰ��������ձó�ȡ������β����Ҫ������1��ʾ������������Դ�ڸû��׳������ֵ��PH3��H2SΪ��ʵ��������ֳ��������
��1 ����β����ɳɷ�
Table 1 Components of yellow phosphorus tail gas
1.1.2 ���ռ����Ʊ�
�Ʊ����ռ���ԭ��Ϊ��������Ca(OH)2��ZnO��Fe2O3��MgO������Ca(OH)2Ϊ���ϣ�ZnO��Fe2O3��MgO��Ϊ���Ӽ������Ӽ��ļ�����Ϊ��������25%(�����������Ӽ���������Ϊ3:1)���Ʊ����ռ�ʱ�������ϡ����Ӽ�����ˮ�ϣ�ˮ��ʱ��Ϊ30 min��ˮ���¶���25 �����ҡ�֮�Բ��벻ͬ���Ӽ������ռ����з�ɴ���������������飬��ɸ�Ƴ�ֱ��Ϊ1.0~1.2 mm�Ŀ�����
1.2 ʵ��װ�ú���
1.2.1 ����С��������װ��
ʵ����ͼ1��ʾ��С����������Ӧװ���н��С����й���ϵͳ����1������Ϊ3.5 m3/h����ձ÷����������β����1������Ϊ7.0 m3/h����ձ÷������������ʹ���������ڷ���ת�������ơ����ػ�����U��ѹ���ƽ��в����Ϳ��ơ�ȼ��ϵͳΪ����С������������Ԥ���ҡ�ȼ�����졢����塢¯��(�ھ�56 mm���߶�600 mm)��ɡ����ⲿ�ù�������ά�������£�¯���¶ȵIJ�����2��S�Ͳ����ȵ�ż�ֱ����Ӳ�������ɡ��ȵ�ż���·�ΧΪ0~1 300 �棬�����ҵľ���ֱ�Ϊ70 mm��500 mm��ȼ�պ����徭��Ϊ0.1 mm���������˺��ŷš�
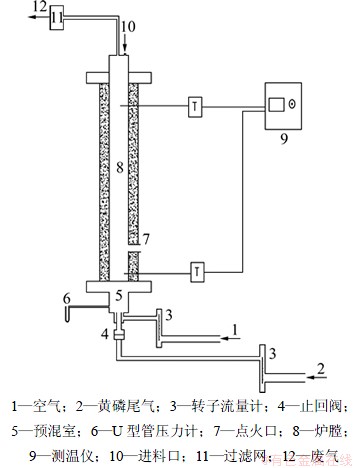
ͼ1 ������ʵ��װ��
Fig. 1 Schematic diagram of experimental setup
1.2.2 ��Ӧ���̼������
������¯���ڼ���100 g���ռ���Ȼ��ͨ������ͻ���β��������β������Ϊ1 m3/h����������Ϊ3.6 m3/h����������Ԥ�����ڻ�ϣ������ͨ����������¯������ȼ��ͬ���ռ���Ӧ������ʵ�������¯���¶���960~980 ��֮�䣬����ѹ��Ϊ1.4 kPa���ҡ������ڷ���SO2ʱ��ֹͣʵ�飬��¼��Ӧʱ�估SO2����Ũ�ȣ�֮��رտ�����ȼ�����ã������ռ���¯������Ȼ��ȴ��ȡ����
1.2.3 ��Ӧǰ��������
��ʵ��װ��ǰ����������ܲ���������Ļ���β����PH3��H2S�ĺ�����ÿ��ʵ��ǰ�ֱ��������1�Ρ�����PH3��������Ϊ0.1~1.5 g/m3��H2S��������Ϊ1.0~20.0 g/m3��ȼ�պ��ų����壬ÿ10 min���1��SO2�ĺ��������ü�������Ϊ0~150 mg/m3�������е�P2O5���չ���GB/T 16036��1995�������������ռ���֮�����ICP-AES��ˮ���е����вⶨ������õ������������ĺ�����
1.3 ���ռ��������
(1) �����IJⶨʹ������Leeman Labs��˾PS1000�͵��ź�ϵ����ӷ������(ICP-AES)�������IJⶨ����EDTA������[12]��
(2) ���ռ�����ṹ����ʹ���ձ���ѧTTRIII��X��ת��������(XRD)������ΪCu K���У��ܵ�ѹΪ40 kV���ܵ���Ϊ200 mA��ɨ������Ϊ10 (��)/min��ɨ�跶ΧΪ5��~90�㡣
(3) ���ռ�������ò����ʹ�÷�����XL30ESEM-TMP�ͻ���ɨ��羵(ESEM)�����Ե�ѹΪ30 kV����Ԫ�ط���ʹ�������˹Phoenix-OIM��X������(EDS)��
1.4 ȥ��Ч�ʼ���
�����ȥ��������100 g���ռ��������������������ȼ�չ����л���β����������������������õ��������������β����PH3����Ũ��Ϊ1.2 g/m3���ң�H2S����Ũ��Ϊ10.0 g/m3���ң�����Ϊ1 m3/h��β������������������ȡ����ȼ��ʱ��(��������β��ʱ��)�����ռ��к��������������ͬһ��Ʒ2�βⶨ��ƽ��ֵ����ó���
���ռ�������β���е���������P2O5�ļ�����ʾ������ʽ���м��㣺
 (1)
(1)
ʽ�У���(PH3)ΪPH3��������Ũ�ȣ�m���ռ�Ϊ���ռ���������w(P2O5)Ϊ���ռ�������(%)��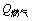 Ϊ����β����������2.09ΪPH3��P2O5��ת��ϵ����
Ϊ����β����������2.09ΪPH3��P2O5��ת��ϵ����
���ռ�������β���е�������SO2������ʾ���ó����ȥ��Ч������ʽ��ʾ��
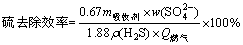 (2)
(2)
ʽ�У���(H2S)ΪH2S��������Ũ�ȣ�m���ռ�Ϊ���ռ���������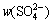 Ϊ���ռ�������(%)��
Ϊ���ռ�������(%)��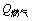 Ϊ����β����������1.88ΪH2S��SO2����ϵ����0.67ΪSO42-��SO2�Ļ���ϵ����
Ϊ����β����������1.88ΪH2S��SO2����ϵ����0.67ΪSO42-��SO2�Ļ���ϵ����
2 ʵ����������
2.1 ȼ���������ȥ����
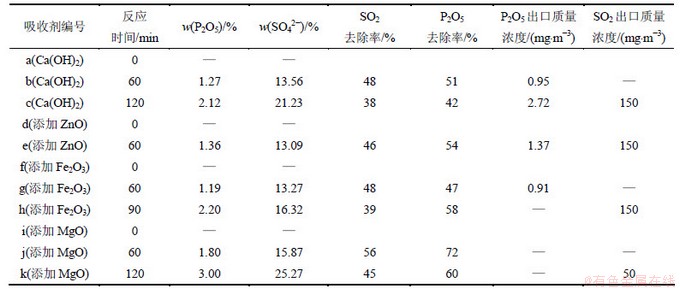
��ȼ�շ�Ӧ������ռ�����1.3��������������������ռ�������ĺ�����������ʽ(1)��(2)���������ȥ���ʣ�������2��ʾ��
�ӱ�2������û�м������Ӽ������ռ�����ȥ����Ϊ42%~51%��SO2��ȥ����Ϊ38%~48%����ֱ����Ӧ����120 min���ڳ��ڲż���SO2��ͬʱP2O5�ij�������Ũ��Ҳ����2.72 mg/m3����˵��������¯���ڱڣ������ռ��ڷ�Ӧ������ĥ�������γɵ�С����������Ҳ�����ԵĹ̶�����[13-14]��
����ZnO��Fe2O3���ڷ�Ӧǰ60 min�����ռ��Ĺ�����Ч��û������Ӱ�졣������ZnO�����ռ�����Ӧ60 min���ڳ��ڱ����SO2������Fe2O3�����ռ�����Ӧ90 min��SO2��ȥ�����½�����39%����ȥ������������58%��������MgO�����ռ�����ȵ�һ��Ca(OH)2��P2O5��SO2��ȥ���ʶ���������ߣ���120 min�ķ�Ӧʱ���ڣ�SO2��ȥ����ƽ�����7.5%����ȥ����ƽ�����19.5%��
2.2 ���ռ���������Ӧ�����������
��Ӧ�¶�Ϊ960~980 ��ʱ����ͬ���ռ���ͬ��Ӧʱ���XRDͼ����ͼ2~5��ʾ���ֲ��Ŵ�ͼ��ͼ6��ʾ��
ͼ2��ʾΪCa(OH)2���ռ���ͬ��Ӧʱ���XRDͼ�ס���ͼ2���Կ�����Ca(OH)2���ռ��ڷ�Ӧ��ʼ��Ѹ�ٷֽ�ΪCaO��ͬSO2��Ӧ����CaSO4���淴Ӧʱ������ӣ�CaSO4�����������ԣ�����2.1�ڵķ������һ�¡�
����ZnO�����ռ���ͬ��Ӧʱ���XRDͼ�ף���ͼ3��ʾ����ˮ�Ϸ�ɹ������γ���ˮ����������п(Ca(Zn(OH)3)2��2H2O, PDF:24-0222)����Ӧ�����������ʧ���γ�ZnO��CaO��ͬʱ���ܷ��֣��ڷ�Ӧ����60 min�����ռ��к��д���δ��Ӧ��CaO������Fe2O3�����ռ���ͬ��Ӧʱ���XRDͼ�ף���ͼ4��ʾ�����Կ�����CaO����SO2��Ӧ�γ�CaSO4�⣬����Fe2O3��Ӧ�γɺڸ�����(Ca2Fe2O5, PDF:71-2108)�������ڷ�Ӧ90 min��Ca2Fe2O5���ɴ��ڡ����2.1�ڵIJ��Խ����֪��Ca2Fe2O5�����������˴�����ͬSO2��Ӧ��CaO����������ռ��ڷ�Ӧ90 min��SO2ȥ����Ѹ�ٵ��½���ͼ5��ʾΪ����MgO���ռ���ͬ��Ӧʱ���XRDͼ�ס���ͼ5���Կ�����MgO������̬�ڷ�Ӧǰ��û�б仯��ҲδͬSO2��Ӧ�γ�����þ��˵��MgO���Ӽ������ռ����������ĸ��ƣ�������Ϊֱ�Ӳ�����Ӧ��ɵġ�
��2 P2O5 ��SO2�����ռ��еĺ�������ȥ����
Table 2 Percentage contents of P2O5 and SO42- and removal efficiency of sorbent
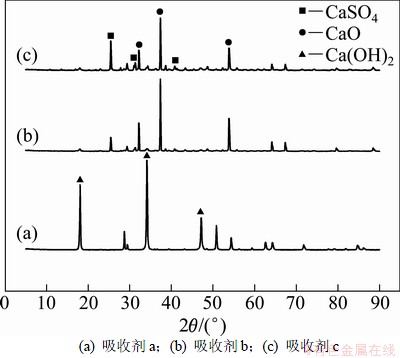
ͼ2 Ca(OH)2���ռ���ͬ��Ӧʱ��XRDͼ��
Fig. 2 XRD patterns of Ca(OH)2 sorbent for different reaction time
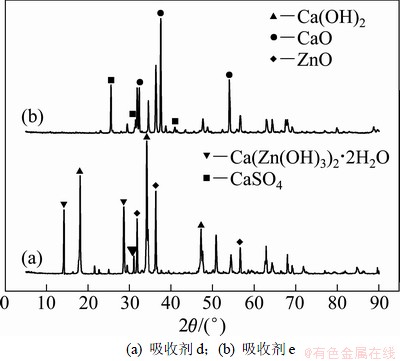
ͼ3 ����ZnO���ռ���ͬ��Ӧʱ��XRDͼ��
Fig. 3 XRD patterns of Ca(OH)2 sorbent promoted by ZnO for different reaction time
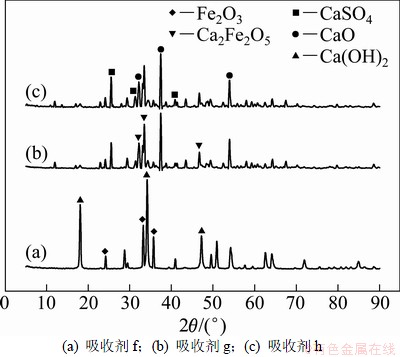
ͼ4 ����Fe2O3���ռ���ͬ��Ӧʱ��XRDͼ��
Fig. 4 XRD patterns of Ca(OH)2 sorbent promoted by Fe2O3 for different reaction time
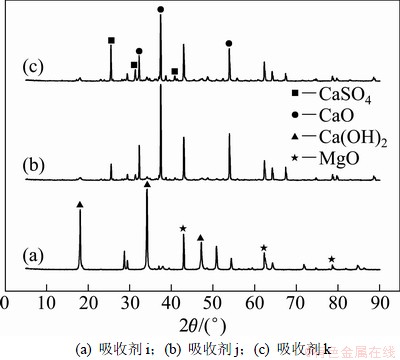
ͼ5 ����MgO���ռ���ͬ��Ӧʱ��XRDͼ��
Fig. 5 XRD patterns of Ca(OH)2 sorbent promoted by MgO for different reaction time
ͼ6��ʾΪ��ͬ���ռ���Ӧ���XRD�ֲ��Ŵ�ͼ����ͼ6���Կ�����Ca(OH)2���ռ�ͬP2O5��Ӧ��������ΪCa3(PO4)2���������ռ�������ZnO��Fe2O3��MgO���Է�����ͬCaOһ�������ͬP2O5�ķ�Ӧ���ֱ��γ�������п��(Ca19Zn2(PO4)14��PDF��48-1196)����������(Ca9Fe(PO4)7��PDF:45-0338)��þ�ʰ���(Ca18Mg2H2(PO4)14��PDF: 70-2064)��
2.3 ���ռ�������ò�ֲ�����Ԫ�ط���
����ɨ��羵(SEM)��X��������(EDS)�Է�Ӧ�����ռ��ı��漰����Ԫ�ؽ��з������ڷ��������У�Ϊ���õ����ֲ�ͬԪ�������ռ�����ķֲ�״����ʹ�ñ�ɢ����ӳ���
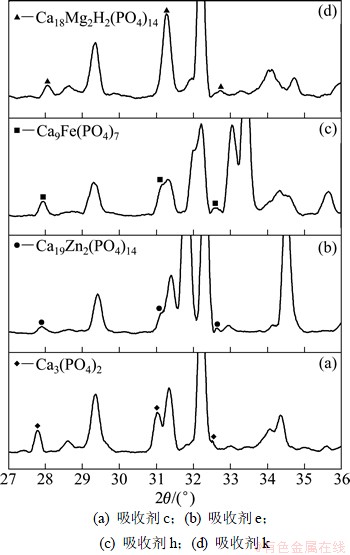
ͼ6 ��ͬ���ռ���Ӧ���XRD�ֲ��Ŵ�ͼ
Fig. 6 Local microscope XRD patterns of different sorbents after reaction
ͼ7��ʾΪCa(OH)2���ռ���Ӧ60 min��120 min��SEM��ɢ�������

ͼ7 Ca(OH)2���ռ���Ӧ60 min��120 min��ɢ�������
Fig. 7 Back-scattering electron images of Ca(OH)2 sorbent reaction for 60 min and 120 min
ͼ7������1~5��EDSԪ�ط������3��ʾ��
��ͼ7���Կ���������Ӧ60 min������ռ��������γ���ֱ��Ϊ2~4 ��m�ľ���������������ŷ�Ӧʱ����ӳ���������������ռ����������ࣻ����Ӧ����120 min�����ռ����沼���˾������������������бȽϹ����ܡ�
��3 Ca(OH)2���ռ�����EDSԪ�ط���(��������)
Table 3 EDS elemental analysis of Ca(OH)2 sorbent surface %
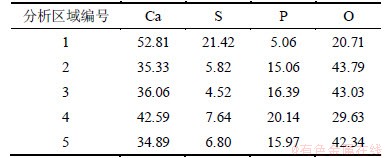
�Ծ�������ͷǾ��������Ԫ�ط������Կ���(����3)���ھ��������CaԪ�ظ�����ͬPԪ�ؽ�ϣ�ʹ�þ��������P����Զ����S���������ڷǾ��������CaԪ���������ͬS������Ӧ��
ͼ8��ʾΪ����ZnO��Fe2O3���ռ���Ӧ60 min��90 min��SEM��ɢ�������
ͼ8������6~11��EDSԪ�ط������4��ʾ��
��ͼ8(c)���Կ���������ZnO�����ռ���Ӧ60 min�������ռ�������γ����ڶ�ľ��������ͬʱEDS��Ԫ�ط�����������������P����Ϊ12.99%~18.72%����˵��ZnO������Լӿ츻��PԪ�ؾ������γɡ����Ա�ͼ7���Կ�������δ�������Ӽ������ռ���ȣ��������������м�Ϊ���ܣ�����ʿ�״�ֲ���ͬʱ��ͼ8(c)�к��ѿ�����С��϶�Ĵ��ڣ��������ֹ��SO2��P2O5���������ռ��ڲ���ɢ���з�Ӧ��ͬʱ���2.1�ڵķ������������ZnO�����ռ���Ӧ60 min���뵥һ��Ca(OH)2���ռ���ȣ������ȥ���ʻ���һ�£����ڳ���������ȴ������SO2��������Ϊ���ռ������γɵ�Ca19Zn2(PO4)14����������ռ������γ�Ӳ�ǣ����������ռ�������ĥ������飬����С�������ռ����γɡ�

ͼ8 ����ZnO��Fe2O3���ռ���Ӧ60 min��90 min��ɢ�������
Fig. 8 Back-scattering electron images of sorbent promoted by ZnO, Fe2O3 reaction for 60 min and 120 min
��4 ����ZnO, Fe2O3���ռ�����EDSԪ�ط���(��������)
Table 4 EDS elemental analysis of Ca(OH)2 sorbent promoted by ZnO, Fe2O3 surface %
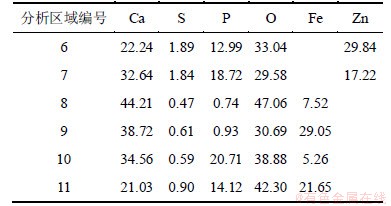
��ͼ8(d)����4������8��9��Ԫ�ط������Կ���������Fe2O3�����ռ��ڷ�Ӧ60 min��������û���γɺ�P�϶�ľ��������ȡ����֮����2�����ʣ�һ��ΪCaO(����8)��һ��ΪCa2Fe2O5(����9)�� P��S�ڿ�������ķֲ�û�й��ɡ�������Ӧ����90 min��������Ѹ���γ��˴����ľ����������������P����Ϊ14.21%~20.71%��������ò������ZnO�����ռ����ơ����2.1�ڵķ�����������Է��֣���Ӧ������Ca2Fe2O5�п��ܻ�ٽ���P�ᾧ���������ɣ��Ӷ�ʹP2O5��ȥ���ʵõ�����ߣ���������һ����ľ���ԭ���д���һ�����о���
ͼ9��ʾΪ����MgO���ռ���Ӧ60 min��120 min��SEM��ɢ�������
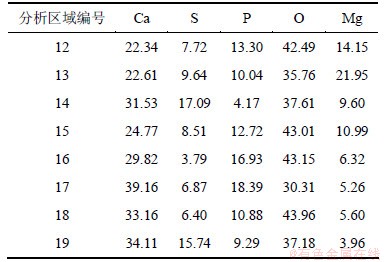
ͼ9������12~19��EDSԪ�ط������5��ʾ��
��ͼ9�ͱ�5���Կ�����������MgO�����ռ��ڷ�Ӧ����60 min�����ռ�����Ҳ�γ��˴�������P�ľ����������������ZnO��Fe2O3����ͬ���ǣ��侧��������С���Ҿ������������в��������ɡ�ͬʱ���ռ����������Ե�С��϶���ڣ���Ӧ����120 min�������������������ߣ������ռ�������òû�з������Ըı䡣��˵�������ռ�������MgO�������Դٽ�������������γɣ����P2O5��ȥ���ʣ�ͬʱʹ���γɵIJ���㲻�ܽ������ӣ��������ռ������������ɣ�SO2��P2O5���Լ��������ռ��ڲ���ɢ���з�Ӧ[15]���Ӷ�ͬʱ��������ռ���P��S��ȥ���ʡ�

ͼ9 ����MgO���ռ���Ӧ60 min��120 min��ɢ�������
Fig. 9 Back-scattering electron image of sorbent promoted by MgO reaction for 60 min and 120 min
��5 ����MgO���ռ�����EDSԪ�ط���(��������)
Table 5 EDS elemental analysis of Ca(OH)2 sorbent promoted by MgO surface %
3 ����
(1) �����ռ�������ZnO��Fe2O3��MgO������CaOһ�������ͬP2O5�ķ�Ӧ���ֱ��γ�������п�ơ��������ƺ�þ�ʰ��ơ�
(2) ����ZnO�����ռ��������ռ������Ѹ���γ�һ�����ܵ�����п�Ʋ㣬��ֹ��SO2��P2O5���������ռ��ڲ���ɢ��ͬʱ�����������ռ�������ĥ������飬�������ռ�Ѹ��ʧ�
(3) ����Fe2O3�����ռ����ڷ�Ӧ���ڶԹ�����û������Ӱ�죻�ڷ�Ӧ���ڣ�����Ca2Fe2O5�����ɣ������˴�����ͬSO2��Ӧ��CaO������SO2ȥ���ʵĽ��͡�ͬʱCa2Fe2O5 ���������ܴٽ���������������ɣ����P2O5��ȥ���ʡ�
(4) ����MgO�����ռ������Դٽ�������������γɣ�ͬʱʹ���γɵIJ���㲻�ܽ������ӣ��������ռ������������ɣ��Ӷ�����˶�SO2��P2O5��ȥ���ʡ�
�ο����ף�
[1] 2010��2011���й���������ҵ�о�����[R]. ����: ˮ��ľ���о�����, 2011: 7-8.
2010��2011 China phosphorite and phosphorous chemical industry report[R]. Beijing: Research in China, 2011: 7-8.
[2] WANG Zhonghua, JIANG Ming, NING Ping, et al. Thermodynamic modeling and gaseous pollution prediction of yellow phosphorus production[J]. Ind Eng Chem Res, 2011, 50: 12194-12202.
[3] ������, ����. ȼ����¯β����������¸�ʴ��ԭ��Ԥ����ʩ[J]. ұ����, 2007(4): 51-54.
HAN Mingjie, LIU Jinjing. Causes of low-temperature Corrosion of Gas-fired Boiler End and preventive measure[J]. Metallurgical Power, 2007(4): 51-54.
[4] �κ���. ���й�����ҵ��չ��˼��[M]. ����: ��ѧ��ҵ������, 2007: 19-21.
HE Haoming. Phosphate industry development in China[M]. Beijing: Chemical Industry Press, 2007: 19-21.
[5] Ԭ��ɽ, �����, ������, ��. ����һ�廯ȼú���Ӽ���ȼ���й��������о�[J]. ȼ�ϻ�ѧѧ��, 2002, 30(1): 36-40.
YUAN Zhongshan, WU Diyong, WANG Shudong, et al. Study on sulfur retention of integrated additive during coal combustion[J]. Journal of Fuel Chemistry and Technology, 2002, 30(1): 36-40.
[6] Abbasion J, Rehmat A. Sulfation of partially calcium-base sorbent[J]. Ind Eng Chem Res, 1991, 30(6): 1990-1995.
[7] �Ż�, ١����, ������, ��. ʹ�����Ӽ����ʸƻ������[J]. ����ѧ��, 2006, 57(2): 385-389.
ZHANG Hu, TONG Huiling, DONG Shanning, et al. Effect of additives on preparation and use of calcium sorbent for SO2 removal[J]. Journal of Chemical Industry and Engineering(China), 2006, 57(2): 385-389.
[8] Prasannan P C. A model for gas solid reactions with structure changes in the presence of insert solid[J]. Chem Eng Sci, 1985, 40: 1251-1261.
[9] Davini P, De Gennaro M, Sisto B. An investigation of the influence of sodium chloride in the desulphurization properties of limestone[J]. Fuel, 1992, 71: 831-834.
[10] ����, ���ػ�, ��ƽ, ��. ������ȼ�ջ���β��������Ca(OH)2�Ĺ�������[J]. ���ϴ�ѧѧ��: ��Ȼ��ѧ��, 2013, 44(2): 835-842.
WANG Lei, WANG Zhonghua, NING Ping, et al. Phosphorus-fixation by hydrated lime in fluidized bed combustion of yellow phosphorus tail gas[J]. Journal of Central South University: Science and Technology, 2013, 44(2): 835-842..
[11] ����, ���ػ�, ��ƽ, ��. Ca(OH)2��������Ĺ���������[J]. �㽭��ѧѧ��: ���̰�, 2013, 47(5): 874-882.
WANG Lei, WANG Zhonghua, NING Ping, et al. Simultaneously capture phosphorus pentoxide and sulfur dioxide process using Ca(OH)2/clays sorbent[J]. Journal of Zhejiang University: Engineering Science, 2013, 47(5): 874-882.
[12] �߷�ϼ, ������, ������, ��. �ƻ�����������ʵIJⶨ����[J]. ������Ⱦ�����, 2000, 22(4): 44-46.
GAO Fengxia, CUI Weidong, CUI Yihong et al. Analysis method of SO2 capture of calcium based sorbents[J]. Environmental Pollution and Control, 2000, 22(4): 44-46.
[13] ����, ·����, ������, ��. ʯ��ʯ��������Ӧ���Ե�ģ���о�[J]. ������ѧѧ��, 2001, 21(2): 172-177.
LIU Ni, LU Chunmei, LOU Zhongyang, et al. Model on desulfurization characteristic of limestone particles[J]��Acta Scientiae Circumstantiae, 2001, 21(2): 172-177.
[14] Shemwell B, Atal A, Levendis Y A, et al. A laboratory investigation on combined in-furnace sorbent injection and hot flue-gas filtration to simultaneously capture SO2, NOx, HCl and particulate emissions[J]. Environ Sci Technol, 2000, 34(22): 4855-4866.
[15] ���, ������, ����ƽ. CaO����Ӧ�����о���չ[J]. ȼ�ϻ�ѧѧ��, 2003, 31(1): 92-96.
YANG Haibo, WU Zenghua, QIU Xinping. Development of mechanism of CaO sulfation reaction[J]. Journal of Fuel Chemistry and Technology, 2003, 31(1): 92-96.
(�༭ ����ƽ)
�ո����ڣ�2012-08-31�������ڣ�2012-12-10
������Ŀ�����Ҹ����о���չ�ƻ�(��863���ƻ�)��Ŀ(2008AA062602)������ʡ��Ȼ��ѧ����������Ŀ(14051184)
ͨ�����ߣ����ػ�(1957-), Ů�����������ˣ���ʿ���´�����Ⱦ�о����绰��15877925068��E-mail��zhonghuakm@googlemail.com
ժҪ������������Ԥ��ȼ�ջ���β��, ��ZnO��Fe2O3��MgO��Ϊ���Ӽ�����Ca(OH)2�����ƻ���β������Ϊ1 m3/h����������Ϊ3.6 m3/h��ʹ¯���¶ȱ�����960~980 �棬���첻ͬ���Ӽ���Ca(OH)2���������õ�Ӱ�죬�����ռ�����XRD��SEM��EDS�����������Ԫ�ط������о����������ZnO���Ӽ���ʹ���ռ������γ�һ�����ܵ�Ca19Zn2(PO4)14���������ռ��ڶ�ʱ����ʧ�Fe2O3���Ӽ���ͬCaO��Ӧ�γ�Ca2Fe2O5������SO2��ȥ���ʣ���Ca2Fe2O5�����ɻ�ʹP2O5��ȥ������ߡ�MgO���Ӽ��ɴٽ�SO2��P2O5���������ռ����е���ɢ���ӿ캬����������γɣ��Ӷ�������ռ���SO2��P2O5��ȥ���ʡ���120 min�ķ�Ӧʱ���ڣ�MgO������Ϊ25%ʱ�����ռ���SO2ȥ����ƽ�����7.5%��P2O5��ȥ����ƽ�����19.5%��
[1] 2010��2011���й���������ҵ�о�����[R]. ����: ˮ��ľ���о�����, 2011: 7-8.
[3] ������, ����. ȼ����¯β����������¸�ʴ��ԭ��Ԥ����ʩ[J]. ұ����, 2007(4): 51-54.
[4] �κ���. ���й�����ҵ��չ��˼��[M]. ����: ��ѧ��ҵ������, 2007: 19-21.
[5] Ԭ��ɽ, �����, ������, ��. ����һ�廯ȼú���Ӽ���ȼ���й��������о�[J]. ȼ�ϻ�ѧѧ��, 2002, 30(1): 36-40.
[7] �Ż�, ١����, ������, ��. ʹ�����Ӽ����ʸƻ������[J]. ����ѧ��, 2006, 57(2): 385-389.
[11] ����, ���ػ�, ��ƽ, ��. Ca(OH)2��������Ĺ���������[J]. �㽭��ѧѧ��: ���̰�, 2013, 47(5): 874-882.
[12] �߷�ϼ, ������, ������, ��. �ƻ�����������ʵIJⶨ����[J]. ������Ⱦ�����, 2000, 22(4): 44-46.
[13] ����, ·����, ������, ��. ʯ��ʯ��������Ӧ���Ե�ģ���о�[J]. ������ѧѧ��, 2001, 21(2): 172-177.
[15] ���, ������, ����ƽ. CaO����Ӧ�����о���չ[J]. ȼ�ϻ�ѧѧ��, 2003, 31(1): 92-96.


