�ǻ�ˮ���������Ͻ�Ϳ��ṹ���绯ѧ���ܵ�Ӱ��
�κ���, ���콭, �ܿƳ�
(���ϴ�ѧ ��ĩұ������ص�ʵ����, ��ɳ 410083)
ժ Ҫ��
������Ϊ��Դ�� �ǻ�ˮ����Ϊ���Լ�, ���øĽ���Wattԡ��ϵ������Ʊ���-��Ͻ�Ϳ��缫, ��SEM�۲�Ϳ�������ò, XRD����Ϳ��ṹ�������, �绯ѧ���Է�������Ϳ��ĵ绯ѧ��Ϊ�� �������, �ǻ�ˮ�����ڵ���������мȴٽ��˾��˵��γ�, ���谭�˾����ij���, ����Ni-S������ľ���ϸ���� �Ǿ�̬���̶Ⱥ���������ߡ� ���Ʊ���Ni-S�Ͻ�Ϳ����нϺõĸ�����, ���ڼ���ˮ���ʱ�нϸߵ�������ԡ� ����Һ�лǻ�ˮ����Ũ��Ϊ5g/Lʱ, Ni-S�Ͻ�Ʋ㸽����������19MPa, �������λ����Լ13mV��
�ؼ���: �ǻ�ˮ����; Ni-S������; �绯ѧ����; ������ ��ͼ�����: O646.54
���ױ�ʶ��: A
Effect of sulphosalicylic acid on structures and electrochemical properties of nickel sulphur alloy coatings
HE Han-wei, LIU Hong-jiang, ZHOU Ke-chao
(State Key Laboratory of Powder Metallurgy, Central South University, Changsha 410083, China)
Abstract: Nickel-sulphur alloy coating electrodes were prepared on the nickel substrates by electrodeposition method in a modified Watts using thiourea (TU) and sulphosalicylic acid as sulphur source and modifier, respectively. Adsorption effect of sulphosalicylic acid on the electrochemical activities, grain sizes, textures and sulphur contents of Ni-S deposits were studied by means of electrochemical methods, SEM and X-ray diffraction. The results show that the sulphosalicylic acid accelerates the nucleation processes and hinders grain growth. The Ni-S deposits obtained from bath containing sulphosalicylic have higher sulphur contents, obvious amorphous textures and much smaller grain sizes than those from the bath without additive. Ni-S alloys as a cathode materials of alkaline water electrolysis have higher hydrogen evolution activities and better adhesion. The adhesion increases with the increase of sulphosalicylic acid concentration, and reaches 19MPa at 5g/L sulphosalicyclic acid. At the same time, the hydrogen evolution overpotential is the lowest at 5g/L sulphosalicylic acid, which is 13mV lower than that of the bath without additive.
Key words: sulphosalicylic acid; Ni-S deposits; electrochemical activity; adhesion
���ˮ������һ����Ҫ�ļ����� ��ҵˮ����ͨ�����������缫, ���ҺΪ6~9mol/L KOH��Һ, �¶�Ϊ60~80��[1]�� ����ܺĴ����������λ�й�, ���ߵ��������λ���ص����������ֵ缫���ϵ�Ӧ�á�
Ϊ�˽����ܺ�, ���ⷴӦ�缫���ϵõ�����㷺���о��� ������, �о������ĵ缫����Ϊ���� �����Ͻ��仯����[2]�� ��������������, ���ڲ��ô����缫, ��Ϊ�����ֳ�һ�ֺܸߵ�ԭʼ�������[3]�� Ȼ��, �ڼ���ˮ�����������ʱ, ���ᱻ�ۻ���ʧȥ�������[4-7], �Ӷ�ʹ�������λ����, �ܺ����� ���ֶۻ����ÿ���ͨ����ijһ�̶���λ�ĵ�����ʧ��ijһ�㶨�������������λ�����ӵõ�֤ʵ�� �����Ͻ�缫��һ�ֱȵ��������������������ԵIJ���, ���ͽ϶ࡣ Ŀǰ��ҵ��Ӧ�����ļ���ˮ�������ĵ缫ΪRaney-Ni�缫, ���õ缫һֱ����ǿ�ȼ���λ�ȶ��Ե����⡣ ���������Ͻ�缫, ����Ͻ���ڼ���ˮ�����һ�ֺܺõ���������[8]�� Hydro��[9] ��һ���õ���������ڶ��C/Ni�������Ʊ����˵绯ѧ���Էdz��ߵ�����缫�� ��25%��KOH��Һ��, ���¶�Ϊ80�桢 �������ܶ�Ϊ100mA/cm2ʱ, �������λ��6������ʼ��ά����60~110mV�� �õ缫���ڲ��ö��C/Ni����, ��Ȼ�ܼ������ߵ缫�����, ���������λ, ��������ǿ�Ȳ���, ������ִ���ѹ����ˮ����������ʹ���������ѡ� Ϊ������ǿ�Ⱥͽ��ͳɱ�, Ҳ�в����Ե�̼��Ϊ���������Ͻ�Ϳ��缫[8-10]�� �Ա���̼�ְ�Ϊ������Ȼ���Խ��͵缫���Ʊ��ɱ������ӵ缫���ϵı���ǿ��, ����϶�ܶȲ���, ���������������Լ����ı�������ܵ�һ��������, �ﲻ��Ԥ�ڵ�Ч��; ������Ϳ��ĺ��һ��Լ20~30��m, ������Ϊ18%~25%, Ϊ���ݶȽṹ, Ӧ���ϴ�, ��ʹ�ù��������ڻ��Բ������䡢 ������� ����, �Ӷ�Ӱ����ʹ�������� Ŀǰ, �ǻ�ˮ�����ڱ��洦�������е�Ӧ�÷dz��㷺, �ر������ڵ�����Ӽ��ɸ��ƶƲ����ѧ���ܵȡ� �ǻ�ˮ����������˫�����������, ���Ի��Ӧ���͡� ��չ�Ժõ�˫�������; �������Ͻ����, ����ǻ�ˮ����, ����߶Ʋ������Ͻ��������; �������������������������Ը��ƶƲ�����, �ر���������ѧ����[11]��
Ϊ�˽������Ϳ�㸽����� �������ʹ�������̵�ȱ��, ��������ͨ����Wattԡ�����ӻǻ�ˮ����, ���õ�����ķ�������Ƭ�������Ʊ������нϴ�ı������������ѧ���ܵ�����Ϳ��缫, ���ڼ���ˮ��⡣ ��Wattԡ������������Դ, ������̬�������߲�����������Ϳ������绯ѧ����, ��XRD ��SEM��������Ϳ�����ò���ṹ, ��EDX��������Ϳ���е�������
1 ʵ��
1.1 ����Ϳ��缫���Ʊ�
�����Һ�䷽Ϊ�Ľ���Wattԡ, �ں�0.1~1.0kg/m3�Ǿ�, 50~300kg/m3NiSO4��6H2O, 10~100kg/m3NaCl, �ǻ�ˮ��������, 10~100kg/m3H3BO3��10~250kg/m3����(TU)�� �ڵ�����Ƭ����(20mm��20mm��0.5mm, �û�����֬��Ϳ��һ��)��ʹ����Ƭ������������Ʊ�����Ͻ�Ϳ�㡣 �����ʱ��Ϊ60min, pHֵΪ4.0~4.3, ���������ܶ�Ϊ10~30mA/cm2, �¶�Ϊ30~45�档
1.2 ����Ϳ�����֯�����븽��������
����Ϳ����������EDX (KYKY-2800LV)����; XRD(D/AX 2550, Japan)��SEM(KYKY-2800LV)�ֱ�������������Ϳ��Ľṹ����ò�� ����������������������ʵ�鷽��, ���Ʊ��õ�����Ϳ��缫��ǿ��������֬���������ճ, ���¹̻�24h��, ��������һ�˵�������������������(LJ-3000A�ͻ�еʽ���������)�����쿨ͷ���ͨ��������ʵ��, ��������Ϊ1mm/min��
1.3 �绯ѧ����
��CHI660b���λ�Dz���Ϳ��ĵ绯ѧ����, Ni-S�Ͻ�Ϊ�����缫�� �αȵ缫Ϊ����Hg/Hg2Cl2, ���������Ϊ�Ե缫, ��������ŷķ���������Զ�У������ʱ��Һ�ĵ�λ���� ���ҺΪ30%KOH(��������)ˮ��Һ, �ⶨ�������������ߡ� ͬʱ����Ƭ����(��Ԥ�������͡� �⡢ ��ϴ)�������缫, ���Һ��������Һ�䷽��ͬ, �αȵ缫Ϊ����Hg/Hg2Cl2�缫, ���������Ϊ�Ե缫, ��CHI660b�绯ѧ�ۺϲ�����(����CH Instrument ��˾)����ѭ������ʵ����迹����, ɨ������Ϊ0.1V/s, ������Ƶ��Ϊ1kHz, ���Ϊ5mV��
2 ���������
2.1 �ǻ�ˮ�����Ϳ����������������Ӱ��
ͼ1��ʾΪ�ǻ�ˮ�����������ԶƲ�������Ӱ�졣 ��ͼ1�пɿ���, ������ǻ�ˮ��������

ͼ1 �ǻ�ˮ�����Ϳ��������Ӱ��
Fig.1 Effect of sulphosalicylic acid concentration on sulfur content of Ni-S coatings
�������Ӷ�����, ��ˮ�����������ﵽ8.0g/Lʱ, ���������ȶ��� ����Wen��[12]���о�, ��Ni-Sϵ��Һ��, Ni2+��CS(NH2)2��Ni[CS(NH2)2]2+ ��Ni[CS(NH2)2]2+2����������ʽ���ڡ� ������ǻ�ˮ����ʱ, Ni2+��������γ�������Ӻ�, ������Ч�����Ӷ�Һ��������ӵ�����, ��������������ǿ�ͺϽ�Ʋ���S����������; ���ǻ�ˮ����������Ϊ8.0g/Lʱ, �������ڵ缫����ǻ�ˮ��������������������ʼ�ﵽƽ��ʱ, �Ͻ�Ʋ���S������ʼ�����ȶ���
Ni-S����ı�����̬���串������������Ľ�������кܴ��Ӱ�졣 һ��Ni-S���������ȡ� ����, ���õ��ĶƲ�Ҳ�����ܡ� ����, ����Ϳ������ĵ�ճ����Ҳ����, ����ɢ�� ϡ���Ni-S��������ĵ�ճ����Ҳ�Ƚϵ͡� ͼ2��ʾΪ�ǻ�ˮ����Ũ�ȶԸ�������Ӱ�졣 ��ͼ2�п��Կ���, Ϳ��������ճ��������ǻ�ˮ���������������������, ��ˮ����Ũ�ȴﵽ5.0g/Lʱ, ճ�����ﵽ���(Ϊ19.5MPa), ������Լ12MPa�� Ȼ��ճ������ǻ�ˮ��������������������͡� �����Ӽ���Ϳ���δ�����Ӽ��õ��ĶƲ�����ĵĸ������д���ȵ���ߡ� �ɻǻ�ˮ�����Ni-S ����������û�����֪, �ǻ�ˮ�����ڵ���������мȴٽ��˾����γ�, ���谭�˾����ijɳ�, ���¶Ʋ����ϸС�� ��������, ������Ϳ��������ճ��������ߡ�

ͼ2 �ǻ�ˮ����Ũ�ȶԸ�������Ӱ��
Fig.2 Effect of sulphosalicylic acid concentrations on adhension force of Ni-S coatings
2.2 �ǻ�ˮ�����Ϳ��ṹ����ò��Ӱ��
2.2.1 Ni-S�������X�����������
ͼ3��ʾΪ�ڲ�ͬ�ǻ�ˮ������������Һ��Ni-S�������X���������ס� ��ͼ3�пɿ���, ���Ӽ���Һ�еõ���Ni-S�������X��������������, ����ײ����п���, ����Ϳ�����Ni-S������ķǾ�̬�ɷ֡� ���۶�Һ���Ƿ�����������Ӽ�, ����õ�Ni-S�������X�����������Ͼ�������Ni���������ṹ��Ӧ��(111)�� (200)��(220)�����ľ���������, ֻ�Ǹ������������ǿ����ʹ�����Ӽ���ͬ���������, ����ɳ�����֯���ı仯�� ��ͼ3���ɿ���, Ni-S������Ľ�ǿ���侧����(111)����, ������ǿ�����Ŷ�Һ�����Ӽ�������������ֲ�ͬ�̶ȵ��½�, �����������Ŀ����̶���������, �ҶƲ��зǾ�̬�̶�ҲԽ���ԡ� �ɴ˿ɼ�, ���Ӽ��ڵ缫�����������Ӱ����������ڵ缫����ĵ绯ѧ��ԭ���̡� һ����, �ǻ�ˮ�����ھ��д����Եij���Ni-S�����Ͽ��ܱ�������[H]��H2��ԭ, ����������ĵ����, ˮ��������ڳ�������, �����˶Ʋ������; ��һ����, �ǻ�ˮ��������Ƭ�缫��������, ռ����ԭ���缫����������ӵ�λ��, ���±������Ni2+���ӵ�����������, �����ڶƲ������������� ͬʱˮ����ҲӰ���ᾧ���̾���������, �Ӷ����³����㾧��ϸ�����ṹ�ı仯��

ͼ3 ��ͬ�ǻ�ˮ����Ũ����Ni-S�Ʋ��X����������
Fig.3 XRD patterns of Ni-S coatings with different sulphosalicylic acid concentrations
���������ߵĿ����̶�, ����Scherrer ��ʽ�������Ʒ��ƽ�������ߴ�, ���������1���С� ��ϸ�����������û���[13]��: ���Ӽ���ԭ�ӻ�����ڳ���������ʱ�����ھ��������Ļ��Ե���, ��Ч�������˾�������, �ٽ��˾��˵��γ�, ʹ�ó�����ᾧϸ���� �ɱ�1�ɿ���, Ni-S�����㾧���ߴ������Ӽ�Ũ�ȵ��������С, �ҵ����Ӽ�Ũ�ȴﵽ5.0g/Lʱ, �����ߴ�ı仯�����ȶ��� ��һ�������, ���Ӽ��ڵ缫�ϵ�����ʹ����������������, �����ھ��˵��γ�, ����������㾧���ߴ��С, ���������ﵽһ����ʱ, ���������Ӽ��������Ӷ���ϸ, �෴, �������ڹ�������Ӽ�, ʹ�缫�����������ӵ�Ũ�ȴ��, �����ھ����γ�, �����ٽ��˾���������, �ҽ�С�����ij�������нϸߵ��ܱ俹��, �Ӷ�ʹ����Ӳ����ߡ�
��1 ��ͬ�ǻ�ˮ����Ũ��ʱNi-S������ľ����ߴ�
Table 1 Grain size of Ni-S deposits with different sulphosalicylic acid concentration

2.2.2 Ni-S�������SEM��ò
ͼ4��ʾΪ��Һ�в�ͬ�ǻ�ˮ����Ũ����Ni-S�Ʋ�ı���SEM�� ��ͼ4�пɿ���, δ�ӻǻ�ˮ����ĶƲ㾧���ִ�, ���Żǻ�ˮ����Ũ�ȵ�����, �Ʋ㾧���ߴ�ϸ���� ��Ũ��Ϊ5.0g/Lʱ, �����ߴ��ϸС, �Ҿ��кܷḻ�ı��档 ��Ũ��Ϊ8.0g/Lʱ, �Ʋ㾧���ߴ��������� ����X��������ó��Ľ��һ�¡� ���ڻǻ�ˮ�����ڵ缫�ϵ������������γ�ϸ���Ʋ�, ����Ũ�ȴﵽһ��ʱ, �����ߴ粻��ϸ��, ������Ũ�ȵ������дֻ�������, ���������ڹ�������Ӽ������ڵ缫����, ʹ�缫�����������ӵ�Ũ�ȴ��, �����ھ����γɡ�
2.3 �ǻ�ˮ�����Ni-S ��������û�����Ӱ��
ͼ5��ʾΪ��Ƭ������Ni-S������ķ������ߡ� ��ͼ5�ɼ�, ����Һ�в����ڻǻ�ˮ����ʱ, ����������-0.625Vʱ��ʼѸ������; ����Һ�м���ǻ�ˮ�����, ���λ������-0.59V�� ����λ����ɨ��ʱ, ��CV���߷ֱ���-0.59V(���ӻǻ�ˮ����)��-0.625V(�ǻ�ˮ����)���µ�λ�����ֽϴ�ĵ���, �����ߵĵ�����ɨ���ѹ�ĸ��Ƴ��������ơ� ����ɨ����������Ӧ�ĵ�λ����ʱ, �ȸ���ɨ��ʱ�ĵ������������ӡ� �����������ᾧ�ɺ˻����й�, �����ڵ�λ����ɨ�����, ��Ƭ�����ϻ��ɺ���������, ��Ӧ�ĵ�ᾧ

ͼ4 ��ͬ�ǻ�ˮ����Ũ����Ni-S�Ʋ��SEM��
Fig.4 SEM images of Ni-S coatings with different sulphosalicylic acid concentrations
����δ�ܷ���, �ʵ����ӽ����㡣 ֻ�е��缫��λ�ﵽ�ɺ�����Ĺ���λ��, ���������������� ���ڵ�λ����ɨ���ڼ�, �����������ͬ, ���ھ�������ɨ��֮�����Ƭ�缫, ����漺�о��˴���, �Ӷ��ڽϵ͵Ĺ���λ�¾��ܹ����е�ᾧ����,������Ϊ�ϴ�ĵ����� ���ŵ��Һ�лǻ�ˮ����ļ���, �����������λ����, �����ǻ�ˮ����ٽ��˾��˵��γɡ�

ͼ5 ��Ƭ������Ni-SͿ���ѭ����������
Fig.5 Cyclic voltammogram curves of Ni-S coatings on nickel substrate with(a) and without(b) sulphosalicylic acid
�ǻ�ˮ���������������Ӱ��Ҳ�����迹��λ�仯��ϵ������֤�� ͼ6��ʾΪ��Ƭ������Ni-S��������迹����λ��ϵ�� ��ͼ6�ɿ���, ����ϵ�迹���λ�ı仯��ϵ��ͼ5�е������λ�ı仯�Ƕ�Ӧ��, ��δ��������ʱ, �迹�͵������������λ����, һ����������ij���, �迹�����½�, �������������� ����Һ�в����ڻǻ�ˮ����ʱ, ��λ����ɨ����-0.65Vʱ, �迹Ѹ�ٽ���, ������-1.45V��, �����λ�ĸ��ƶ��������� ����Һ�м���ǻ�ˮ�����, �����迹Ѹ���½�, ��λ������-0.61V������, ͬ���������ŵ�λ����, �迹�������������, ����-1.48V������ת�ۡ� ������ϱ仯��ԭ������������������ʿ��Ʋ����ת���йء� ���ڵ�λɨ�������, ���迹�ﵽ��Сֵ֮ǰ, Ũ�����������, ��Ҫ�Ե绯ѧ����Ϊ��, ��ʱ��λԽ��, �绯ѧ��Ӧ�迹ԽС, ����������λ������, ��ɢ����������Ϊ������λ, ���ճ�Ϊ�ٿز���, ��ʱWarberg�迹�㲻����������λ�����Ӷ����ӡ�

ͼ6 ��Ƭ������Ni-S��������迹�͵�λ�ı仯����
Fig.6 Change curves of impedance and potential for Ni-S coatings on nickel substrate with(a) and without(b) sulphosalicylic acid
��ͼ6���ɿ���, ���Һ���ǻ�ˮ����ʱ���迹���ڲ����ǻ�ˮ����ʱ���迹�� ���ڻǻ�ˮ��������Ƭ�缫��������, ռ����ԭ���缫����������ӵ�λ��, ���±�����������������Ľ���, �Ӷ��谭������ij����� �ǻ�ˮ���������������Ҫ��ͨ��Ӱ��绯ѧ���Ʋ����������, ��˵���ǻ�ˮ�����ڵ���������мȴٽ��˾����γ�, ���谭�˾����ijɳ�, ���, �ں��ǻ�ˮ����Ķ�Һ�еõ��ĶƲ�����Ƚ�ϸС, �Ʋ�Ƚ�����, ��X���������SEM�����Ľ��һ�¡�
2.4 �ǻ�ˮ���������Ϳ�������λ��Ӱ��
������ʵ�鷽���ⶨ��Ni-S�Ͻ�Ʋ�缫�����⼫������, ���⼫����ǻ�ˮ����Ũ�ȵı仯������ͼ7��ʾ�� ��ͼ7�ɿ���, Ni-S�Ͻ�Ʋ���������λ���ҺŨ�ȵ����������, ���ǻ�ˮ����Ũ��Ϊ8.0g/Lʱ, �Ʋ���������λ�����ȶ�, ������ǻ�ˮ����Ũ�ȶ��仯; ����Һ�лǻ�ˮ����Ũ��Ϊ5.0g/Lʱ, �ȶ�Һ��δ�ӻǻ�ˮ����ĶƲ��������λ��13mV���ҡ� ��������һ����, ���������缫�������ӵijߴ���ֱ�ӵĹ�ϵ, �缫�������ԽϸС, ������Խ�ḻ, ��Խ���������⡣ ��X���������SEM���������֪, ����Һ�лǻ�ˮ����Ũ��Ϊ5.0g/Lʱ, ���������С, ������ḻ; ��һ����, ����[14]��������[15]��Ϊ, �������Ʋ�Ļ��Աȵ������Ʋ�ĸ�, Ni-S�Ʋ�Ǿ�̬�̶�Խ��, ��������Ծ�Խ�á� ��������������X����������֪, ��ǻ�ˮ����Ũ�ȵ�����, ��������ʱ, �Ǿ����̶�Ҳ��֮����, ��������߶Ʋ�Ĵ����ԡ� ���, �ǻ�ˮ��������߶Ʋ�ĵ������, ����ѻǻ�ˮ����Ũ��Ϊ5.0g/L��
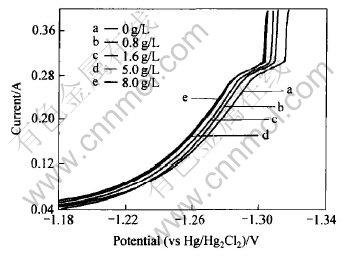
ͼ7 ��ͬ�ǻ�ˮ����Ũ��ʱNi-S�Ʋ�����⼫������
Fig.7 Polarization curves of Ni-S coatings with various concentrations
3 ����
1) ͨ��ѭ���������ͽ���-�迹���о��˻ǻ�ˮ�����Ni-S ����������û����� �ǻ�ˮ�����ڵ���������мȴٽ��˾��˵��γ�, ���谭�˾����ijɳ���
2) X���������ס� ����SEM�����������, �ǻ�ˮ����Գ����㾧��ϸ���� �������Ʋ�ṹ�кܴ�Ӱ�졣
3) ����Һ�лǻ�ˮ����Ũ��Ϊ5.0g/Lʱ, ���Ʊ���Ni-S�Ͻ�Ʋ���δ�����Ӽ���Ni-S�Ͻ�Ʋ����, ������������Լ12MPa, �������λ����Լ13mV��
REFERENCES
[1]Divisek J, Wendt H. Electrochemical hydrogen technologies: electrochemical production and combustion of hydrogen[M]. New York: Elsevier, 1990. 162-165.
[2]Paseka I. Hydrogen evolution reaction on amorphous Ni-P and Ni-S electrodes and the internal stress in a layer of these electrodes[J]. Electrochimica Acta, 2001, 47(6): 921-931.
[3]Miles M H, Kessel G, Lu P M T, et al. Effect of temperature on electrode kinetic parameters for hydrogen and oxygen evolution reactions on nickel electrodes in alkaline solutions[J]. J Electrochem Soc, 1976, 123(4): 332-336.
[4]Huot J Y, Brossard L. Time dependence of the hydrogen discharge at 70�� on nickel cathodes[J]. Int J Hydrogen Energy, 1987, 12(12): 821-830.
[5]Rommal H E G, Moran P J. Time-dependent energy efficiency losses at nickel cathodes in alkaline water electrolysis systems[J]. J Electrochem Soc, 1985, 132(5): 325-328.
[6]Rommal H E G, Moran P J. Role of absorbed hydrogen on the voltage-time behavior of nickel cathodes in hydrogen evolution[J]. J Electrochem Soc, 1988, 135(8): 343-345.
[7]Soares D M , Teschke O, Torriani I. Hydride effect on the kinetics of the hydrogen evolution reaction on nickel cathodes in alkaline media[J]. J Electrochem Soc, 1992, 139(7): 98-100.
[8]Hu C C , Wen T C. Effects of the nickel oxide on the hydrogen evolution and para-nitroaniline reduction at Ni-deposited graphite electrodes in NaOH[J]. Electrochimica Acta, 1998, 43(12): 1747-1756.
[9]Oslo N H. Electrolyte cell active cathode with low overvoltage[P]. Nederlands, 7801955. 1978-08-28.
[10]Han Q, Liu K, Chen J, et al. A study on the electrodeposited Ni-S alloys as hydrogen evolution reaction cathodes[J]. International Journal of Hydrogen Energy, 2003, 28(11): 1207 -1212.
[11]��ˮ��. �ǻ�ˮ�����ڵ�ƹ�ҵ�е�Ӧ��[J]. ���漼��, 1995, 24(4): 1-5.
WU Shui-qing. Application of sulphosalicylic acid in electroplating industry[J]. Surface Technology, 1995, 24(4): 1-5.
[12]Wen T C, Lin S M, Tsai J M. Preparation and research on Ni-NiS alloy electrode of hydrogen evolution reaction[J]. J Appl Electrochem, 1994, 24(6): 233-235.
[13]Watanabe T. �Ǿ�̬��Ʒ�����Ӧ��[M]. ��άƽ, �� ݶ, ��. ����: �������պ����ѧ������, 1992. 4-75.
Watanabe T. Technology and Application of Amorphous Electrodeposition[M]. YU Wei-ping, LI Di, tral. Beijing: Beihang University Publishing Com-pany, 1992. 4-75.
[14]����, ���ٽ�, κ����. �����Ni-S�Ͻ��������ⷴӦ[J]. ��Դ����, 2001, 25(6): 223-224.
DU Min, GAO Rong-jie, WEI Xu-jun. Hydrogen evolution reaction of Ni-S electrodeposited cathode[J]. Chinese Journal of Power Sources, 2001, 25(6): 223-224.
[15]����, �κ���, �ܿƳ�, ��. �����Ni-S�Ͻ�������Ӱ������[J]. ��ĩұ����Ͽ�ѧ�빤��, 2005, 10(1): 60-64.
LIU Fang, HE Han-wei, ZHOU Ke-chao, et al. Dependence of sulphur content during electrodeposition of Ni-S alloys[J]. Materials Science and Engineering of Powder Metallurgy, 2005, 10(1): 60-64.
������Ŀ: ���Ҹ����о���չ�ƻ�������Ŀ(2003AA305980)
�ո�����: 2005-07-15; ������: 2005-08-20
�����: �κ���(1964-), ��, ��ʿ, ����
ͨѶ����: �κ���; �绰: 0731-8836311; E-mail: hehanwei@163.com
[11]��ˮ��. �ǻ�ˮ�����ڵ�ƹ�ҵ�е�Ӧ��[J]. ���漼��, 1995, 24(4): 1-5.
[13]Watanabe T. �Ǿ�̬��Ʒ�����Ӧ��[M]. ��άƽ, �� ݶ, ��. ����: �������պ����ѧ������, 1992. 4-75.
[14]����, ���ٽ�, κ����. �����Ni-S�Ͻ��������ⷴӦ[J]. ��Դ����, 2001, 25(6): 223-224.
[15]����, �κ���, �ܿƳ�, ��. �����Ni-S�Ͻ�������Ӱ������[J]. ��ĩұ����Ͽ�ѧ�빤��, 2005, 10(1): 60-64.


