DOI��10.19476/j.ysxb.1004.0609.2018.08.21
�����ٺ�Һ������ķ�������չ���
���ֱ���֣�Žܣ���С��
(���ϴ�ѧ ұ���뻷��ѧԺ����ɳ 410083)
ժ Ҫ����ͭ�����ദ���еij����ٺ�ҺΪԭ�ϣ������������Ƴ����������������SO2��ԭ�õ��ڷۺͻ�ԭ�ں�Һ���ڻ�ԭ�ں�Һ�м����������Ƴ�������˵õ������飬���������м�������������Һ�����Ƶ������顣��������������������Ƶ��ڳ����ٺ�ҺpHΪ6����Ӧ�¶�20~25 �桢��Ӧʱ��Ϊ1 hʱ�������ٺ�Һ���ں�������ʷֱ�ﵽ99.91%��99.96%�������ٺ�Һ�õ��ij����������������������3 mol/L�����1.5 mol/L���������Ϊ2:1��H+Ũ��Ϊ3 mol/L����Ӧ�¶�Ϊ50 �棬��Ӧʱ��Ϊ2 h������ڵĽ����ʷֱ�Ϊ99.93%��98.21%���ڸ�������Ľ���Һ��ͨ��SO2��ԭ����SO2����Ϊ0.25 L/min����Ӧ�¶�Ϊ70 �桢��Ӧʱ��Ϊ50 minʱ���ڵĻ�ԭ��Ϊ96.59%����ԭ�ڷ����ں����ﵽ79.45%������麬����Ϊ0.003%��0.067%(��������)����SO2��ԭ�ں�Һ�м����������Ƶ�����ҺpHֵΪ2�����˺�õ������飻���������м���6 mol/L����������Һ����Һ�̱�Ϊ3:1����Ӧ�¶�Ϊ80 �桢��Ӧʱ��Ϊ2 hʱ����������������������麬���ﵽ93.80%��
�ؼ��ʣ��ڣ��飻���������ܣ���ԭ
���±�ţ�1004-0609(2018)-08-1660-09���� ��ͼ����ţ�TF803.2���� ���ױ�־�룺A
�ڡ�����кܶ����������ܣ���ұ�𡢹������ϡ����䡢̫���ܡ�������ҽҩ��������й㷺��;[1-3]�������������վ����������ڡ������Դ�����ޣ��ڡ���Ļ��վ�����Ҫ��ֵ�������ڿ�����Դ�٣�ֱ�Ӵӿ�������ȡ���о����٣�����Ҫ��Դ��ͭ�������Ǧ�����ࡣ�����������������ɲ��ÿ�ⷨ�ӵ�Ʒλ�Ķ�����������ȡ��[4]��ͭ��Ǧұ���ĸ�����Ҳ����ȡ�����Ҫԭ�ϡ�ͭ�������Ǧ�������Ǻ���������ϣ������������л����ں���ķ�����ԭ�ϳɷֲ�ͬ�����죬��������Ҫ���õķ����м��ܵ���ͭ�ۻ�ԭ����[5-7]�����ù����м����-��������-�������������-��ԭ-�û���[8-11]����������Ҫ���û��գ���������Ŀ����ϴ�����С��ģ������Ļ��ա��Ӻ��������Һ�л�������Ĵ��������϶࣬���ܼ���ȡ����SO2��ԭ�������������û�����[12]����Щ�����ں���ķ������������ɱ��ߡ����̷�����ȱ�㡣ͭ�����ྭ���Ȼ��ֽ�-��ԭ��-п�ۻ�ԭ���ٵõ��ij����ٺ�Һ�к���һ�������ڡ��飬�߱�һ���Ļ��ռ�ֵ����ҵ�ϴ��������ٺ�Һһ�����NaOH�������������ļ��ܽ�õ�Na2TeO3��Һ��Na2TeO3��Һ�����������������ᴿ����Ʊ������ڣ��ù������̷����������ɱ���[14-15]������������ͭ������ij����ٺ�ҺΪԭ�ϣ�������������ʹ�����ٺ�Һ���ں��鹲���������û����ܽ��ں��飬�ں���ֱ��1.40 g/L��6.72 g/L��ߵ�12.05 g/L��56.33 g/L������Һ���ں���ֱ���8.59����8.39����Ȼ����ö�������ԭʹ������룬�������Ƴ��������ȷֱ�õ�����Ϊ79.45%���ڷۺʹ���Ϊ93.80%�����飬�ں����ܻ����ʷֱ�ﵽ96.44%��93.41%[16]���ù�����������������ڡ��鷽����Ⱦ��и���Ч���á������ʸߡ����ռ��ʺ��ڹ�ҵ������
1 ʵ��
1.1 ʵ��ԭ��
ʵ��ԭ��Ϊͭ�������Ȼ��ֽ��п���û����ٺ�õ��ij����ٺ�Һ�� pHֵΪ0.02����ICP�����ɷ����1���С�
�ɱ�1��֪�������ٺ�Һ����Ҫ�ɷ�Ϊ�ڡ�����飬�京���ֱ�Ϊ1402 mg/L��6731 mg/L��1588 mg/L��
��1 �����ٺ�ҺԪ�غ���
Table 1 Element components of precipitating platinum and palladium solution (mg/L)

1.2 ʵ�鲽��
ȡһ�����ij����ٺ�Һ��������ƿ�У��������貢���ȣ�����Ũ��Ϊ2.5 mol/L����������Һ����pH����Ӧʱ��Ϊ1 h�����ˡ���ɵõ���������ȡ��������������������ƿ�У���Һ�̱�(mL:g)Ϊ6:1��������Ļ���������ᣬ�������裬��һ���ķ�Ӧ�¶��뷴Ӧʱ���£���Ӧ��ɺ���˵õ���������Ľ���Һ��
���õ��ĸ�������Ľ���Һ��������ƿ�м��Ȳ��������裬ͨ��SO2����һ���¶��·�Ӧ����ˡ�ϴ�Ӳ���ɵõ��ڷۺͻ�ԭ�ں�Һ������ԭ�ں�Һ��������ƿ�У�����Ũ��Ϊ5 mol/L������������Һ����pHֵ���ڷ�Ӧʱ��Ϊ2 h����Ӧ�¶�Ϊ50 �������³��������˵õ������飬�����õ���������������Ⱥ���ˡ���ɵõ����������顣
1.3 ��������
��������ʵ����̣������乤��������ͼ1��ʾ��
1.4 ��������
���������ȵ�Ԫ�ع�˾��Intrepid II XSP�͵����ϵ������巢�������(ICP)������Һ�ɷ֣�X����ӫ�������(XRF)���붨�������������ʳɷ֣��ձ���ѧD/max-TTR III��X����������(XRD)���������������࣬�ձ�������ʽ����JSM-6300��ɨ��羵(SEM)�۲�����������ò��
2 ���������
�����ٺ�Һ�л������飬����Ҫ�о��ں���ķ���ͻ��չ����⣬���ڳ����ٺ�Һ����Ϊ��Ҫ�ɷ�֮һ�������ij��������Ҳ�������о���
2.1 pHֵ�Գ����ٺ�Һ���顢�ڡ�������ʵ�Ӱ��
��200 mL�����ٺ�Һ��������ƿ�У�������������Ũ��Ϊ2.5 mol/L������������Һ����pHֵ����Ӧ�¶�Ϊ25 �棬��Ӧʱ��Ϊ1 h�� pHֵ�Գ����ٺ�Һ���顢�ڡ�������ʵ�Ӱ����ͼ2��ʾ��
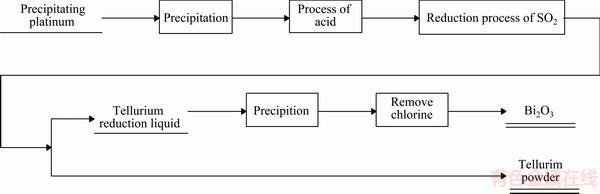
ͼ1 �����ٺ�Һ����ķ�������չ�������ͼ
Fig. 1 Separation and recovery process of tellurium and bismuth flow diagram from precipitating platinum and palladium solution
��ͼ2��֪��pHֵ��2���ӵ�13ʱ��������ʻ������䡣pHֵΪ2~6ʱ���ڵij���������pHֵ�����Ӷ����ӣ�pHֵΪ6~9ʱ�ڵij���������pHֵ�����ӻ������䣬pHֵ��9ʱ�ڵij���������pHֵ�����Ӷ����͡�������ˮ�������������ڳ���������������������ʱ��ʹ�������ڳ��������ܽ�����Na2TeO3������ڵij������½�[15]��pHֵΪ2~9ʱ����ij���������pHֵ�����Ӷ����ӣ�pHֵ��9ʱ��ij���������pHֵ�����Ӷ����ͣ�����������������ơ������ٺ�Һ�У�����Ҫ�� As(��)��̬���ڣ���H3AsO4��H2AsO4-��HAsO42- ��AsO43-����̬����[17]������������������⣬�������ڳ�������������ij�����Ҫ�������������ڶ���ĸ�����̬�������������ã���pHֵ����9ʱ�������������ܽ�������ʷ����½�������ط�Ӧ���£�
BiCl3+3NaOH=Bi(OH)3��+3NaCl��������������(1)
H2TeCl6+6NaOH=Te(OH)4��+6NaCl+2H2O (2)
Te(OH)4+2NaOH=Na2TeO3+3H2O (3)
Bi3++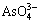 =BiAsO4�� (4)
=BiAsO4�� (4)
��pHֵΪ6~9ʱ���ں���ij����ʶ��ﵽ99.10%��As�����ʴ�33.53%���ӵ�53.21%��ȡ5 L�����ٺ�Һ���зŴ�ʵ�飬pHֵ�Գ����ٺ�Һ���顢�ڡ�������ʵ�Ӱ����ͼ3��ʾ��
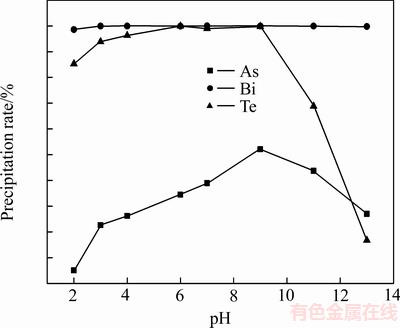
ͼ2 pHֵ���顢�ڡ�������ʵ�Ӱ��
Fig. 2 Effects of pH value on precipitation rate of As��Te and Bi
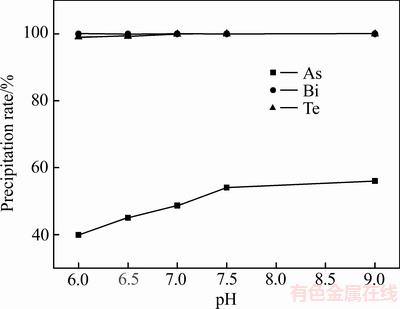
ͼ3 �Ŵ�ʵ��pHֵ���顢�ڡ�������ʵ�Ӱ��
Fig. 3 Effects of amplification experiment pH value on precipitation rate of As��Te and Bi
��ͼ3��֪����pHֵ��6���ӵ�7ʱ���ڳ����ʴ�99.08%���ӵ�99.91%��������ʴ�99.92%���ӵ�99.96%��������ʴ�39.99%���ӵ�48.63%��pHֵ��������ʱ���ں���ij����ʲ��䣬��������ʼ������ӣ��Ŵ�ʵ������Сʵ����һ�¡�ʵ��ȡpHֵΪ7�ij���������60����ո��XRDʵ������ͼ4��ʾ���������ɷ����2���С�
��ͼ4��֪������60 ����ո�����������������������ڡ��ɱ�2��֪������������Ҫ�����顢�ڡ����п��
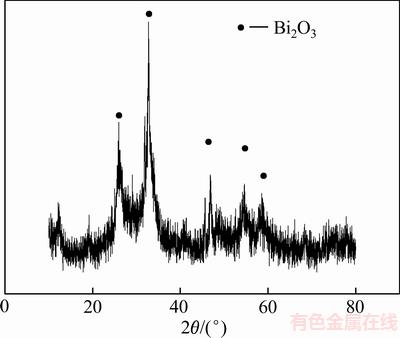
ͼ4 pH=7ʱ��������XRD��
Fig. 4 XRD patterns of precipitate at pH=7
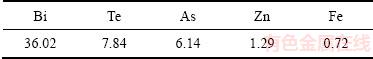
��2 ��������ѧ�ɷ�(����������%)
Table 2 Chemical components of precipitate (mass fraction, %)
2.2 ����������ܽ�������ĸ���
2.2.1 ����Ũ�ȶ������ܽ��ʵ�Ӱ��
ȡ����������100 g����Һ�̱�(mL:g)Ϊ6:1��������600 mL���������裬����Ӧ�¶�Ϊ60 �桢��Ӧʱ��Ϊ0.5 hʱ������Ũ�ȶ�����������ʵ�Ӱ����ͼ5��ʾ��
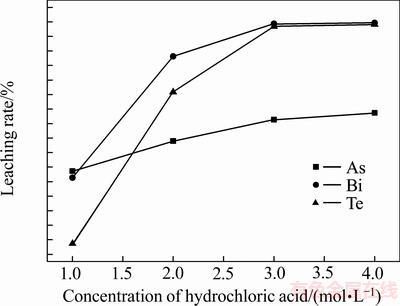
ͼ5 ����Ũ�ȶԳ��������顢�ڡ�������ʵ�Ӱ��
Fig. 5 Effect of concentration of hydrochloric acid on leaching rates of As, Te and Bi in precipitate
��ͼ5��֪�����������ڡ������Ľ�������������Ũ�ȵ����Ӷ����ӣ�������Ũ��Ϊ3 mol/Lʱ������Ľ����ʷֱ�Ϊ98.43%��99.35%��������ʽ�Ϊ66.32%������Һ���ڡ�������Ũ�ȷֱ�Ϊ12.05 g/L��56.33 g/L��6.341 g/L��������ٺ�Һ��Ƚϣ��ڡ���ֱ���8.59����8.39�������ǣ�������Ũ�ȼ������ӣ�����Ļӷ���������[18]�����²���������Ҷ�����Ľ�����Ӱ�첻������������̵ķ�Ӧ���£�
Bi2O3+6HCl=2BiCl3+3H2O (5)
TeO2+4HCl=TeCl4+2H2O (6)
�����������ʱ��H+Ũ��Խ�ߣ��ں��������Խ�ߡ�������ӽ���ȫ����ʱ������Ũ��Ϊ3 mol/L����Һ�̱�Ϊ6:1ʱ��H+Ũ��Ϊ�����ں�����������2.25����
2.2.2 ��ͬ����ȵĻ���Խ����ʵ�Ӱ��
������ʵ���֪��ʹ�������ܽ�������������˵�H+����Ϊ������������������2.25������H+��������������£�ѡȡ3 mol/L�����1.5 mol/L�������ڲ�ͬ������½��н���������Ӧ�¶�Ϊ50�棬Һ�̱�(mL:g)Ϊ6:1����Ӧʱ��Ϊ2 hʱ���������������3���С�
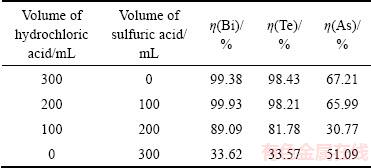
�ɱ�3��֪����ȫʹ���������ʱ���顢�ڡ���Ľ����ʷֱ�Ϊ99.38%��98.43%��67.21%����ȫʹ�������ܽ�ʱ�顢�ڡ���Ľ����ʷֱ��Ϊ33.62%��33.57%��51.09%������������������ȷֱ�Ϊ2:1��1:2ʱ�顢�ڡ���Ľ����ʷֱ�Ϊ99.93%��98.21%��65.99%��89%��81.78%��30.77%��ʵ���������顢�ڡ���Ľ��������������������Ӷ����ͣ�����������������Ϊ2:1ʱ�������Ч������ȫʹ���������Ч���൱��������Ũ�ȷֱ�Ϊ12.01 g/L��56.46 g/L�����������ڳ�����������Ľ��������������������ʱ���������ӿ����γ������ (xΪ1~6)�����������ӿ����γ������
(xΪ1~6)�����������ӿ����γ������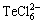 ��[19]��
��[19]��
��3 ��ͬ����ȵĻ���������顢�ڡ�������ʵ�Ӱ��
Table 3 Effect of different volume ratio of mixed acid on leaching rate of As, Te and Bi in precipitate
2.3 SO2��ԭ�����ں���
���������Һ��ϣ�����Һ�ɷ����4���С���Һ�к���Cl-������SO2��ԭ�������ڡ���ķ���[20]��
��4 ��������Ľ���Һ���顢�ڡ���Ũ��
Table 4 Concentration of As, Te and Bi in solution of enriching Bi and Te (g/L)

2.3.1 ��Ӧ�¶ȶ��ڡ��顢�黹ԭ�����ʵ�Ӱ��
ʵ��ȡ����Һ300 mL��ͨ������Ϊ0.25L/min��SO2������Ӧʱ��Ϊ0.5 hʱ����Ӧ�¶ȶԻ�ԭ������������ʵ�Ӱ����ͼ6��ʾ��
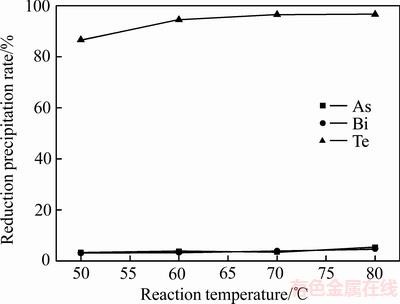
ͼ6 ��Ӧ�¶ȶ��顢�ڡ��黹ԭ�����ʵ�Ӱ��
Fig. 6 Effect of on reduction precipitation rate of As, Bi and Te
��ͼ6��֪���ڻ�ԭ���������ŷ�Ӧ�¶ȵ����Ӷ����ӣ����¶�Ϊ50�����ӵ�70��ʱ�ڻ�ԭ�����ʴ�86.66%���ӵ�96.56%���������ӷ�Ӧ�¶��ڻ�ԭ������û���������ӡ���ˣ����˵ķ�Ӧ�¶�Ϊ70�档
2.3.2 ��Ӧʱ����顢�ڡ��黹ԭ�����ʵ�Ӱ��
���Ʒ�Ӧ�¶�Ϊ70 �棬����ʵ���������䣬��Ӧʱ����顢�ڡ��黹ԭ�����ʵ�Ӱ����ͼ7��ʾ��
��ͼ7��֪������Ӧʱ��ﵽ50 min���ڵĻ�ԭ������Ϊ96.59%���������ӷ�Ӧʱ���ڵĻ�ԭ�����ʲ������ӡ�ʵ��ȡSO2����Ϊ0.25 L/min����Ӧ�¶�Ϊ70�桢��Ӧʱ��Ϊ50 min�������µõ��Ļ�ԭ����ɺ����XRD��SEMʵ�飬ʵ������ͼ8��9��ʾ��

ͼ7 ��Ӧʱ����顢�ڡ��黹ԭ�����ʵ�Ӱ��
Fig. 7 Effect of reaction time on reduction precipitation rate of As, Te and Bi

ͼ8 ��ԭ��������XRD��
Fig. 8 XRD pattern of reduction precipitate

ͼ9 ��ԭ������SEM��
Fig. 9 SEM image of reduction precipitate
��ͼ8��֪������SO2��ԭ�õ��IJ���Ϊ�����ڣ���ͼ9��֪����ԭ����ΪϸС��ĩ״����SO2����Ϊ0.25 L/min����Ӧ�¶�Ϊ70 �桢��Ӧʱ��Ϊ50 min��ʵ�������µõ��Ļ�ԭ����Ϊ�����ڣ������ں���Ϊ79.95%������麬����Ϊ0.067%��0.003%�������������ܽ��뻹ԭ�����ܻ�����Ϊ96.44%��
�����ٺ�Һ�����������Ƴ����������õ���������Ľ���Һ������Һ���顢�ڡ�����Ҫ��H3AsO4��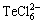 ��
��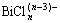 ����ʽ����[21-23]��SO2��ԭ��ϵ�У�������Ӽ��仯������缫��λ���5���С�
����ʽ����[21-23]��SO2��ԭ��ϵ�У�������Ӽ��仯������缫��λ���5���С�
��5 ��ص缫��Ӧ�����缫����[24]
Table 5 Related electrode reaction and standard electrode potential

�ɱ�5��֪��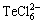 ��������λ��ߣ��ױ�SO2��ԭ����
��������λ��ߣ��ױ�SO2��ԭ����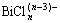 ��������λ��SO2��ԭ��λ�������
��������λ��SO2��ԭ��λ�������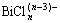 ������ԭ������Һ��ʵ������ķ��룬H3AsO4��������λ��SO2�Ļ�ԭ����H3AsO4�ױ���ԭΪHAsO2��SO2��ԭ��Ӧ���£�
������ԭ������Һ��ʵ������ķ��룬H3AsO4��������λ��SO2�Ļ�ԭ����H3AsO4�ױ���ԭΪHAsO2��SO2��ԭ��Ӧ���£�
2SO2+4H2O+H2TeCl6=Te��+6HCl+2H2SO4 (7)
H3AsO4+SO2=HAsO2+H2SO4 (8)
2.4 ��ԭ�ں�Һ�������ȡ�����
����SO2��ԭ���ں���õ����룬��ԭ�ں�Һ����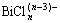 ��ʽ���ڡ�ͨ���������Ƶ���pHֵ������õ������飬Ȼ�������������ȵõ������飬ʵ����Ļ���[25]��
��ʽ���ڡ�ͨ���������Ƶ���pHֵ������õ������飬Ȼ�������������ȵõ������飬ʵ����Ļ���[25]��
2.4.1 pHֵ����ij����ʵ�Ӱ��
ʵ��ȡ������ԭ�ں�Һ�Ļ����Һ300 mL�������顢�ڡ���Ũ�ȷֱ�Ϊ5.778 g/L��0.3955 g/L��52.336 g/L����������ƿ�У�����5 mol/L������������Һ������Һ��pHֵ������Ӧ�¶�Ϊ50 �棬��Ӧʱ��Ϊ 1.0 hʱ��pHֵ���顢�ڡ�������ʵ�Ӱ����ͼ10��ʾ��
��ͼ10��֪���顢�ڡ������������pHֵ�����߶����ӣ���pHֵ��5ʱ����ij����ʴ�99.98%���ڵij����ʡ�99.94%��pHֵ��1���ӵ�7��������ʴ�6.15%���ӵ�63.28%����ԭ�ں�Һ������Ҫ��As(��)���ڣ�pHֵ�ϵ�ʱAs(��)��Ҫ��AsO+��HAsO2��̬���ڣ�����pHֵ�����ߣ���ҪAs(��)ת��ΪAsO2-��ʽ��AsO2-����ؽ��������γ��������γ���[17]��
Ϊ����֤Сʵ������ȡ5 L��ԭ�ں�Һ���зŴ�ʵ�顣���������Ƶ���pHֵΪ2����Ӧ�¶�Ϊ50 �棬��Ӧʱ��0.5 h����˵õ�������������120 ���ɺ����XRF��XRD��������ʵ�����ֱ����6����ͼ11��ʾ���顢�ڡ�������ʺ���Һ����Ũ�����7���С�

ͼ10 pHֵ���顢�ڡ�������ʵ�Ӱ��
Fig. 10 Effect of pH value on precipitation rate of As, Te and Bi

ͼ11 ��������XRD��
Fig. 11 XRD pattern of precipitate
��6 �������Ƴ������ﻯѧ�ɷ�(����������%)
Table 6 Chemical components of bismuth chloride (mass fraction, %)
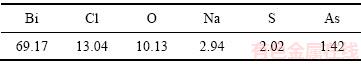
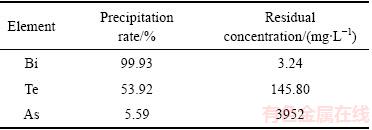
�ɱ�7��֪��pHֵΪ2ʱ������ʴﵽ99.93%����ͼ11��֪����pHֵΪ2��ʵ�������õ��IJ���Ϊ�����飬��ʵ�����������ܽ�Ư���������NaOH�������һ��[25]��
�ɱ�6��֪�������������ȡ��顢���ĺ����ֱ�Ϊ13.04%��10.13%��69.17%�����������У�������ܻ�����Ϊ93.41%��
ʵ������������ƽ������ȴ���������������Ũ��Ϊ6 mol/L��Һ�̱�Ϊ3:1����Ӧ�¶�Ϊ80 �桢��Ӧʱ��Ϊ2 h����ˣ�ϴ�ӣ���ɺ�XRD��SEM��XRFʵ�����ֱ���ͼ12��ͼ13�ͱ�8��ʾ��
��7 �Ŵ�ʵ���顢�ڡ�������ʺ���Һ�в���Ũ��
Table 7 Precipitation rates of As, Te and Bi and residual concentration in filtrate
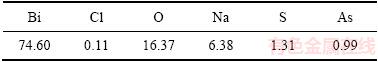
��8 ��������ѧ�ɷ�(����������%)
Table 8 Chemical components of dechlorination precipitate (mass fraction, %)
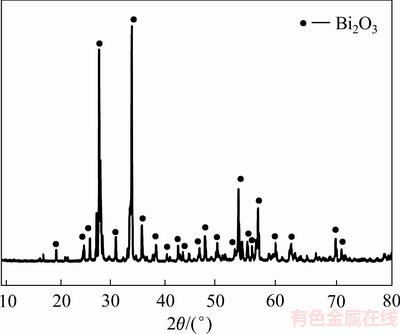
ͼ12 ������XRD��
Fig. 12 XRD pattern of dechlorination precipitate
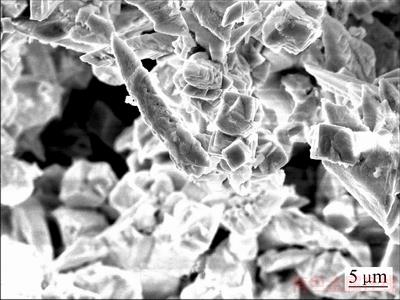
ͼ13 ������SEM��
Fig. 13 SEM image of dechlorination precipitate
�ɱ�8��֪����������ת�����Ⱥ����������麬��Ϊ74.60%���Ⱥ�����Ϊ0.11%��ʵ��������������ܹ���Ч��ȥBiOCl�е��ȡ�ͼ12��֪������Ϊ��б�Ħ�-Bi2O3[24]����ͼ13��֪����ɵõ���������òΪ��ά״���䷴Ӧԭ�����£�
2BiOCl+2NaOH=Bi2O3+2NaCl+H2O (9)
��ԭ�ں�Һ�����飬��298.15 K��Bi-Cl-H2Oϵ��������ʵļ���˹���������9���С�
��9 298.15 KʱBi-Cl-H2Oϵ��������ʵı�����˹������[26]
Table 9 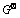 values of the relaitive substances in Bi-Cl-H2O system at 298.15 K[26]
values of the relaitive substances in Bi-Cl-H2O system at 298.15 K[26]
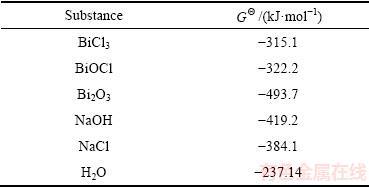
���ݱ�9���㣬����������Ƴ���������ת����ط�Ӧ���������£�
BiCl3+2NaOH=BiOCl��+2NaCl+H2O
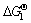 =-174.04 kJ/mol (10)
=-174.04 kJ/mol (10)
2BiOCl+2NaOH=Bi2O3+2NaCl+H2O
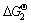 =-16.24 kJ/mol (11)
=-16.24 kJ/mol (11)
����������Ӧ�� ��С��0��������ԭ�ں�Һ��BiCl3ת��Ϊ�������������ת��Ϊ������������ѧ���ǿ��еġ�
��С��0��������ԭ�ں�Һ��BiCl3ת��Ϊ�������������ת��Ϊ������������ѧ���ǿ��еġ�
3 ����
1) ��NaOH��Һ���ڳ����ٺ�Һ��pHֵ�������飬��pHֵ��2���ӵ�13ʱ������ʲ��䣬���鹲�������˵�pHֵΪ6~9���ں���ij����ʶ�����99.10%��������������ڡ��麬���ֱ�Ϊ7.84%��36.02%��
2) ������������������Ļ��Һ�����������������H+Ũ��Ϊ3 mol/L����Ӧ�¶�Ϊ50 �棬��Ӧʱ��Ϊ2 hʱ���ں�������ʷֱ�ﵽ98.43%��99.35%������Һ���ں���Ũ�ȷֱ�Ϊ12.05 g/L��56.33 g/L��������ٺ�Һ������Ũ�ȱȽϣ���������Һ�зֱ���8.59����8.39����
3) ����SO2��ԭ��������Ľ���Һ�е��ڣ�����Ӧ�¶�Ϊ70 �桢��Ӧ50 min����˵õ��ڷۺͻ�ԭ�ں�Һ���ڻ�ԭ������Ϊ96.59%����ԭ�������ں����ﵽ79.45%�������顢�麬����Ϊ0.003%��0.067%�������������ܽ��뻹ԭ�����ܻ�����Ϊ96.44%��
4) ����������Һ���ڻ�ԭ�ں�ҺpHֵ����pH��5ʱ��������ʴ���99.94%��ˮ�����ΪBiOCl��������BiOCl�м���6 mol/L������������Һ��Һ�̱�Ϊ3:1����Ӧ�¶�Ϊ80 ��ʱ����Ӧ2 h����ˡ���ɵõ������飬�����麬���ﵽ74.60%������Ϊ93.80%��������������ܻ�����Ϊ93.41%��
REFERENCES
[1] SARGAR B M, ANUSE M A. Liquid-liquid extraction study of tellurium(��) with N-n-octylaniline in halide medium and its separation from real samples[J]. Tatanta, 2001, 55(3): 469-478.
[2] JEON S J, OH M, JEON H, HYUN S, LEE H J. Effects of post-annealing on thermoelectric properties of bismuth�Ctellurium thin films deposited by co-sputtering[J]. Microelectronic Engineering, 2011, 88(55): 541-544.
[3] SHIM M, KIM Y M, LEE H H, HONG S J, LEE H J. Separation behavior of impurities and selenium reduction by the reactive zone refining process using high-frequency induction heating to purify Te[J]. Journal of Crystal Growth, 2016, 455: 6-12.
[4] ������, ��ެ, ������. ��ⷨ�����龫����о�[J]. ��ɫ����, 1992, 36(2): 8-12.
WANG Cheng-yan, QIU Ding-fan, ZHANG Yin-sheng. Treatment of bismuth concentrate slurry electrolysis research[J]. Nonferrous metals, 1992, 36(2): 8-12.
[5] SHIBASAKI T, ABE K, TAKEUCHI H. Recovery of tellurium from decopperizing leach solution of copper refinery slimes by a fixed bed reactor[J]. Hydrometallurgy, 1992, 29(1/3): 399-412.
[6] GUO X, XU Z, LI D, TIAN Q, XU R, ZHANG Z. Recovery of tellurium from high tellurium-bearing materials by alkaline sulfide leaching followed by sodium sulfite precipitation[J]. Hydrometallurgy, 2017, 171: 355-361.
[7] HA Y C, SOHN H J, JEONG G J, LEE C K, RHEE K I. Lectrowinning of tellurium from alkaline leach liquor of emented Te [J]. Applied Electrochemistry, 2000, 30(3): 315-322.
[8] ZHANG F Y, ZHENG Y J, PENG G M. Selection of reductants for extracting selenium and tellurium from degoldized solution of copper anode slimes[J]. Transactions of Nonferrous Metals Society of China, 2017, 27(4): 917-924.
[9] RHEE K, LEE C K, HA Y C, JEONG G J, KIM H S, SOHN H J. Tellurium recovery from cemented tellurium with minimum aste disposal [J]. Hydrometallurgy, 1999, 53(2): 189-201.
[10] YANG J G, TANG M T, TANG C B, LIU W. The solvent extraction separation of bismuth and molybdenum from a low grade bismuth glance flotation concentrate[J]. Hydrometallurgy, 2009, 96 (4): 342-348.
[11] CHEN S L, GUO X Y, LIANG Y X. Remove of arsenic, antimony and bismuth from crude crystal copper sulfate[J]. Journal of Central South University, 2010, 41(4): 1251-1255.
[12] �� ��. �������н����ͷ����ڵĹ����о�[D]. ��ɳ: ���ϴ�ѧ, 2009: 7-14.
MA Hui. Studies on the technics for leaching and separation of tellurium from tellurium slag[D]. Changsha: Central South University, 2009: 7-14..
[13] �ֺ촺. �к������ڵ���ȡ������Ʊ��ߴ����о�[D]. ��ɳ: ���ϴ�ѧ, 2012: 28-39.
LE Hong-chun. Research on extraction of tellurium from neutralizationsludge and electrolytic preparation of high puritytellurium[D]. Changsha: Central South University, 2012: 28-39.
[14] ������, Ǯ ��, �̴���. �ڷ۵�⾫����������������Ե���������Ӱ��[J]. ʪ��ұ��, 2004, 23(3): 162.
LAI Jian-lin, QIAN Yong, CAI Chun-xiu. The influence of area current on the quality of electric Te in the process of electrolytic refining of Te powder[J]. Hydrometallurgy, 2004, 23(3): 162.
[15] ������, ������, �� ��, ������. �Ӹ�Ǧ�����н����ڵ�����ѧ������ʵ��[J]. ���ϴ�ѧѧ��(��Ȼ��ѧ��), 2011, 37(3): 499-503.
MA Yu-tian, GONG Zhu-qing, WU Jun, CHEN Wen-mi. Thermodynamic analysis and experimental studies of leaching lead-rich tellurium slag[J]. Journal of Central South University (Science and Technology), 2011, 37(3): 499-503.
[16] ֣�Ž�, ���ֱ�, �� ΰ, ��С��, ���ذ�. һ�ִ���Һ�и���������������ķ���: �й�, 201610813922.3[P]. 2016-09-12.
ZHENG Ya-jie, ZHANG Lin-bao, LI Wei, AN Xiao-kai, L�� Zhong-ang. A method for the enrichment and separation of tellurium and bismuth from solution��China, 201610813922.3[P]. 2016-09-12.
[17] �� ��. ͭұ�������ˮ�����¹��ռ�����������о�[D].��ɳ: ���ϴ�ѧ, 2009: 44-49.
WANG Yong. Study on new treatment technology and fundamental theory of arsenic waste water produced in copper metallurgy[D]. Changsha: Central South University, 2009: 43-49.
[18] ������. ͭ���������ڵĻ������ᴿ������������о�[D]. ��ɳ: ���ϴ�ѧ, 2012: 27-29.
SUN Zhao-ming. Study on recovery and purification of tellurium from copper anode slime and relative fundamental theory[D]. Changsha: Central South University, 2012: 27-29.
[19] ���ܻ�, ������, ��Ң��. �����û�����������Ķ���ѧ�о�[J]. ʪ��ұ��, 2007, 29(3): 140-142.
WU Shao-hua, LIU Chun-yan, LAN Yao-zhong. Kinetic study on cementation of bismuth from solution using iron powder[J]. Hydrometallurgy, 2007, 29(3): 140-142.
[20] �����S, ֣�Ž�, ������, ������, �����, �Ÿ�Ԫ. ±�����Ӵ�������SO2��ԭ�����Һ��������ѧ����[J]. �й���ɫ����ѧ��, 2016, 26(4): 903-905.
MA Ya-yun, ZHENG Ya-jie, DING Guang-yue, WANG Jun-wen, DONG Jun-fei, ZHANG Fu-yuan. Precipitated gold solution reduced by SO2 under halogen ion composite catalyst andits thermodynamic characteristics[J]. The Chinese Journal of Nonferrous Metals, 2016, 26(4): 903-905.
[21] SEBY F, POTIN-GAUTIER M, GIFFAUT E, BORGE G, DONARD O F X. A critical review of thermodynamic data for selenium species at 25 ��[J]. Chemical Geology, 2001, 171(3/4): 173-194.
[22] GRUNDLER P, BRUGGER J, ETSCHMANN B E. Speciation of aqueoustellurium(��) in hydrothermal solutions and vapors and the role of oxidized tellurium species in Te transport and gold deposition[J]. Geochimica et Cosmochimica Acta, 2013, 120: 298-325.
[23] MOKMELI M, DREISINGER D, WASSINK B. Thermodynamics and kinetics study of tellurium removal with cuprous ion[J]. Hydrometallurgy, 2014, s147/148(8): 20-29.
[24] ��ά��, �����, �ұ. ���缫��λ�����ֲ�[M]. ����: ��ѧ������, 1991.
WU Wei-chang, FENG Hong-qing, WU Kai-ye. Standard electrode potential datasheet[M]. Beijing: Science Press, 1991.
[25] ֣�Ž�, �� ��. Ư����������������������鹤��[J]. ���ϴ�ѧѧ��(��Ȼ��ѧ��), 2011, 42(8): 2220-2226.
ZHENG Ya-jie, HONG Bo. Enrichment of Au and Ag and recovery of Sb and Bi from floating anode slime[J]. Journal of Central South University (Science and Technology), 2011, 42(8): 2220-2226.
[26] J.A.�ϰ�. ���ϻ�ѧ�ֲ�[M]. ����: ��ѧ������, 1998.
DEAN J A. Lang��s handbook of chemistry[M]. Beijing: Science Press, 1998.
Separation and recovery process of tellurium and bismuth from precipitating platinum and palladium solution
ZHANG Lin-bao, ZHENG Ya-jie, AN Xiao-kai
(School of Metallurgy and Environment, Central South University, Changsha 410083, China)
Abstract: Tellurium powder and tellurium reduction liquid were obtained through a sets of steps including precipitation process of NaOH, HCl leaching process of slag producing in the previous process, and the reduction process of SO2. The BiOCl was obtained after reduction tellurium liquid was precipitated using sodium hydroxide and then the slurry was filtered. The Bi2O3 was obtained by using NaOH to remove chlorine from BiOCl. The results show that the precipitation rates of Te and Bi are 99.91% and 99.96%, respectively, using NaOH as pH regulator, when the pH value is 6, temperature is 20-25 �� and the reaction time is 1 h. The leaching rates of Te and Bi are 98.21% and 99.93%, respectively, when the volume ratio of 3 mol/L HCl to 1.5 mol/L H2SO4 is 2:1, the concentration of H+ is 3 mol/L, the reaction temperature is 50 �� and the reaction time is 2 h. The reduction rate of Te is 96.59%, and the contents of Te, As and Bi in the tellurium powder are 79.45%, 0.003% and 0.067% (mass fraction), respectively. The BiOCl is obtained by filtering when the pH of Te reduction solution is 2. Finally, the Bismuth content reaches 93.80% after adding 6 mol/L NaOH to the BiOCl when the ratio of liquid to solid is 3:1, the reaction temperature is 80 �� and the reaction time is 2 h.
Key words: tellurium; bismuth; precipitation; acid dissolution; reduction
Foundation item: Project(2013A090100013) supported by the Teaching and Research Program of Guangdong Province, China
Received date: 2017-06-12; Accepted date: 2017-10-08
Corresponding author: ZHENG Ya-jie; Tel: +86-731-88836285; E-mail: ZYJ@csu.edu.cn
(�༭ �� ��)
������Ŀ���㶫ʡ��������ѧ���ش���Ŀ(2013A090100013)
�ո����ڣ�2017-06-12�������ڣ�2017-10-08
ͨ�����ߣ�֣�Žܣ����ڣ���ʿ���绰��0731-88836285��E-mail: ZYJ@csu.edu.cn