ΈΡ’¬±ύΚ≈ΘΚ1004-0609(2010)04-0788-07
ΟφΑϋΫΆΡΗΨζ‘Ύ«ΠΆ≠ΡΘΡβΖœΥ°÷–ΒΡΈϋΗΫΕ·ΝΠ―ß
¥ζ»ΚΆΰ1, 2Θ§Ε≠ΖΔ«Ύ1Θ§M. J. NOONAN3Θ§’≈ ΈΑ1
(1. ΈςΡœΩΤΦΦ¥σ―ß ΙΧΧεΖœΈο¥Πάμ”κΉ ‘¥Μ·ΫΧ”ΐ≤Ω÷ΊΒψ Β―ι “Θ§Ού―τ 621010ΘΜ
2. ΈςΡœΩΤΦΦ¥σ―ß ΜΖΨ≥”κΉ ‘¥―ß‘ΚΘ§Ού―τ 621010ΘΜ
3. Ν÷Ωœ¥σ―ß ≈©“Β”κ…ζΟϋΩΤ―ßœΒΘ§–¬ΈςάΦ ΜυΕΫ≥«8006)
’Σ “ΣΘΚΧΫΧ÷ΡΘΡβ÷ΊΫπ τPb2+-Cu2+ΜλΚœΖœΥ°÷–ΟφΑϋΫΆΡΗΨζΒΡΕ·ΝΠ―ßΈϋΗΫ––ΈΣΚΆΗςάκΉ”ΦδΒΡΒψΈΜΨΚ’υΈϋΗΫΙΐ≥ΧΓΘ―Γ‘ώΟφΑϋΫΆΡΗΨζΈΣΈϋΗΫΦΝΘ§Ζ÷±πΕ‘≤ΜΆ§ΒΡPb2+-Cu2+ΖœΥ°Ϋχ––Ε·ΝΠ―ßΈϋΗΫΖ÷ΈωΚΆΕΰΦΕΕ·ΝΠ―ßΡΘ–ΆΦΤΥψΘ§Ά§ ±Θ§“≤Ϋχ––SEM/EDSΖ÷ΈωΓΘΫαΙϊ±μΟςΘΚ‘ΎΉν≥θ60 min ±Θ§ΫΆΡΗΨζΕ‘Pb2+-Cu2+ΖœΥ°÷–άκΉ”“―”–ΫœΚΟΒΡΈϋΗΫ–ßΙϊΘ§‘Ύ’ϊΗωΕ·ΝΠ―ßΈϋΗΫΙΐ≥Χ÷–Θ§ΫΆΡΗΨζΕ‘ΖœΥ°÷–άκΉ”ΒΡΈϋΗΫΙΊœΒΉή «¥φ‘Ύ ΘΨ
ΘΨ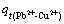 ΘΨ
ΘΨ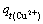 ΓΘΕΰΦΕΕ·ΝΠ―ßΖΫ≥ΧΦΤΥψΫαΙϊœ‘ ΨΘΚ‘ΎCu2+ΨΚ’υ–≤Τ»ΜΖΨ≥œ¬Θ§‘ω¥σCu2+ΒΡ±»άΐ ΙΫΆΡΗΨζΕ‘Pb2+ΒΡΈϋΗΫΥΌ¬ ΗϋΩλΘ§“≤÷ΛΟςPb2+‘ΎΈϋΗΫΒψΈΜΨΚ’υΙΐ≥Χ÷–ΒΡΟςœ‘”≈ ΤΘ§EDS≤β ‘ΫαΙϊ“≤÷Λ Β’βΒψΓΘSEMΖ÷ΈωΖΔœ÷ΘΚΫΆΡΗΨζΈϋΗΫCu2+ΚΆPb2+ΚσΘ§ΨζΧε≥ωœ÷≤ΜΙφ‘ρ±δ–Έ≤Δ‘β ή“ΜΕ®ΒΡΤΤΜΒΘ§”–ΡΎ≤ΩΈο÷ Άβ–Ιœ÷œσΓΘΫΆΡΗΨζΕ‘Cu2+ΚΆPb2+ΕΦ”–“ΜΗωΩλΥΌΈϋΗΫΙΐ≥ΧΘ§œύΕ‘Εχ―‘ΤδΕ‘Pb2+ΒΡΈϋΗΫΗϋΨΏ”≈ ΤΓΘ
ΓΘΕΰΦΕΕ·ΝΠ―ßΖΫ≥ΧΦΤΥψΫαΙϊœ‘ ΨΘΚ‘ΎCu2+ΨΚ’υ–≤Τ»ΜΖΨ≥œ¬Θ§‘ω¥σCu2+ΒΡ±»άΐ ΙΫΆΡΗΨζΕ‘Pb2+ΒΡΈϋΗΫΥΌ¬ ΗϋΩλΘ§“≤÷ΛΟςPb2+‘ΎΈϋΗΫΒψΈΜΨΚ’υΙΐ≥Χ÷–ΒΡΟςœ‘”≈ ΤΘ§EDS≤β ‘ΫαΙϊ“≤÷Λ Β’βΒψΓΘSEMΖ÷ΈωΖΔœ÷ΘΚΫΆΡΗΨζΈϋΗΫCu2+ΚΆPb2+ΚσΘ§ΨζΧε≥ωœ÷≤ΜΙφ‘ρ±δ–Έ≤Δ‘β ή“ΜΕ®ΒΡΤΤΜΒΘ§”–ΡΎ≤ΩΈο÷ Άβ–Ιœ÷œσΓΘΫΆΡΗΨζΕ‘Cu2+ΚΆPb2+ΕΦ”–“ΜΗωΩλΥΌΈϋΗΫΙΐ≥ΧΘ§œύΕ‘Εχ―‘ΤδΕ‘Pb2+ΒΡΈϋΗΫΗϋΨΏ”≈ ΤΓΘ
ΙΊΦϋ¥ ΘΚΜΖΨ≥±ΘΜΛΘΜ«ΠΘΜΆ≠ΘΜΖœΥ°ΘΜΟφΑϋΫΆΡΗΨζΘΜ…ζΈοΈϋΗΫΘΜΕ·ΝΠ―ß
÷–ΆΦΖ÷άύΚ≈ΘΚX703ΓΓΓΓ ΈΡœΉ±ξ÷Ψ¬κΘΚA
Biosorption kinetics of BakerΓ·s yeast in lead and copper waste water
DAI Qun-wei1, 2, DONG Fa-qin1, M. J. NOONAN3, ZHANG Wei1
(1. Key Laboratory of Solid Waste Treatment and Resource Recycle, Ministry of Education,
Southwest University of Science and Technology, Mianyang 621010, China;
2. School of Environment and Resource, Southwest University of Science and Technology, Mianyang 621010, China;
3. Agriculture and Life Science Division, Lincoln University, Christchurch 8006, New Zealand)
Abstract: The kinetics biosorption behavior of BakerΓ·s yeast in the simulation heavy metal waste water of Pb2+-Cu2+ was investigated. The autoclaved BakerΓ·s yeast was chosen as a biosorbent, and then the kinetics biosorption process and second-kinetics model were analyzed, respectively. The results show that there is very good biosorption effect at first 60 min. At the same initial concentration for heavy metal ions, there are the relations: 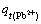 ΘΨ
ΘΨ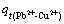 ΘΨ
ΘΨ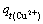 . The second-kinetics biosorption modelΓ·s analysis shows that the biosorption speed to Pb2+ becomes rapid with the initial concentration of Cu2+ increasing, proving that there is obvious advantage to Pb2+ in the biosorption sites competition process. And the analysis results of EDS approve it also. The analysis of SEM shows that the BakerΓ·s yeast cells are broken after the biosorption of Pb2+ and Cu2+ ions. The toxicity of heavy ions to yeast cells makes the cells distort and break. The cytoplasm leaks out from the yeast cells. The biosorption of bakerΓ·s yeast to Pb2+ and Cu2+ is a rapid and preferable process, and there is a more obvious advantage for BakerΓ·s yeast to Pb2+ than Cu2+.
. The second-kinetics biosorption modelΓ·s analysis shows that the biosorption speed to Pb2+ becomes rapid with the initial concentration of Cu2+ increasing, proving that there is obvious advantage to Pb2+ in the biosorption sites competition process. And the analysis results of EDS approve it also. The analysis of SEM shows that the BakerΓ·s yeast cells are broken after the biosorption of Pb2+ and Cu2+ ions. The toxicity of heavy ions to yeast cells makes the cells distort and break. The cytoplasm leaks out from the yeast cells. The biosorption of bakerΓ·s yeast to Pb2+ and Cu2+ is a rapid and preferable process, and there is a more obvious advantage for BakerΓ·s yeast to Pb2+ than Cu2+.
Key words: environmental protection; copper; lead; waste water; BakerΓ·s yeast; biosorption; kinetics
“±ΫπΙΛ“ΒΖœΥ°÷–Κ§”–¥σΝΩΒΡCu2+ΓΔPb2+ΓΔZn2+ΚΆCd2+Β»÷ΊΫπ τάύ”–ΚΠΈο÷ Θ§Τδ≈®Ε»Ά®≥ΘΫ”Ϋϋ200~500 mg/LΘ§‘Ε‘ΕΗΏ”Ύ‘ –μ≈≈Ζ≈ΒΡ±ξΉΦΘ§“ρ¥ΥΘ§―Α«σ»γΚΈ¥”ΙΛ“ΒΖœΥ°÷–»Ξ≥ΐ÷ΊΫπ τάκΉ”≥…ΈΣ“Μœν÷Ί“ΣΒΡΙΛΉςΓΘ¥ΪΆ≥ΒΡ¥ΠάμΖΫΖ®÷ς“ΣΑϋά®Μ·―ß≥ΝΒμ[1]ΓΔάκΉ”ΫΜΜΜ[2]ΓΔΡΛΖ÷ άκ[3]ΓΔ’τΖΔ[4]ΚΆΒγΜ·―ߥΠάμ[5]Β»ΓΘ’κΕ‘’β–©ΖΫΖ®¥φ‘ΎΚΡΡήΗΏΓΔ–ß¬ ΒΆ“‘ΦΑ≥…±ΨΗΏΒ»≤ΜΉψΚΆ»’“φ―œ÷ΊΒΡ÷ΊΫπ τΈέ»Ψœ÷Ή¥Θ§ΫϋΡξά¥“Μ–©ΙζΡΎΆβ―ß’ΏΕ‘≤ΜΆ§…ζΈοΈϋΗΫΦΝΕ‘ΖœΥ°÷–÷ΊΫπ τΒΡΈϋΗΫ–ßΙϊΚΆΜζάμΫχ––ΝΥœύΙΊΧΫΧ÷ΓΘΡΩ«ΑΘ§»ΥΟ«“―Ψ≠άϊ”ΟœΗΨζΓΔ’φΨζΚΆ‘εάύΒ»≤ΜΆ§άύ–ΆΒΡΈΔ…ζΈοΈϋΗΫΦΝΕ‘Cu2+ΓΔPb2+ΓΔCr6+ΚΆZn2+Β»÷ΊΫπ τάκΉ”ΒΡΈϋΗΫΧθΦΰΓΔΈϋΗΫ–ßΙϊΚΆΈϋΗΫΜζάμΫχ––ΝΥΧΫΧ÷[6-10]ΓΘΤδ÷–Θ§άϊ”ΟΈΔ…ζΈοΈϋΗΫΦΝΕ‘Pb2+ΚΆCu2+Ϋχ––ΈϋΗΫ¥ΠάμΒΡ―–ΨΩ”–ΫœΕύ±®Βά[11-13]ΓΘΫΆΡΗΨζ±ΜΙψΖΚ”Π”Ο”Ύ ≥ΤΖΚΆ“ϊΝœΙΛ“ΒΘ§ΙΛ“ΒΖœΤζΫΆΡΗΨΏ”–Ν°ΦέΓΔά¥‘¥Έ»Ε®ΓΔΝΩ¥σΓΔ“Ή”ΎΜώΒΟΚΆΑ≤»ΪΒΡΧΊΒψΘ§”–άϊ”Ύ…ζΈοΈϋΗΫΒΡΙΛ“ΒΜ·”Π”Ο[14-15]ΓΘΡΩ«ΑΘ§“―”–ΫΆΡΗΨζΕ‘Pb2+ΚΆCu2+ΒΡΒΞάκΉ”ΚΆΥΪάκΉ”ΒΡΈϋΗΫ―–ΨΩ[15]ΓΘ»ΜΕχΘ§ΡΩ«Α”–ΙΊΕύάκΉ”ΖœΥ°÷–≤ΜΆ§÷ΊΫπ τάκΉ”ΦδΗ¥‘”ΒΡœύΜΞΨΚ’υΕ‘”ΎΫΆΡΗΨζΦΑΤδΥϋ…ζΈοΈϋΗΫΦΝΒΡΈϋΗΫΙΐ≥ΧΒΡ”ΑœλΜζάμΜΙ≤Μ °Ζ÷«ε≥ΰΘ§«“―–ΨΩ’ΏΕύΦ·÷–ΧΫΧ÷ΖœΥ°÷–ΤδΥϋάκΉ”Ε‘Ρ≥ΒΞ“ΜάκΉ”ΒΡΈϋΗΫ–‘ΡήΒΡ”ΑœλΘ§Κω¬‘ΝΥ…ζΈοΈϋΗΫΦΝΕ‘ΕύάκΉ”ΖœΥ°÷–άκΉ”ΉήΈϋΗΫΡήΝΠΒΡ±δΜ·«ιΩωΒΡ―–ΨΩΓΘ
±ΨΈΡΉς’Ώ―Γ‘ώΟπΜνΟφΑϋΫΆΡΗΨζΉςΈΣΈϋΗΫΦΝΘ§Ε‘Κ§Pb2+-Cu2+ΖœΥ°ΒΡΈϋΗΫΕ·ΝΠ―ßΙΐ≥ΧΫχ––ΧΫΧ÷Θ§―–ΨΩΝΫ÷÷άκΉ”œύΜΞΉς”ΟΒΡΆ§ ±Θ§ΫΪΝΫ÷÷άκΉ”ΒΞΕάΜρΙ≤Ά§¥φ‘Ύ ±ΫΆΡΗΨζΒΡΉήΧεΈϋΗΫΡήΝΠΫχ––Ε‘±»Θ§Ϋχ“Μ≤ΫΧΫΧ÷ΟφΑϋΫΆΡΗΨζΕ‘Pb2+ΚΆCu2+ΒΡΈϋΗΫΡήΝΠΦΑΤδΕ‘÷ΊΫπ τΒΡΉήΧεΈϋΗΫΡήΝΠΘ§ΈΣ―–ΨΩΕύάκΉ”ΖœΥ°Η¥‘”ΒΡ…ζΈοΈϋΗΫΜζάμΧαΙ©≤ΈΩΦΘ§“≤ΈΣΫχ“Μ≤Ϋ―–ΨΩΗϋΈΣΗ¥‘”“Κœύ÷–ΫΆΡΗΨζΒΡΈϋΗΫ––ΈΣΚΆ ΒΦ ”Π”ΟΧαΙ©≤ΈΩΦΓΘ
1 Β―ι
1.1 ≤ΡΝœΒΡΉΦ±Η
ΟφΑϋΫΆΡΗΨζ(±Χγς ≥ΤΖ≥ωΩΎ”–œόΙΪΥΨ…ζ≤ζ(»π Ω))‘Ύ0.15 MPaΓΔ125 Γφœ¬ΟπΜν20 minΘ§»ΜΚσ‘ΎΗ…‘οœδ÷–”Ύ60 Γφœ¬Η…‘ο24 hΘ§»Γ≥ωΉΑΤΩ≤ΔΖ≈»κΗ…‘οΟσ÷–±Η”ΟΓΘCu(NO3)2ΚΆPb(NO3)2ΈΣΖ÷Έω¥ΩΓΘ
1.2 Β―ιΖΫΖ®
Ζ÷±π≥Τ»Γ“ΜΕ®ΝΩΒΡCu(NO3)2ΓΔPb(NO3)2»ήΫβ”ΎΈόΨζΥ°÷–Θ§≈δ÷Τ≥…10.0 mmol/LΒΡCu2+»ή“ΚΚΆ10.0 mmol/LΒΡPb2+»ή“ΚΓΘ Β―ι ±ΫΪΝΫ÷÷άκΉ”»ή“ΚΖ÷±π“ά¥ΈΧίΕ»œΓ ΆΜρΑ¥“Σ«σ≈δ±»ΚσœΓ ΆΘ§ΜώΒΟΥυ–ηœύ”ΠΒΡΒΞάκΉ”ΖœΥ°ΚΆCu2+-Pb2+ΒΡΥΪάκΉ”ΖœΥ°ΓΘpH÷Β”Ο0.5 mol/LΒΡHNO3ΚΆNaOHΒςΫΎΘ§ΈΣΦθ…ΌΆβΦ”―τάκΉ”Ε‘ΈϋΗΫΙΐ≥ΧΒΡ”ΑœλΘ§‘ΎpHΒςΫΎΙΐ≥Χ÷–Θ§ΨΓΝΩ÷Μ”ΟHNO3ΜΚ¬ΐΒςΫΎΓΘ
Β―ι―Γ”ΟΟφΑϋΫΆΡΗΨζΒΡ≥θ Φ≈®Ε»ΈΣ4.0 g/LΘ§»ή“Κ≥θ ΦpHΈΣ4.5Θ§ΈϋΗΫΈ¬Ε»ΈΣ30 ΓφΘ§’ώΒ¥ΥΌΕ»ΈΣ150 r/minΘ§ΤΫΚβΈϋΗΫ ±ΦδΈΣ1 440 minΓΘ Β―ι ±Θ§ΗυΨί“―≈δ÷ΤΚΟΒΡ÷ΊΫπ τάκΉ”ΖœΥ°Θ§Ζ÷±πΫΪ“ΜΕ®ΝΩΟφΑϋΫΆΡΗΨζΦ”»κΉΑ”–100 mL Β―ιΥυ–η»ή“ΚΒΡ250 mLΉΕ–ΈΤΩ÷–Θ§Ζ≈»κ’ώΒ¥Τς÷–’ώΒ¥Θ§ΟΩ¥Έ»Γ―υ2 mLΘ§»Γ≥ωΚσ‘ΎΗ«≤ΘΤ§…œΒΈΦ”ΜλΚœ“Κ―υΤΖ÷Τ±ΗSEM≤β ‘―υΘΜ Θ”ύ―υΤΖΝΔΦ¥‘Ύ 4 000 r/minΓΔ4 ΓφΧθΦΰœ¬άκ–Ρ8 minΘ§»Γ…œ«ε“Κ Β±œΓ ΆΘ§≤ΔΑ¥―υΤΖΧεΜΐ±»άΐΒΡ1%ΧμΦ”≈®œθΥαΚσ”Ύ4 Γφœ¬±Θ¥φΈΣAAS ‘―υΘ§¥ΐ≤βΘΜΥυΒΟ≥ΝΒμ”ΟΈόΨζ’τΝσΥ°Ζ¥Η¥œ¥Β”≤Δάκ–Ρ3¥ΈΚσ ’Φ·Θ§‘Ύ45 Γφœ¬ΚφΗ…24 hΉςΈΣEDS ‘―υΓΘ
Β―ι÷–÷ΊΫπ τάκΉ”ΒΡ÷ ΝΩ≈®Ε»”ΟAAS≤βΕ®Θ§ΜΜΥψ≥…ΡΠΕϊ≈®Ε»ΚσΘ§ΫΆΡΗΨζΒΡΈϋΗΫΝΩΚΆΈϋΗΫ–ß¬ ”Οœ¬ Ϋ±μ ΨΘΚ

1.3 ÷ς“Σ“«ΤςΚΆ…η±Η
÷ς“Σ“«ΤςΚΆ…η±Η”–AA700–Ά‘≠Ή”Έϋ ’ΙβΤΉ“«(AASΘ§ΟάΙζ)Θ§LEO S440–Ά…®ΟηΒγΉ”œ‘ΈΔΨΒ(SEMΘ§”ΔΙζ)Θ§X…δœΏΡήΤΉΝΣ”Ο“«(EDSΘ§ΟάΙζ)ΚΆLab-Line–Ά’ώΒ¥Τς(ΟάΙζ)Θ§Varifuge 3.0R–Άάκ–ΡΜζ(Β¬Ιζ)ΓΘ
2 ΫαΙϊ”κΖ÷Έω
2.1 Cu2+≥θ Φ≈®Ε»Ε‘ΫΆΡΗΨζΈϋΗΫΕ·ΝΠ―ßΒΡ”Αœλ
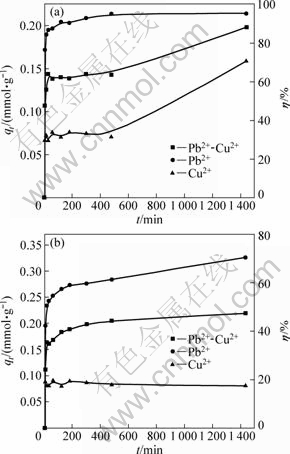
ΆΦ1Υυ ΨΈΣPb2+-Cu2+ΖœΥ°÷–Pb2+ΒΡ≥θ Φ≈®Ε»ΈΣ2.0 mmol/L«ιΩωœ¬Θ§Cu2+ΒΡ≥θ Φ≈®Ε»Ε‘ΫΆΡΗΨζΈϋΗΫCu2+ΚΆPb2+ΒΡ”ΑœλΓΘ”…ΆΦ1(a)Ω…Ω¥≥ωΘ§‘Ύ’ϊΗωΈϋΗΫΙΐ≥Χ÷–Θ§ΫΆΡΗΨζΕ‘Cu2+ΒΡΒΞΈΜΈϋΗΫΝΩΜυ±Ψ…œ «ΥφΉ≈Cu2+≥θ Φ≈®Ε»ΒΡ‘ωΦ”Εχ‘ω¥σΘΜ«“‘ΎΈϋΗΫΖ¥”Π≥θΤΎΘ§ΥφΉ≈ΈϋΗΫΖ¥”ΠΒΡΫχ––Θ§ΫΆΡΗΨζΕ‘Cu2+ΒΡΒΞΈΜΈϋΗΫΝΩ”–“ΜΗωΩλΥΌ‘ωΦ”Ιΐ≥ΧΘ§≤Δ‘ΎΈϋΗΫΫχ––ΒΫ60 min ±Θ§¥οΒΫΉν¥σΓΘΕχΥφΉ≈ΈϋΗΫ ±ΦδΒΡΦΧ–χ―”≥ΛΘ§ΫΆΡΗΨζΕ‘Cu2+ΒΡΈϋΗΫΝΩ≥ωœ÷ΝΥœ¬ΫΒΘ§«“’β÷÷±δΜ·ΥφΉ≈Cu2+≥θ Φ≈®Ε»ΒΡΧαΗΏΕχ±μœ÷ΒΟ”»ΈΣΟςœ‘ΓΘάΐ»γΘ§Β±Cu2+ΒΡ≥θ Φ≈®Ε»ΈΣ4.0 mmol/L ±Θ§ΈϋΗΫΫχ––ΒΫ60 min ±ΒΡΈϋΗΫΝΩΚΆΈϋΗΫ–ß¬ Ζ÷±πΈΣ0.221 mmol/gΚΆ20.14%ΘΜΒ±ΈϋΗΫΫχ––ΒΫ1 440 min ±Θ§ΈϋΗΫΝΩΚΆΈϋΗΫ–ß¬ Ζ÷±πΈΣ0.137 mmol/gΚΆ12.51%ΓΘ‘ΎΈϋΗΫΫχ––ΒΫ1 440 minΘ§Cu2+≥θ Φ≈®Ε»ΈΣ0.5ΓΔ1.0ΓΔ2.0ΚΆ4.0 mmol/L ±Θ§ΫΆΡΗΨζΕ‘Cu2+ΒΡΈϋΗΫΝΩΖ÷±πΈΣ60 min ±ΒΡ1.23ΓΔ0.80ΓΔ0.72ΚΆ0.62±ΕΓΘ”…ΆΦ1(b)Ω…“‘Ω¥≥ωΘ§Ε‘”ΎPb2+ΈϋΗΫΘ§ΥφΉ≈ΖœΥ°÷–Cu2+≥θ Φ≈®Ε»ΒΡ‘ωΦ”Θ§ΤδΕ‘ΫΆΡΗΨζΈϋΗΫPb2+ΒΡ“÷÷ΤΉς”Ο÷πΫΞ‘ω«ΩΓΘΒ±ΈϋΗΫΖ¥”ΠΫχ––1 440 min ±Θ§ΈϋΗΫΕ·ΝΠ―ß¥οΒΫΤΫΚβΘ§qtΖ÷±πΈΣ0.243ΓΔ0.203ΓΔ0.182ΚΆ0.141 mmol/gΘ§ΈϋΗΫ–ß¬ Ζ÷±πΈΣ54.79%ΓΔ45.79%ΓΔ41.05%ΚΆ31.90%ΓΘ
ΆΦ1 Cu2+ΒΡ≥θ Φ≈®Ε»Ε‘ΫΆΡΗΨζΈϋΗΫCu2+ΚΆPb2+ΒΡ”Αœλ
Fig.1 Effects of initial concentration of Cu2+ on biosorption of Cu2+ (a) and Pb2+ (b) by BakerΓ·s yeast
2.2 Pb2+ΒΡ≥θ Φ≈®Ε»Ε‘ΫΆΡΗΨζΈϋΗΫΕ·ΝΠ―ßΒΡ”Αœλ
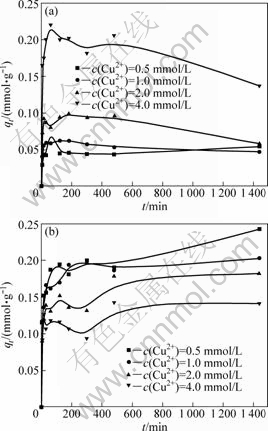
ΆΦ2Υυ ΨΈΣPb2+-Cu2+ΖœΥ°÷–Cu2+ΒΡ≥θ Φ≈®Ε»ΈΣ2.0 mmol/L«ιΩωœ¬Θ§Pb2+ΒΡ≥θ Φ≈®Ε»Ε‘ΫΆΡΗΨζΈϋΗΫPb2+ΚΆCu2+ΒΡ”ΑœλΓΘ”…ΆΦ2(a)Ω…Ω¥≥ωΘ§ΫΆΡΗΨζΕ‘Pb2+ΒΡΈϋΗΫΥφΉ≈Τδ≥θ Φ≈®Ε»ΒΡ‘ωΦ”Εχ‘ω¥σΘ§«“‘Ύ1 440 min ±¥οΒΫΈϋΗΫΉν¥σ÷ΒΘ§¥Υ ±≤ΜΆ§Pb2+≥θ Φ≈®Ε»œ¬ΒΡqtΖ÷±πΈΣ0.048ΓΔ0.114ΚΆ0.182 mmol/gΘ§ΈϋΗΫ–ß¬ Ζ÷±πΈΣ43.46%ΓΔ45.56%ΚΆ41.05%ΓΘ”…ΆΦ2(b)Ω…Ω¥≥ωΘ§‘Ύ≤ΜΆ§Pb2+≥θ Φ≈®Ε»œ¬Θ§ΫΆΡΗΨζΕ‘Cu2+ΒΡΈϋΗΫ‘Ύ≤ΜΆ§Pb2+ΒΡ≥θ Φ≈®Ε»œ¬Θ§Ζ÷±π‘Ύ480ΓΔ300ΚΆ180 minΚσ≥ωœ÷ΝΥΫΒΒΆœ÷œσΘ§ΥΒΟς‘ΎΥΪάκΉ”ΖœΥ°÷–Θ§Cu2+”κPb2+ΒΡΒψΈΜΨΚ’υΙΐ≥Χ÷–Pb2+Ηϋ’Φ”≈ ΤΓΘ‘ΎΨ≠Ιΐ≥θΤΎΒψΈΜ’ΦΨίΚσΘ§Pb2+÷πΫΞΧφ¥ζΒτ“―‘ΎΫΆΡΗΨζ…œ’ΦΨίΒψΈΜΒΡCu2+Θ§ ΙΒΟ≤ΩΖ÷Cu2+÷Ί–¬”ΈάκΒΫ»ή“Κ÷–ΓΘΥφΉ≈Pb2+≥θ Φ≈®Ε»ΒΡ‘ωΦ”Θ§ΖœΥ°÷–≤Έ”κΕ‘Cu2+ΒψΈΜΨΚ’υΒΡPb2+ ΐΝΩ‘ω¥σΘ§ ΙΒΟPb2+ΒΡΨΚ’υ”≈ ΤΗϋΡήΩλΥΌ±μœ÷≥ωά¥Θ§¥”Εχ ΙΒΟΫΆΡΗΨζΕ‘Cu2+ΒΡΉν¥σΈϋΗΫΝΩ≥ωœ÷ΒΡ ±Φδ÷πΫΞΥθΕΧΓΘ
ΆΦ2 Pb2+ΒΡ≥θ Φ≈®Ε»Ε‘ΫΆΡΗΨζΈϋΗΫPb2+ΚΆCu2+ΒΡ”Αœλ
Fig.2 Effects of initial concentration of Pb2+ on biosorption of Pb2+ (a) and Cu2+ (b) by BakerΓ·s yeast
2.3 ΖœΥ°ΉήάκΉ”ΒΡΕ·ΝΠ―ßΖ÷Έω
ΆΦ3Υυ ΨΈΣPb2+-Cu2+ΖœΥ°÷–ΉήάκΉ”≈®Ε»Ζ÷±πΈΣ1.0ΚΆ2.0 mmol/L ±ΫΆΡΗΨζΒΡάκΉ”ΈϋΗΫ”κPb2+ΚΆCu2+ΒΞάκΉ”ΖœΥ°≥θ ΦάκΉ”≈®Ε»Ζ÷±πΈΣ1.0 mmol/LΚΆ2.0 mmol/L ±ΒΡΕ‘±»«ιΩωΓΘ”…ΆΦ3Ω…Ω¥≥ωΘ§ΝΫ÷÷«ιΩωœ¬ΒΡΈϋΗΫΖ¥”Π‘Ύ1 440 min ±Μυ±Ψ¥οΒΫΤΫΚβΘ§«“‘Ύ’ϊΗωΈϋΗΫΕ·ΝΠ―ßΙΐ≥Χ÷–ΕΦ¥φ‘Ύ ΘΨ
ΘΨ ΘΨ
ΘΨ ΓΘΒ±ΗςΖœΥ°ΉήάκΉ”≈®Ε»ΈΣ1.0 mmol/L ±Θ§ΫΆΡΗΨζ‘ΎPb2+ΒΞάκΉ”ΖœΥ°ΒΡΈϋΗΫ‘Ύ480 min ±“―Μυ±Ψ¥οΒΫΤΫΚβΘΜΕχ‘ΎCu2+ΒΞάκΉ”ΖœΥ°ΚΆPb2+-Cu2+ΥΪάκΉ”ΖœΥ°÷–Θ§‘ΎΈϋΗΫΫχ––480 minΚσΘ§ΫΆΡΗΨζΒΡΈϋΗΫΡήΝΠΜΙ”–Οςœ‘‘ωΦ”ΓΘ¥Υœ÷œσ‘ΎΗςΖœΥ°ΉήάκΉ”≈®Ε»ΈΣ2.0 mmol/LΒΡ«ιΩωœ¬±μœ÷≤ΜΟςœ‘Θ§Ω…Ρή «”…”Ύ‘ΎΗΏάκΉ”≈®Ε»«ιΩωœ¬Θ§ΖœΥ°÷–άκΉ” ΐΝΩœύΕ‘”ΎΒψΈΜ ΐΝΩΒΡ±»÷ΒΫœ¥σΘ§άκΉ”’ΦΨίΈϋΗΫΒψΈΜΒΡΥΌΕ»Φ”ΩλΕχ ΙΜυ±ΨΈϋΗΫΤΫΚβΒΡ ±ΦδΥθΕΧΓΘ
ΓΘΒ±ΗςΖœΥ°ΉήάκΉ”≈®Ε»ΈΣ1.0 mmol/L ±Θ§ΫΆΡΗΨζ‘ΎPb2+ΒΞάκΉ”ΖœΥ°ΒΡΈϋΗΫ‘Ύ480 min ±“―Μυ±Ψ¥οΒΫΤΫΚβΘΜΕχ‘ΎCu2+ΒΞάκΉ”ΖœΥ°ΚΆPb2+-Cu2+ΥΪάκΉ”ΖœΥ°÷–Θ§‘ΎΈϋΗΫΫχ––480 minΚσΘ§ΫΆΡΗΨζΒΡΈϋΗΫΡήΝΠΜΙ”–Οςœ‘‘ωΦ”ΓΘ¥Υœ÷œσ‘ΎΗςΖœΥ°ΉήάκΉ”≈®Ε»ΈΣ2.0 mmol/LΒΡ«ιΩωœ¬±μœ÷≤ΜΟςœ‘Θ§Ω…Ρή «”…”Ύ‘ΎΗΏάκΉ”≈®Ε»«ιΩωœ¬Θ§ΖœΥ°÷–άκΉ” ΐΝΩœύΕ‘”ΎΒψΈΜ ΐΝΩΒΡ±»÷ΒΫœ¥σΘ§άκΉ”’ΦΨίΈϋΗΫΒψΈΜΒΡΥΌΕ»Φ”ΩλΕχ ΙΜυ±ΨΈϋΗΫΤΫΚβΒΡ ±ΦδΥθΕΧΓΘ
ΆΦ3 ΖœΥ°÷–ΉήάκΉ”ΒΡΈϋΗΫΕ·ΝΠ―ßΖ÷Έω
Fig.3 Biosorption kinetics analysis of BakerΓ·s yeast to total ions: (a) c0=1.0 mmol/L; (b) c0=2.0 mmol/L
ΝμΆβΩ…“‘Ω¥≥ωΘ§‘Ύ’ϊΗωΕ·ΝΠ―ßΈϋΗΫΙΐ≥Χ÷–Θ§Pb2+-Cu2+ΖœΥ°άκΉ”ΈϋΗΫΉήΝΩΉή «¥Π”ΎPb2+ΚΆCu2+ΒΡΒΞάκΉ”ΖœΥ°άκΉ”ΈϋΗΫΝΩ÷°ΦδΘ§±μΟςΖœΥ°÷–Cu2+ΒΡΦ”»κΕ‘Pb2+ΒΡΈϋΗΫ¥φ‘Ύ―œ÷Ί”ΑœλΘ§≤ΜΫωΫΒΒΆΝΥPb2+ΒΡΈϋΗΫΝΩΘ§“≤Ά§ ±ΫΒΒΆΝΥ’ϊΧεάκΉ”ΈϋΗΫΝΩΓΘ”…¥ΥΩ…“‘»œΈΣΘ§ΫΆΡΗΨζΕ‘÷ΊΫπ τάκΉ”ΈϋΗΫΒΡ―Γ‘ώΡήΝΠ «Pb2+¥σ”ΎCu2+ΓΘ
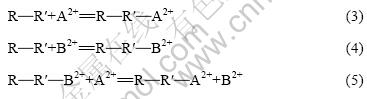
Ϋ(1)ΚΆ(2)ΈΣάκΉ”¬γΚœΖ¥”ΠΘ§ Ϋ(3)ΈΣάκΉ”ΫΜΜΜΖ¥”ΠΓΘ‘ΎΥΪάκΉ”ΖœΥ°÷–ΈϋΗΫΒΡΉν≥θΫΉΕΈΘ§ΨζΧεΈϋΗΫΒψΈΜœύΕ‘≥δΉψΘ§ΝΫ÷÷άκΉ””≈œ»÷±Ϋ””κΨζΧεΈϋΗΫΒψΈΜΫχ––¬γΚœΉς”ΟΓΘΒ±Ζ¥”ΠΫχ––ΒΫ“ΜΕ® ±ΦδΚσΘ§ΈϋΗΫΒψΈΜ“―±ΜάκΉ”¥σΝΩ’ΦΨίΘ§ΒψΈΜ ΐœύΕ‘≤ΜΉψΓΘ‘Ύ’β÷÷«ιΩωœ¬Θ§ΒψΈΜΨΚ’υΡήΝΠ«ΩΒΡάκΉ”ΩΣ Φœ‘ Ψ”≈ ΤΘ§“ΜΕ®≥ΧΕ»…œΫΜΜΜ≤ΩΖ÷ΤδΥϋ“―ΈϋΗΫάκΉ”Θ§ΦΧ–χΜΚ¬ΐ’ΦΨίΒψΈΜΘ§ΕχΆ§ ±“≤ΒΦ÷¬ΤδΥϋάκΉ”ΈϋΗΫΝΩΒΡœύΕ‘ΫΒΒΆΓΘ“ρ¥ΥΘ§Ε‘”ΎΕύάκΉ”ΖœΥ°Θ§≤Δ≤Μ «ΈϋΗΫΖ¥”ΠΫχ––ΒΡ ±Φδ‘Ϋ≥ΛΘ§–ßΙϊ‘ΫΚΟΓΘάΐ»γΘ§‘Ύ Β―ι…ηΕ®≤ΜΆ§≥θ Φ≈®Ε»œ¬Θ§Ε‘”ΎΉή≈®Ε»ΈΣ2.0 mmol/LΒΡPb2+-Cu2+ΖœΥ°÷–ΫΆΡΗΨζΕ‘Cu2+ΒΡΈϋΗΫ‘Ύ60 minΡή¥οΒΫΫœΚΟΒΡΈϋΗΫ–ßΙϊΘ§ΕχΥφΉ≈ΈϋΗΫ ±ΦδΒΡ―”≥ΛΘ§ΫΆΡΗΨζΕ‘Pb2+ΈϋΗΫΝΩ‘ωΦ”ΒΡΆ§ ± ΙΤδΕ‘Cu2+ΒΡΈϋΗΫΝΩ”–ΥυΫΒΒΆΓΘ‘Ύ ΒΦ ΙΛ≥Χ”Π”ΟΙΐ≥Χ÷–Θ§Έ“Ο«Ω…“‘”ΟΖ÷≤ΫΈϋΗΫΖ®Ϋχ––¥ΠάμΘ§œ»‘ΎΕΧ ±ΦδΡΎ”≈œ»Ε‘Cu2+Ϋχ––ΈϋΗΫ¥ΠάμΘ§»ΜΚσ‘Ύ”ΟΫΆΡΗΨζΕ‘ Θ”ύάκΉ”Ϋχ––‘Ό¥ΠάμΓΘ
2.4 ΕΰΦΕΕ·ΝΠ―ßΙΐ≥ΧΖ÷Έω
Ε·ΝΠ―ß―–ΨΩ «ΙΛ“’…ηΦΤΒΡΜυ¥ΓΘ§≤Δ”–÷ζ”ΎΧΫΧ÷ΈϋΗΫΜζάμΓΘ…ζΈοΈϋΗΫ÷ΊΫπ τάκΉ”ΒΡΙΐ≥ΧΘ§ΤδœΏ–‘œύΙΊ«Ω”Ύ“ΜΦΕΥΌ¬ ΖΫ≥ΧΒΡΘ§≥Θ≥Θ”ΟΉΦΕΰΦΕΥΌ¬ ΖΫ≥Χά¥Οη ωΘΚ

“‘…œΙΪ Ϋ÷–ΘΚk2ΈΣΥΌ¬ ≥Θ ΐΘ§g/(mg?min)ΘΜqeΈΣΤΫΚβΈϋΗΫΦΝΒΞΈΜ÷ ΝΩΒΡΫπ τάκΉ”ΈϋΗΫΝΩΘ§mg/gΘΜqtΈΣt ±ΩΧΈϋΗΫΦΝΒΡΒΞΈΜ÷ ΝΩΒΡΫπ τάκΉ”ΈϋΗΫΝΩΘ§mg/gΘΜhΈΣΈϋΗΫ≥θ ΦΥΌ¬ Θ§mg/(g?min)ΓΘ
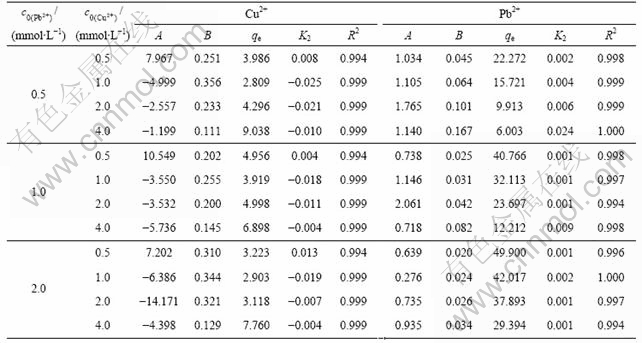
±μ1ΥυΝ–ΈΣPb2+-Cu2+ΖœΥ°÷–ΫΆΡΗΨζΕΰΦΕΕ·ΝΠ―ßΡΘ–ΆΒΡΦΤΥψΫαΙϊΓΘ”…±μ1Ω…“‘Ω¥≥ωΘ§ΖœΥ°÷–ΫΆΡΗΨζΒΡΕ·ΝΠ―ßΕΰΦΕΈϋΗΫΡΘ–ΆΦΤΥψΫαΙϊ÷–R¥ο0.994Θ§±μΟςΤδΡβΚœ–ßΙϊΕΦ±»ΫœΚΟΘ§ΥΒΟςΖ¥”ΠΙΐ≥Χ÷–œόΥΌ≤Ϋ÷η «Μ·―ßΈϋΗΫΙΐ≥Χ[16-17]ΓΘΕ‘≤ΜΆ§Pb2+-Cu2+ΖœΥ°÷–ΫΆΡΗΨζΈϋΗΫCu2+ΒΡΡΘΡβΦΤΥψΫαΙϊœ‘ ΨΘ§≥ΐΝΥΖœΥ°÷–Cu2+≥θ Φ≈®Ε»ΈΣ0.5 mmol/L“‘ΆβΘ§ΤδΥϊΦΗ÷÷≥θ Φ≈®Ε»œ¬ΥυΦΤΥψΒΡK2ΚΆhΕΦ≥ωœ÷ΗΚ÷Βœ÷œσΘ§’β±μΟςΫΆΡΗΨζΕ‘ΖœΥ°÷–Cu2+ΒΡΈϋΗΫ‘Ύ’βΦΗ÷÷Cu2+ΒΡ≥θ Φ≈®Ε»œ¬‘Ύ’ϊΗωΖœΥ°ΈϋΗΫΤΫΚβ«ΑΨΆ“―Ψ≠¥οΒΫΉν¥σ÷ΒΘ§≤Δ‘Ύ¥ΥΚσΘ§ΈϋΗΫΝΩ≥ωœ÷œ¬ΫΒΘ§¥”Εχ ΙΒΟΤδΦΤΥψΫαΙϊ≥ωœ÷ΗΚ÷ΒΓΘ’β“≤”κΆΦ1(a)ΚΆΆΦ2(b)ΒΡΫαΙϊ“Μ÷¬ΓΘ“ρ¥ΥΘ§Ε‘”ΎPb2+-Cu2+ΖœΥ°Θ§Ε‘Cu2+ΒΡ¥Πάμ“Σ±»Ε‘Pb2+ΒΡ¥ΠάμΥΌΕ»ΩλΘ§“≤ΨΆ «Ε‘Cu2+ΒΡ¥Πάμ≤Μ“Υ”κΕ‘Pb2+ΒΡ¥Πάμ“Μ―υΨΏ”–Ϋœ≥ΛΒΡ ±ΦδΓΘΕ‘”ΎPb2+Θ§‘ΎPb2+≥θ Φ≈®Ε»ΈΣ0.5 mmol/LΒΡΖœΥ°÷–Θ§ΥφΉ≈Cu2+≥θ Φ≈®Ε»ΒΡ‘ωΦ”Θ§‘ΎΫΆΡΗΨζΕ‘ΖœΥ°÷–Pb2+ΒΡΈϋΗΫΙΐ≥Χ÷–Θ§K2ΚΆh÷πΫΞ‘ω¥σΘ§±μΟς‘ΎCu2+ΨΚ’υ–≤Τ»ΜΖΨ≥œ¬Θ§Cu2+ΒΡ±»άΐ‘ω¥σ ΙΫΆΡΗΨζΕ‘Pb2+ΒΡΈϋΗΫΥΌ¬ œ‘ΒΟΗϋΩλΘ§“≤÷ΛΟςΝΥPb2+‘ΎΈϋΗΫΒψΈΜΨΚ’υ÷–ΒΡΟςœ‘”≈ ΤΓΘ
±μ1 Pb2+-Cu2+ΖœΥ°÷–ΫΆΡΗΨζΕΰΦΕΕ·ΝΠ―ßΡΘ–ΆΒΡΦΤΥψΫαΙϊ
Table 1 Calculation results of second-kinetics biosorption model to different waste waters of Pb2+-Cu2+
2.5 SEMΚΆEDSΖ÷Έω
ΆΦ4Υυ ΨΈΣΟφΑϋΫΆΡΗΨζ”κPb2+-Cu2+ΥΪάκΉ”ΖœΥ°÷–÷ΊΫπ τάκΉ”Ής”Ο«ΑΓΔΚσΒΡSEMœώΓΘ”…ΆΦ4Ω…“‘Ω¥≥ωΘ§Ής”Ο«ΑΘ§ΟφΑϋΫΆΡΗΨζ±μΟφΙβΜ§Θ§ΨζΧε…œ”–…ΌΝΩœΗ–ΓπΛΗΫΈο(ΦϊΆΦ4(a))ΘΜΉς”Ο1 440 minΚσΘ§ΨζΧε±μΟφΗ≤Η«ΒΡπΛΗΫΈο¥σ¥σ‘ωΦ”Θ§ΨζΧε≥ωœ÷≤ΜΙφ‘ρ±δ–ΈΘ§“≤ΖΔœ÷ΨζΧεΆβ”–¥σΝΩΤ§Ή¥ΓΔΆχΉ¥Έο÷ (ΦϊΆΦ4(b))ΓΘ’β «ΖώΈΣΨζΧεœΗΑϊΤΤΝ―ΚσΘ§≤–”ύœΗΑϊ±ΎΚΆΡΎ≤ΩΈο÷ Άβ–Ι≤Δ”κCu2+ΚΆPb2+Β»άκΉ”–Έ≥…ΒΡ¬γΚœΈο÷ Θ§ΜΙ–ηΫχ“Μ≤Ϋ―–ΨΩΘ§’β”–Ω…Ρή «‘λ≥…ΨζΧε±μΟφπΛΗΫΈο‘ωΕύΒΡ‘≠“ρ÷°“ΜΓΘ”…¥ΥΩ…“‘Ω¥≥ωΘ§‘ΎΫΆΡΗΨζΕ‘÷ΊΫπ τάκΉ”ΈϋΗΫΙΐ≥Χ÷–Θ§ΨζΧεΆ§ ±“≤‘β ή“ΜΕ®≥ΧΕ»ΒΡΤΤΜΒΓΘ
ΆΦ5Υυ ΨΈΣ‘Ύ≤ΜΆ§άκΉ”ΖœΥ°÷–ΫΆΡΗΨζΈϋΗΫ24 hΚσΒΡEDSΖ÷ΈωΓΘ”…ΆΦ5(a)ΚΆ(b)Ω…ΡξΩ¥≥ωΘ§‘ΎΟφΑϋΫΆΡΗΨζΖ÷±πΈϋΗΫCu2+ΚΆPb2+ΚσΘ§≥ωœ÷Οςœ‘ΒΡCu2+ΚΆPb2+ΒΡΈϋ ’ΖεΓΘ”…ΆΦ5(c)Ω…“‘Ω¥≥ωΘ§‘ΎΗΟΖœΥ°÷–Θ§Pb2+ΚΆCu2+ΒΡΈϋ ’ΖεΗΏΕΦ”–ΫΒΒΆΘ§ΧΊ±π «Cu2+ΒΡΫΒΒΆΗϋΈΣΟςœ‘ΓΘ”…”ΎPb2+ΒΡΦ”»κΘ§ΫΆΡΗΨζΈϋΗΫΒΫΨζΧε…œΒΡCu2+ΚΆPb2+ΕΦΟςœ‘ΟΜ”–ΒΞάκΉ”ΖœΥ°÷–ΒΡΕύΘ§Ϋχ“Μ≤ΫΥΒΟς‘Ύ Β―ι≈®Ε»œ¬Θ§Pb2+”κCu2+œύΜΞΕΦ”–Οςœ‘ΒΡ“÷÷ΤΉς”ΟΘ§«“Pb2+ΚΆCu2+‘ΎΈϋΗΫΒψΈΜΨΚ’υΙΐ≥Χ÷–Θ§«Α’Ώ’Φ”≈ ΤΘ§’β“≤”κ«ΑΟφΕ·ΝΠ―ßΖ÷Έω÷–“―”–Ϋα¬έœύΖϊΓΘ

ΆΦ4 Pb2+-Cu2+ΖœΥ°÷–ΫΆΡΗΨζΈϋΗΫ«ΑΚΆΈϋΗΫ1 440 minΚσΒΡSEMœώ
Fig.4 SEM images of BakerΓ·s yeast in waste water of Pb2+-Cu2+ before adsorption (a) and after absorption for 1 440 min (b)
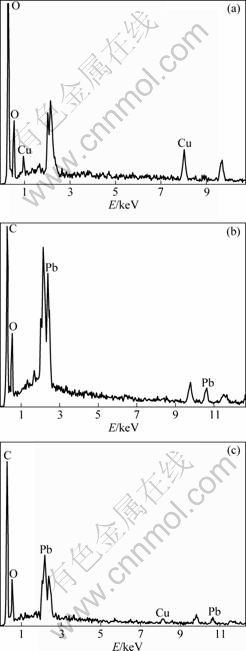
ΆΦ5 ≤ΜΆ§άκΉ”ΖœΥ°÷–ΫΆΡΗΨζΈϋΗΫ24 hΚσΒΡEDSΖ÷Έω
Fig.5 EDS analyses of BakerΓ·s yeast after absorption for 24 h in different ions systems: (a) Cu2+; (b) Pb2+; (c) Pb2+-Cu2+
3 Ϋα¬έ
1) ‘Ύ’ϊΗωΕ·ΝΠ―ßΈϋΗΫΙΐ≥Χ÷–Θ§Ήν≥θ60 min ±Θ§ΫΆΡΗΨζΕ‘ΗςάκΉ”ΒΡΈϋΗΫ“―Ψ≠¥οΒΫΫœΚΟΒΡΈϋΗΫ–ßΙϊΘ§ΫΆΡΗΨζΕ‘≤ΜΆ§άκΉ”ΖœΥ°ΒΡΈϋΗΫΙΊœΒ¥φ‘Ύ ΘΨ
ΘΨ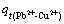 ΘΨ
ΘΨ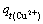 Θ§±μΟςΖœΥ°÷–Cu2+ΒΡΦ”»κΕ‘”ΎPb2+ΒΡΈϋΗΫ¥φ‘Ύ―œ÷Ί”ΑœλΘ§≤ΜΫωΫΒΒΆΝΥPb2+ΒΡΈϋΗΫΝΩΘ§“≤Ά§ ±ΫΒΒΆΝΥ’ϊΧεάκΉ”ΒΡΈϋΗΫΝΩΓΘ
Θ§±μΟςΖœΥ°÷–Cu2+ΒΡΦ”»κΕ‘”ΎPb2+ΒΡΈϋΗΫ¥φ‘Ύ―œ÷Ί”ΑœλΘ§≤ΜΫωΫΒΒΆΝΥPb2+ΒΡΈϋΗΫΝΩΘ§“≤Ά§ ±ΫΒΒΆΝΥ’ϊΧεάκΉ”ΒΡΈϋΗΫΝΩΓΘ
2) ΕΰΦΕΕ·ΝΠ―ßΖΫ≥ΧΦΤΥψΫαΙϊœ‘ ΨΘ§ΥφΉ≈Cu2+≈®Ε»ΒΡ‘ωΦ”Θ§ΫΆΡΗΨζΕ‘Pb2+ΒΡΈϋΗΫΥΌ¬ ≥Θ ΐK2”κh÷πΫΞ‘ω¥σΘ§ΥΒΟς‘ΎCu2+ΨΚ’υ–≤Τ»ΜΖΨ≥œ¬Θ§Cu2+ΒΡ±»άΐ‘ω¥σ ΙΫΆΡΗΨζΕ‘Pb2+ΒΡΈϋΗΫΥΌ¬ œ‘ΒΟΗϋΩλΘ§“≤÷ΛΟςPb2+‘ΎΈϋΗΫΒψΈΜΨΚ’υΙΐ≥Χ÷–”–Οςœ‘”≈ ΤΘ§EDS≤β ‘ΫαΙϊ“≤÷Λ ΒΝΥ’βΒψΓΘ
3) SEMΖ÷ΈωΖΔœ÷Θ§ΫΆΡΗΨζΈϋΗΫCu2+ΚΆPb2+ΚσΘ§ΨζΧε≥ωœ÷≤ΜΙφ‘ρ±δ–Έ≤Δ‘β ή“ΜΕ®ΒΡΤΤΜΒΘ§ΨζΧεΆβ”–¥σΝΩΤ§Ή¥ΓΔΆχΉ¥Έο÷ Θ§’β“≤Ω…Ρή «‘λ≥…ΨζΧε±μΟφπΛΗΫΈο‘ωΕύΒΡ‘≠“ρ÷°“ΜΓΘ
4) ΫΆΡΗΨζΕ‘Cu2+ΚΆPb2+ΕΦ”–“ΜΗωΩλΥΌΈϋΗΫΙΐ≥ΧΘ§œύΕ‘Εχ―‘ΤδΕ‘Pb2+ΒΡΈϋΗΫΗϋΨΏ”≈ ΤΓΘ
REFERENCES
[1] PENG Chang-sheng, MENG Hong, SONG Shao-xian, LU Shou-ci, LOPEZ-VAIDIVIESO A. Elimination of Cr(Δω) from electroplating wastewater by electrodialysis following chemical precipitation[J]. Separation Science and Technology, 2004, 39(7): 1501-1517.
[2] BERBER-MENDOZa M S, LEYVA-RAMOS R, ALONSO- DAVIL a P, FUENTES-RUBIO L, GUERRERO-CORONADO R M.Comparison of isotherms for the ion exchange of Pb(Δρ) from aqueous solution onto homoionic clinoptilolite[J]. Journal of Colloid and Interface Science, 2006, 301 (1): 40-45.
[3] DING Shao-lan, ZHAO Quan-yong, REN Hui-jun, ZHAO Chuan-chuan, JING Ya-zhuo. Experimental study of separating Cr(Δω) using a mixed carrier emulsion membrane[J]. Journal of the Society of Leather Technologists and Chemists, 2005, 89(3): 111-116.
[4] bERNARD S, FAUCHAIS P, JARRIGE J. Process achievement for the treatment by transferred arc of fly ashes from waste incenerators by on line measurement of heavy metal evaporation[J]. High Temperature Material Processes, 2001, 5(2): 181-194.
[5] WATANAB e T, JIN H W, CHO K J, KURODA M. Application of a bio-electrochemical reactor process to direct treatment of metal pickling wastewater containing heavy metals and high strength nitrate[J]. Water Science and Technology, 2004, 50(8): 111-118.
[6] ¥ζ γΨξ, ΈΚΒ¬÷ό, ΑΉάωΟΖ, ÷ήΕΪ«Ό, Άθ”ώΨξ, ΝθΈΡΗ’. …ζΈοΈϋΗΫ-≥ΝΫΒΖ®»Ξ≥ΐΒγΕΤΖœΥ°÷–ο”[J]. ÷–Ιζ”–…ΪΫπ τ―ß±®, 2008, 18(10): 1945-1950.
DAI Shu-juan, WEI De-zhou, BAI Li-mei, ZHOU Dong-qin, WANG Yu-juan, LIU Wen-gang. Removing cadmium from cadmium-containing electroplating wastewater by biosorption- sedimentation[J]. The Chinese Journal of Nonferrous Metals, 2008, 18(10): 1945-1950.
[7] SILVA E A, COSSICH E S, TAVARES C G, CARDOZO F L, GUIRARDELLO R. Biosorption of binary mixtures of Cr(III) and Cu(Δρ) ions by Sargassum sp[J]. Brazilian Journal of Chemical Engineering, 2003, 20(3): 213-227.
[8] AKAR T, TUNALI S. Biosorption characteristics of Aspergillus flavus biomass for removal of Pb(Δρ) and Cu(Δρ) ions from an aqueous solution[J]. Bioresource Technology, 2006, 97(15): 1780-1787.
[9] CHEN Xin-cai, SHI Ji-yan,CHEN Ying-xu, XU Xiang-hua, XU Sheng-you, WANG Yuan-peng. Tolerance and biosorption of copper and zinc by Pseudomonas putida CZ1 isolated from metal-polluted soil[J]. Canadian Journal of Microbiology, 2006, 52(4): 308-316.
[10] TUNALI S, AKAR T, OZCAN A S, KIRAN I, OZCAN A. Equilibrium and kinetics of biosorption of lead(Δρ) from aqueous solutions by Cephalosporium aphidicola[J].Separation and Purification Technology, 2006, 47(3): 105-112.
[11] ALIMOHAMADI M, ABOLHAMD G, KESHTKARA. Pb(Δρ) and Cu(Δρ) biosorption on Rhizopus arrhizus modeling mono- and multi-component systems[J]. Minerals Engineering, 2005,18(13/14): 1325-1330.
[12] KIRAN I, AKAR T, TUNALI S. Biosorption of Pb(Δρ) and Cu(Δρ) from aqueous solutions by pretreated biomass of Neurospora crassa[J]. Process Biochemistry, 2005, 40(11): 3550-3558.
[13] DURSUN A Y. A comparative study on determination of the equilibrium, kinetic and thermodynamic parameters of biosorption of copper(Δρ) and lead(Δρ) ions onto pretreated Aspergillus niger[J]. Biochemical Engineering Journal, 2006, 28(2): 187-195.
[14] OZER A, OZER D. Comparative study of the biosorption of Pb(Δρ), Ni(Δρ) and Cr(Δω) ions onto S-cerevisiae: Determination of biosorption heats[J]. Journal of Hazardous Materials, 2003, 100(1/3): 219-229.
[15] HAN Run-ping, LI Hong-kui, LI Yan-hu, ZHANG Jing-hua, XIAO Hui-jun, SHI Jie. Biosorption of copper and lead ions by waste beer yeast[J]. Journal of Hazardous Materials, 2006, 137(3): 1569-1576.
[16] ≥¬ ≤”, ΆθΫ®Νζ. ΡπΨΤΫΆΡΗΈϋΗΫ÷ΊΫπ τάκΉ”ΒΡ―–ΨΩΫχ’Ι[J]. ÷–Ιζ…ζΈοΙΛ≥Χ‘”÷Ψ, 2006, 26(1): 69-76.
CHEN Can, WANG Jian-long. Review on biosorption of heavy metal by Saccharomyces cerevisiae[J]. China Biotechnology, 2006, 26(1): 69-76.
[17] PADMAVATHY V, VASUDEVAN P, DHINGRA S C. Biosorption of nickel(Δρ) ions on BakerΓ·s yeast[J]. Process Biochemistry, 2003, 38(10): 1389-1395.
(±ύΦ≠ άν―όΚλ)
ΜυΫπœνΡΩΘΚΙζΦ“Ή‘»ΜΩΤ―ßΜυΫπΉ ÷ζœνΡΩ(10776027)ΘΜΩΤΦΦ≤Ω≈ΖΟΥΙζΦ ΚœΉςΉ®œνΉ ÷ζœνΡΩ(06zg0101)
’Ηε»’ΤΎΘΚ2009-04-14ΘΜ–όΕ©»’ΤΎΘΚ2009-07-13
Ά®–≈Ής’ΏΘΚΕ≠ΖΔ«ΎΘ§ΫΧ ΎΘ§≤© ΩΘΜΒγΜΑΘΚ0816-6089013ΘΜE-mailΘΚfqdong@swust.edu.cn